"Naître, c'est recevoir tout un univers en cadeau." Jostein Gaarder
“Décider d’avoir un enfant c’est accepter que votre coeur se sépare de votre corps et marche à vos côtés pour toujours.” Katharine Hadley
Intermediate-dose versus low-dose low-molecular-weight heparin in pregnant and post-partum women with a history of venous thromboembolism (Highlow study): an open-label, multicentre, randomised, controlled trial
Héparine de bas poids moléculaire à dose intermédiaire versus à faible dose chez les femmes enceintes et en post-partum ayant des antécédents de thromboembolie veineuse (étude Highlow) : un essai ouvert, multicentrique, randomisé et contrôlé
Ingrid M Bistervels, Andrea Buchmüller, Hanke M G Wiegers*, Fionnuala Ní Áinle, Bernard Tardy, Jennifer Donnelly, Peter Verhamme,Anne F Jacobsen, Anette T Hansen, Marc A Rodger, Maria T DeSancho, Roman G Shmakov, Nick van Es, Martin H Prins, Céline Chauleur,
Saskia Middeldorp, for the Highlow block writing committee† and Highlow Investigators‡Lancet 2022; 400: 1777–87
Saskia Middeldorp, for the Highlow block writing committee† and Highlow Investigators‡Lancet 2022; 400: 1777–87
Article libre d'accés

#ISTH2022, très belle étude
La thromboembolie veineuse liée à la grossesse est une cause majeure de morbidité et de mortalité maternelles, et la thromboprophylaxie est indiquée chez les femmes enceintes et en post-partum ayant des antécédents de thromboembolie veineuse. La dose optimale d'héparine de bas poids moléculaire pour prévenir la thromboembolie veineuse récurrente pendant la grossesse et la période post-partum est incertaine.
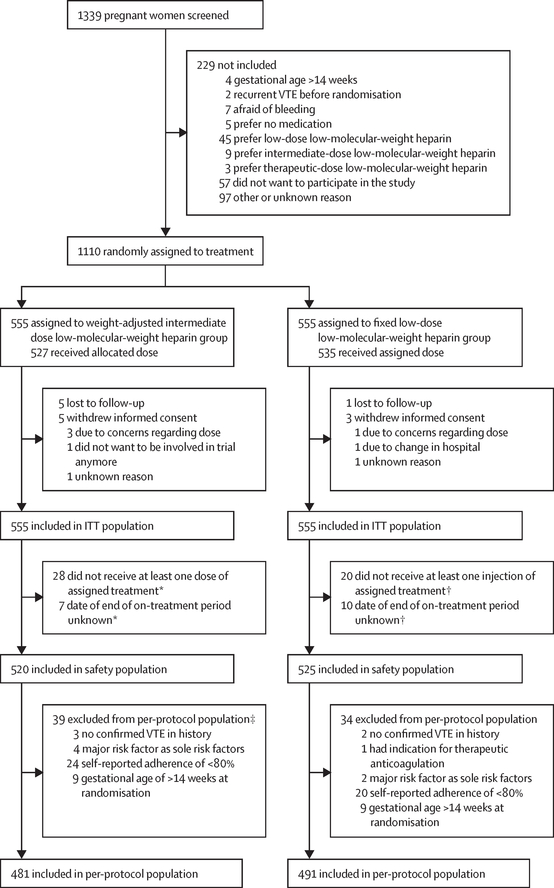
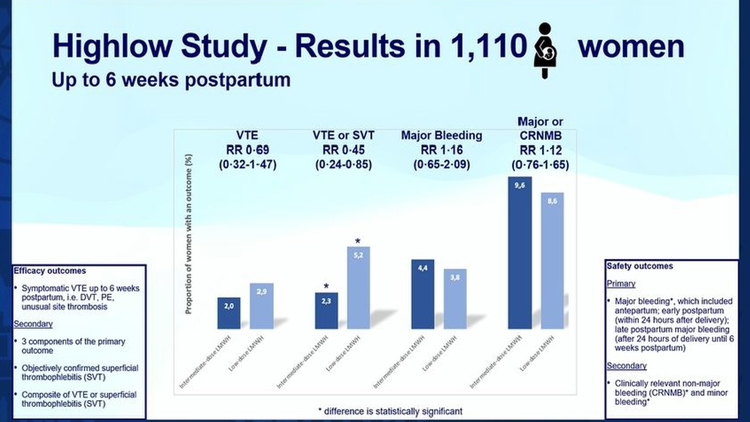
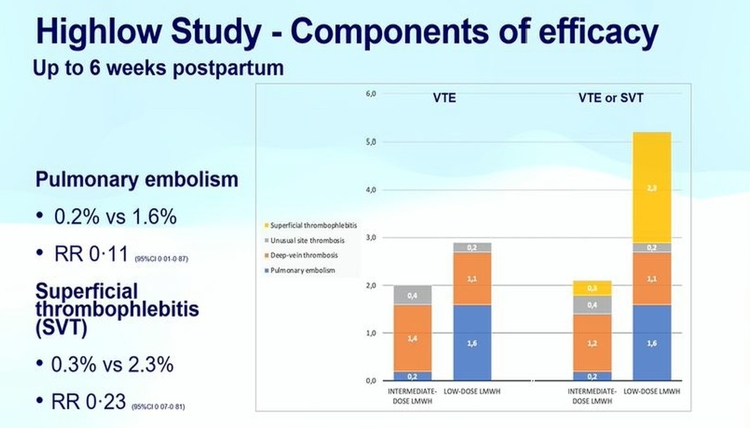
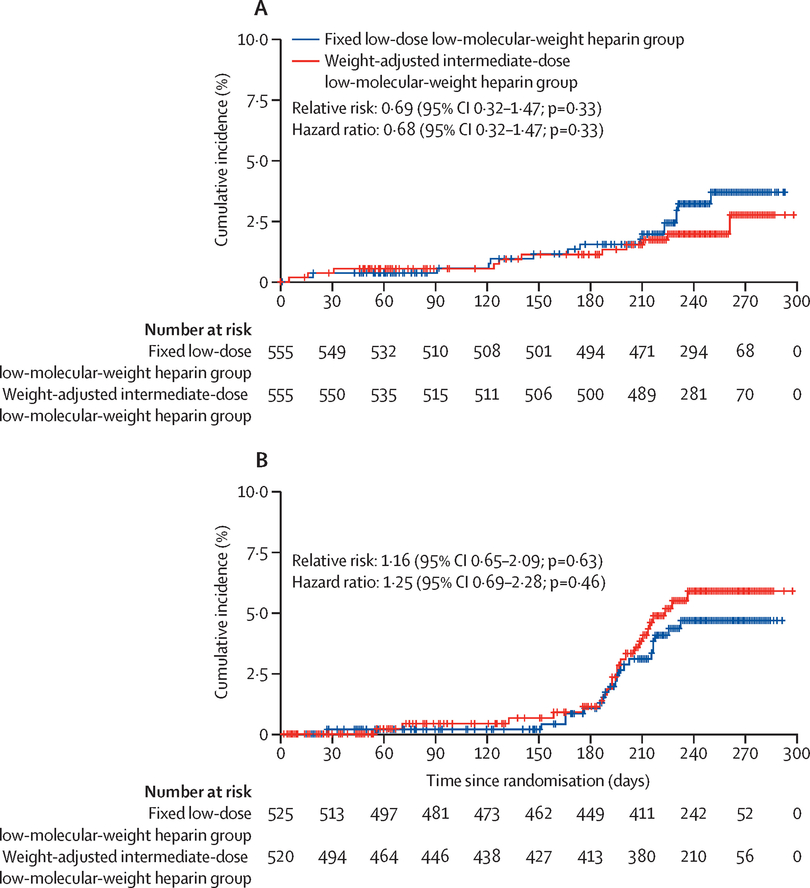
Entre le 24 avril 2013 et le 31 octobre 2020, 1 339 femmes enceintes ont été examinées pour déterminer leur éligibilité, dont 1 110 ont été assignées au hasard à une dose intermédiaire ajustée en fonction du poids (n = 555) ou à une faible dose fixe (n = 555) à faible dose. héparine de poids moléculaire (population ITT). Une thromboembolie veineuse est survenue chez 11 (2 %) des 555 femmes du groupe à dose intermédiaire ajustée en fonction du poids et chez 16 (3 %) des 555 femmes du groupe à faible dose fixe (risque relatif [RR] 0,69 [IC à 95 % 0·32–1·47] ; p=0·33). Une thromboembolie veineuse est survenue avant l'accouchement chez cinq (1 %) femmes du groupe à dose intermédiaire et chez cinq (1 %) femmes du groupe à faible dose, et après l'accouchement chez six (1 %) femmes et 11 (2 %) femmes. Une hémorragie majeure pendant le traitement dans la population de sécurité (N=1045) est survenue chez 23 (4 %) des 520 femmes du groupe à dose intermédiaire et chez 20 (4 %) des 525 femmes du groupe à faible dose (RR 1·16 [IC à 95 % 0·65–2·09]).
Chez les femmes ayant des antécédents de thromboembolie veineuse, l'héparine de bas poids moléculaire à dose intermédiaire ajustée en fonction du poids pendant les périodes combinées antepartum et post-partum n'a pas été associée à un risque de récidive plus faible que l'héparine de bas poids moléculaire à faible dose fixe . Ces résultats indiquent que l'héparine de bas poids moléculaire à faible dose pour la thromboprophylaxie pendant la grossesse est la dose appropriée pour la prévention de la thromboembolie veineuse récurrente liée à la grossesse.


Commentaire
Contexte
La thromboembolie veineuse liée à la grossesse est une cause majeure de morbidité et de mortalité maternelles, et la thromboprophylaxie est indiquée chez les femmes enceintes et en post-partum ayant des antécédents de thromboembolie veineuse. La dose optimale d'héparine de bas poids moléculaire pour prévenir la thromboembolie veineuse récurrente pendant la grossesse et la période post-partum est incertaine.
Méthodes
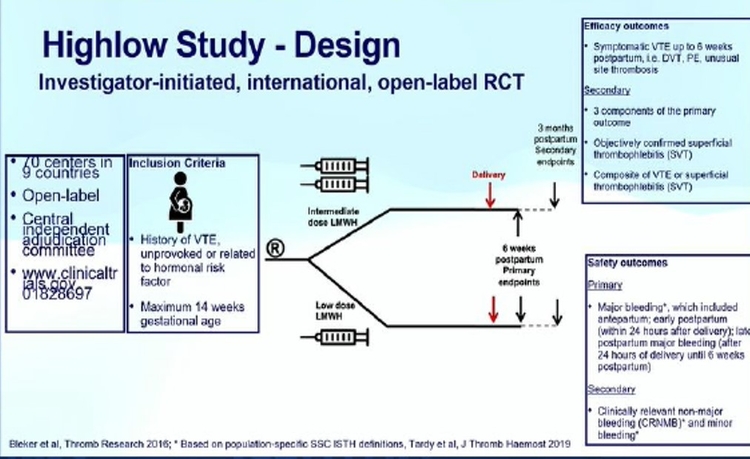
Dans cet essai ouvert, randomisé et contrôlé (Highlow), des femmes enceintes ayant des antécédents de maladie thromboembolique veineuse ont été recrutées dans 70 hôpitaux de neuf pays (Pays-Bas, France, Irlande, Belgique, Norvège, Danemark, Canada, États-Unis et Russie). Les femmes étaient éligibles si elles étaient âgées de 18 ans ou plus avec des antécédents de thromboembolie veineuse objectivement confirmée et avec un âge gestationnel de 14 semaines ou moins. Les femmes éligibles ont été assignées au hasard (1:1), avant 14 semaines d'âge gestationnel, à l'aide d'un système en ligne et d'une randomisation par blocs permutés (taille de bloc de six), stratifiée par centre, soit à une dose intermédiaire ajustée en fonction du poids, soit à une faible dose fixe - doser de l'héparine de bas poids moléculaire par voie sous-cutanée une fois par jour jusqu'à 6 semaines post-partum. Le principal critère d'évaluation de l'efficacité était la thromboembolie veineuse objectivement confirmée (c.-à-d. thrombose veineuse profonde, embolie pulmonaire ou thrombose veineuse de site inhabituel), tel que déterminé par un comité d'adjudication central indépendant, dans la population en intention de traiter (ITT) (c'est-à-dire toutes les femmes affectées au hasard au traitement). Le principal critère de jugement de sécurité était l'hémorragie majeure qui incluait l'hémorragie ante-partum, post-partum précoce (dans les 24 h après l'accouchement) et l'hémorragie majeure post-partum tardive (24 h ou plus après l'accouchement jusqu'à 6 semaines post-partum), évaluée chez toutes les femmes ayant reçu au moins une dose du traitement assigné et dont la date de fin de traitement était connue. Cette étude est enregistrée auprès de post-partum précoce (dans les 24 h après l'accouchement) et saignement majeur post-partum tardif (24 h ou plus après l'accouchement jusqu'à 6 semaines post-partum), évalués chez toutes les femmes ayant reçu au moins une dose du traitement assigné et présentant une date de fin de traitement. Cette étude est enregistrée auprès de post-partum précoce (dans les 24 h après l'accouchement) et saignement majeur post-partum tardif (24 h ou plus après l'accouchement jusqu'à 6 semaines post-partum), évalués chez toutes les femmes ayant reçu au moins une dose du traitement assigné et présentant une date de fin de traitement. Cette étude est enregistrée auprès deClinicalTrials.gov , NCT01828697 , et est maintenant terminée.
Dans cet essai ouvert, randomisé et contrôlé (Highlow), des femmes enceintes ayant des antécédents de maladie thromboembolique veineuse ont été recrutées dans 70 hôpitaux de neuf pays (Pays-Bas, France, Irlande, Belgique, Norvège, Danemark, Canada, États-Unis et Russie). Les femmes étaient éligibles si elles étaient âgées de 18 ans ou plus avec des antécédents de thromboembolie veineuse objectivement confirmée et avec un âge gestationnel de 14 semaines ou moins. Les femmes éligibles ont été assignées au hasard (1:1), avant 14 semaines d'âge gestationnel, à l'aide d'un système en ligne et d'une randomisation par blocs permutés (taille de bloc de six), stratifiée par centre, soit à une dose intermédiaire ajustée en fonction du poids, soit à une faible dose fixe - doser de l'héparine de bas poids moléculaire par voie sous-cutanée une fois par jour jusqu'à 6 semaines post-partum. Le principal critère d'évaluation de l'efficacité était la thromboembolie veineuse objectivement confirmée (c.-à-d. thrombose veineuse profonde, embolie pulmonaire ou thrombose veineuse de site inhabituel), tel que déterminé par un comité d'adjudication central indépendant, dans la population en intention de traiter (ITT) (c'est-à-dire toutes les femmes affectées au hasard au traitement). Le principal critère de jugement de sécurité était l'hémorragie majeure qui incluait l'hémorragie ante-partum, post-partum précoce (dans les 24 h après l'accouchement) et l'hémorragie majeure post-partum tardive (24 h ou plus après l'accouchement jusqu'à 6 semaines post-partum), évaluée chez toutes les femmes ayant reçu au moins une dose du traitement assigné et dont la date de fin de traitement était connue. Cette étude est enregistrée auprès de post-partum précoce (dans les 24 h après l'accouchement) et saignement majeur post-partum tardif (24 h ou plus après l'accouchement jusqu'à 6 semaines post-partum), évalués chez toutes les femmes ayant reçu au moins une dose du traitement assigné et présentant une date de fin de traitement. Cette étude est enregistrée auprès de post-partum précoce (dans les 24 h après l'accouchement) et saignement majeur post-partum tardif (24 h ou plus après l'accouchement jusqu'à 6 semaines post-partum), évalués chez toutes les femmes ayant reçu au moins une dose du traitement assigné et présentant une date de fin de traitement. Cette étude est enregistrée auprès deClinicalTrials.gov , NCT01828697 , et est maintenant terminée.
Résultats
Entre le 24 avril 2013 et le 31 octobre 2020, 1 339 femmes enceintes ont été examinées pour déterminer leur éligibilité, dont 1 110 ont été assignées au hasard à une dose intermédiaire ajustée en fonction du poids (n = 555) ou à une faible dose fixe (n = 555) à faible dose. héparine de poids moléculaire (population ITT). Une thromboembolie veineuse est survenue chez 11 (2 %) des 555 femmes du groupe à dose intermédiaire ajustée en fonction du poids et chez 16 (3 %) des 555 femmes du groupe à faible dose fixe (risque relatif [RR] 0,69 [IC à 95 % 0·32–1·47] ; p=0·33). Une thromboembolie veineuse est survenue avant l'accouchement chez cinq (1 %) femmes du groupe à dose intermédiaire et chez cinq (1 %) femmes du groupe à faible dose, et après l'accouchement chez six (1 %) femmes et 11 (2 %) femmes. Une hémorragie majeure pendant le traitement dans la population de sécurité (N=1045) est survenue chez 23 (4 %) des 520 femmes du groupe à dose intermédiaire et chez 20 (4 %) des 525 femmes du groupe à faible dose (RR 1·16 [IC à 95 % 0·65–2·09]).
Interprétation
Chez les femmes ayant des antécédents de thromboembolie veineuse, l'héparine de bas poids moléculaire à dose intermédiaire ajustée en fonction du poids pendant les périodes combinées antepartum et post-partum n'a pas été associée à un risque de récidive plus faible que l'héparine de bas poids moléculaire à faible dose fixe . Ces résultats indiquent que l'héparine de bas poids moléculaire à faible dose pour la thromboprophylaxie pendant la grossesse est la dose appropriée pour la prévention de la thromboembolie veineuse récurrente liée à la grossesse.







Commentaire
Une des présentations majeures de l'ISTH (@MiddeldorpS) et celle de Anne Godier ( @GodierAnne) sur un tout autre sujet .
Revenons à l'histoire naturelle de ma MTEV au cous de la grossesse et en post partum
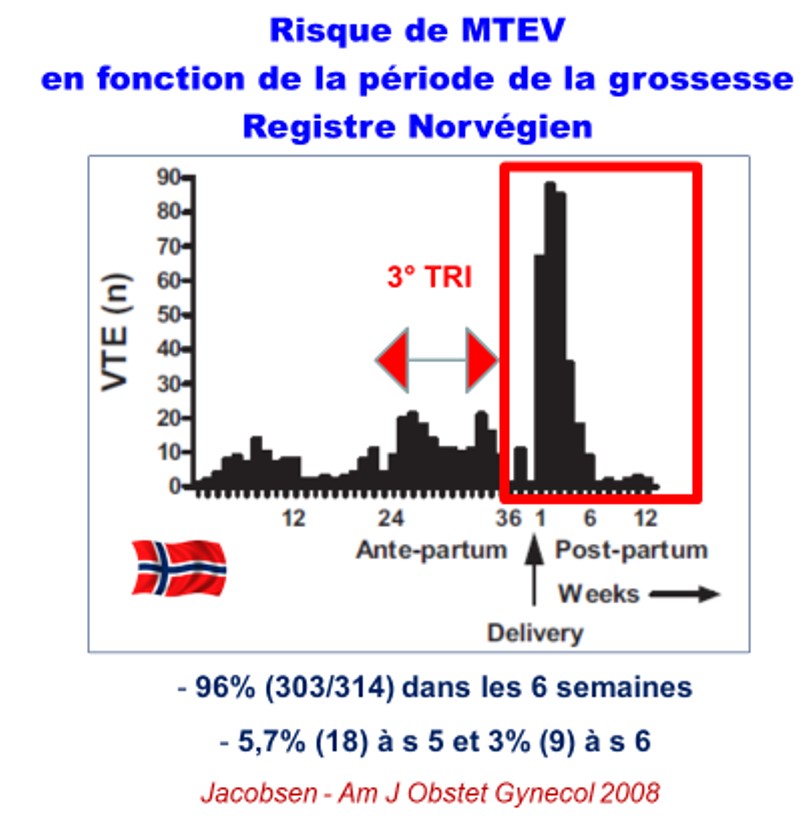
Revenons à l'histoire naturelle de ma MTEV au cous de la grossesse et en post partum

C'est le 3° trimeste qui à risque de MTEV et surtout le post partum, c'est un fait majeur.
Compte tenu du risque hémoragique et du bénéfice sur le risque de MTEV, cette étude ouvre la porte "au cas par cas" d'une prévention à dose intermédiaire dans le post partum.
Chez qui ?
Essentiellement des patientes à haut risque de MTEV de par leurs antécédents de MTEV personnels et ou familiaux, et leurs FDR MTEV et ce dans les cadre d'une RCP THROMBOSE.
A discuter surtout dans le post partum pour l'instant
Chez qui ?
Essentiellement des patientes à haut risque de MTEV de par leurs antécédents de MTEV personnels et ou familiaux, et leurs FDR MTEV et ce dans les cadre d'une RCP THROMBOSE.
A discuter surtout dans le post partum pour l'instant


