"L'IA n'est pas une béquille, mais un tremplin : elle augmente notre intelligence sans jamais la remplacer... enfin, du moins, je l'espère !" Sylvain Montmory
"Je pense, donc je suis encore un être de chair et de neurones." Sylvain Montmory
European Heart Journal - Digital Health, 2025;, ztaf057, https://doi.org/10.1093/ehjdh/ztaf057
https://academic.oup.com/ehjdh/advance-article/doi/10.1093/ehjdh/ztaf057/8158674
Article libre d'accès
L'intelligence artificielle (IA) appliquée à un électrocardiogramme monodérivation (ECG-IA) permet de détecter une dysfonction systolique ventriculaire gauche altérée [DSVG : fraction d'éjection ventriculaire gauche (FEVG) ≤ 40 %].
Cette étude visait à déterminer si l'ECG-IA permet également de prédire le risque à deux ans d'événements cardiovasculaires majeurs (MACI) et de mortalité toutes causes confondues, indépendamment de la DSVG.
Les résultats cliniques après un suivi de deux ans ont été recueillis chez les patients qui se sont présentés pour une échocardiographie de routine et ont bénéficié d'un enregistrement simultané d'ECG à une seule dérivation pour l'analyse de l'ECG-AI.
Les MACE et la mortalité toutes causes confondues ont été comparés par régression de Cox, mesurée par rapport à la classification de la FEVG ≤ ou ≤ 40 %. Une analyse de sous-groupe a été réalisée sur les patients avec une FEVG échocardiographique ≥ 50 %. Avec des seuils précédemment établis, un ECG-AI « positif » a été défini comme une FEVG prédite ≤ 40 %, et un ECG-AI négatif signifiait une FEVG prédite > 40 % ; 1007 patients ont été inclus pour l'analyse (âge moyen, 62,3 ans ; 52,4 % d'hommes). 339 (33,7 %) avaient une FEVG prédite par l'ECG-AI ≤ 40 % et avaient un taux de MACE plus élevé (FEVG ≤ 40 % contre > 40 % : 34,2 % contre 11,9 % ; rapport de risque ajusté (aHR) 1,93 ; IC à 95 %, 1,39–2,69 ; P < 0,001), principalement dû à une mortalité accrue (23 % contre 9,6 % ; P < 0,001 ; aHR 1,56 ; IC à 95 %, 1,06–2,29 ; P = 0,0239). Chez les patients présentant une FEVG échocardiographique ≥ 50 %, il y avait une incidence plus élevée de MACE chez ceux ayant une prédiction « faussement positive » de FEVG ≤ 40 % à l'ECG-AI (27,2 % contre 11,9 % ; P < 0,001 ; aHR 1,71 et IC à 95 %, 1,11–2,47) et de mortalité toutes causes confondues (20,4 % contre 9,6 % ; P < 0,001 ; aHR 1,59, IC à 95 %, 1,09–2,42).
Cette étude a plusieurs implications cliniques.
Premièrement, des outils de prédiction d'ECG IA améliorés sont désormais accessibles grâce à la technologie ECG monodérivation (comme celle actuellement déployée à grande échelle dans les soins cliniques de routine au sein du NHS, NCT05987670). Ces outils offrent la possibilité d'améliorer la stratification du risque, en particulier dans les milieux de proximité ou à ressources limitées où l'accès aux ECG multidérivations ou à l'échocardiographie peut être limité. En identifiant les patients à haut risque d'accident vasculaire cérébral majeur (MACI) ou de mortalité toutes causes confondues, l'ECG IA monodérivation peut contribuer à orienter les investigations diagnostiques ultérieures, comme la priorisation de l'échocardiographie ou l'orientation vers un spécialiste. Cela souligne le potentiel de l'ECG IA comme outil complémentaire de stratification du risque.
Deuxièmement, avec l'augmentation de la préférence pour les technologies grand public/portables pour l'ECG monodérivation, cela pourrait permettre aux patients de jouer un rôle actif dans la gestion de leur santé et conduire à une meilleure détection précoce des problèmes cardiaques, à une meilleure prise en charge des maladies chroniques et à une augmentation de la satisfaction et de la confiance des patients.
Troisièmement, le score de probabilité met en évidence les informations utiles que peuvent apporter les modèles d'ECG-IA au-delà de leur objectif intrinsèque. Ces scores peuvent aider à stratifier les patients sur un continuum de risque, permettant potentiellement des stratégies de suivi personnalisées.
Quatrièmement, nos résultats soulignent le potentiel de l'ECG-IA pour compléter les outils diagnostiques existants plutôt que de les remplacer. Dans les cas où une échographie a déjà été réalisée, l'ECG monodérivation offre une dimension supplémentaire de stratification du risque. L'ECG-IA capture de subtiles modifications morphologiques et temporelles de l'activité électrique du cœur, qui peuvent ne pas être directement corrélées aux paramètres échocardiographiques traditionnels. L'ECG-IA a également démontré une valeur pronostique significative, même chez les patients présentant une FEVG préservée, en identifiant des risques que la FEVG échocardiographique seule peut ne pas détecter.
Notamment, les FC plus élevées observées avec l'ECG-IA par rapport à la FEVG échocardiographique suggèrent une association plus étroite avec les effets indésirables.
Cependant, il est important de noter que cette comparaison était limitée à la FEVG, une mesure échocardiographique unique couramment utilisée concrètement clinique. Bien que nos résultats suggèrent que l’ECG-AI peut détecter des risques qui peuvent ne pas être entièrement capturés par la FEVG échocardiographique, c’est-à-dire chez les patients avec une FEVG préservée, d’autres paramètres échocardiographiques, tels que les dimensions de la chambre et la fonction valvulaire, contribuent également à la stratification des risques et sont associés à des résultats indésirables. Ce rôle complémentaire souligne l'intérêt de l'IA-ECG comme outil de dépistage rentable et évolutif, susceptible de rationaliser l'allocation des ressources de santé en identifiant les patients qui bénéficieraient le plus d'un repos ou d'une intervention supplémentaires. L'évolution évidente de ces travaux s'oriente vers un algorithme d'IA spécifiquement entraîné à l'identification des MACE et de la mortalité toutes causes confondues à l'aide d'un ECG monodérivation. Leurs performances devraient naturellement être supérieures à celles obtenues avec l'algorithme d'IA-ECG entraîné pour une FEVG ≤ 40 %.
L'association de l'IA-ECG avec une incidence plus élevée de MACE et de mortalité toutes causes confondues serait naturellement attendue étant donné la forte corrélation avec une fraction d'éjection réduite de 40 % ou moins, un prédicteur de renom de décès cardiovasculaire.
La capacité d'identifier un MACE dans une FEVG > 50 % est probablement liée à une maladie, cardiovasculaire (par exemple, ischémie ou anomalies du rythme) ou autre, qui affecte la morphologie de l'ECG et a eu un impact sur les résultats de l'IA-ECG. Pour la mortalité toutes causes confondues, cela reflète probablement le fait que le résultat de l'IA-ECG est influencé par des schémas ECG qui peuvent signifier un stress myocardique précoce, un remodelage électrique ou un dysfonctionnement cardiaque latent. Cette observation concorde avec les résultats d'autres études qui ont tenté de décrire les caractéristiques ECG qui informent le plus les résultats du modèle IA-ECG. Grâce à des méthodes d'interprétabilité telles que la cartographie de saillance et la cartographie d'activation de classe pondérée par gradient, ces études ont démontré que les modèles d'ECG-IA s'appuient souvent fortement sur des caractéristiques telles que la morphologie du complexe QRS ou les propriétés de l'onde T, pour prédire les résultats cardiovasculaires. Il est important de noter que ces relations ne sont pas linéaires ; elles représentent plutôt des interactions complexes et multidimensionnelles qui dépassent l'interprétation clinique conventionnelle. Cela suggère que des caractéristiques morphologiques beaucoup plus subtiles, dépassant la capacité de détection du cerveau humain, sont en jeu. De plus, d'autres études ont suggéré que l'ECG-IA peut potentiellement identifier un dysfonctionnement cardiaque subtil, difficilement observable à l'échocardiographie. Des études antérieures, en effet, ont montré que l'ECG-IA était associé à un risque quatre fois plus élevé de développer un dysfonctionnement ventriculaire.
En fin de compte, les avantages cliniques potentiels de cette technologie pourraient l'emporter sur les inquiétudes concernant le manque d'explicabilité, bien que les méthodes pour ce faire continuent d'évoluer.
Un algorithme d'ECG IA conçu pour détecter une FEVG ≤ 40 % permet également d'identifier les patients à risque d'accident vasculaire cérébral majeur (MACI) et de mortalité toutes causes confondues à partir d'un enregistrement ECG monodérivation, indépendamment de la FEVG réelle à l'écho. Cet outil de stratification du risque au point d'intervention nécessite une évaluation plus approfondie.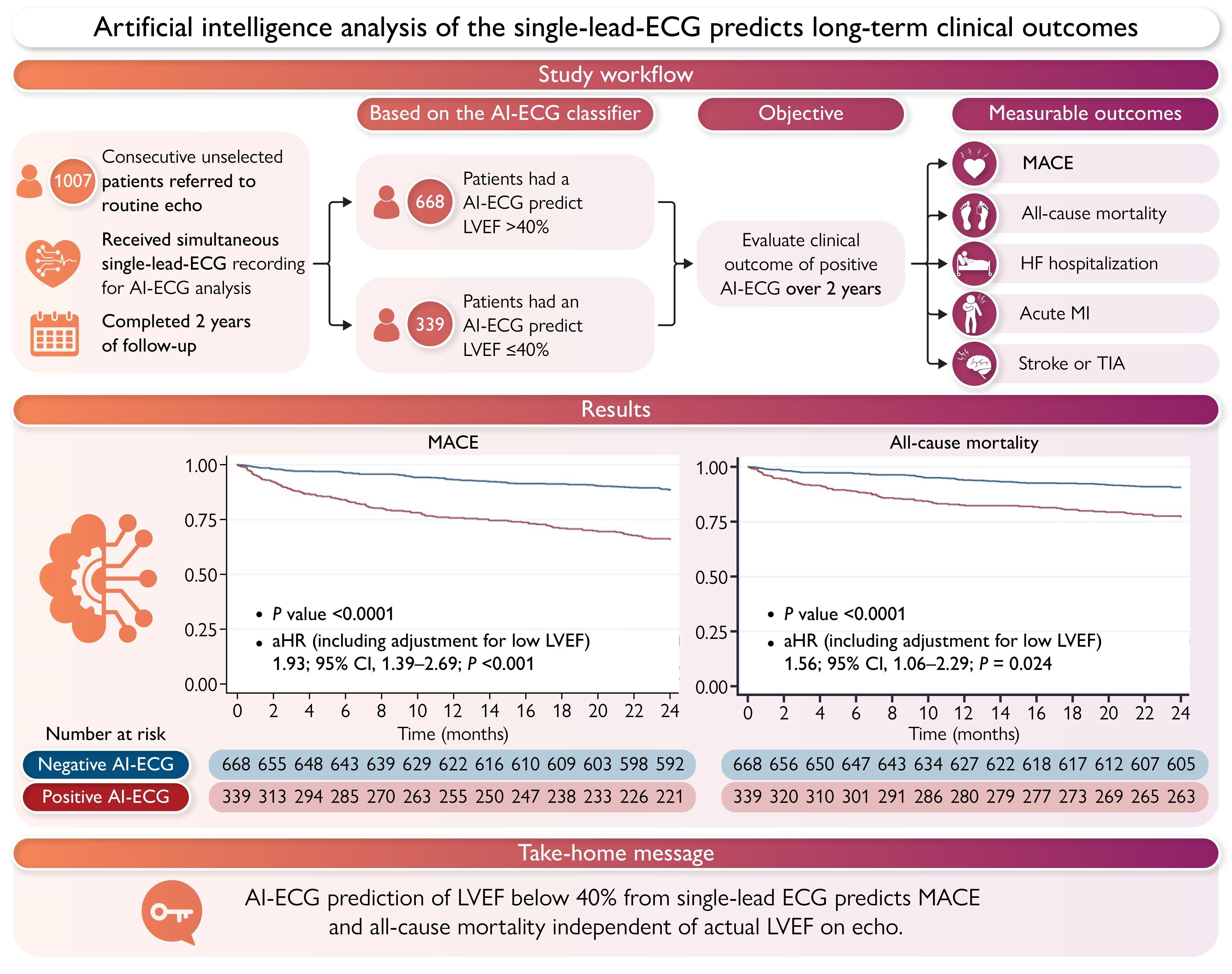
Décryptage de l’article : « Artificial intelligence analysis of the single-lead ECG predicts long-term clinical outcomes » par PERPLEXITY.IA
Résumé de l’étude
L’article examine l’utilisation de l’intelligence artificielle (IA) appliquée à l’ECG monocanal (single-lead ECG) pour prédire les risques à long terme d’événements cardiovasculaires majeurs (MACE) et de mortalité toutes causes confondues, indépendamment de la fraction d’éjection du ventricule gauche (LVEF).
Principaux résultats
-
L’IA appliquée à l’ECG monocanal permet de détecter une dysfonction systolique ventriculaire gauche (LVEF ≤ 40 %).
-
Sur 1007 patients analysés (âge moyen 62,3 ans), ceux dont l’IA-ECG prédisait une LVEF ≤ 40 % présentaient un taux plus élevé de MACE (34,2 % vs 11,9 %) et une augmentation du risque ajusté (HR ajusté )
-
L’IA-ECG a montré une valeur pronostique significative même chez les patients avec une LVEF préservée (≥ 50 %), identifiant des risques non capturés par l’échocardiographie seule
-
L’IA-ECG capture des modifications subtiles de l’activité électrique cardiaque, offrant une dimension supplémentaire à la stratification du risque par rapport aux mesures échocardiographiques traditionnelles.
Implications cliniques
-
Outil de dépistage : l’IA-ECG monocanal, accessible via des dispositifs portables ou connectés, peut servir de méthode de dépistage de masse, notamment dans les contextes communautaires ou à ressources limitées, où l’accès à l’échocardiographie est restreint.
-
Stratification du risque : L’IA-ECG permet d’identifier les patients à haut risque, facilitant la priorisation des examens complémentaires (échocardiographie, avis spécialisé).
-
Complémentarité : L’IA-ECG ne remplace pas l’échocardiographie mais la complète, en apportant des informations pronostiques additionnelles, notamment chez les patients avec une LVEF normale
-
Autonomisation du patient : L’essor des dispositifs de santé connectés favorise l’autosurveillance et une détection plus précoce des troubles cardiaques.
Perspectives et limites
-
L’algorithme IA utilisé était initialement entraîné pour détecter une LVEF ≤ 40 % et non directement pour prédire les MACE ou la mortalité ; des modèles spécifiquement entraînés pour ces issues pourraient améliorer la performance.
-
L’IA-ECG apparaît comme un biomarqueur digital non-invasif, prometteur pour la prévention et la gestion personnalisée du risque cardiovasculaire, mais nécessite des validations complémentaires avant une adoption généralisée15.
Conclusion
L’analyse IA de l’ECG monocanal offre une nouvelle approche pour la prédiction du risque cardiovasculaire à long terme, avec un potentiel d’application large grâce à la simplicité et l’accessibilité de la technologie. Elle permet de détecter des patients à risque élevé, même en l’absence de dysfonction cardiaque apparente à l’échocardiographie, et pourrait transformer les stratégies de dépistage et de prévention cardiovasculaire.
SYNTHESE
Ce texte, tiré du European Heart Journal — Digital Health, examine comment l'intelligence artificielle (IA) analysant un électrocardiogramme (ECG) à une seule dérivation peut prévoir les résultats cliniques à long terme. Plus précisément, il évalue si une IA conçue pour détecter une fraction d'éjection ventriculaire gauche (FEVG) faible (≤ 40 %) peut également prédire des événements cardiovasculaires majeurs (MACE) et la mortalité toutes causes confondues sur deux ans. Cela est-il valable même chez les patients dont la FEVG est préservée ? ? L'étude conclut que l'IA-ECG est un outil de stratification des risques indépendant, potentiellement utile au-delà de sa fonction initiale de détection de la FEVG. Ces découvertes suggérèrent l'opportunité d'utiliser l'IA-ECG comme un instrument de dépistage généralisé, susceptible d'améliorer la priorisation des soins et la gestion des patients. (NotebooKLM)
Commentaire
L'IA-ECG va-t-elle faire disparaître le score calcique coronarien et autres score de prévention CV ?

