“Le plus grand secret de la réussite, c'est de se fixer un but et de ne le perdre jamais de vue.” Christine de Suède,
Advancements in Noncontrast Ultrasound Imaging for Low-Velocity Flow: A Technical Review and Clinical Applications in Vascular Medicine,
Progrès en imagerie ultrasonore sans contraste pour les flux à faible vitesse : revue technique et applications cliniques en médecine vasculaire
Seddiki R, Mirault T, Sitruk J, Mohamedi N, Messas E, Pernot M, Baranger J, Goudot G. HEGP, INSERM U070, INSERM U1273, Paris, Ultrasound Med Biol 2025 ;10 :38 (https://doi.org/10.1016/j.ultrasmedbio.2025.03.001)https://www.sciencedirect.com/science/article/pii/S0301562925000699
Analyse et décryptage par :

Professeur Michel Dauzat
Professeur émérite - Université de Montpellier - UFR de Médecine de Montpellier-Nîmes
couleur permettent de visualiser des flux sur des artères de plus de 0,3 mm de diamètre
avec des vitesses circulatoires de plus de 5 cm/s.
Les auteurs ont ainsi identifié 7 techniques distinctes :
* BFlow TM (General Electric),
- Advanced Dynamic Flow TM (ADF, Canon),
- * Micro-Flow Imaging TM (MFI, Philips),
- * MV-Flow TM (Samsung),
- * Micro-V TM (Esaote),
- * E-Flow TM (Hitachi),
* AngioPLUS TM (Supersonic Imagine).
L’une des plus anciennes et plus singulières approches est le mode BFlow TM , fondé sur l’émission d’une impulsion codée de longue durée, ce qui permet d’améliorer le rapport signal/bruit tout en maintenant une très fine résolution spatiale grâce à l’identification, par autocorrélation, du code sur les échos obtenus en réception.
Les signaux provenant de cibles fixes s’annulent et ne sont ainsi visualisés que les signaux renvoyés par des cibles mobiles. Il s’agit donc d’une méthode d’imagerie échographique et non Doppler.
Les techniques fondées sur l’effet Doppler se heurtent en effet à une difficulté majeure pour la détection des flux très lents : il est très difficile de séparer par simple filtrage les signaux provenant de cibles fixes ou des mouvements lents (comme les parois vasculaires) des signaux provenant de flux sanguins très lents, générant des fréquences Doppler basses très proches. Il est en revanche possible de les différencier en observant la cohérence spatio- temporelle des signaux : cette cohérence reste élevée lorsque les signaux proviennent de tissus solides, dont la structure interne ne varie pas lors de leur déplacement, contrairement aux éléments figurés du sang circulant qui, lors de l’écoulement, se déplacent aussi les uns par rapport aux autres. Cette approche implique cependant une très haute cadence d’imagerie, qui n’est pas possible avec les modalités conventionnelles d’imagerie échographique reposant sur l’émission d’un faisceau ultrasonore focalisé, donc sur un balayage ligne par ligne du plan examiné, ce qui limite le nombre d’images pouvant être construites chaque seconde.
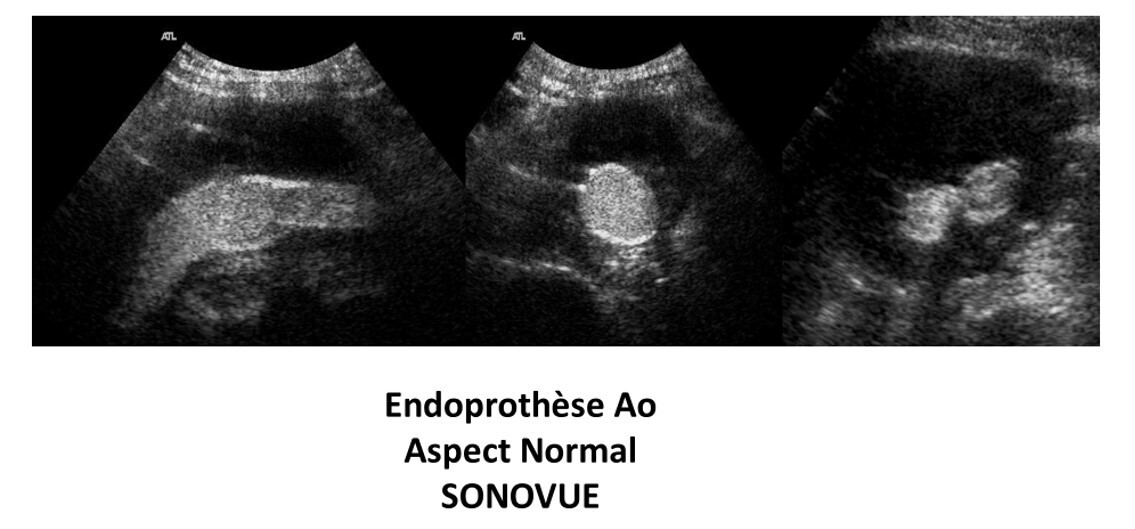
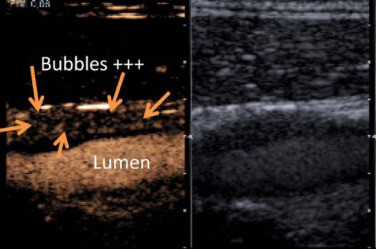
dominées par leur détection de sang hors de la lumière vasculaire normale (notamment
pour les fuites sur endoprothèse, bien que le mode SMI™ ait aussi montré des résultats
remarquables à cet égard). En d’autres termes, le rôle essentiel des produits de contraste n’est pas de rendre visible des flux sanguins simplement en améliorant le rapport signal / bruit ou en abaissant le seuil de vitesse circulatoire détectable, car l’association de l’effet Doppler et de ces nouvelles techniques d’imagerie des flux apporte des progrès considérables dans ce domaine.
ICONOGRAPHIE
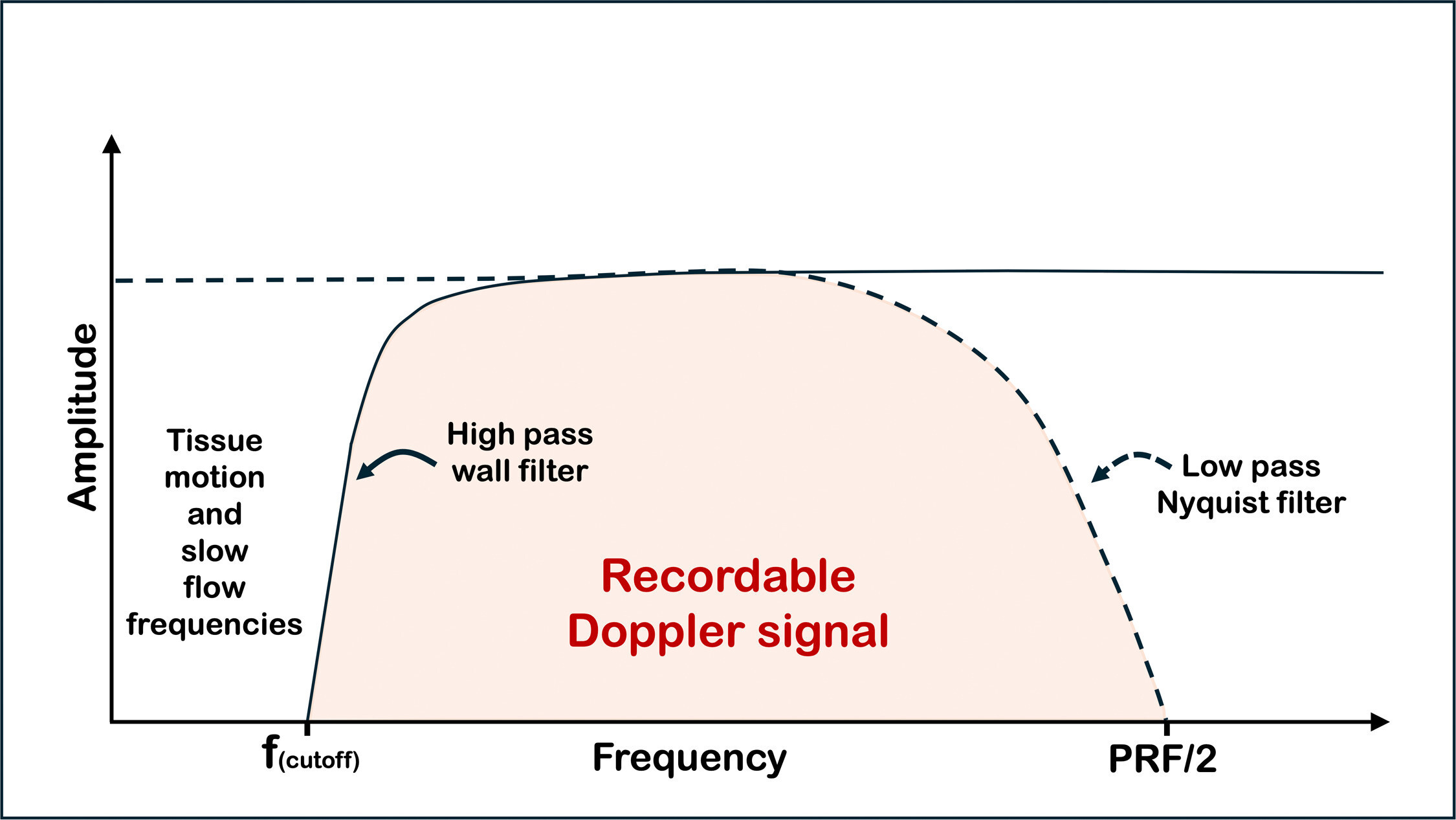
Représentation de la fréquence détectée par Doppler et du filtre passe-bas de Nyquist avec une fréquence de coupure de fréquence de répétition d'impulsion (PRF)/2 et un filtre passe-haut mural avec une coupure sélectionnable par l'utilisateur. (Adapté de Szabo TL. Doppler Modes)
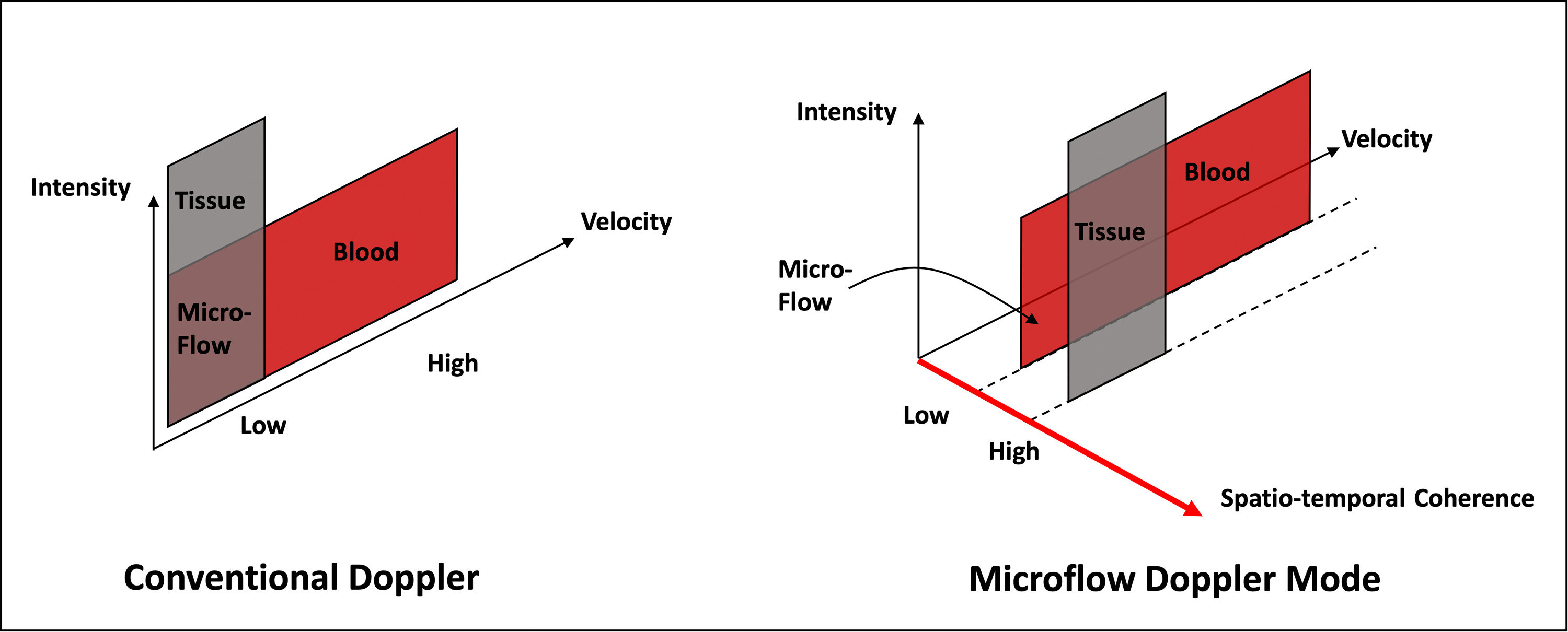
Schéma explicatif généralement proposé par les entreprises pour mettre en évidence les modes d'imagerie des flux micro vasculaires (MVFI) : le Doppler conventionnel (modes Doppler couleur et Doppler de puissance), présenté en A, est limité dans la visualisation des flux lents en raison de filtres conçus pour réduire le bruit lié aux mouvements des tissus. Grâce à des fréquences d'images plus élevées et à des filtres optimisés, les modes MVFI améliorent la distinction entre flux et tissu grâce à une meilleure cohérence spatio-temporelle.
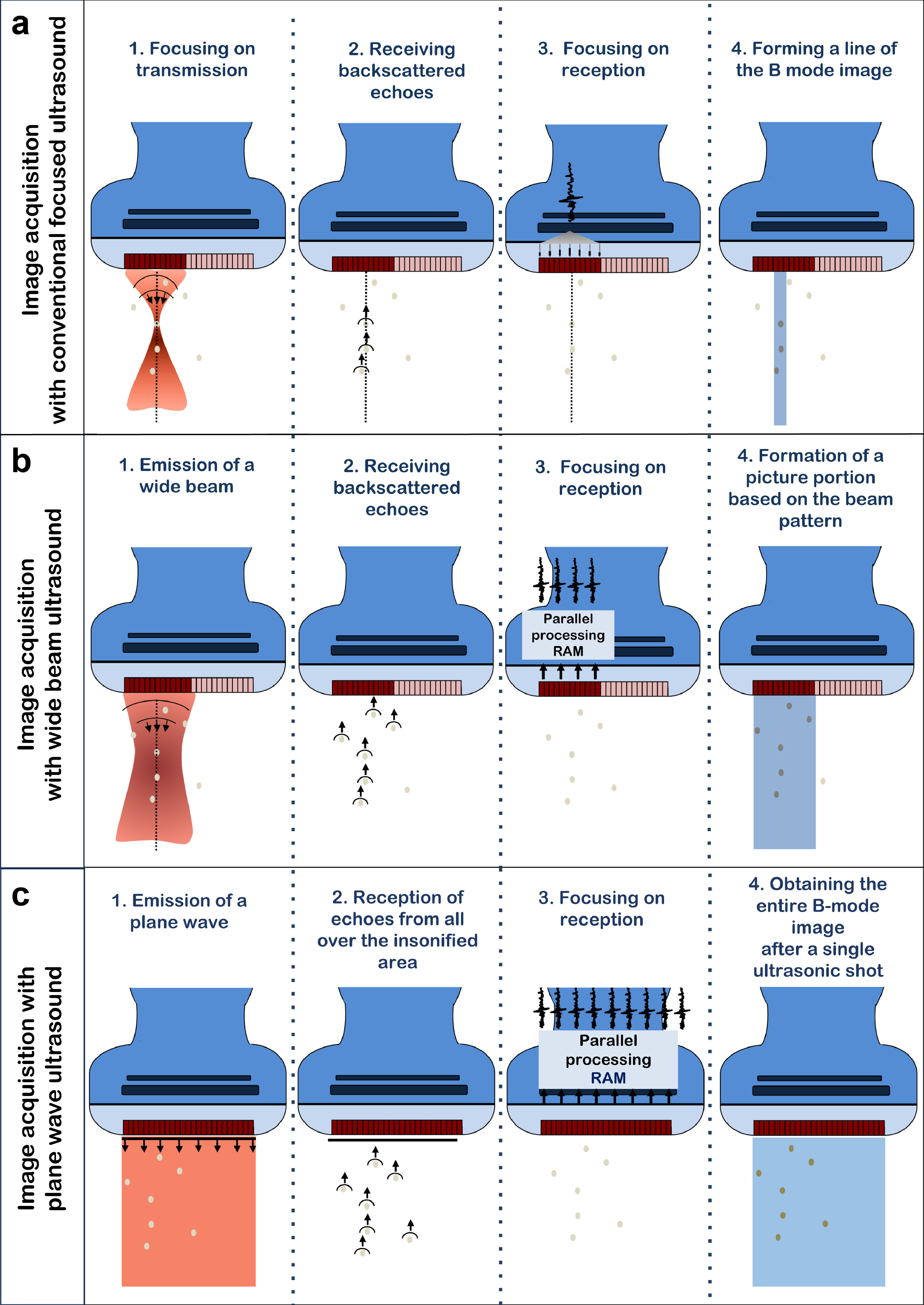
Différences techniques entre l'échographie conventionnelle utilisant des ultrasons focalisés (a), où la fréquence d'images est limitée par la nécessité d'une transmission-réception d'ultrasons répétée ligne par ligne pour former une image complète en mode B, et les possibilités de fréquence d'images améliorées permises par les technologies à faisceau large (b) et à ondes planes (c), où une acquisition de champ d'image (b) ou d'une image complète (c) est rendue possible par le traitement parallèle des échos retransmis.
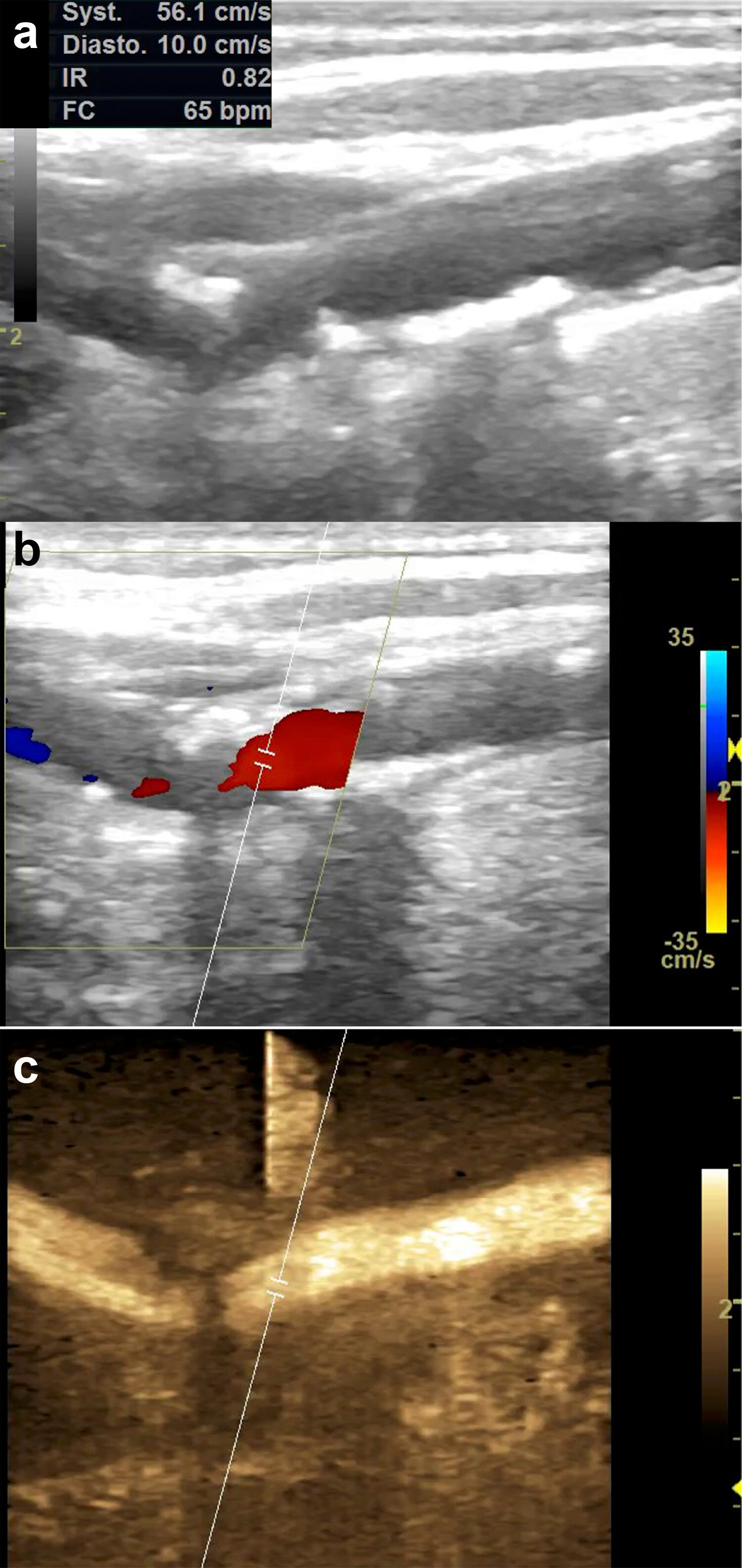
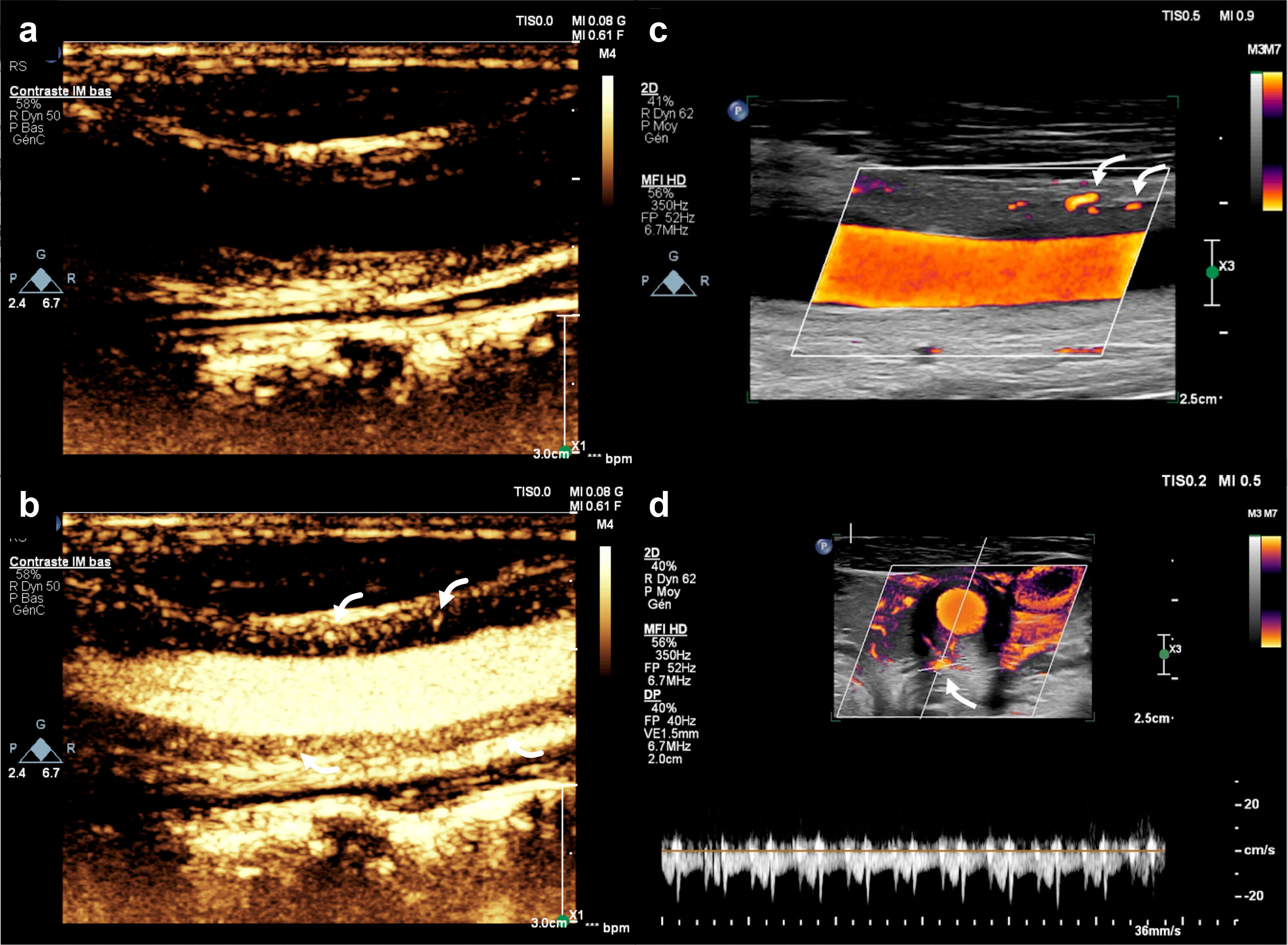
Visualisation d'une bifurcation carotidienne par échographie en mode B (a), Doppler couleur (b) et mode B-flow™ (c). L'avantage du mode B-flow ™ illustré ici est la large zone d'évaluation, correspondant à l'intégralité du champ d'exploration permis par la sonde, avec une meilleure continuité du flux carotidien malgré les artéfacts liés aux calcifications artérielles.
SYNTHESE
"Ce document examine les progrès récents de l'échographie sans contraste pour visualiser le flux sanguin à basse vitesse, en particulier dans la microcirculation et les petits vaisseaux qui échappent aux modes Doppler conventionnels. Il décrit les nouvelles techniques d'imagerie développées par divers fabricants pour surmonter les limites des méthodes antérieures, en se concentrant sur l'amélioration de la détection du flux sanguin grâce à des fréquences d'images plus élevées et des filtres de traitement du signal avancés. Le texte aborde ensuite diverses applications cliniques de ces modes micro vasculaires améliorés, notamment dans l'évaluation des maladies vasculaires, la caractérisation des plaques artérielles et la visualisation de la perfusion des organes et de la néo vascularisation tumorale, tout en reconnaissant certaines limites actuelles." (NotebooKLM)
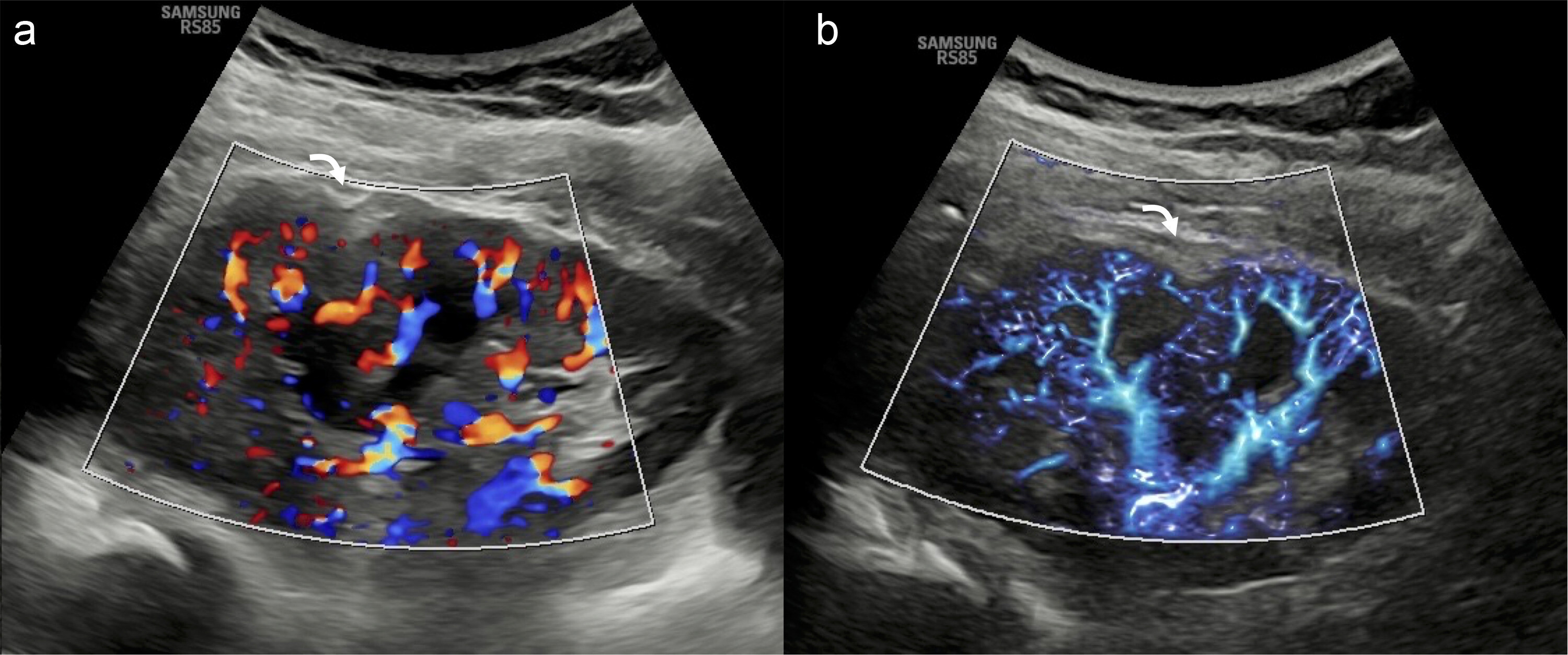
ICONOGRAPHIE personnelle et autres : FUJIFILM Puissance /eFLOW MC / DFI MC
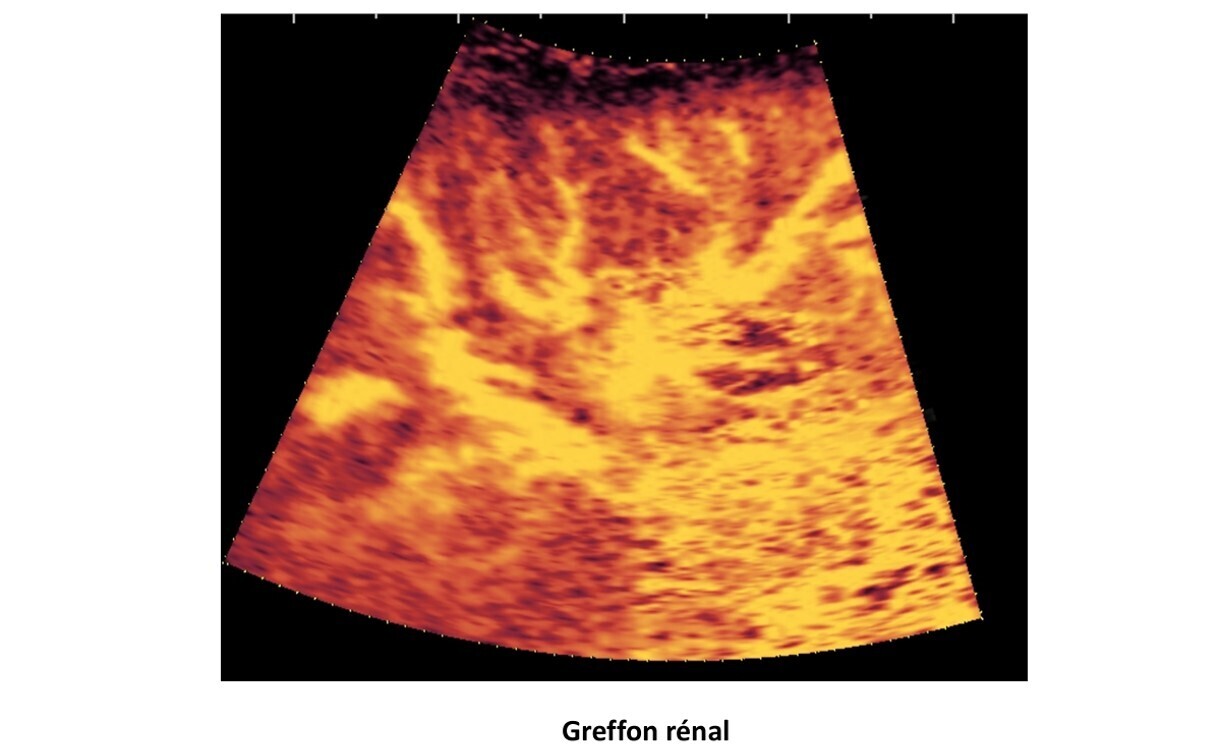
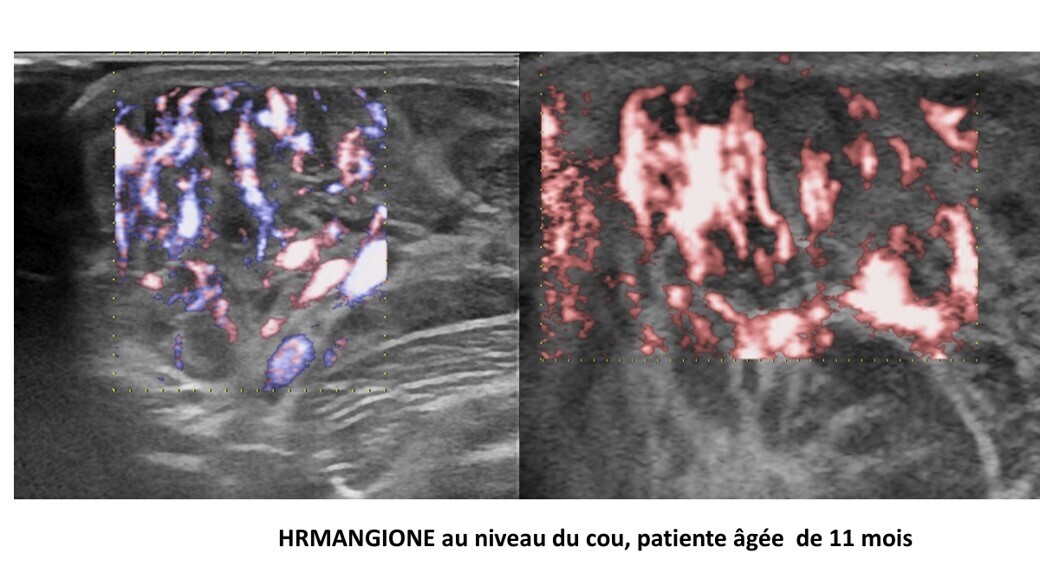
 Doc J.-M. Baud, F. Becker, A. Maurizot, F. Pico, L’échographie avec contraste peut montrer des lésions carotidiennes symptomatiques non visualisées en angio-RM, Journal des Maladies Vasculaires, Volume 38, Issue 6, 2013,
Doc J.-M. Baud, F. Becker, A. Maurizot, F. Pico, L’échographie avec contraste peut montrer des lésions carotidiennes symptomatiques non visualisées en angio-RM, Journal des Maladies Vasculaires, Volume 38, Issue 6, 2013,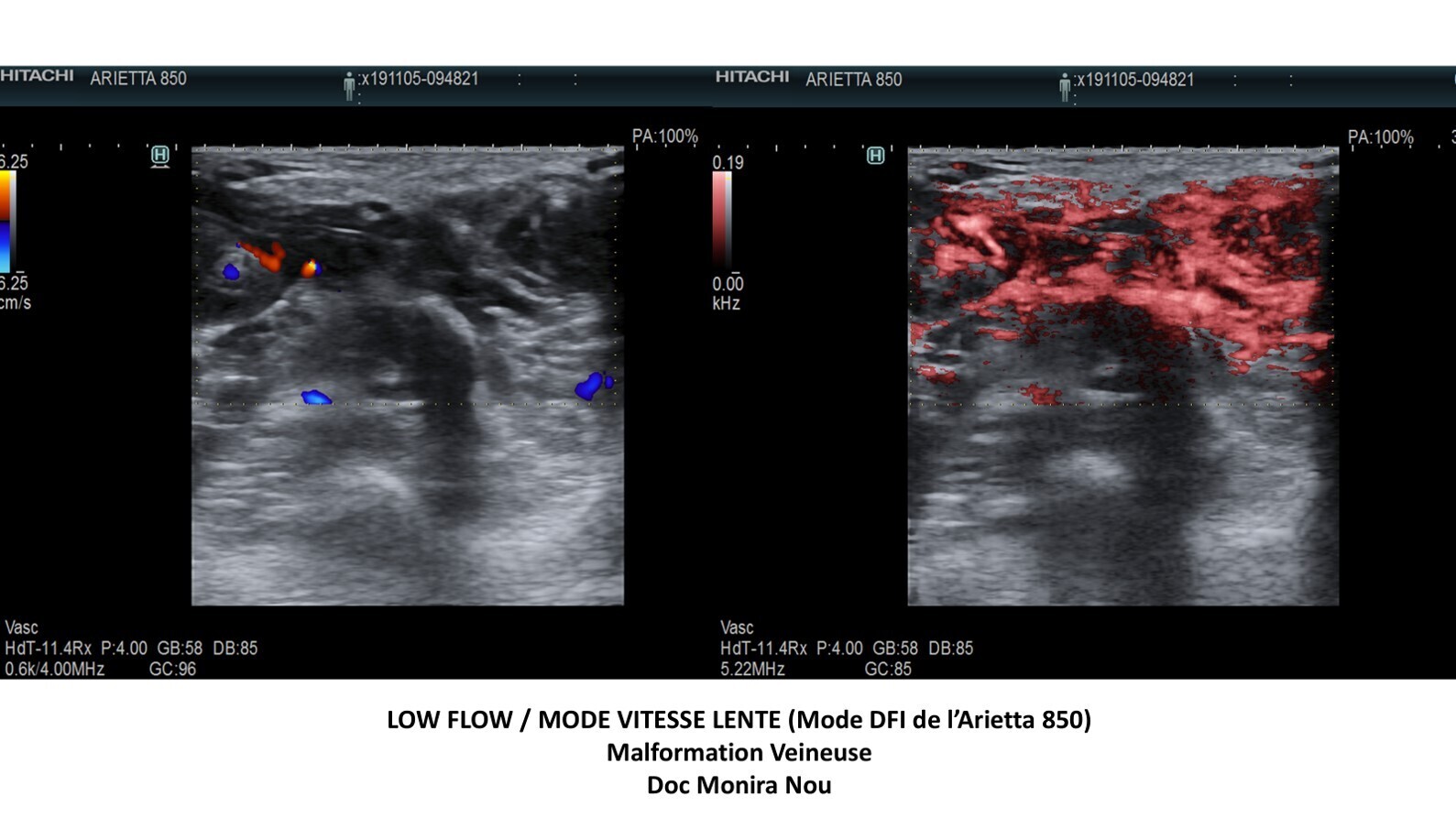 Mon utilisation du DFI
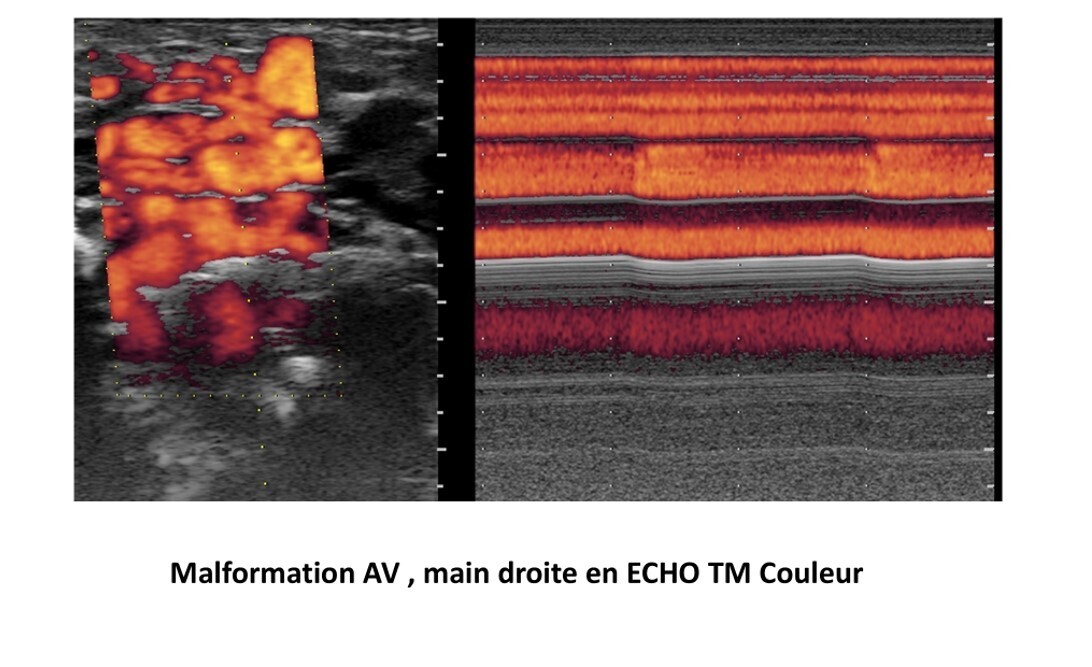
Mon utilisation du DFI1/ Les malformation veineuses
2/ Une interface plaque /carotide de meilleure qualité
3/ La vicariance en cas de collatérales de petits calibres
4/ Recherche de flux intra plaque mais avec difficulté ; problème de sonde je pense
5/ Les anfractuosités de la plaque carotidienne
5/ En de dissection artérielle
6/ Tumeur glomique de la bifurcation carotidienne
9/ Toutes atteintes artérielle périphérique de type inflammatoire
......... et au au cas par cas .........

Commentaire de PERPLEXITY/IA
Les techniques modernes d’imagerie de flux micro vasculaire (AngioPlus™, DFI™, MFI™, MicroV™, MV-Flow™, SMI™) sont conçues pour visualiser et analyser la micro vascularisation, c’est-à-dire les flux sanguins dans les plus petits vaisseaux, avec une sensibilité et une résolution bien supérieures à celles du Doppler conventionnel. Elles reposent sur des innovations majeures dans la manière dont les signaux ultrasonores sont émis, reçus et traités.
Contrairement à l’échographie classique, où l’émission des ultrasons est focalisée ligne par ligne (séquentielle), ces techniques utilisent une émission « plane » ou en « faisceau large » qui insonifie l’ensemble du champ d’exploration en une seule fois. Cela permet de recueillir simultanément les échos provenant de tous les points de la zone étudiée, à chaque émission. Les systèmes dotés d’une architecture logicielle et matérielle avancée, comme ceux de SuperSonic Imagine® (Aixplorer, MACH 20), peuvent ainsi acquérir des images jusqu’à 200 fois plus rapidement que les échographes classiques
Ce mode d’acquisition ultrarapide, dit « ultrafast », permet :
-
Une très haute cadence d’imagerie (nombre d’images par seconde très élevé)
-
L’analyse de la cohérence spatio-temporelle des signaux sur plusieurs images successives, ce qui distingue les mouvements des parois vasculaires (lents) de ceux du sang (rapides et pulsés)
-
La détection de flux très lents, souvent invisibles en Doppler standard, tout en supprimant efficacement les artefacts liés aux mouvements des tissus
Le traitement « en parallèle » des signaux reçus (échos) est rendu possible par la puissance de calcul des systèmes modernes et le nombre élevé de canaux d’acquisition. Cela permet :
-
D’exploiter la totalité des informations issues de chaque émission ultrasonore
-
D’appliquer des algorithmes sophistiqués pour séparer les signaux de flux sanguin des mouvements tissulaires (ce que fait par exemple le SMI™ de Toshiba ou l’Angio PL.U.S.™ de SuperSonic Imagine®)
-
De maintenir une excellente résolution spatiale et une très grande sensibilité aux faibles vitesses de flux
Sur certains appareils moins puissants (avec moins de canaux), il n’est pas possible d’analyser simultanément tous les signaux. L’émission se fait alors sans focalisation (faisceau large), ce qui permet néanmoins d’obtenir la cadence d’imagerie élevée nécessaire à l’analyse de la micro vascularisation, mais avec une sensibilité parfois moindre.
Ces techniques sont particulièrement utiles pour :
-
L’analyse fine de la vascularisation des ganglions (détection de vascularisation centrale vs périphérique, recherche de micro-métastases)
-
L’évaluation de la perfusion tumorale, des organes (foie, rein, prostate), et des tissus superficiels (thyroïde, sein)
-
Le suivi des pathologies inflammatoires ou vasculaires
| Nom de la technologie | Fabricant | Caractéristiques clés |
|---|---|---|
| AngioPlus™ | SuperSonic Imagine | Imagerie ultrafast, haute sensibilité, analyse micro vasculaire sans contraste |
| SMI™ | Toshiba (Canon Medical) | Algorithme Doppler avancé, séparation flux/mouvement, excellente résolution1 |
| MVI™ | GE Healthcare | Acquisition continue, haute sensibilité aux flux lents |
| MV-Flow™, MicroV™, DFI™ | Samsung, Esaote, Fujifilm | Approches similaires, basées sur l’émission plane et le traitement parallèle |
Conclusion
Les techniques d’imagerie de flux micro vasculaire modernes exploitent l’émission ultrasonore plane et le traitement parallèle des échos pour offrir une visualisation inégalée de la micro vascularisation.
Elles permettent de détecter des flux très lents et de très petits vaisseaux, ouvrant de nouvelles perspectives pour le diagnostic précoce et le suivi de nombreuses pathologies, en particulier en oncologie et en pathologie ganglionnaire
Commentaire : bravo Guillaume et à toute ton équipe, Guillaume Goudot notre référent ultrason/ IA-VASC
Merci Michel de tes commentaires judicieux et toujours dans la pertinence et le vrai
Copyright : Dr Jean Pierre Laroche/2025

