-
“Un cerveau plein de paresse est l’atelier du diable.” Proverbe Italien“La poésie est une maladie du cerveau.” Alfred de Vigny
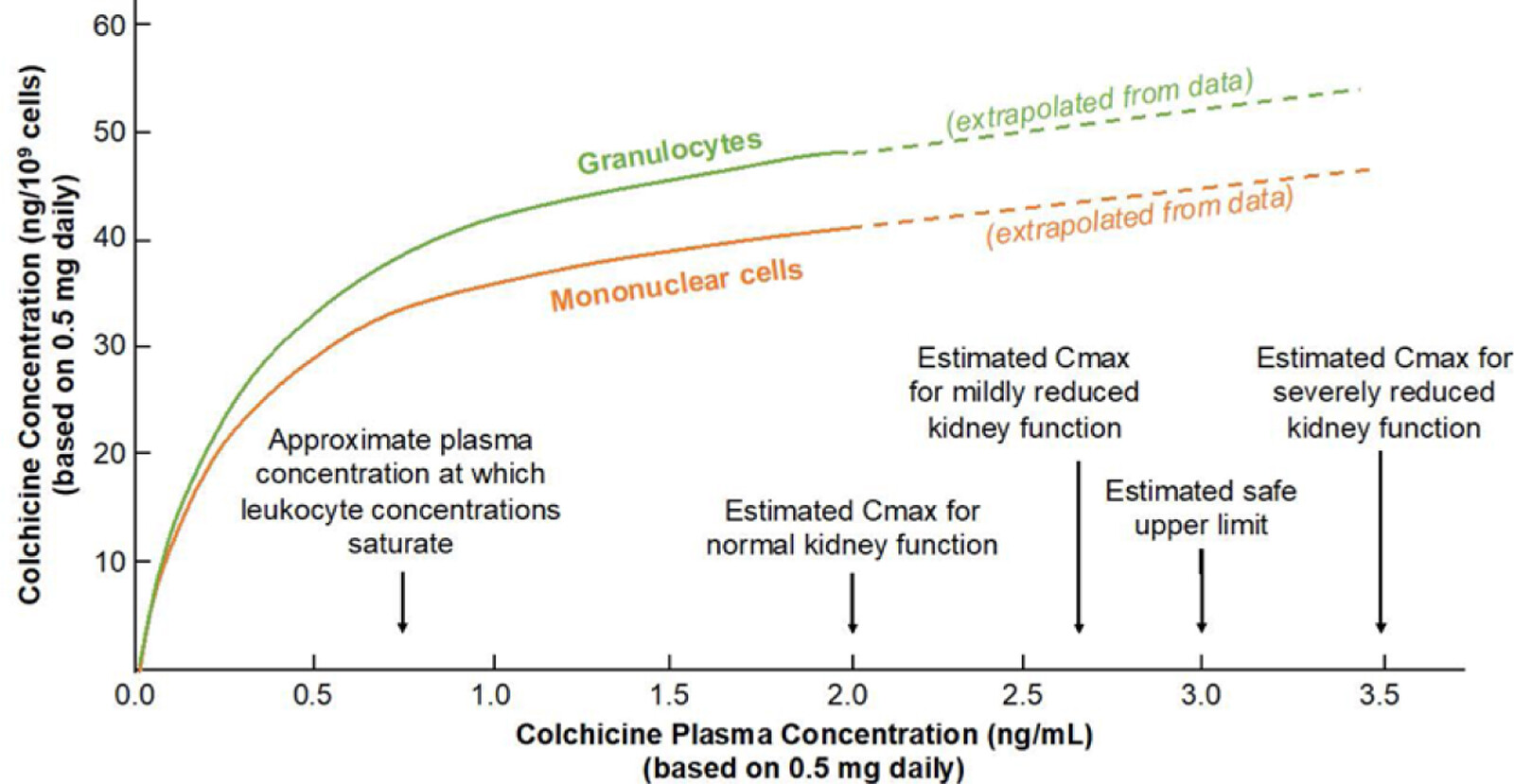
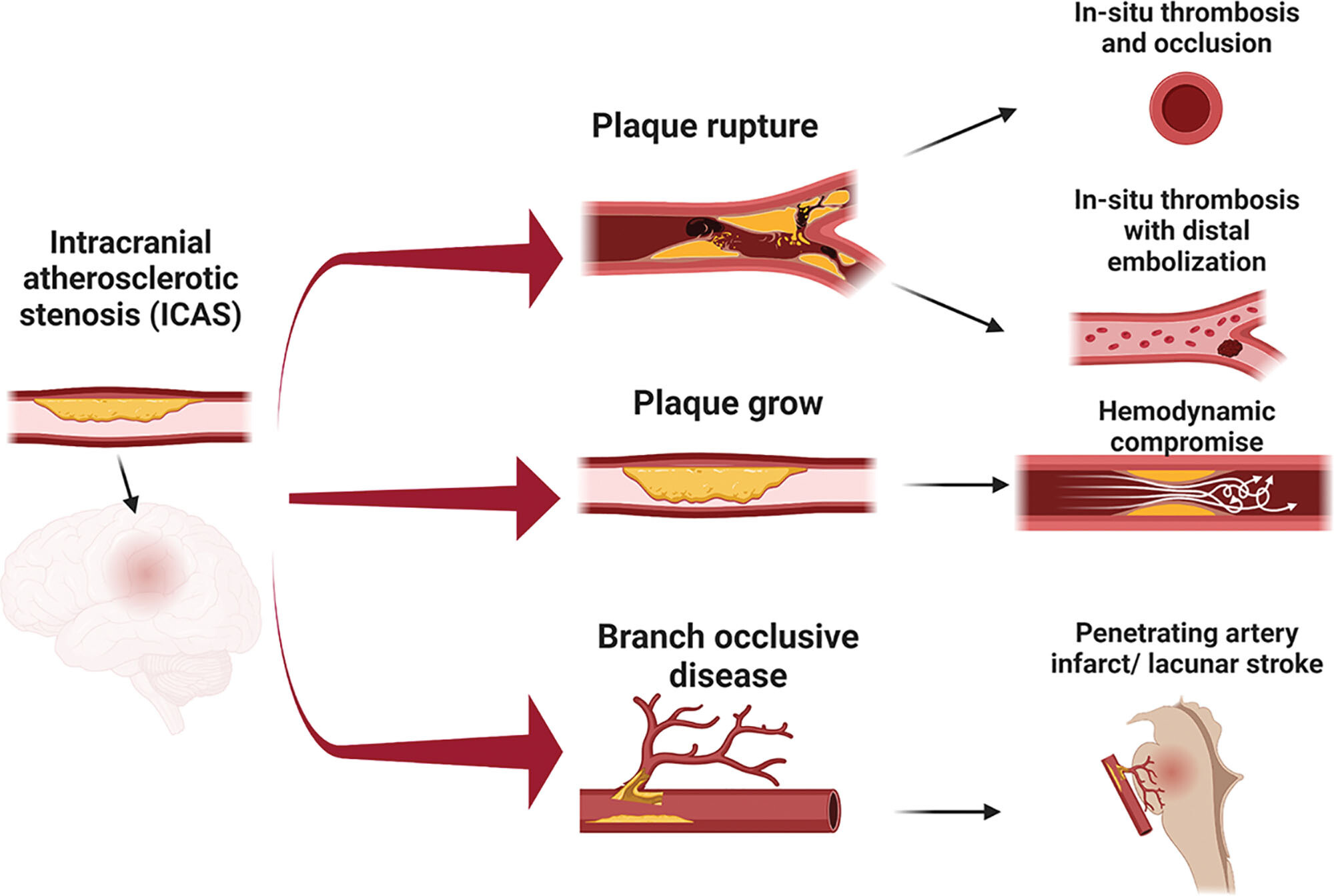
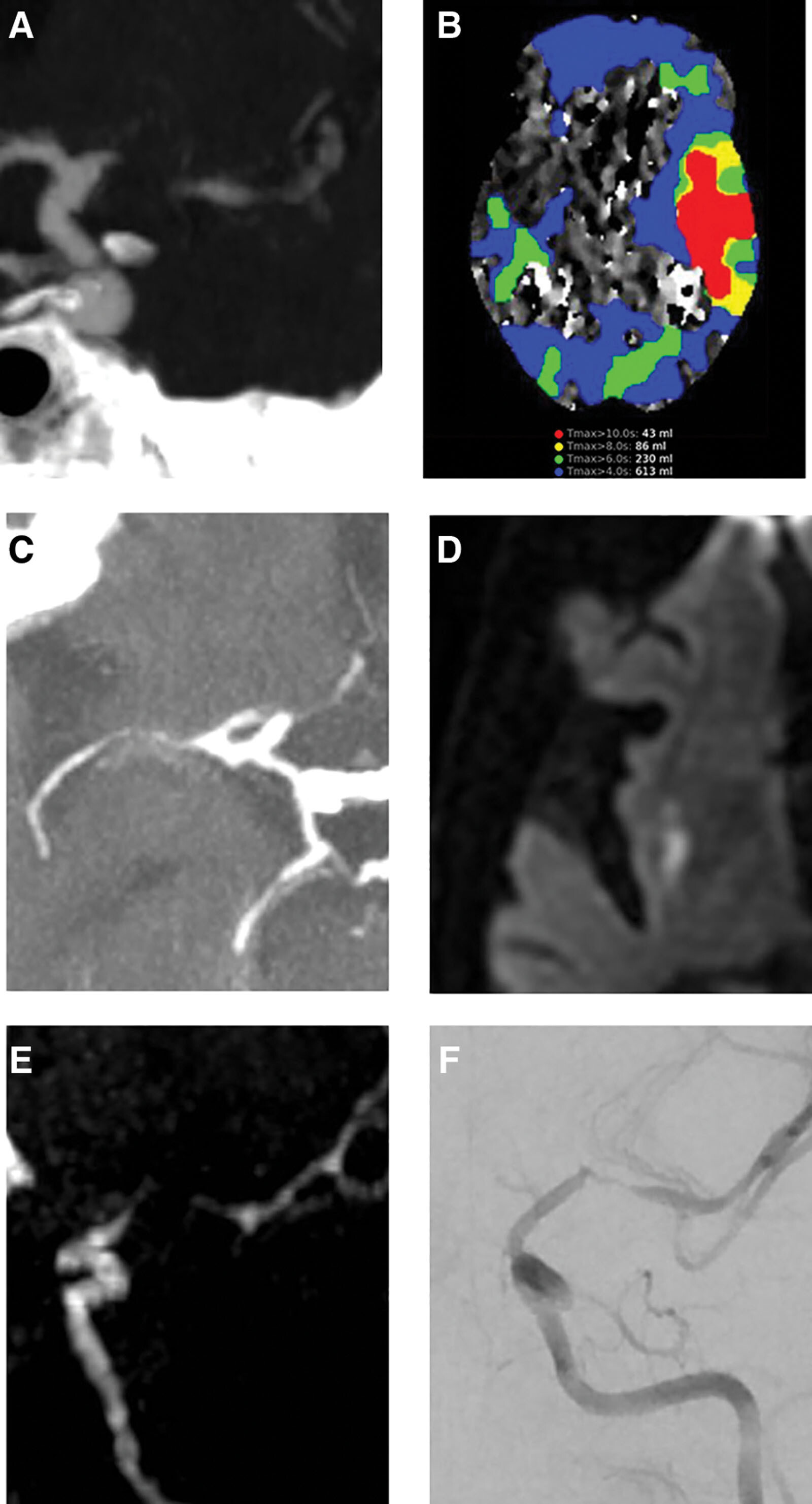
De : Chen : Stroke, Volume 55(2).Février 2024.311-323
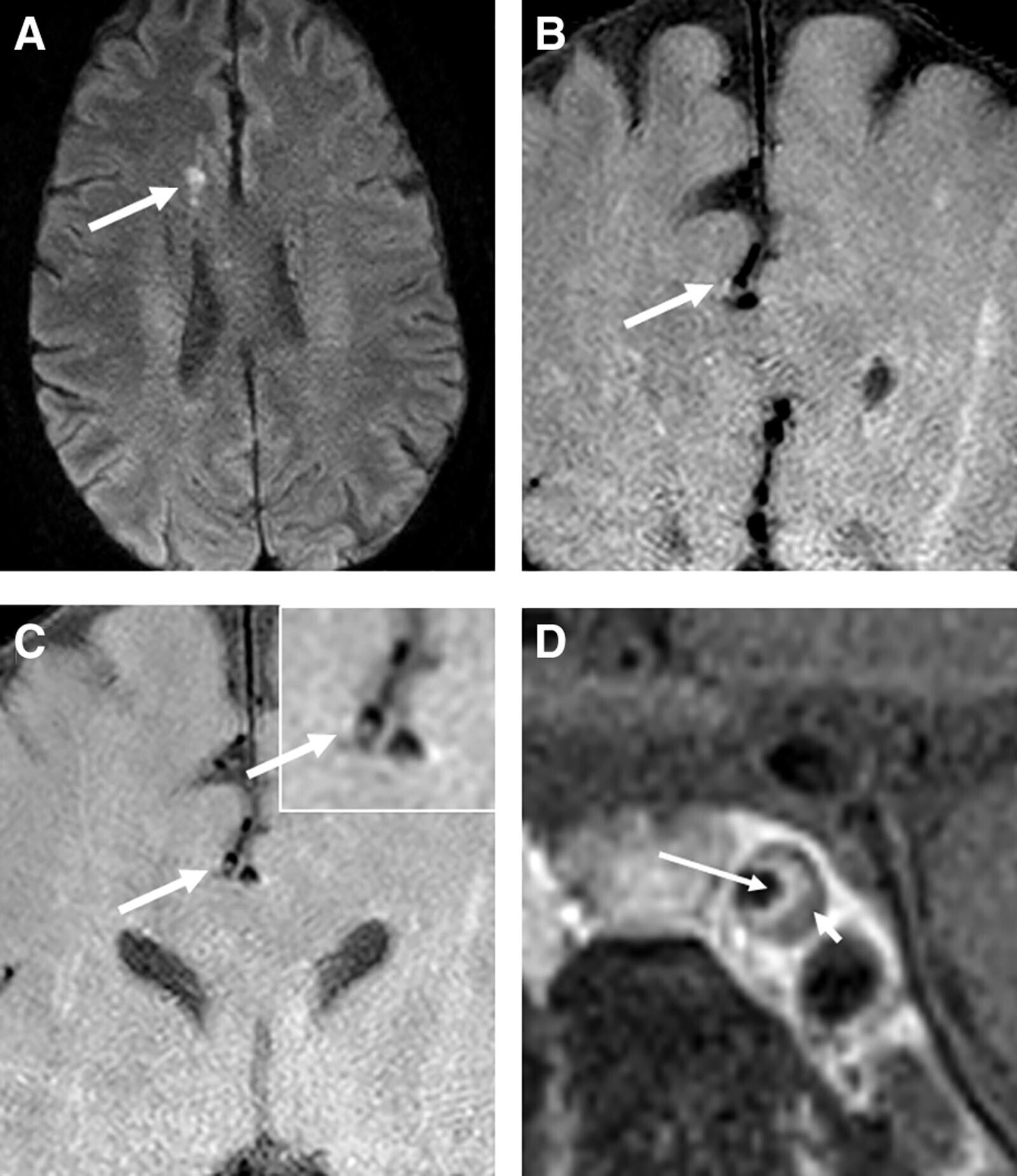
|
CONCLUSIONS
|
A LIRE
Recommandations canadiennes sténose carotidienne extra crânienne et sténoses intra crânienne , 2020
Sténose artérielle intracrânienne symptomatique
- Chez les patients ayant récemment subi un AVC ischémique ou un AIT lié à une sténose artérielle intracrânienne symptomatique de 70 à 99 %, un traitement médical est recommandé plutôt qu’une pose d’endoprothèse pour la prévention secondaire de l’AVC [niveau de preuve B].
- Remarque : Le protocole SAMMPRIS consistait en un traitement antiplaquettaire à double modalité de trois mois comprenant de l’acide acétylsalicylique et du clopidogrel (à l’exclusion des patients à haut risque d’hémorragie), suivi d’une monothérapie antiplaquettaire, puis d’un traitement hypolipidémiant intensif comprenant des doses élevées de statine, d’un traitement de la pression artérielle et d’une modification structurée du mode de vie, visant notamment l’abandon du tabagisme, l’activité physique et le régime alimentaire.
- Pour ce qui est des patients qui ont suivi un traitement médical maximal en présence de sténose intracrânienne et qui subissent une récidive d’AVC, il manque de données claires en ce qui a trait à la prise en charge optimale. L’angioplastie intracrânienne (avec ou sans pose d’une endoprothèse) peut être envisagée chez des patients minutieusement sélectionnés [niveau de preuve C].
Prévalence, facteurs prédictifs et pronostic des sténoses intra crâniennes symptomatiques après accident ischémique transitoire (AIT) ou infarctus mineurs : étude de cohorte de population générale
https://www.societe-francaise-neurovasculaire.fr/single-post/pr%C3%A9valence-facteurs-pr%C3%A9dictifs-et-pronostic-des-st%C3%A9noses-intra-craniennes-symptomatiques-apr%C3%A8s
Le traitement endovasculaire par rapport au traitement médical conventionnel pour la sténose symptomatique des artères intracrâniennes (COCHRANE/2023)
Cette revue fournit des données probantes d’un niveau de confiance modéré suggérant que la thérapie endovasculaire (TEV) combinée au traitement médical conventionnel (TMC) par rapport au TMC seul augmente le risque d'accident vasculaire cérébral (AVC) à court terme et de décès chez les personnes présentant une sténose athéromateuse intracrânienne sévère symptomatique récente.
Cet effet était encore apparent lors du suivi à long terme mais semblait être dû aux risques précoces de la TEV ; par conséquent, il pourrait ne pas y avoir de différence nette entre les interventions en termes d'effets sur les AVC et les décès à long terme. L'impact d'une intervention tardive de la TEV (plus de trois semaines après un événement qualifiant) mérite d'être étudié plus avant.
https://www.cochrane.org/fr/CD013267/STROKE_le-traitement-endovasculaire-par-rapport-au-traitement-medical-conventionnel-pour-la-stenose
Commentaire
La sténose carotidienne extra crânienne symptomatique ne pose pas de problème majeur : correction des FDRCV, statine, antiplaquettaire et chirurgie ou stenting si elle est > 70% . Il existe un consensus fort
La sténose carotidienne extra crânienne asymptomatique si elle ne pose pas ce problème pour la correction des FDRC et le traitement médical . Pour la chirurgie ou le stenting le débat est permanent pour les sténoses supérieures à 60%
La sténose artérielle intra crânienne symptomatique , le traitement médical cité précédemment fait consensus. La discussion reste ouverte sur l'angioplastie intracrânienne voire la thrombolyse, on est dans la cas par cas et pour quel délai
Quid de la sténose intra crânienne asymptomatique : correction FDRCV, traitement médical optimal.
Occlusion intra crâniennes des gros vaisseaux
Stroke. 2023 Jun;54(6):1695-1705. doi: 10.1161/STROKEAHA.122.040008. Epub 2023 Mar 20. PMID: 36938708; PMCID: PMC10202848.
https://pubmed.ncbi.nlm.nih.gov/36938708/
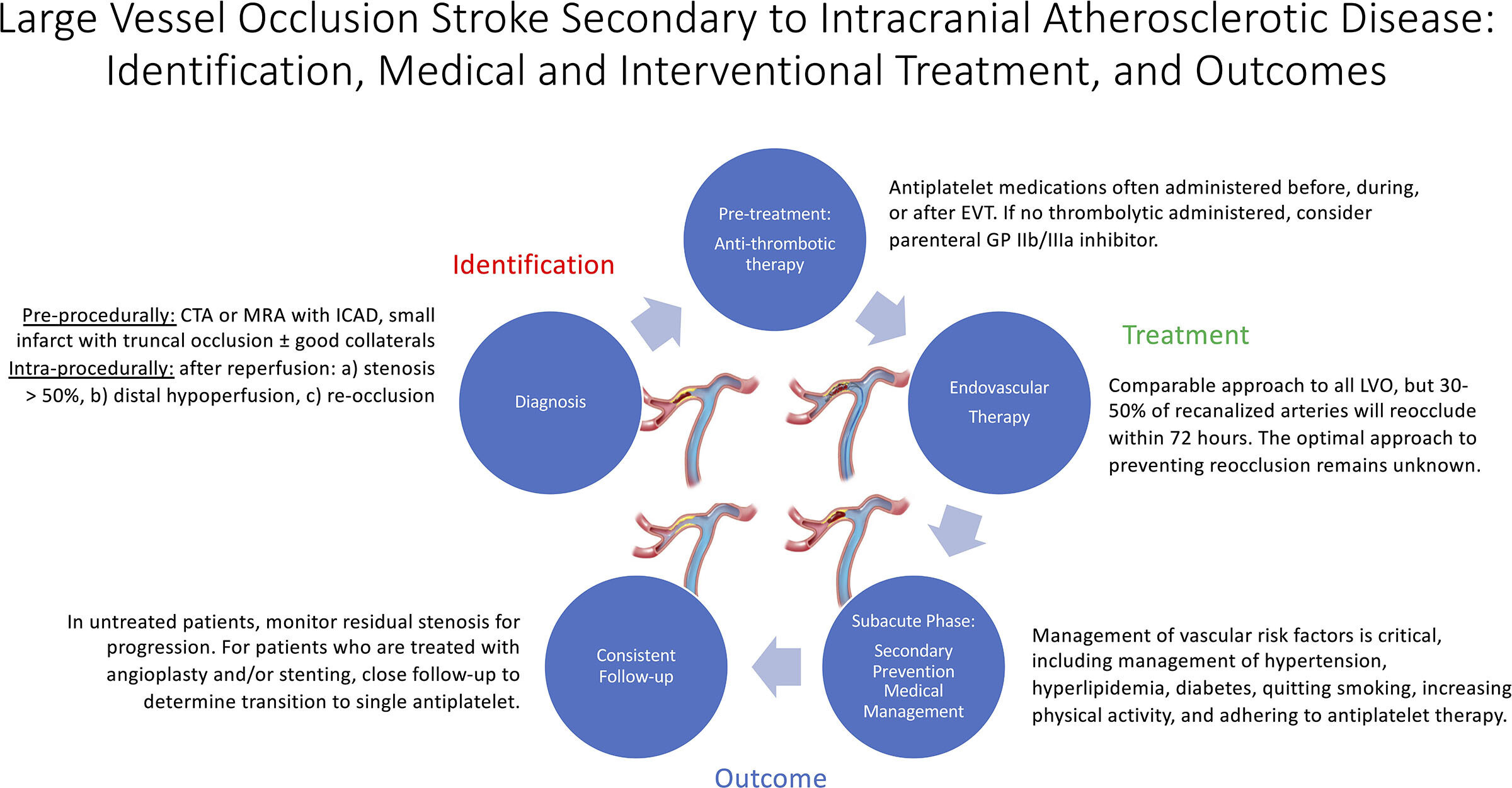
"L'accident vasculaire cérébral par occlusion de gros vaisseaux dû à une maladie athéroscléreuse intracrânienne sous-jacente (ICAD-LVO) est répandu dans 10 à 30 % des LVO en fonction de facteurs liés au patient tels que les facteurs de risque vasculaire, la race, l'origine ethnique et l'âge.
Les patients atteints d'ICAD-LVO tirent des résultats fonctionnels similaires de la thrombectomie endovasculaire à ceux des autres mécanismes de LVO, mais jusqu'à la moitié des patients ICAD-LVO réoccluent après revascularisation.
Par conséquent, l’identification précoce et la planification du traitement pour ICAD-LVO sont importantes compte tenu des considérations uniques avant, pendant et après la thrombectomie endovasculaire.
Dans cette revue de l'ICAD-LVO, nous proposons une approche en plusieurs étapes pour l'identification de l'ICAD-LVO, les considérations liées au prétraitement et à la thrombectomie endovasculaire, les médicaments d'appoint et la prise en charge médicale. Aucun essai contrôlé randomisé à grande échelle n'ayant été consacré à l'étude de l'ICAD-LVO, cette revue se concentre sur les études observationnelles.
ICAD-LVO est un sous-groupe de LVO de plus en plus reconnu avec des considérations diagnostiques et thérapeutiques uniques. Bien que l'ICAD-LVO présente généralement un accident vasculaire cérébral moins grave, les résultats fonctionnels sont équivalents à ceux des autres mécanismes de LVO en raison du taux élevé de réocclusion et du taux élevé d'accidents vasculaires cérébraux récurrents. ICAD-LVO justifie des recherches dédiées pour établir une base de données probantes pour des décisions de traitement individualisées
Mazighi M, Köhrmann M, Lemmens R, Lyrer PA, Molina CA, Richard S, Toni D, Plétan Y, Sari A, Meilhoc A, Jandrot-Perrus M, Binay S, Avenard G, Comenducci A, Grouin JM, Grotta JC; ACTIMIS Study Group. Safety and efficacy of platelet glycoprotein VI inhibition in acute ischaemic stroke (ACTIMIS): a randomised, double-blind, placebo-controlled, phase 1b/2a trial. Lancet Neurol. 2024 Feb;23(2):157-167. doi: 10.1016/S1474-4422(23)00427-1. PMID: 38267188.
Contexte
Les antagonistes de l'activation plaquettaire déclenchée par la glycoprotéine VI, utilisés en association avec des thérapies de recanalisation, constituent une approche thérapeutique prometteuse dans le traitement des accidents vasculaires cérébraux ischémiques aigus. Le glenzocimab est un fragment d'anticorps qui inhibe l'action de la glycoprotéine plaquettaire VI. Notre objectif était de déterminer et d'évaluer l'innocuité et l'efficacité de la dose optimale de glenzocimab chez les patients ayant subi un AVC ischémique aigu éligibles pour recevoir de l'altéplase avec ou sans thrombectomie mécanique.
Méthodes
Cette étude randomisée, en double aveugle, contrôlée par placebo, avec phases d'augmentation de dose (1b) et de confirmation de dose (2a) (ACTIMIS) a été réalisée dans 26 centres d'AVC dans six pays européens. Les participants étaient des adultes (≥ 18 ans) ayant subi un accident vasculaire cérébral ischémique aigu invalidant avec un score sur l'échelle des accidents vasculaires cérébraux du National Institutes of Health de 6 ou plus avant l'administration d'alteplase. Les patients se sont vu attribuer un traitement au hasard à l'aide d'une procédure électronique centrale. La dose totale administrée à la fin de l'administration intraveineuse était de 125 mg, 250 mg, 500 mg et 1 000 mg de glenzocimab ou de placebo en phase 1b et de 1 000 mg de glenzocimab ou de placebo en phase 2a. Le traitement a été initié 4,5 heures ou plus tôt après l'apparition des symptômes de l'AVC chez les patients traités par altéplase avec ou sans thrombectomie mécanique. Le promoteur, l'investigateur et le personnel de l'étude, les patients et les laboratoires centraux étaient tous masqués pour étudier le traitement jusqu'au verrouillage de la base de données. Les critères d'évaluation principaux des deux phases étaient l'innocuité, la mortalité et l'hémorragie intracrânienne (symptomatique, totale et mortelle), évalués chez tous les patients ayant reçu au moins une dose partielle du médicament à l'étude (ensemble de sécurité). L'essai est enregistré sur ClinicalTrials.gov, NCT03803007 et est terminé.
Résultats
Entre le 6 mars 2019 et le 27 juin 2021, 60 patients recrutés ont été répartis au hasard pour recevoir 125 mg, 250 mg, 500 mg ou 1 000 mg de glenzocimab, ou un placebo en phase 1b (n=12 par groupe) et ont été inclus dans l’analyse de sécurité. Le glenzocimab 1 000 mg a été bien toléré et sélectionné comme dose recommandée pour la phase 2a ; du 2 octobre 2020 au 27 juin 2021, 106 patients ont été répartis au hasard pour recevoir glenzocimab 1 000 mg (n = 53) ou un placebo (n = 53). Un patient du groupe placebo a reçu du glenzocimab par erreur et, par conséquent, 54 et 52, respectivement, ont été inclus dans l'ensemble de sécurité. Au cours de la phase 2a, l'événement indésirable survenu pendant le traitement le plus fréquent était une transformation hémorragique non symptomatique, survenue chez 17 (31 %) des 54 patients traités par glenzocimab et 26 (50 %) des 52 patients traités par placebo. Une hémorragie intracrânienne symptomatique n'est survenue chez aucun patient traité par glenzocimab, contre cinq (10 %) patients du groupe placebo. Les décès toutes causes confondues étaient plus faibles avec le glenzocimab 1 000 mg (quatre [7 %] patients) qu'avec le placebo (11 [21 %] patients).
Interprétation
Le glenzocimab 1000 mg en complément de l'altéplase, avec ou sans thrombectomie mécanique, a été bien toléré et pourrait réduire les événements indésirables graves, les hémorragies intracrâniennes et la mortalité. Ces résultats confirment la nécessité de recherches futures sur l'inhibition thérapeutique potentielle de la glycoprotéine VI avec le glenzocimab plus l'altéplase chez les patients ayant subi un accident vasculaire cérébral ischémique aigu.
"Ces résultats très prometteurs plaident pour poursuivre l’évaluation du glenzocimab (1 000 mg) en association à la thrombolyse, sans ou avec thrombectomie mécanique, pour le traitement de l’AVC afin de réduire le risque hémorragique et la mortalité.
Le produit est actuellement en étude clinique de phase 2b/3 dans l’essai Actisave, qui a été approuvé par l’Agence européenne du médicament (EMA). Le laboratoire a également lancé en novembre l’essai Liberate pour tester l’antiplaquettaire dans l’infarctus du myocarde."
https://www.lequotidiendumedecin.fr/actu-medicale/avc-ischemique-le-glenzocimab-un-nouvel-antiplaquettaire-prometteur
Affaire à suivre de très prés......

