-
"La partie la plus cérébrale du jeu - de beaucoup la plus importante - demeure invisible ; c’est donc que le muscle y sert d’écran à l’intelligence." Pierre de Coubertin
-
"Le coeur est le seul muscle strié dont la contraction échappe à la volonté."Jennifer Kouassi
"Si je soulève des haltères, je me muscle les biceps, mais si je pense que je les soulève, je me muscle le cerveau." Philippe Geluck

Turner DC, Raastad T, Ullrich M, Christiansen SF, Sutherland H, Boot J, Wozniak E, Mein C, Dalbram E, Treebak JT, Owens DJ, Hughes DC, Bodine SC, Jarvis JC, Sharples AP. Repeated Disuse Atrophy Imprints a Molecular Memory in Skeletal Muscle: Transcriptional Resilience in Young Adults and Susceptibility in Aged Muscle, L’atrophie musculaire due à l’inactivité répétée laisse une empreinte moléculaire dans le muscle squelettique : résilience transcriptionnelle chez les jeunes adultes et susceptibilité chez les personnes âgées. Adv Sci (Weinh). 2026 ; 25 février : e22726. doi : 10.1002/advs.202522726. Publication en ligne avant impression. PMID : 41736525.
https://advanced.onlinelibrary.wiley.com/doi/10.1002/advs.202522726https://advanced.onlinelibrary.wiley.com/doi/10.1002/advs.202522726
Article en libre accès
L'atrophie musculaire induite par l'inactivité survient fréquemment après une maladie, une blessure ou une chute, et sa fréquence augmente avec l'âge.
On ignore si le muscle squelettique conserve une « mémoire » de l'inactivité répétée.
Afin de permettre des comparaisons robustes selon l'âge, nous avons combiné des données précédemment publiées sur de jeunes rats avec de nouvelles données générées chez des rats âgés. Chez les jeunes adultes, l'inactivité répétée a induit des perturbations transcriptionnelles atténuées dans les voies oxydatives et mitochondriales, suggérant une mémoire moléculaire protectrice, malgré une atrophie similaire à celle observée lors de l'inactivité initiale. En revanche, le muscle âgé a présenté une mémoire délétère, caractérisée par une atrophie plus importante, une suppression exagérée des gènes du métabolisme aérobie malgré la récupération après l'inactivité initiale, une déplétion en NAD + et en ADN mitochondrial, et une activation des voies protéasomales, de la matrice extracellulaire et de réparation de l'ADN. Alors que les jeunes rats récupéraient leur masse musculaire après une période d'inactivité initiale, les rats âgés n'y parvenaient pas. Chez différentes espèces, l'inactivité répétée induisait une hyperméthylation de l'ADN et une diminution de l'expression des gènes impliqués dans le métabolisme aérobie et les réseaux de gènes mitochondriaux. NR4A1 et NR4A3 figuraient parmi les gènes les plus fortement réprimés par l'inactivité ; NR4A1 acquérait une hyperméthylation en phase de récupération qui maintenait sa répression transcriptionnelle, tandis que NR4A3 était le gène le plus fortement sous-exprimé après l'atrophie initiale et restait constamment réprimé pendant la récupération. Les gènes codant pour les sous-unités du récepteur de l'acétylcholine (CHRNA1, CHRND) étaient prédisposés épigénétiquement, présentant une hypométhylation et une forte surexpression après l'inactivité, et une amplification supplémentaire après une atrophie répétée, tandis que CHRNG était induit de manière sélective uniquement après une atrophie répétée. Le gène NMRK2, impliqué dans la biosynthèse du NAD + , était le plus fortement sous-exprimé au cours des deux périodes d'atrophie. La supplémentation en son substrat, le nicotinamide riboside (NR), a amélioré la taille des myotubes dans les cellules souches musculaires dérivées après l'atrophie. Globalement, l'atrophie répétée due à l'inactivité laisse une empreinte moléculaire dans le muscle squelettique, influençant la résilience transcriptionnelle chez les jeunes adultes et exacerbant la vulnérabilité du muscle âgé.
RÉSUMÉ GÉNÉRATIF
Ce document explore la mémoire moléculaire de la atrophie musculaire due à l'inactivité répétée, en mettant en évidence les différences entre les muscles jeunes et âgés au niveau transcriptionnel, épigénétique et métabolique.
Mémoire moléculaire de la atrophie musculaire par désuétude
Une étude approfondie explore comment la désuétude musculaire répétée influence la transcription, l’épigénétique et la susceptibilité à la atrophie, en distinguant les réponses chez les jeunes adultes et les muscles âgés.
Impact de la désuétude répétée sur la transcription musculaire
La désuétude répétée modifie la réponse transcriptionnelle différemment selon l’âge, avec une mémoire protectrice chez les jeunes et une susceptibilité accrue chez les vieux.
- * Chez les jeunes, la désuétude répétée entraîne une atténuation des perturbations transcriptionnelles dans les voies oxydatives et mitochondriales.
- * Malgré cette atténuation, la perte musculaire reste similaire après chaque épisode de désuétude.
- * Chez les muscles âgés, la désuétude répétée cause une atrophie plus importante.
- * Les muscles âgés montrent une suppression exacerbée des gènes liés au métabolisme aérobie, même après récupération.
- * Déplétion de NAD+ et de l’ADN mitochondrial observée dans les muscles âgés.
- * Activation accrue des voies protéasomales, de la matrice extracellulaire et des dommages à l’ADN chez les vieux.
Récupération musculaire chez les jeunes et les vieux
Les jeunes récupèrent leur masse musculaire après la première désuétude, contrairement aux vieux qui échouent à récupérer.
- * Les jeunes rats retrouvent leur masse musculaire initiale après la désuétude.
- * Les rats âgés ne récupèrent pas la masse musculaire, montrant une vulnérabilité accrue.
- * La réponse transcriptionnelle est rétablie après la premier épisode chez les jeunes, mais pas chez les vieux.
Modifications épigénétiques et expression génique
La désuétude répétée induit une hyperméthylation de l’ADN et une répression des gènes liés au métabolisme mitochondrial.
- * NR4A1 et NR4A3 sont parmi les gènes fortement réprimés après désuétude.
- * NR4A1 acquiert une hyperméthylation lors de la phase de récupération, maintenant sa répression.
- * NR4A3 est le plus fortement réprimé après la première atrophie et reste sous-exprimé lors de la récupération.
- * Les gènes des récepteurs à l’acétylcholine (CHRNA1, CHRND, CHRNG) sont hypométhylés et fortement régulés après désuétude, avec amplification lors de la répétition.
- * CHRNG est induit uniquement après la désuétude répétée.
Rôle de NMRK2 et la supplémentation en NR
NMRK2, un gène clé de la biosynthèse de NAD+, est le plus réprimé lors des deux phases d’atrophie.
- * La supplémentation en nicotinamide riboside (NR) augmente la taille des myotubes dérivés de MuSC après atrophie.
- * La réduction de NMRK2 pourrait contribuer à la vulnérabilité musculaire chez les vieux.
- * La supplémentation en NR pourrait représenter une stratégie thérapeutique pour améliorer la récupération musculaire.
Conclusion générale
La mémoire moléculaire de la désuétude musculaire diffère selon l’âge, avec une protection chez les jeunes et une vulnérabilité accrue chez les vieux, impliquant des modifications épigénétiques, une déplétion mitochondriale et des altérations du métabolisme NAD+.
Analyse des réponses musculaires à l'atrophie et à la récupération
Ce texte explore comment la masse, la structure, la composition en fibres et l'expression génique du muscle réagissent à l'atrophie, à la récupération et à la répétition de ces processus chez des jeunes adultes humains et des rats âgés, en utilisant diverses techniques moléculaires et histologiques.
Effets de l'atrophie et de la récupération chez l'humain jeune
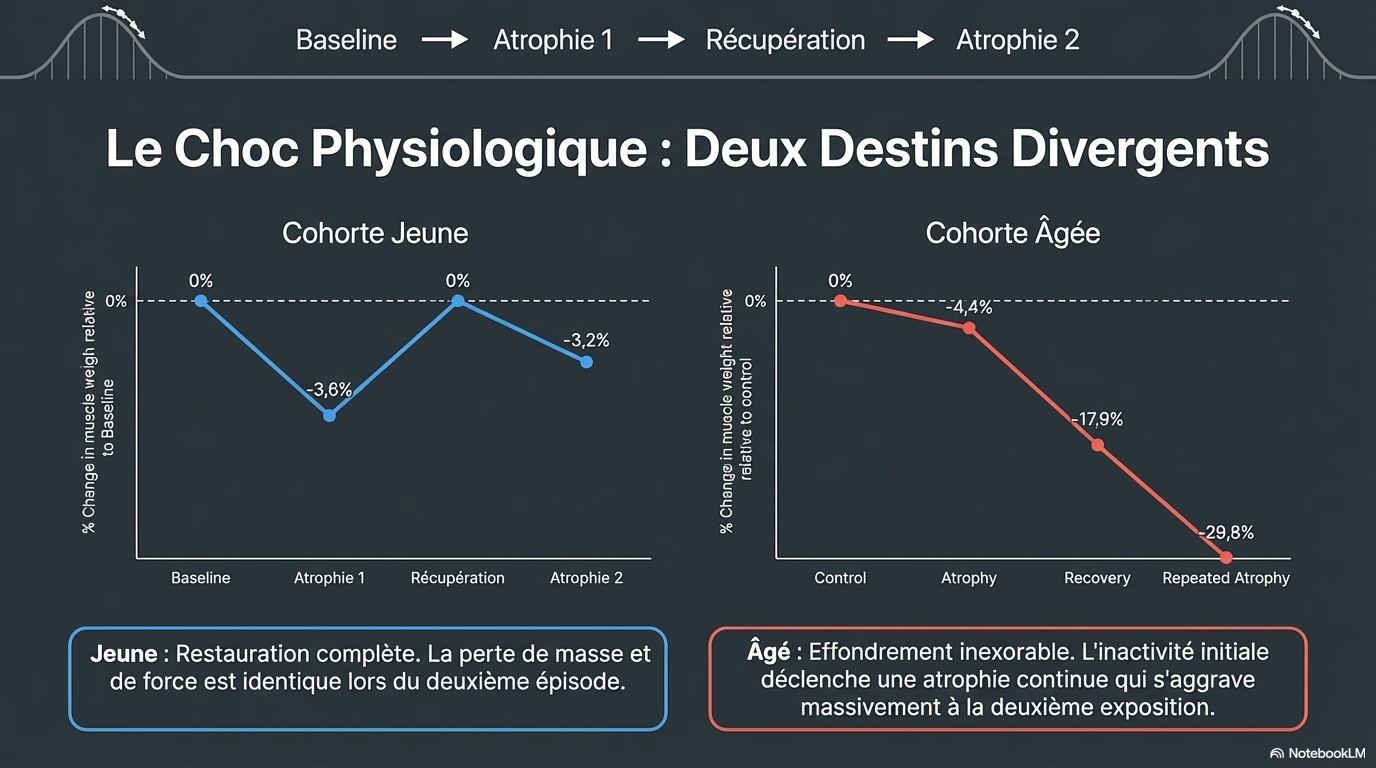
- * L'atrophie induite par immobilisation réduit la masse musculaire de -3,6% (LLM) et la taille du muscle VL de -9%, avec une récupération complète.
- * La force musculaire (MVC) diminue de -14,3% à 90° de flexion du genou après atrophie, puis se rétablit.
- * La composition en fibres montre une augmentation de 60% de fibres de type II, avec une réduction des fibres de type I.
- * Les analyses transcriptomiques révèlent une baisse de l'expression des gènes MYH et Myl, notamment ceux liés aux fibres lentes, avec une augmentation de MYH1 (type IIX).
- * La majorité des changements génétiques sont liés à la respiration mitochondriale, au métabolisme oxydatif et à la structure musculaire, avec une atténuation lors de la répétition de l'atrophie.
Réponse musculaire chez le rat âgé
- * La perte musculaire lors de l'atrophie induite par TTX est plus importante après la répétition (-29,8%) comparée à la première phase.
- * La masse musculaire continue de diminuer après la récupération, malgré une expression accrue des gènes de myosine embryonnaire (Myh3/8).
- * La composition en fibres montre une réduction des fibres de type I et IIA, avec une augmentation des fibres de type IIX/IIB.
- * Les analyses transcriptomiques montrent une forte perturbation génétique, notamment une suppression accrue des gènes liés au métabolisme et à la respiration mitochondriale.
- * La transcription de gènes liés à la jonction neuromusculaire (AChR) est augmentée après atrophie et répétition, indiquant une réponse adaptative.
Profilage temporel des réponses génétiques
- Chez l'humain jeune, la majorité des gènes diminue après atrophie, avec une atténuation lors de la répétition, indiquant une protection transcriptionnelle.
- Certains gènes liés au développement et à la régénération montrent une réponse amplifiée ou persistante après répétition, suggérant une mémoire transcriptionnelle.
- Chez le rat âgé, la majorité des gènes sont restaurés après la récupération, mais une forte perturbation subsiste, avec une réponse transcriptionnelle moins protectrice.
- La majorité des gènes dans le rat âgé montrent une restauration partielle ou une réponse amplifiée lors de la répétition, mais avec une perturbation plus importante que chez le jeune.
Implications pour la santé musculaire liée à l'âge
- * La capacité de récupération musculaire diminue avec l'âge, avec une perturbation accrue des voies métaboliques et structurales.
- * La transcription de gènes clés, notamment ceux liés à la respiration mitochondriale, est plus fortement réprimée chez le rat âgé.
- * La réponse neuromusculaire et la régénération musculaire sont altérées, avec une réponse génétique moins protectrice et plus perturbée lors de la répétition de l'atrophie.
Mémoire moléculaire de la atrophie musculaire par désuétude
Le muscle squelettique conserve une mémoire moléculaire de l'atrophie répétée, avec des différences selon l'âge, impliquant des voies métaboliques, mitochondriales et épigénétiques.
- * Chez les jeunes adultes, l'atrophie répétée entraîne une atténuation des réponses transcriptionnelles, notamment dans les voies de la respiration, du NAD+/NADH, de la chaîne respiratoire et de la synthèse d'ATP.
- * Chez les animaux âgés, ces mêmes voies sont davantage réprimées lors de l'atrophie répétée, malgré une récupération transcriptionnelle, mais avec une poursuite de la perte musculaire.
- * La mémoire moléculaire est partiellement encodée par des modifications épigénétiques, notamment la méthylation de l'ADN, affectant des gènes clés comme NMRK2, impliqué dans la biosynthèse du NAD+.
- * La perte de contenu mitochondrial et de l'ADN mitochondrial est plus marquée chez les muscles âgés après l'atrophie répétée.
- *La réponse épigénétique et transcriptionnelle est conservée entre l'humain et le rat, notamment dans les voies métaboliques oxydatives et mitochondriales.
Réponse transcriptionnelle à l'atrophie et récupération
L'atrophie induite par désuétude modifie fortement l'expression génique, avec une récupération partielle lors de la reprise d'activité, mais avec des différences selon l'âge.
- * Chez les jeunes adultes, la majorité des gènes réprimés lors de l'atrophie se rétablissent après la reprise, montrant une résilience transcriptionnelle.
- * Chez les rats âgés, la masse musculaire ne récupère pas, malgré une récupération transcriptionnelle, et la perte musculaire continue.
- * La réponse transcriptionnelle est amplifiée lors de l'atrophie répétée chez les rats âgés, avec une suppression accrue des voies métaboliques et mitochondriales.
- * Des voies spécifiques comme la protéasome, la matrice extracellulaire (ECM) et la réparation de l'ADN sont activées dans les muscles âgés lors de l'atrophie répétée.
- *La transcription de gènes liés à la jonction neuromusculaire (AChR) est amplifiée après l'atrophie répétée, avec des modifications épigénétiques associées.
Régulation épigénétique des voies métaboliques
L'intégration des données épigénétiques et transcriptomiques montre une régulation conservée des gènes liés au métabolisme oxydatif et à la mitochondrie, avec des modifications de méthylation inverses de l'expression.
- * Chez l'humain, 57 gènes hypermethylés et downregulés après l'atrophie, puis restaurés lors de la récupération.
- * Chez le rat, 33 gènes hypermethylés et downregulés après l'atrophie, avec une régulation inverse lors de la récupération.
- * La gene NMRK2, impliquée dans la biosynthèse du NAD+, est fortement downregulée et hypermethylée dans les deux modèles.
- * La méthylation de l'ADN est associée à la répression des voies de la respiration, du cycle de Krebs, et de la synthèse d'ATP.
- * La régulation épigénétique pourrait servir de biomarqueur de la mémoire de désuétude musculaire.
Impact de la désuétude répétée sur la mitochondrie
La désuétude répétée entraîne une perte significative de contenu mitochondrial et d'ADN mitochondrial, avec des effets plus marqués chez les muscles âgés.
- * Chez l'humain, la perte d'ADN mitochondrial est de 18% après l'atrophie, 41% après la récupération, et 50% après l'atrophie répétée.
- * Chez le rat âgé, la perte d'ADN mitochondrial atteint 50% après l'atrophie répétée.
- * La transcription des gènes de la chaîne respiratoire est fortement réprimée lors de l'atrophie et de l'atrophie répétée.
- * La protéine de la chaîne respiratoire et la citrate synthase ne changent pas significativement, mais la content mitochondrial diminue.
- * La vulnérabilité mitochondriale accrue pourrait aggraver la susceptibilité à la désuétude répétée, même chez les jeunes.
Effets de la supplémentation en Nicotinamide Riboside (NR)
La supplémentation en NR, précurseur du NAD+, améliore la croissance des myotubes dérivés de cellules souches musculaires après atrophie.
- * NMRK2, clé dans la biosynthèse du NAD+, est fortement downregulée après atrophie, mais la supplémentation en NR augmente la taille des myotubes.
- * La réponse est plus marquée dans les cellules dérivées après atrophie, avec une modulation de MYOD et MYOG.
- * Le contenu mitochondrial tend à être plus faible dans les cellules post-atrophie, mais la NR favorise la croissance myoblastique.
- * La supplémentation pourrait représenter une stratégie pour améliorer la récupération musculaire chez les sujets âgés ou désuets.
Remodelage de la matrice extracellulaire dans le vieillissement
Les gènes liés à la matrice extracellulaire, à la collagénèse et à l'organisation structurale sont spécifiquement régulés lors de la récupération chez les muscles âgés.
- * Ces gènes indiquent un remodelage structurel pouvant augmenter la rigidité musculaire, caractéristique du vieillissement.
- * La matrice extracellulaire, la protéolyse et les voies ubiquitines sont activées après l'atrophie répétée, suggérant une résilience compromise.
- * Ces modifications pourraient influencer la capacité de récupération et la susceptibilité à de futures désuétudes.
Rôle des gènes NR4A dans la régulation métabolique
NR4A1 et NR4A3, gènes clés du métabolisme énergétique, montrent une mémoire
* NR4A1 reste hypermethylée et sous-exprimée même après récupération complète.
- * NR4A3 est fortement réduit après l'atrophie, avec une régulation inverse lors de la récupération.
- * Ces gènes sont sensibles à l'exercice et à l'inactivité, et leur modulation pourrait améliorer la récupération musculaire.
- * Ils sont candidats pour des interventions visant à prévenir ou réduire la désuétude musculaire liée à l'âge.
Limites et perspectives de l'étude
L'étude combine des analyses physiologiques, transcriptomiques, épigénétiques et mitochondriales, mais présente des limites.
- * La réponse moléculaire ne traduit pas toujours la récupération musculaire en volume ou force.
- * La comparaison interespèces doit être interprétée avec prudence en raison des différences de protocoles et de modèles.
- * La majorité des études in vitro ont été réalisées sur des cellules musculaires humaines jeunes, avec peu de données sur le vieillissement.
- * La variabilité liée au sexe, à la souche animale et à la taille des échantillons doit être considérée.
- * Des études futures sont nécessaires pour valider les interventions en NAD+ et explorer les mécanismes épigénétiques en contexte clinique.
Effets de l'immobilisation sur la masse musculaire
L'immobilisation prolongée entraîne une atrophie musculaire significative, avec des pertes rapides de masse et de fonction.
- * Une semaine d'immobilisation de la jambe provoque une atrophie spécifique des muscles
- 5 jours d'inactivité musculaire suffisent pour une perte substantielle de masse musculaire.
- * La perte de masse musculaire peut atteindre des niveaux critiques en seulement 5 jours.
- * L'inactivité réduit le taux de synthèse des protéines myofibrillaires et induit une résistance anabolique à l'ingestion de protéines.
- * La récupération musculaire après immobilisation est souvent limitée, surtout chez les personnes âgées.
Impact de l'exercice excentrique et de l'entraînement
L'exercice excentrique et l'entraînement régulier peuvent atténuer ou inverser les effets négatifs de l'inactivité musculaire.
- * L'exercice excentrique endommageur musculaire peut temporairement prévenir la perte musculaire lors de désuétude.
- * L'entraînement en résistance durant l'immobilisation peut réduire la sarcopénie et modifier la distribution des isoformes de myosine.
- * La rééducation par entraînement de résistance favorise la récupération de la masse et de la fonction musculaire.
- * La mémoire musculaire, via des modifications épigénétiques, permet une récupération plus rapide après désuétude.
Changements moléculaires et épigénétiques
Les mécanismes moléculaires et épigénétiques jouent un rôle clé dans la réponse musculaire à l'inactivité et à l'entraînement.
- * La désuétude modifie l'expression génique musculaire et le profil protéomique.
- * La méthylation de l'ADN et d'autres modifications épigénétiques sont associées à la mémoire musculaire.
- * L'exercice et l'entraînement peuvent réinitialiser ou moduler le méthylome musculaire, même après plusieurs années.
- * La mémoire épigénétique contribue à la rapidité de la récupération musculaire après désuétude.
Effets de la microgravité et du confinement spatial
Les missions spatiales et le confinement prolongé affectent la composition et la fonction musculaire.
- * 5 à 11 jours de vol spatial modifient la taille et les propriétés enzymatiques des fibres musculaires.
- * La proteomique musculaire change après des missions spatiales, avec des altérations spécifiques à chaque astronaute.
- * La déplétion mitochondriale et la dysrégulation de la dynamique mitochondriale sont observées après le confinement.
- * La réadaptation musculaire post-vol spatial peut nécessiter des interventions ciblées pour restaurer la santé musculaire.
Mécanismes de récupération et interventions
La récupération musculaire après désuétude peut être améliorée par des stratégies spécifiques.
- * La rééducation par entraînement de résistance accélère la récupération de la masse musculaire.
- * La modulation épigénétique et la mémoire musculaire facilitent la reprise de la fonction.
- * La supplémentation en nicotinamide riboside peut améliorer la biogenèse mitochondriale.
- La prévention de l'atrophie passe par l'activité physique régulière et des interventions précoces.
Influence de l'âge et de l'activité physique
L'âge et le niveau d'activité influencent la réponse musculaire à l'inactivité et à l'entraînement.
- * La musculation régulière induit une hypométhylation des gènes liés au métabolisme et à la myogenèse.
- * L'activité physique tout au long de la vie est associée à une hypométhylation des promoteurs génétiques.
- * La mémoire musculaire épigénétique est présente chez les jeunes et les personnes âgées.
- * La réactivité moléculaire et épigénétique est plus faible chez les personnes inactives ou âgées
- .
Mécanismes de régulation génétique et protéique
Les voies de régulation génétique et protéique contrôlent l'adaptation musculaire.
- * La régulation par des récepteurs nucléaires comme nor-1 influence la résistance à la fatigue.
- * La synthèse protéique et la dégradation sont modulées par des ligases ubiquitines comme UBR5.
- * La réponse à l'exercice implique une intégration multi-omique, incluant méthylation, transcriptome et protéome.
- * La compréhension de ces mécanismes permet de développer des stratégies pour prévenir ou traiter la sarcopénie.
Conclusion
Les recherches montrent que l'inactivité musculaire induit des changements rapides et profonds, mais que l'exercice, la mémoire épigénétique et les interventions ciblées peuvent favoriser la récupération et la prévention.
SYNTHESE NOTEBOOKLM
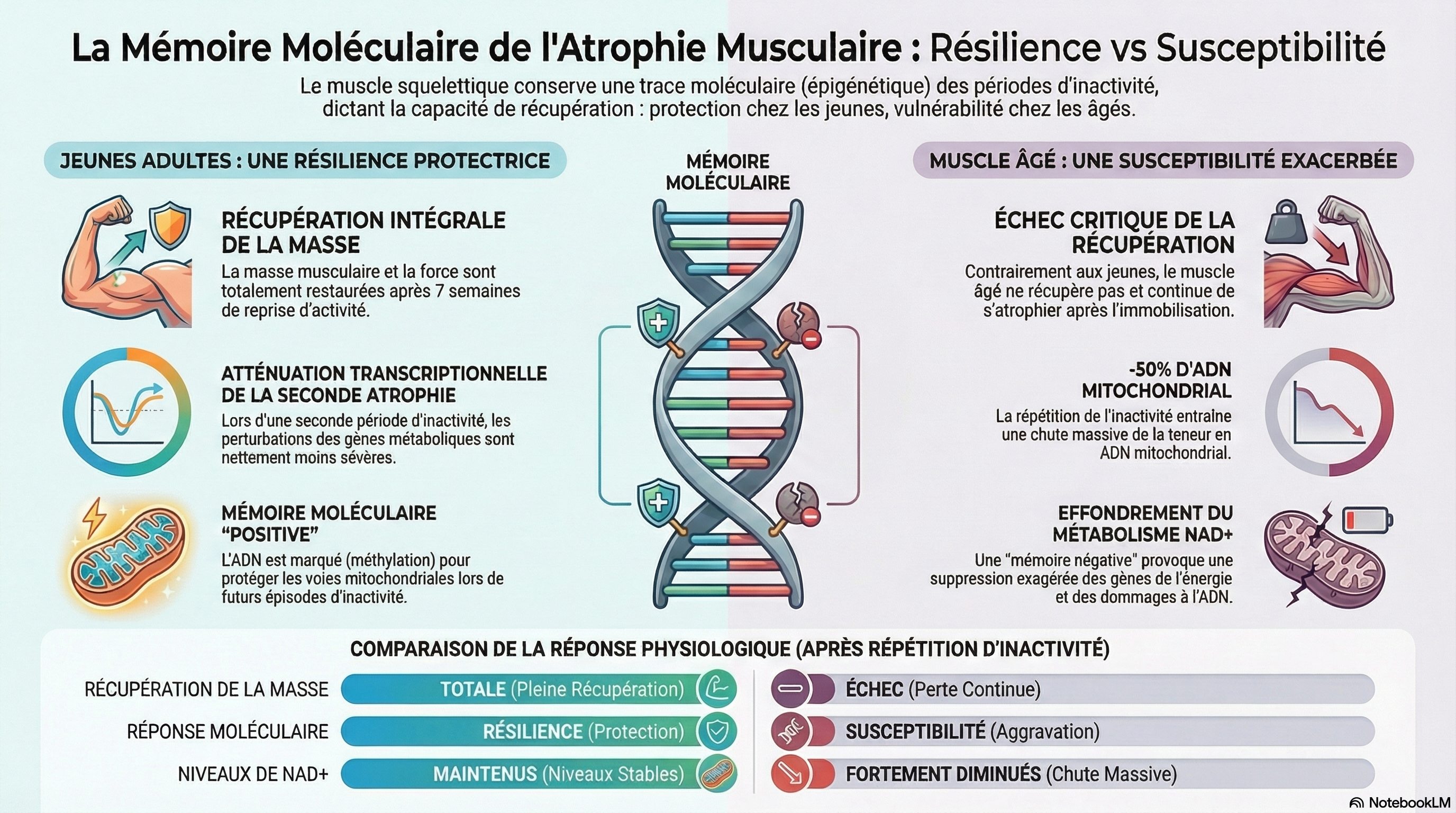
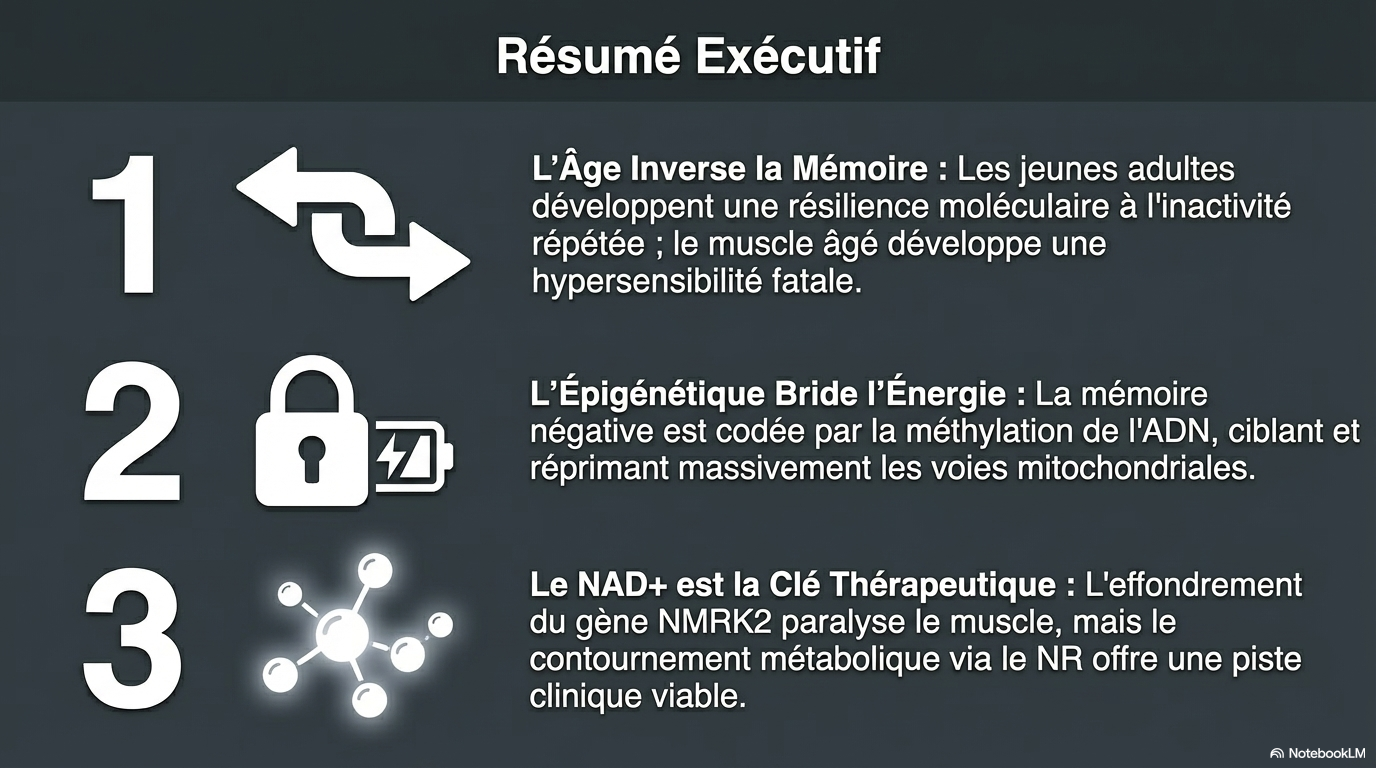
Cette étude scientifique explore l'existence d'une mémoire moléculaire du muscle squelettique face à l'atrophie par désuétude répétée, en comparant des sujets humains jeunes et des modèles de rats âgés. Les chercheurs démontrent que les muscles des adultes jeunes font preuve d'une résilience transcriptionnelle, atténuant les perturbations métaboliques lors d'un second épisode d'immobilisation, tandis que les muscles âgés manifestent une vulnérabilité accrue et une incapacité à récupérer leur masse initiale. L'analyse révèle que ces réponses contrastées sont régulées par des modifications épigénétiques, notamment la méthylation de l'ADN, qui altèrent durablement l'expression des gènes liés au métabolisme aérobie et aux mitochondries. Enfin, l'identification du gène NMRK2 comme acteur clé de cette dégradation suggère que la supplémentation en nicotinamide riboside pourrait offrir une piste thérapeutique pour restaurer la taille des fibres musculaires après une période d'inactivité.





Voici un décryptage détaillé de cet article de Turner et al. (2026), publié dans Advanced Science .[1] by OPEN EVIDENCE
Question centrale de l'étude
Cette étude explore un concept novateur : le muscle squelettique conserve-t-il une « mémoire moléculaire » de l'atrophie de désuétude répétée , et cette mémoire diffère-t-elle entre le muscle jeune et le muscle âgé ? L'atrophie de désuétude (immobilisation, altération, blessure) est fréquente et s'aggrave avec le vieillissement. Jusqu'ici, la notion de mémoire épigénétique avait surtout été étudiée dans le contexte de l'exercice et de l'hypertrophie, mais jamais dans celui de la désuétude répétée.[2-3]
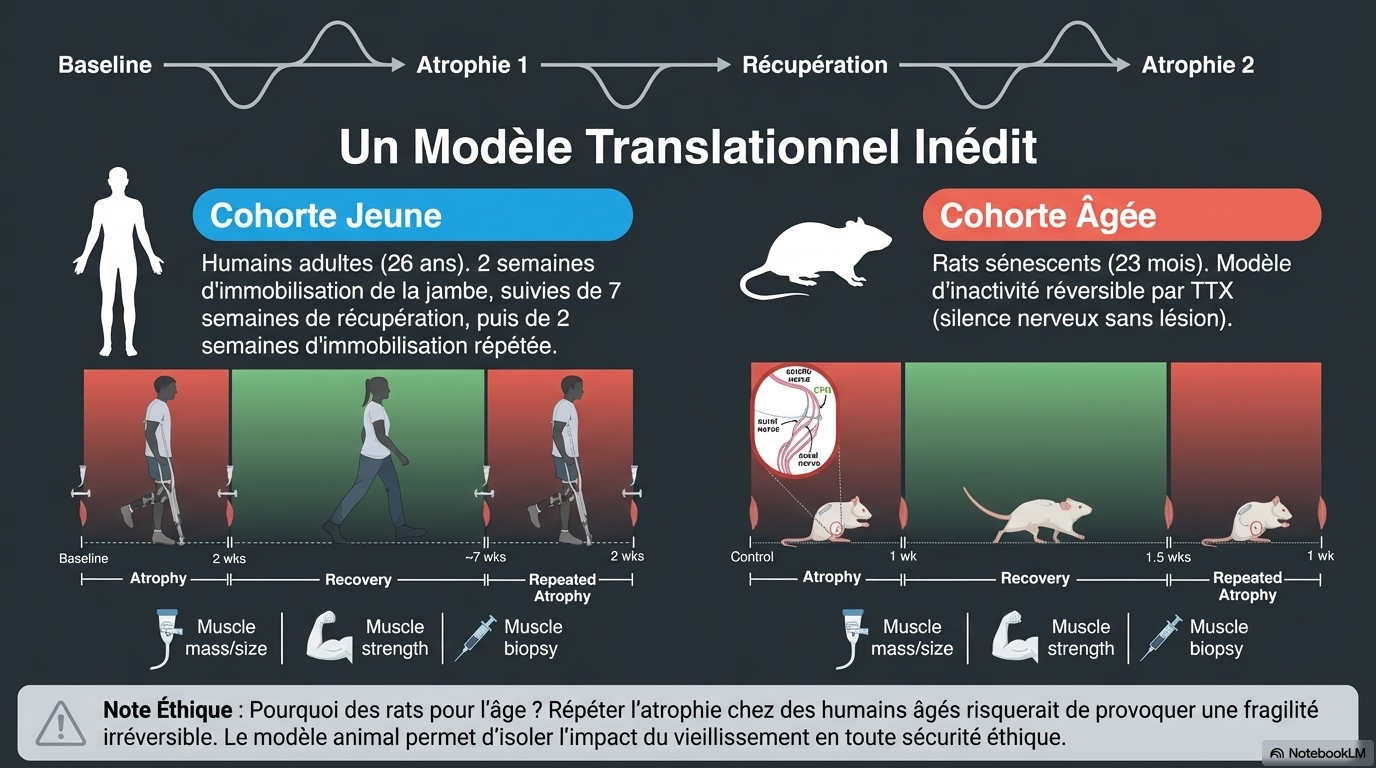
Conception expérimentale
L'étude combine un modèle humain (jeunes adultes soumis à deux périodes d'immobilisation du membre inférieur) et un modèle animal (rats âgés vs jeunes), avec une approche multi-omique intégrant transcriptomique, méthylomique (ADN), immunohistochimie, biochimie, et analyses sur cellules souches musculaires humaines primaires (MuSC). Les données de rats jeunes proviennent d'une publication antérieure, intégrées aux nouvelles données de rats âges pour permettre une comparaison robuste inter-âge.[1]
Résultats clés
1. Mémoire protectrice chez le jeune vs mémoire délétère chez l'âgé
Chez les jeunes adultes , la deuxième période de désuétude provoque une atténuation des perturbations transcriptionnelles dans les voies oxydatives et mitochondriales, malgré une atrophie similaire à la première période. Cela suggère une mémoire moléculaire protectrice : le muscle « apprend » à mieux tolérer le stress de désuétude. À l'inverse, le[1] muscle âgé développe une mémoire délétère, caractérisée par une atrophie plus sévère, une suppression exagérée des gènes du métabolisme aérobie, une déplétion en NAD⁺ et en ADN mitochondrial, et l'activation de voies protéasomales, de la matrice extracellulaire et de réparation des dommages à l'ADN.[1]Ces résultats sont cohérents avec les travaux montrant que le muscle âgé présente une réponse transcriptomique dysrégulée à l'alitement, avec activation de voies fibrotiques et inflammatoires, et une récupération de masse musculaire altérée après immobilisation.[4-5]
2. Échec de récupération chez le rat âgé
Alors que les rats jeunes récupèrent leur masse musculaire après la première période de désuétude, les rats âgés échouent à récupérer , confirmant la vulnérabilité liée à l'âge.[1][5]
3. Mécanismes épigénétiques : hyperméthylation et gènes clés
Chez les deux espèces, la désuétude induit de manière répétée une hyperméthylation de l'ADN et une sous-expression des réseaux géniques du métabolisme aérobie et mitochondrial.[1]Cela contraste avec la mémoire de l'exercice, où l'on observe plutôt une hypométhylation retenue après l'entraînement.[2-3][6]
Parmi les gènes les plus affectés :
-
NR4A1 (Nur77) et NR4A3 (NOR1) : parmi les gènes les plus fortement réprimés par la désuétude. NR4A1 acquiert une hyperméthylation en phase de récupération, maintenant sa répression transcriptionnelle. NR4A3 est le gène le plus sous-exprimé après la première atrophie et reste supprimé pendant la récupération. Ces récepteurs nucléaires orphelins sont des régulateurs majeurs de la taille des fibres musculaires (NR4A1 induit IGF-1 et inhibe les atrogènes MuRF1/MAFbx) et du métabolisme du glucose (la perte de NR4A3 réduit l'oxydation du glucose de 18 % et la synthèse protéique de 25 %).[1][7-8]
-
Gènes des récepteurs à l'acétylcholine (CHRNA1, CHRND, CHRNG) : ces gènes sont « épigénétiquement amortis » par hypométhylation et fortement surexprimés après la désuétude, avec une amplification supplémentaire après l'atrophie répétée. CHRNG est sélectivement induit uniquement après l'atrophie répétée. La surexpression de CHRNA1 est connue pour induire la sarcopénie via l'élimination synaptique neuromusculaire, et la dégénérescence des récepteurs à l'acétylcholine à la jonction neuromusculaire est un mécanisme central du vieillissement musculaire.[1][9-10]
-
NMRK2 : gène de biosynthèse du NAD⁺, c'est le gène le plus sous-exprimé lors des deux périodes d'atrophie.[1]
4. Piste thérapeutique : le nicotinamide riboside (NR)
La supplémentation en NR (substrat de NMRK2) a amélioré la taille des myotubes dans les cellules musculaires dérivées de muscles post-atrophie.[1]Cette observation est cohérente avec les données précliniques montrant que le NR améliore la biogenèse mitochondriale musculaire, la différenciation des cellules satellites et la fonction des cellules souches musculaires.[11-13]Cependant, les essais cliniques chez les personnes âgées n'ont pas encore démontré de bénéfice significatif sur la masse et la fonction musculaire, soulignant le fossé entre les résultats précliniques et la traduction clinique.[14-15]
Implications cliniques
Cette étude a des implications directes pour la prise en charge des patients hospitalisés, immobilisés ou qualifiés de façon répétée, en particulier les personnes âgées.
Elle suggère que chaque épisode de désuétude laisse une empreinte épigénétique cumulative dans le muscle âgé, aggravant progressivement la vulnérabilité à l'atrophie. Cela renforce l'importance de la mobilisation précoce et de la prévention de la désuétude répétée chez les patients gériatriques, et ouvre des pistes pharmacologiques ciblant le métabolique du NAD⁺ ou les récepteurs NR4A.

Utilisé sous licence du New England Journal of Medicine.
Cette figure illustre les voies cataboliques et anaboliques du muscle squelettique, incluant les cascades de signalisation impliquées dans l'atrophie (désuétude, dénervation, vieillissement) et les mécanismes protecteurs (exercice, sestrines), offrant un cadre conceptuel complémentaire aux découvertes de Turner et al.
Commentaire
Pour entretenir ses muscles, il n'y a qu'une solution : pratiquer une activité physique quotidienne, on ne le dira jamais assez !
L'activité physique est un véritable médicament : posologie, effets positifs, effets secondaires, indications, conte indications etc !
A LIRE
SARCOPENIE et GEROSCIENCE
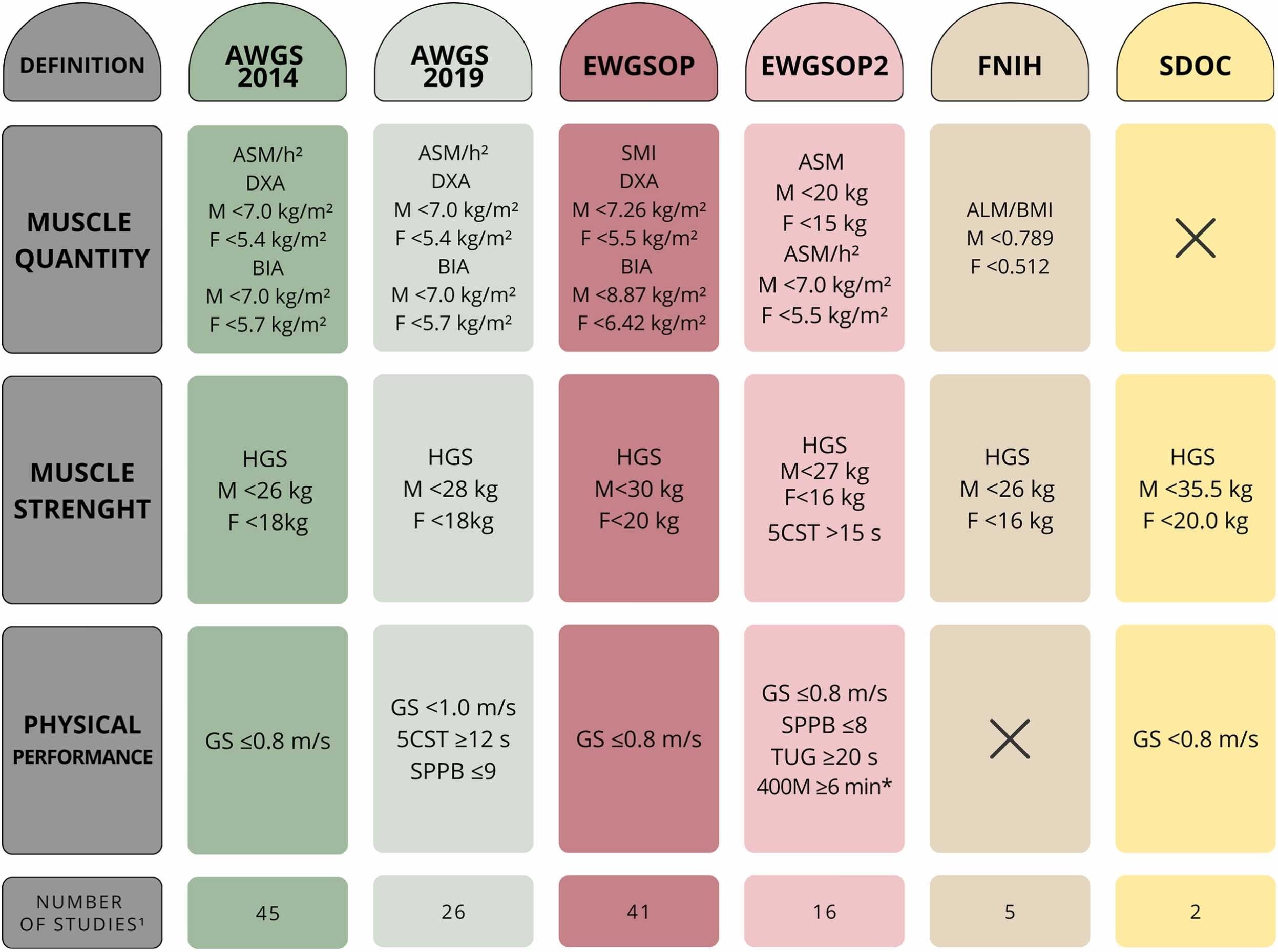
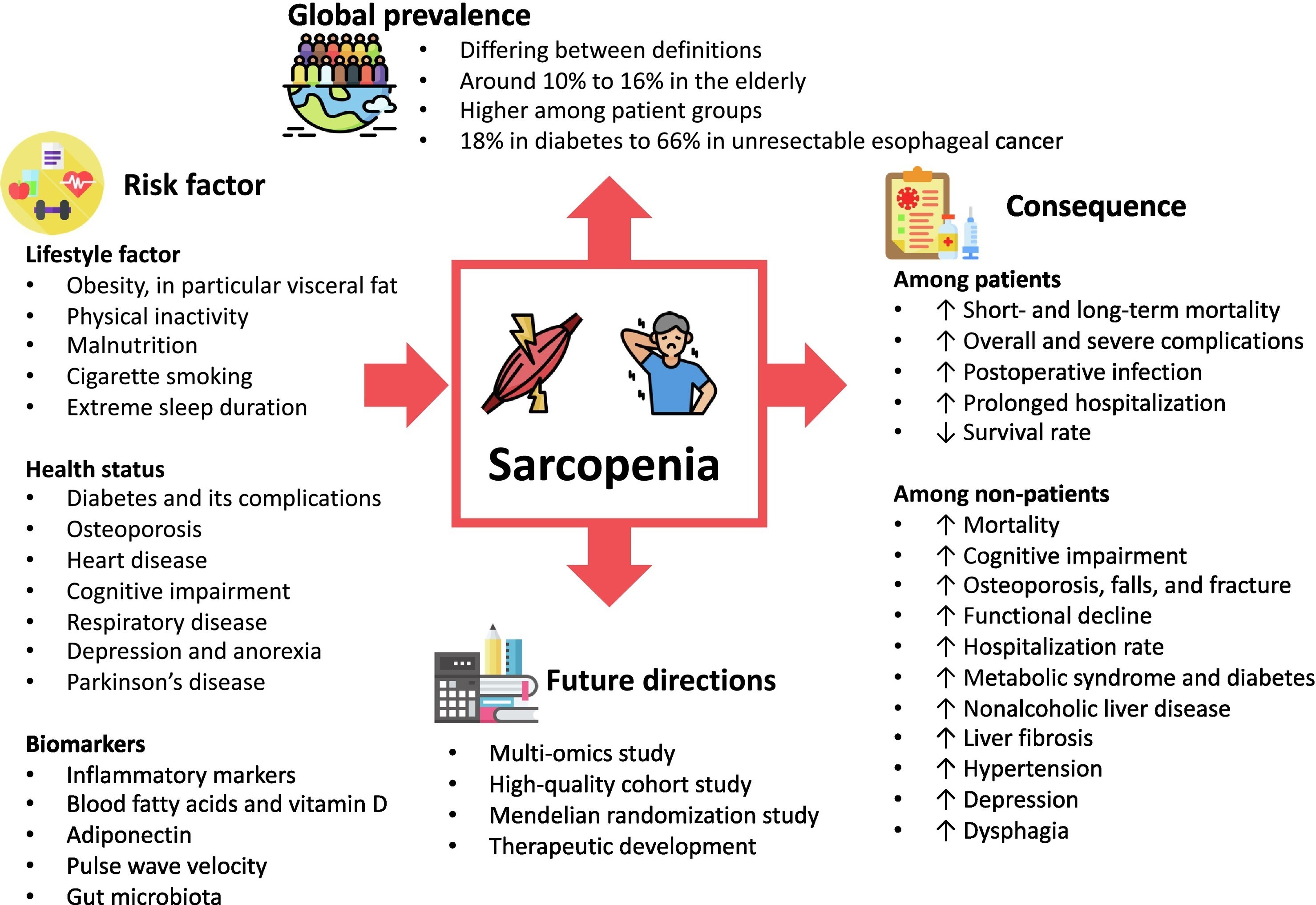
Critères et points limites utilisés pour diagnostiquer la sarcopénie dans les articles inclus. AWGS : Groupe de travail asiatique sur la sarcopénie (2014 ( Chen et al., 2014 ) et 2019 ( Chen et al., 2020 )) ; EWGSOP : Groupe de travail européen sur la sarcopénie chez les personnes âgées (2010 ( Cruz-Jentoft et al., 2010 ) et 2019 ( Cruz-Jentoft et al., 2019 )) ; FNIH : Fondation pour les National Institutes of Health ( Studenski et al., 2014 ) ; SDOC : Consortium pour les définitions et les résultats de la sarcopénie ( Bhasin et al., 2020 ) ; H : homme ; F : femme ; DXA : absorptiométrie à rayons X en double énergie ; BIA : analyse d'impédance bioélectrique ; ASM/h² : masse musculaire squelettique appendiculaire divisée par le carré de la taille ; SMI : indice de masse musculaire squelettique (masse musculaire squelettique appendiculaire/taille²) ; ASM : masse musculaire squelettique appendiculaire ; ALM/BMI : masse maigre appendiculaire standardisée à l' indice de masse corporelle ; HGS : force de préhension ; 5CST : test de station debout sur chaise (cinq levées) ; GS : vitesse de marche ; SPPB : batterie de tests de performance physique courte ; TUG : test chronométré de montée et de descente ; 400 M : test de marche de 400 mètres ; * ou non-achèvement du test. ¹ Certaines études ont utilisé plus d'une de ces méthodes de diagnostic.
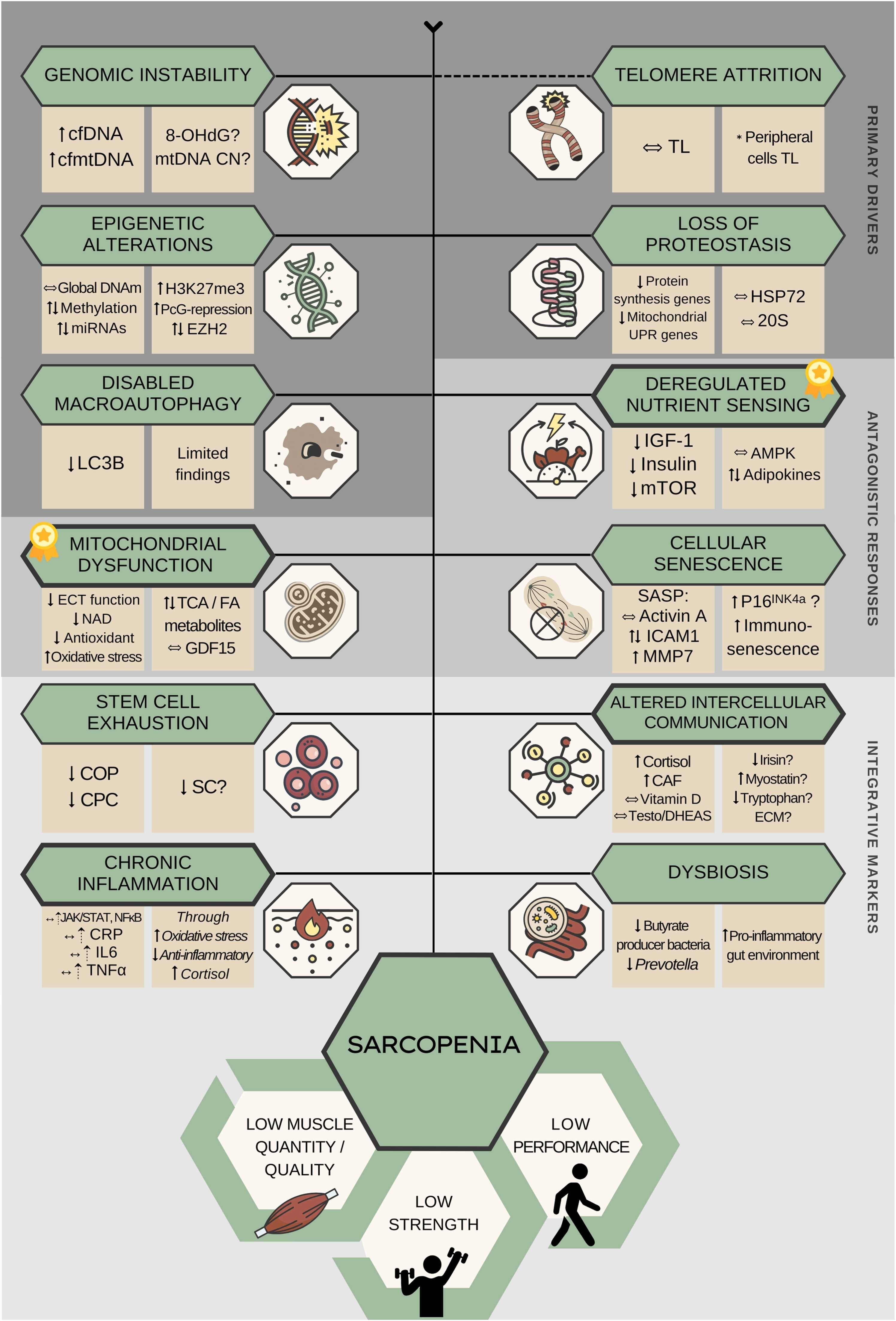
Sarcopénie et caractéristiques du vieillissement. cfDNA : ADN acellulaire circulant ; cfmtDNA : ADN mitochondrial acellulaire circulant ; 8-OHdG : 8-hydroxydésoxyguanosine ; mtADN CN : nombre de copies d'ADN mitochondrial ; TL : longueur des télomères ; ADNm : méthylation de l'ADN ; miARN : microARN ; H3K27me3 : triméthylation de l'histone H3 lysine 27 ; PcG-répression : répression génique médiée par le groupe polycomb ; EZH2 : amplificateur de Zeste Homologue 2 ; UPR : réponse protéique dépliée ; HSP72 : protéine de choc thermique 72 ; 20S : protéasome 20S ; LC3B : chaîne légère 3B de la protéine 1 associée aux microtubules ; IGF1 : facteur de croissance analogue à l'insuline 1 ; mTOR : cible mécanistique de la rapamycine ; AMPK : protéine kinase activée par l'AMP ; ECT : chaîne de transport d'électrons ; NAD : nicotinamide adénine dinucléotide ; TCA : cycle de l'acide tricarboxylique ; AG : métabolisme des acides gras ; GDF15 : facteur de différenciation de croissance 15 ; SASP : phénotype sécrétoire associé à la sénescence ; ICAM1 : molécule d'adhésion intercellulaire 1 ; MMP7 : métalloprotéinase matricielle 7 ; COP : cellules ostéoprogénitrices circulantes ; CPC : cellules progénitrices circulantes ; SC : cellules satellites ; CAF : fragment d'agrine C-terminal circulant ; Testo : testostérone ; DHEAS : déhydroépiandrostérone ; ECM : matrice extracellulaire ; JAK/STAT : Janus kinase/transducteur de signal et activateur de la transcription ; NFκB : facteur nucléaire-κB ; CRP : protéine C-réactive ; IL6 : interleukine-6 ; TNF-α : Facteur de nécrose tumorale alpha. ↓ : diminution dans le groupe sarcopénique ; ↑ : augmentation dans le groupe sarcopénique ; ↔ : absence de différence entre les groupes sarcopénique et non sarcopénique ; ↔⇡ : la plupart des données probantes ne suggèrent aucune différence entre les groupes, bien que certaines études indiquent des taux légèrement élevés dans le groupe sarcopénique. La ligne pointillée indique l'absence de lien entre ce marqueur et la biologie de la sarcopénie. Les lignes plus épaisses représentent les marqueurs associés à un plus grand nombre d'études, tandis que les drapeaux jaunes indiquent ceux plus fortement liés à la sarcopénie d'après les données probantes recueillies.
https://medvasc.info/archives-blog/sarcopenie-et-geroscience
SARCOPENIE et ses CONSÉQUENCES