"L'esprit c'est comme un parachute : s'il reste fermé, on s'écrase." Franck Zappa
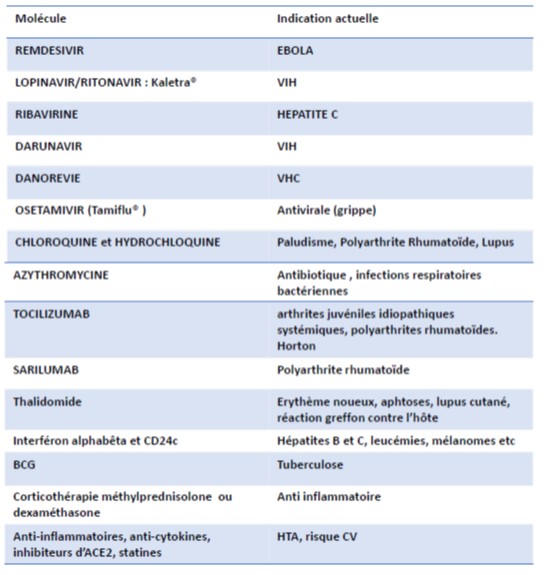
 Rappel : toutes ces molécules ont déjà des indications, elles sont connues et prescrites.Le COVID-19 est une affection virale, il était donc logique de tester les médicaments existants qui sont soient des anti viraux, soit des anti inflammatoires puissants. De plus la plupart de ces médicaments sont utilisés au quotidien dans leurs indications spécifiques, on connaît donc leur mode d'utilisation, les effets secondaires potentiels et la manière de les surveiller.On ne part pas l'aventure.
Rappel : toutes ces molécules ont déjà des indications, elles sont connues et prescrites.Le COVID-19 est une affection virale, il était donc logique de tester les médicaments existants qui sont soient des anti viraux, soit des anti inflammatoires puissants. De plus la plupart de ces médicaments sont utilisés au quotidien dans leurs indications spécifiques, on connaît donc leur mode d'utilisation, les effets secondaires potentiels et la manière de les surveiller.On ne part pas l'aventure.Remarque : Durant tout le développement d’un médicament, la balance entre les bénéfices et les risques est constamment évaluée. Cette évaluation est d’abord réalisée en amont du lancement de l’essai, à partir des données préalablement acquises. Et elle l’est aussi au terme de l’essai : il faut alors déterminer si le médicament produit suffisamment de résultats positifs pour justifier sa mise sur le marché. Quant aux molécules déjà commercialisées pour un autre usage thérapeutique, elles doivent confirmer les bénéfices qu’elles peuvent apporter, pour ne pas exposer inutilement les patients à de potentiels effets indésirables : c’est ce que l’essai Discovery pour le COVID-19 cherche à établir par le biais d’un essai randomisé, en procédant à une répartition aléatoire de différents traitements.
Sources :
https://www.e-cancer.fr/Comprendre-prevenir-depister/Comprendre-la-recherche/A-quoi-sert-la-recherche/Les-essais-cliniques
https://theconversation.com/essais-cliniques-en-situation-de-pandemie-quelles-sont-les-regles-133730
- Les essais de phase I ont pour objectif d'évaluer la tolérance de l’organisme et la toxicité d’un tout nouveau traitement (c’est-à-dire l’ensemble des effets indésirables liés à son administration). Le but est de déterminer la dose recommandée pour l’administration de ce nouveau traitement. Le traitement évalué est donné à un petit nombre de malades (10 à 40). Pour le COVID - 19 ce n'est pas le cas car les molécules testées sont déjà utilisées et connues
- Les essais de phase IIprécisent l’activité clinique ou pharmacologique d'un traitement à la dose recommandée à l’issue de la phase I. Ils nécessitent en général l'inclusion de 40 à 80 malades. Pour le COVID - 19 ce n'est pas le cas car les molécules testées sont déjà utilisées et connues mais adapatation posologique vraisemblable
- Les essais de phase III sont des essais comparatifs . Ils permettent de comparer le nouveau traitement avec le traitement utilisé habituellement, dit "traitement de référence" ou "traitement standard", afin de déterminer son efficacité. Deux groupes de patients sont constitués par tirage au sort (randomisation), de manière à constituer des groupes homogènes et comparables (âge, sexe, caractéristiques de la maladie…) : l'un recevra le traitement de référence (dans ce cas le traitement classique de réanimation) , l'autre le nouveau traitement plus le traitement classique, ou un placebo .Dans certains cas, les patients ne sauront pas quel est le traitement reçu (traitement de référence ou nouveau traitement). On parle d’essai en aveugle. Il est dit "en double aveugle" lorsque ni le patient, ni le personnel soignant ne savent quel traitement est donné. Ce n'est donc pas le médecin qui décide de l'attribution de l'un ou l'autre des traitements à son patient. Quelque soit l'approche la comparaison est le princeps de base de tous les essais thérapeutiques, nul ne peut s'y soustraire.... comparer à rien c'est l'assurance de ne rien, trouver ni prouver...... sauf le parachute qui n'a pas fait l'objet d'un essai en double aveugle .....mais si ça vous dit, n'hésitez pas!
Ces essais nécessitent normalement l'inclusion d'un grand nombre de patients (plusieurs centaines ou milliers) pour établir une différence entre les traitements, mais face à l'urgence du COVID-19 ce n'est pas possible Pour ces essais ,les statisticiens calculent le nombre de patients à inclure pour avoir un résultat significatif. Lorsque l'on teste une nouvelle moécule, tout ce processus prend 10 ans. Dans le cas de l'urgence c'est évidemment impossible. Mais faire les choses "à l'envers" : NON, car alors on ne sait pas où on va, c'est imposible à évaluer. Nous parlons de traitements "lourds" sur un patient en détresse, qui peut décéder , il ne faut pas faire n'importe quoi, même si on est .......the best of the world, justement on montre le très bon exemple....à moins que je n'ai rien compris depuis le début, "à l'insu de mon plein gré".
#1MASQUEPOURTOUS, ça vous protège et ça protège les autres