llantyne C, Banka P, Mendez G, et al. Efficacy and safety of the oral PCSK9 inhibitor MK-0616: a phase 2b randomized controlled trial. J Am Coll Cardiol. null2023, 0 (0) .https://doi.org/10.1016/j.jacc.2023.02.018
Efficacité et sécurité de l'inhibiteur oral de PCSK9 MK-0616 : un essai contrôlé randomisé de phase 2b
file:///E:/Downloads/j.jacc.2023.02.018.pdf
Objectifs
Cet essai multicentrique de phase 2b, randomisé, en double aveugle, contrôlé par placebo (NCT05261126) visait à évaluer l'efficacité et l'innocuité du MK-0616 chez les participants atteints d'hypercholestérolémie.
Laboratoire MSD
Méthodes
Cette étude prévoyait d'inclure 375 participants adultes présentant un large éventail de risques d'ASCVD. Les participants ont été assignés au hasard (rapport 1:1:1:1:1) au MK-0616 (6, 12, 18 ou 30 mg QD) ou au placebo correspondant. Les principaux critères d'évaluation comprenaient la variation en pourcentage par rapport au départ du LDL-C à la semaine 8 et la proportion de participants présentant des événements indésirables (EI) et des interruptions d'intervention de l'étude en raison d'EI ; les participants ont été surveillés pour les EI pendant 8 semaines supplémentaires après la période de traitement.

Résultats
Sur les 381 participants randomisés, 49 % étaient des femmes et l'âge médian était de 62 ans. Parmi les 380 participants traités, toutes les doses de MK-0616 ont démontré des différences statistiquement significatives (p<0,001) dans le pourcentage de changement moyen LS du taux de LDL-C entre le départ et la semaine 8 par rapport au placebo : -41,2 % (6 mg), -55,7 % ( 12 mg), -59,1 % (18 mg) et -60,9 % (30 mg). Les EI sont survenus chez une proportion similaire de participants dans les bras MK-0616 (39,5 % à 43,4 %) et dans le groupe placebo (44,0 %). Des abandons en raison d'EI sont survenus chez 2 participants ou moins dans n'importe quel groupe de traitement.
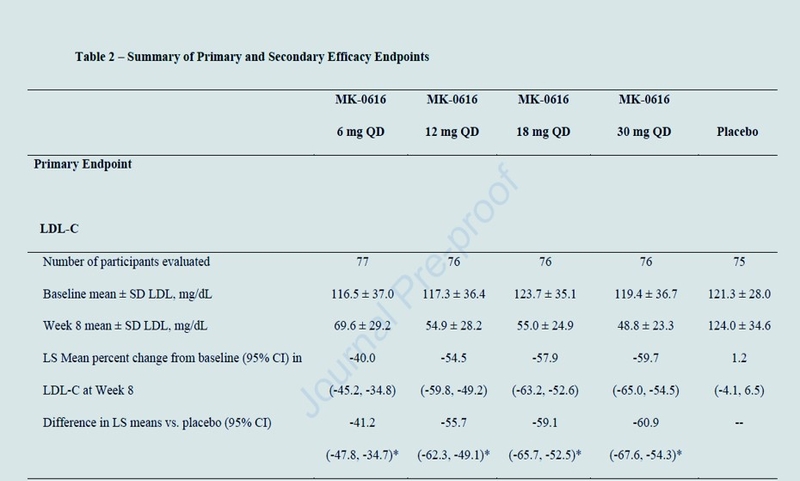
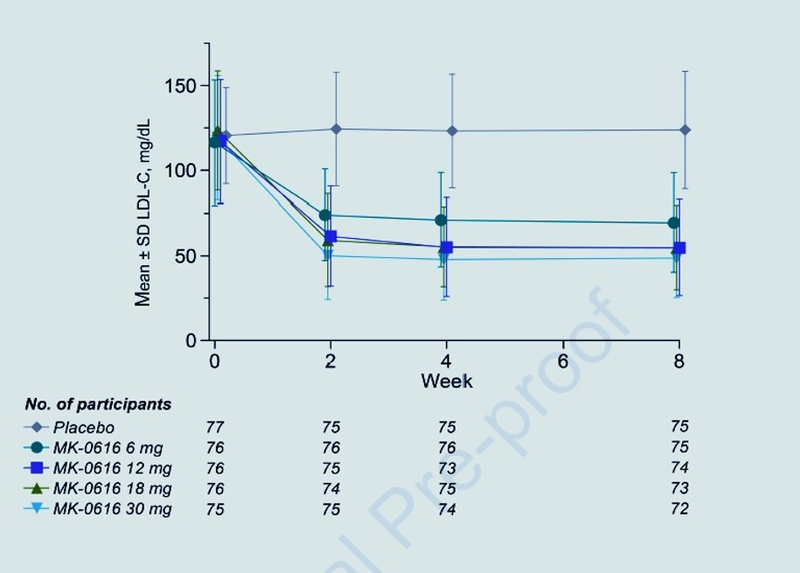
Conclusion
MK-0616 a démontré des réductions statistiquement significatives et robustes, dépendantes de la dose, du LDL-C à la semaine 8 allant jusqu'à 60,9 % par rapport au départ et a été bien toléré pendant 8 semaines de traitement et 8 semaines supplémentaires de suivi
Synthèse
Commentaire
Etude prometteuse, un avantage qui est aussi un inconvénient par rapport aux Anti PCSK9 . La voie orale c'est bien mais la voie injectable est un plus en ce qui concerne la compliance. Si la voie orale fait aussi bien que la voie injectable, leur coût respectif sera un élémént décisionnel important. Attendons les résultats de la phase 3, le suivi au long cours, nouvelle aventure pour la saga LDL.......


