- “Mon médecin m’a recommandé d’arrêter les petits dîners pour quatre. A moins qu’il n’y ait trois autres personnes.” Orson Welles
-
https://academic.oup.com/eurheartj/advance-article/doi/10.1093/eurheartj/ehae179/7738955#

A LIRE
Les maladies artérielles périphériques et aortiques (MAAP) sont très répandues et augmentent considérablement la mortalité et la morbidité cardiovasculaires (CV) dans la population générale, par conséquent, des stratégies de prévention intensives sont nécessaires.
Cependant, les patients atteints de MAAP sont généralement sous-diagnostiqués et sous-traités par rapport aux patients atteints de coronaropathie (CAD).
Les facteurs de risque courants de la MAAP coexistent souvent, ce qui nécessite une approche multidisciplinaire pour une prise en charge efficace.
Un diagnostic précoce est essentiel pour de meilleurs résultats. Ces lignes directrices abordent la MAAP, en mettant à jour et en fusionnant les lignes directrices de 2017 sur les maladies artérielles périphériques et de 2014 sur les maladies aortiques. L'accent est principalement mis sur les maladies artérielles athéroscléreuses, mais elles abordent également certaines maladies génétiques non athéroscléreuses. Bien qu'elles ne soient pas exhaustives, ces lignes directrices de 2024 offrent des conseils sur le diagnostic, la surveillance et le traitement. Un certain nombre de recommandations nouvelles et révisées sont résumées dans les tableaux 3 et 4 , respectivement. Les lecteurs doivent tenir compte des affections non athéroscléreuses et se référer à des documents spécifiques.
EXTRAITS en images.....
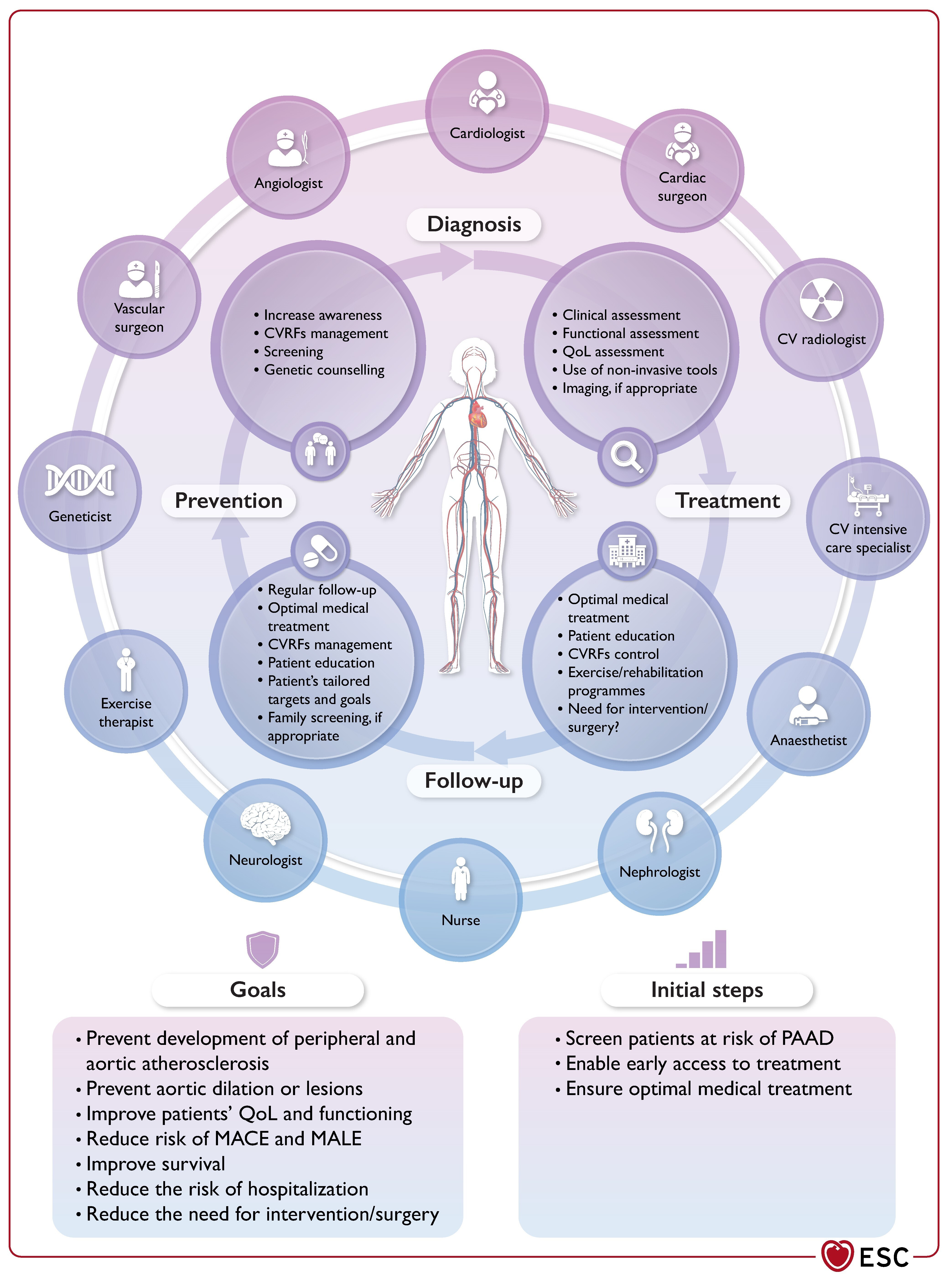
Illustration centrale : du diagnostic au traitement, une approche holistique et multidisciplinaire des maladies artérielles et aortiques périphériques.
CV, cardiovasculaire ; CVRF, facteurs de risque cardiovasculaire ; MACE, événement cardiaque indésirable majeur ; MALE, événement indésirable majeur des membres ; PAAD, maladies artérielles et aortiques périphériques ; QoL, qualité de vie.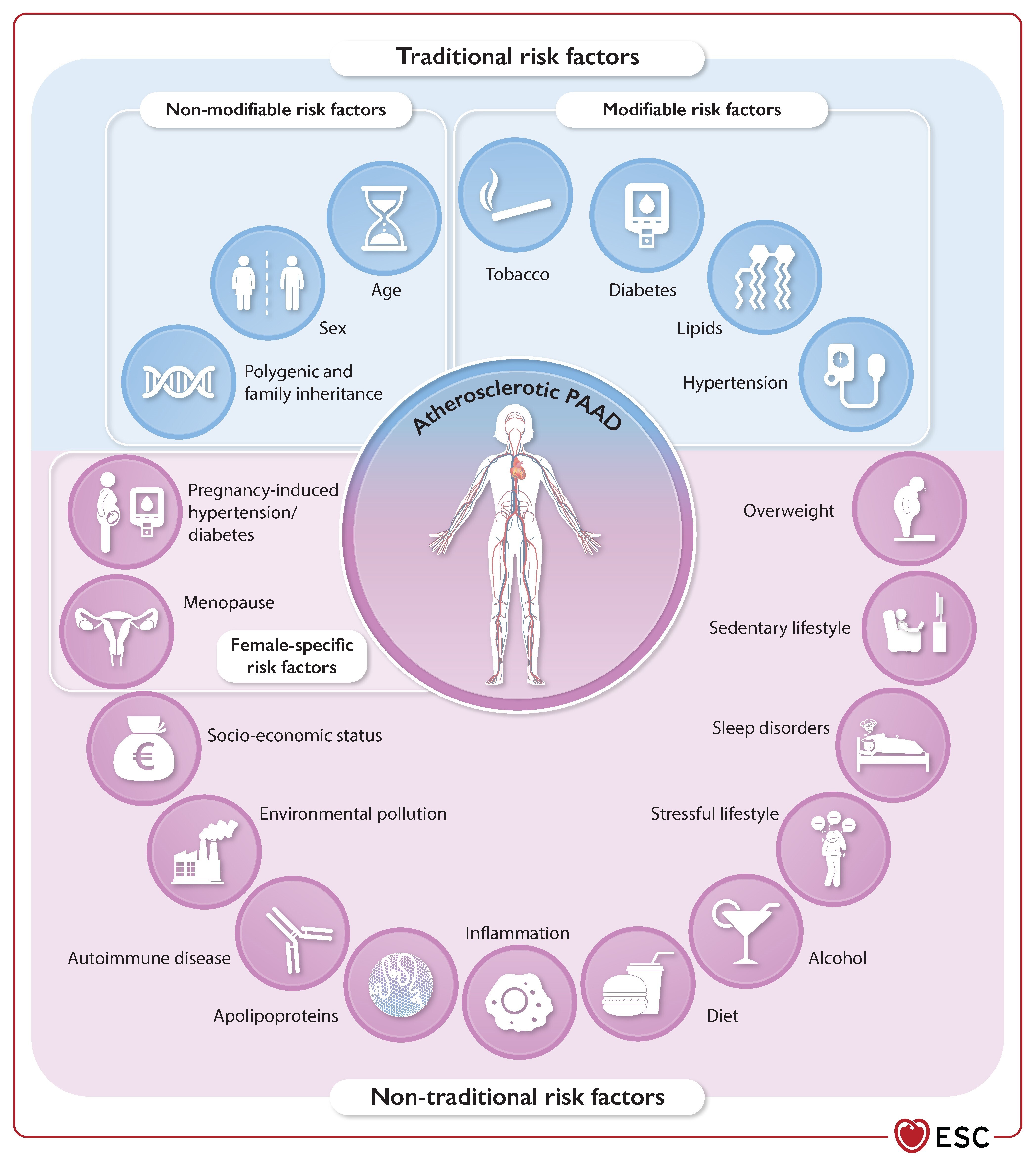
Principaux facteurs de risque associés à l'athérosclérose dans les maladies artérielles et aortiques périphériques.
PAAD, maladies artérielles et aortiques périphériques.
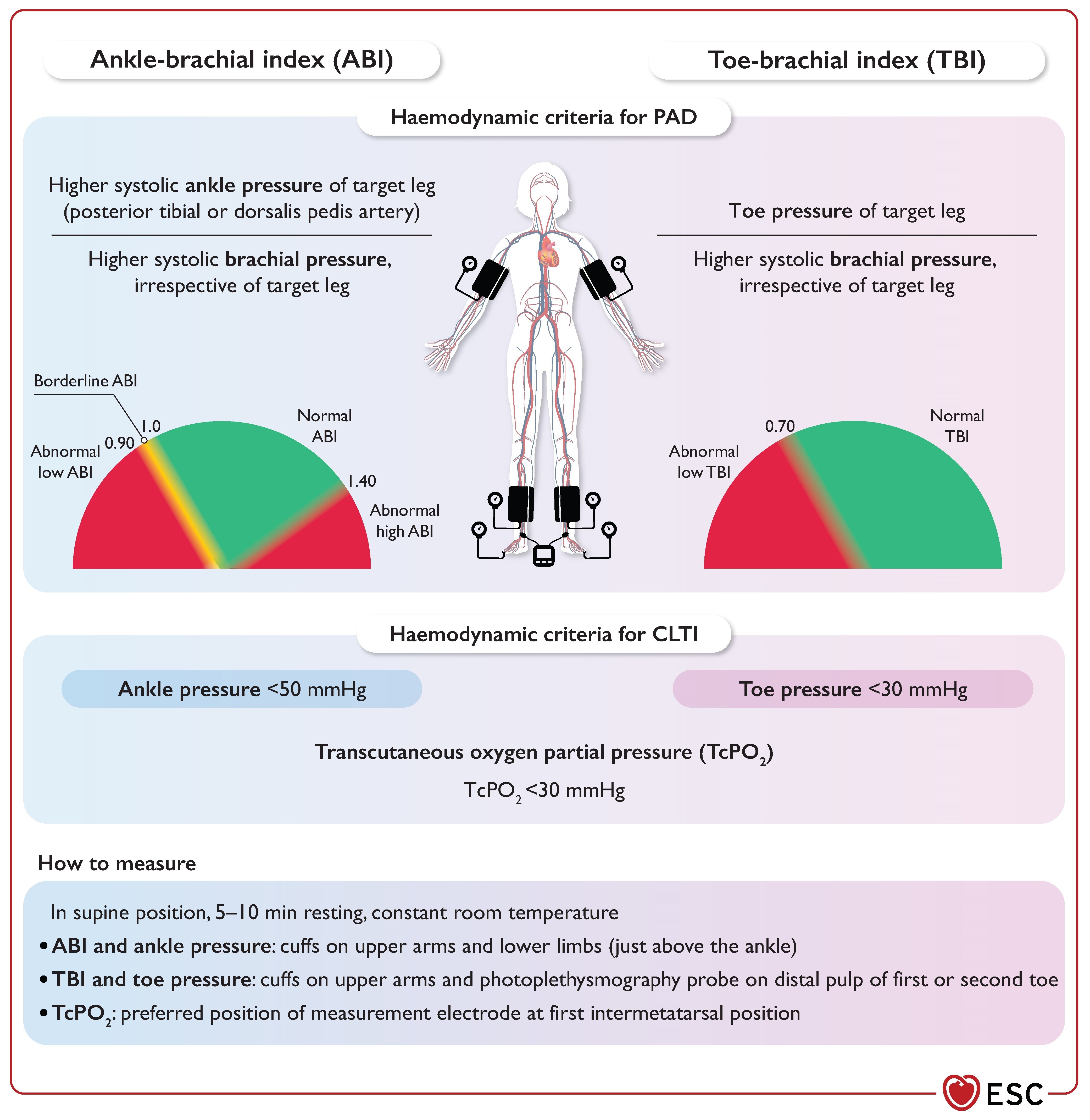
Évaluation hémodynamique de la maladie artérielle périphérique.
ABI, index cheville-bras ; CLTI, ischémie chronique menaçant les membres ; MAP, maladie artérielle périphérique ; TBI, index orteil-bras ; TcPO 2 , pression transcutanée d'oxygène
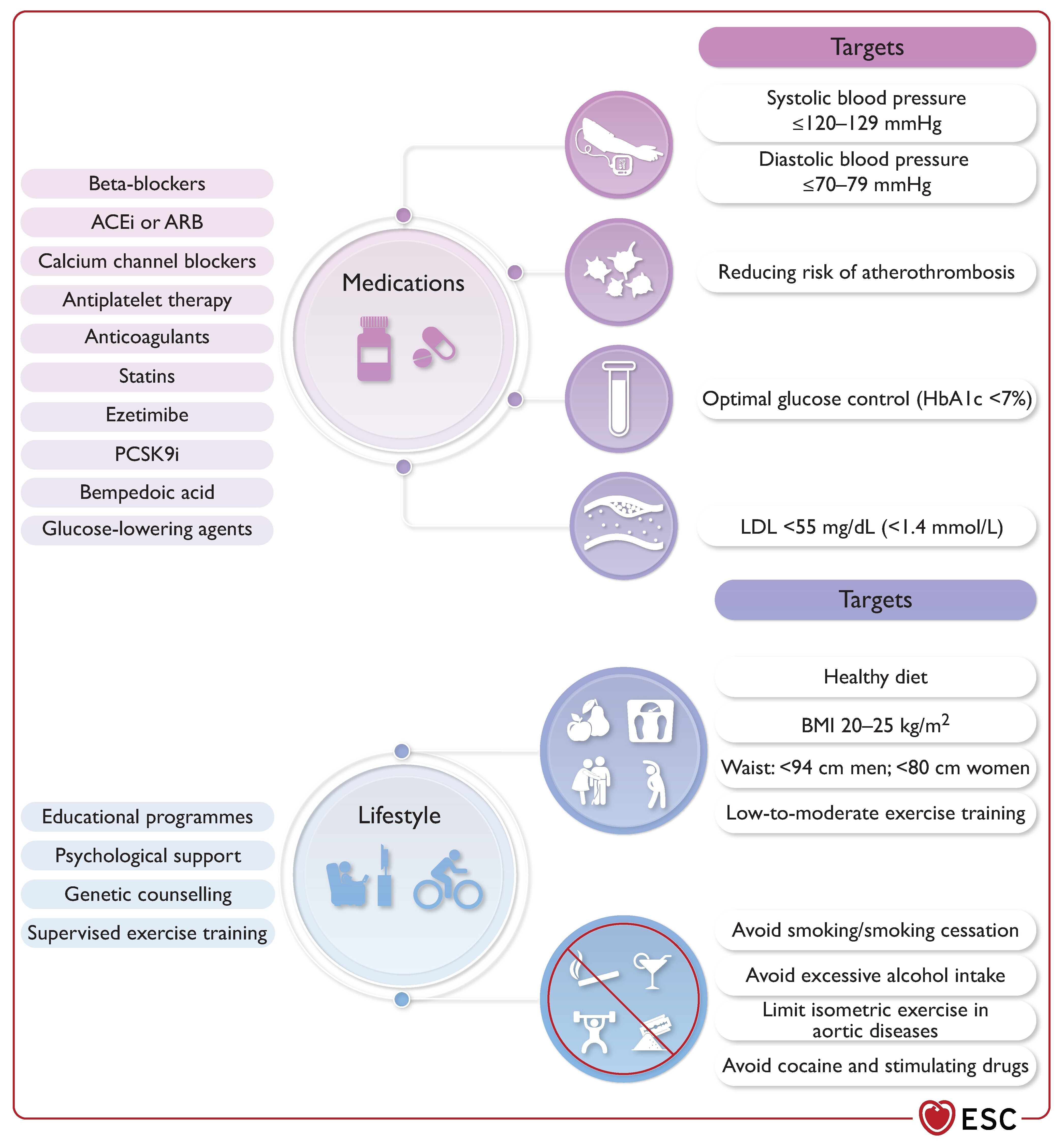
Modification du risque cardiovasculaire et interventions et objectifs en matière de mode de vie sain chez les patients atteints de maladies artérielles et aortiques périphériques.
IEC, inhibiteurs de l'enzyme de conversion de l'angiotensine ; ARA, bloqueur des récepteurs de l'angiotensine ; IMC, indice de masse corporelle ; LDL, lipoprotéines de basse densité ; PCSK9i, inhibiteur de la proprotéine convertase subtilisine/kexine de type 9 ; HbA1c, hémoglobine glyquée.
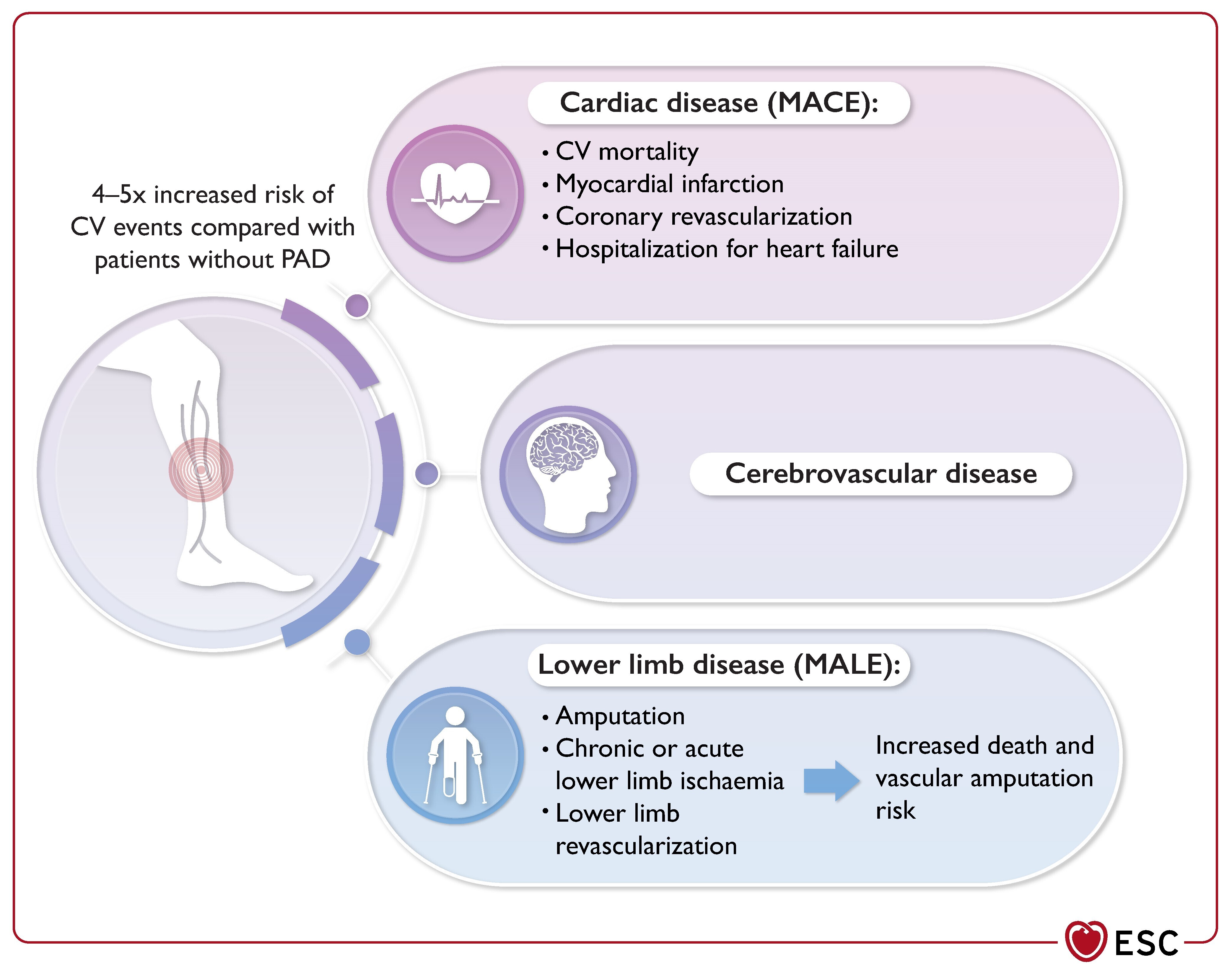
Risque cardiovasculaire chez les patients atteints d'une maladie artérielle périphérique.
CV, cardiovasculaire ; MACE, événement cardiaque indésirable majeur ; MALE, événement indésirable majeur des membres ; MAP, maladie artérielle périphérique.
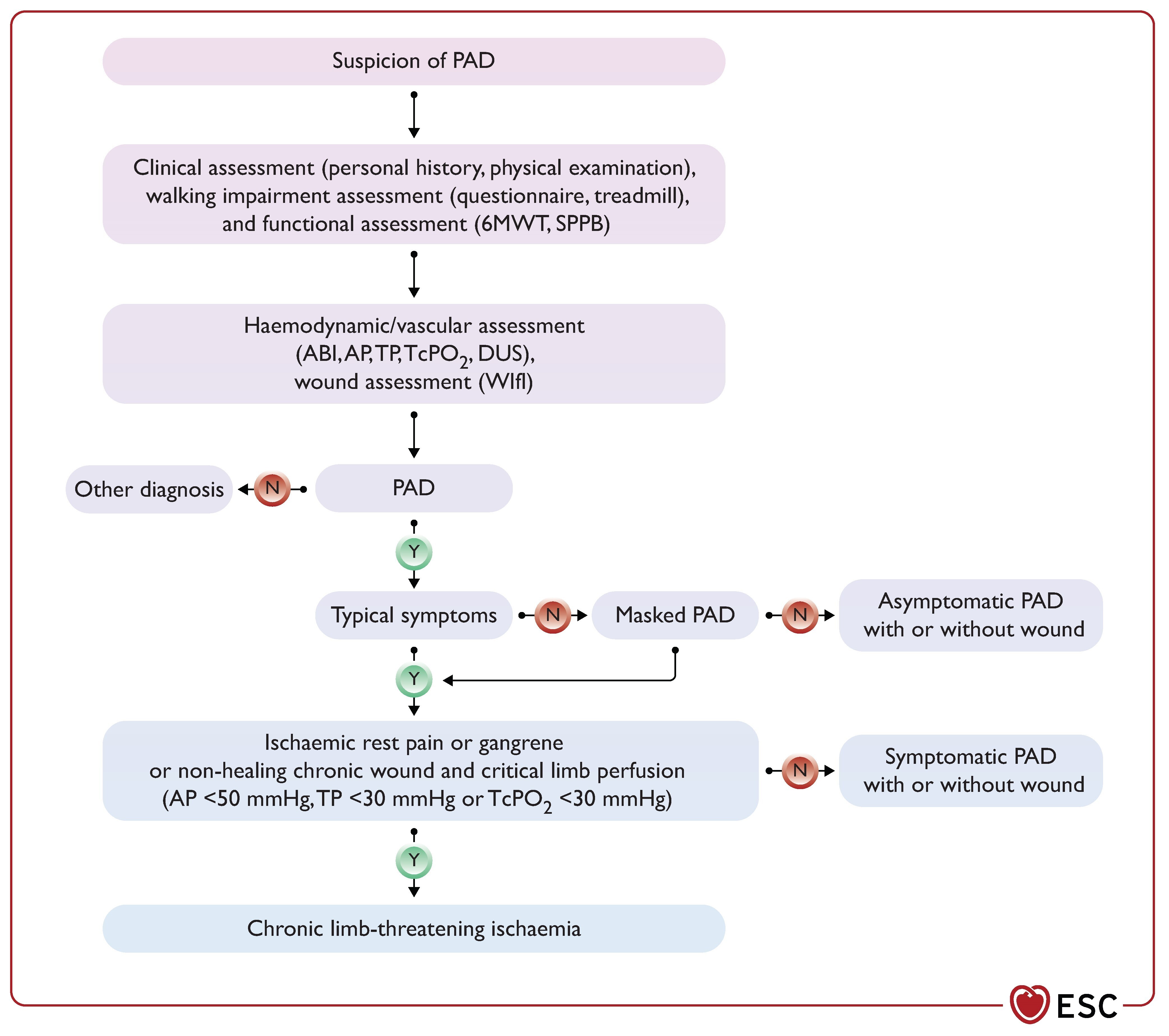
Algorithme de diagnostic de la maladie artérielle périphérique.
6MWT, test de marche de six minutes ; ABI, index cheville-bras ; AP, pression à la cheville ; DUS, échographie duplex ; PAD, maladie artérielle périphérique ; SPPB, batterie de performance physique courte ; TcPO 2 , pression transcutanée d'oxygène ; TP, pression aux orteils ; WIfI, classification des plaies, des ischémies et des infections du pied.
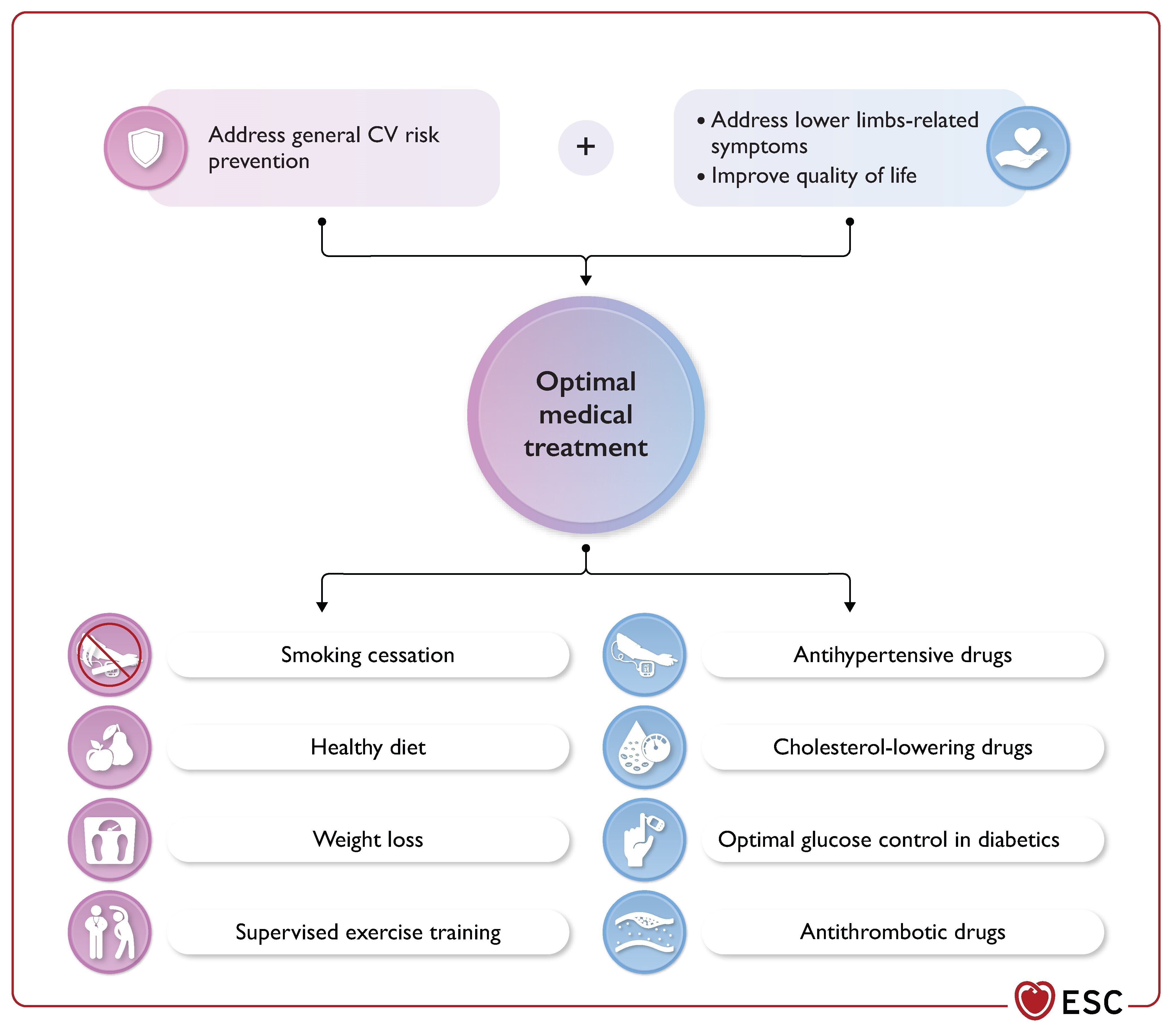
Traitement médical optimal chez les patients atteints d'une maladie artérielle périphérique.
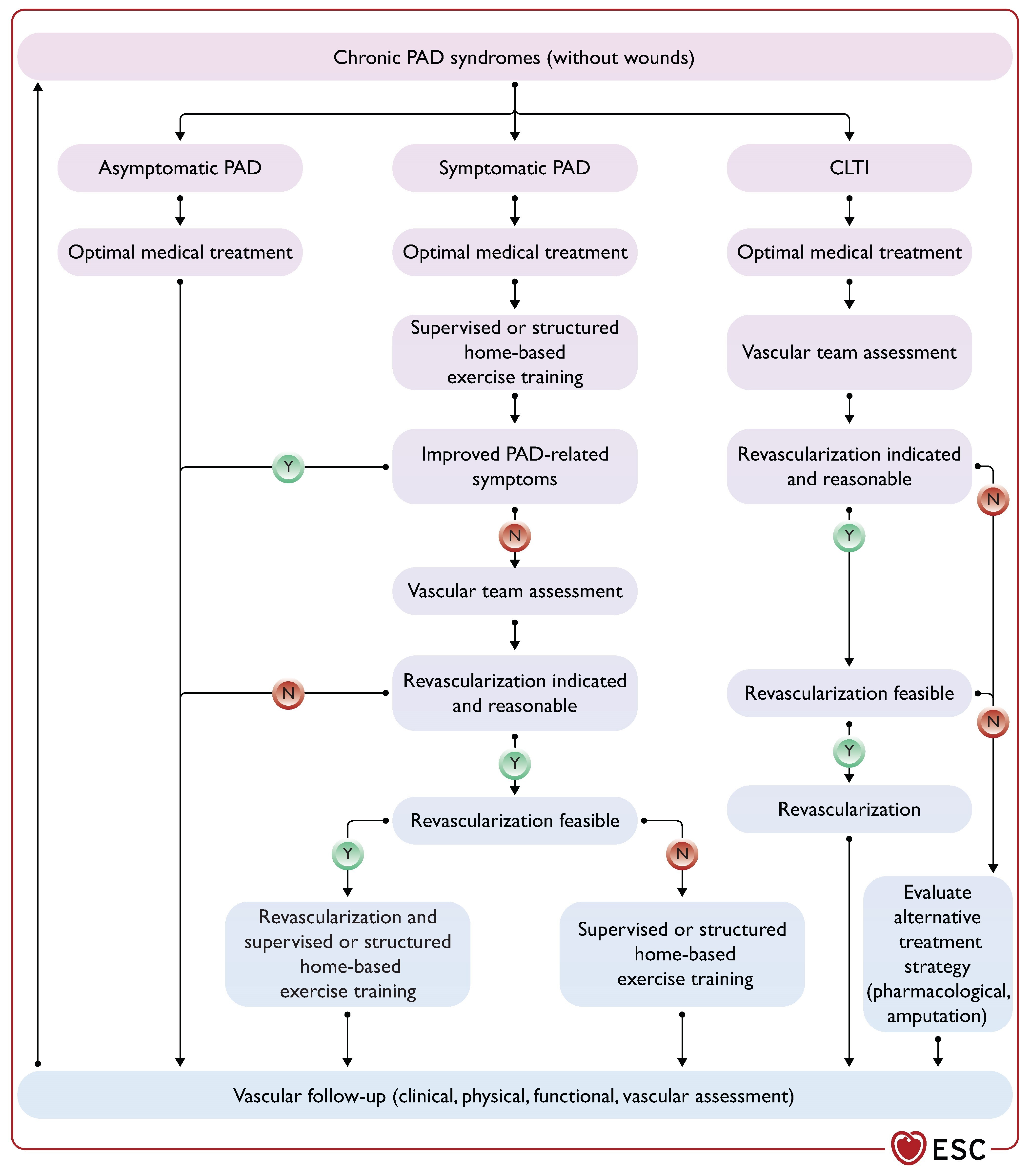
Algorithme de traitement de la maladie artérielle périphérique sans plaies.
CLTI, ischémie chronique menaçant les membres ; MAP, maladie artérielle périphérique.
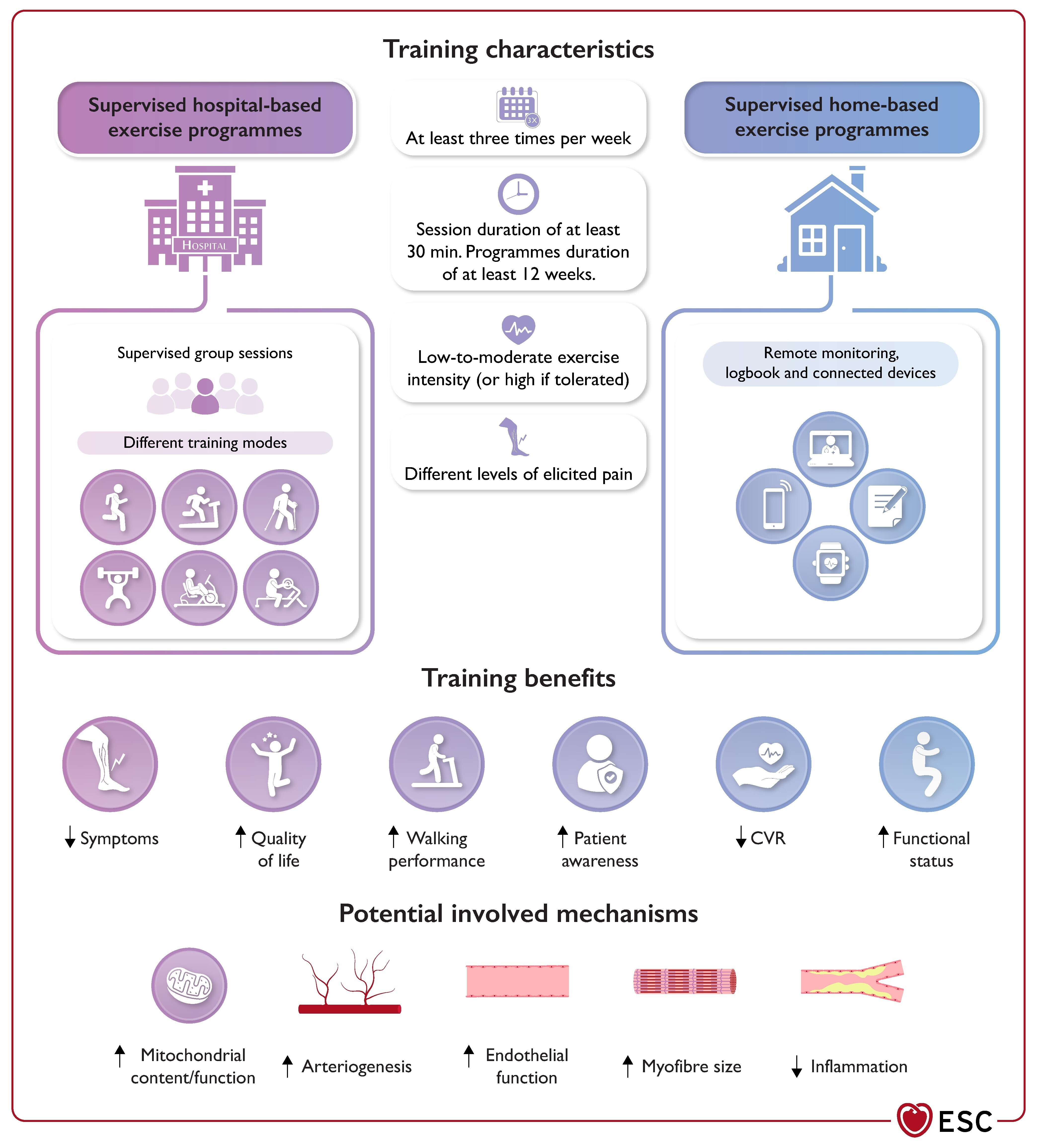
Caractéristiques et avantages de l’entraînement physique chez les patients atteints d’une maladie artérielle périphérique.
RVC, risque cardiovasculaire.
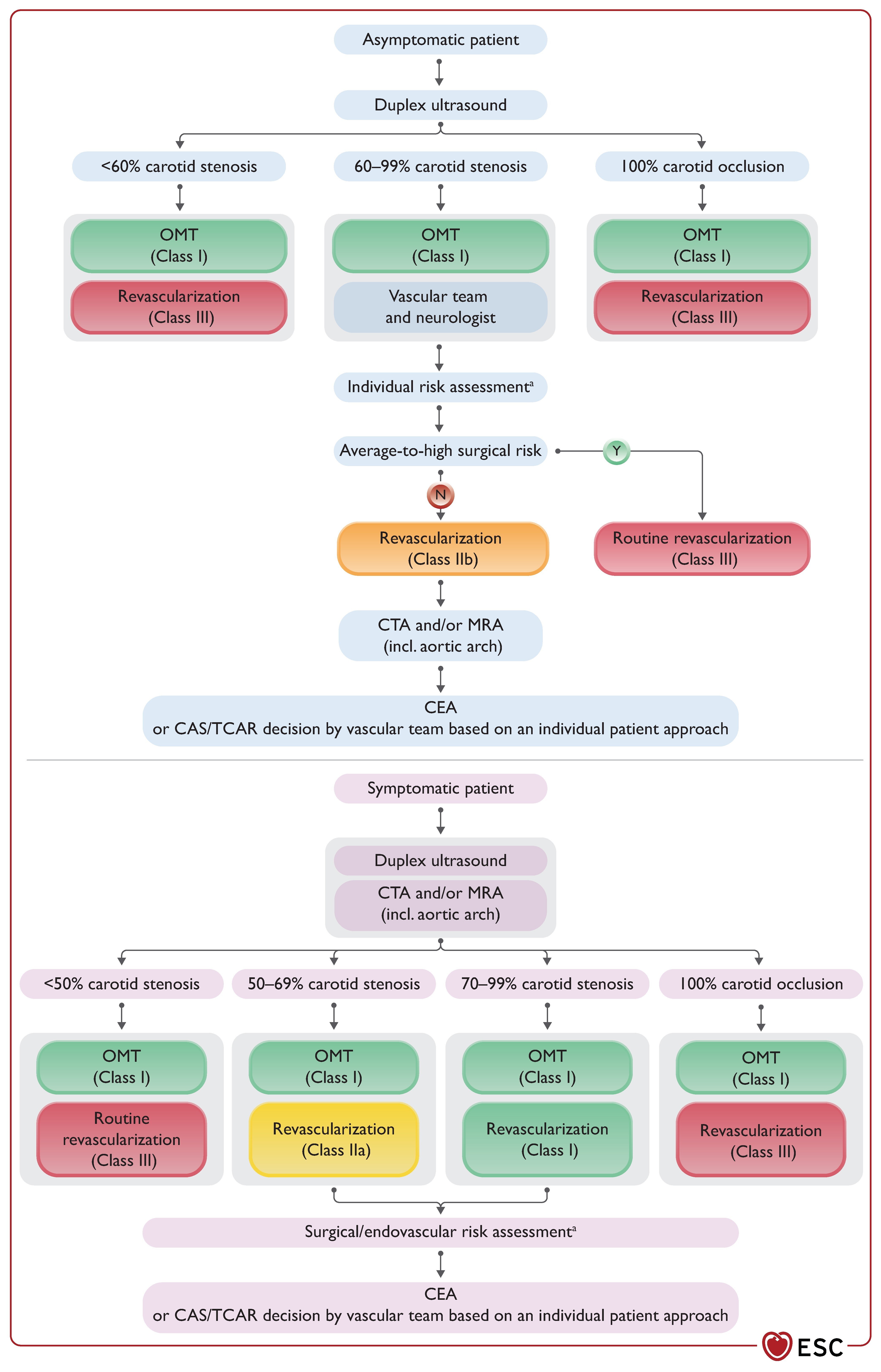
Algorithme de gestion de la sténose de l'artère carotide.
CAS, stenting de l'artère carotide ; CEA, endartériectomie carotidienne ; CTA, angiographie par tomodensitométrie ; ARM, angiographie par résonance magnétique ; OMT, traitement médical optimal ; TCAR, revascularisation de l'artère transcarotide ; AIT, accident ischémique transitoire. a Évaluer la présence de caractéristiques à haut risque conformément au Tableau 11. Si une intervention chirurgicale/revascularisation est envisagée, évaluer le risque global lié à l'intervention chirurgicale
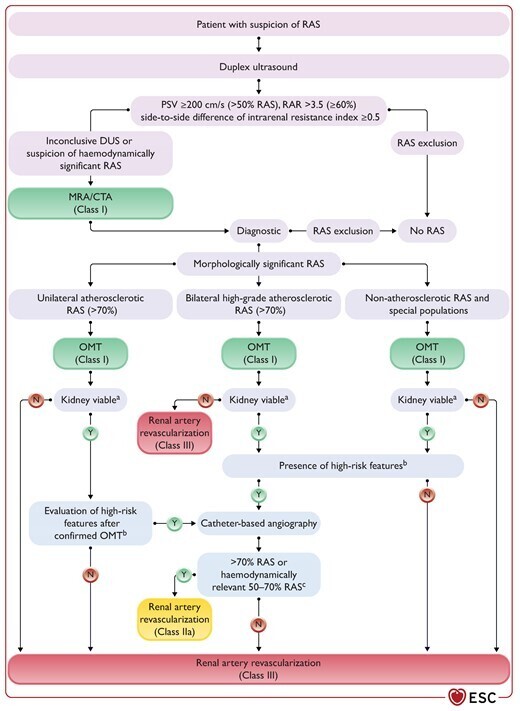
Algorithme de diagnostic et de traitement de la sténose de l'artère rénale.
CTA, angiographie par tomodensitométrie ; ARM, angiographie par résonance magnétique ; OMT, traitement médical optimal ; Pd/Pa, rapport pression coronaire distale/pression aortique ; PSV, vitesse systolique de pointe ; RAR, rapport vitesse de débit de pointe rénal-aortique ; RAS, sténose de l'artère rénale.
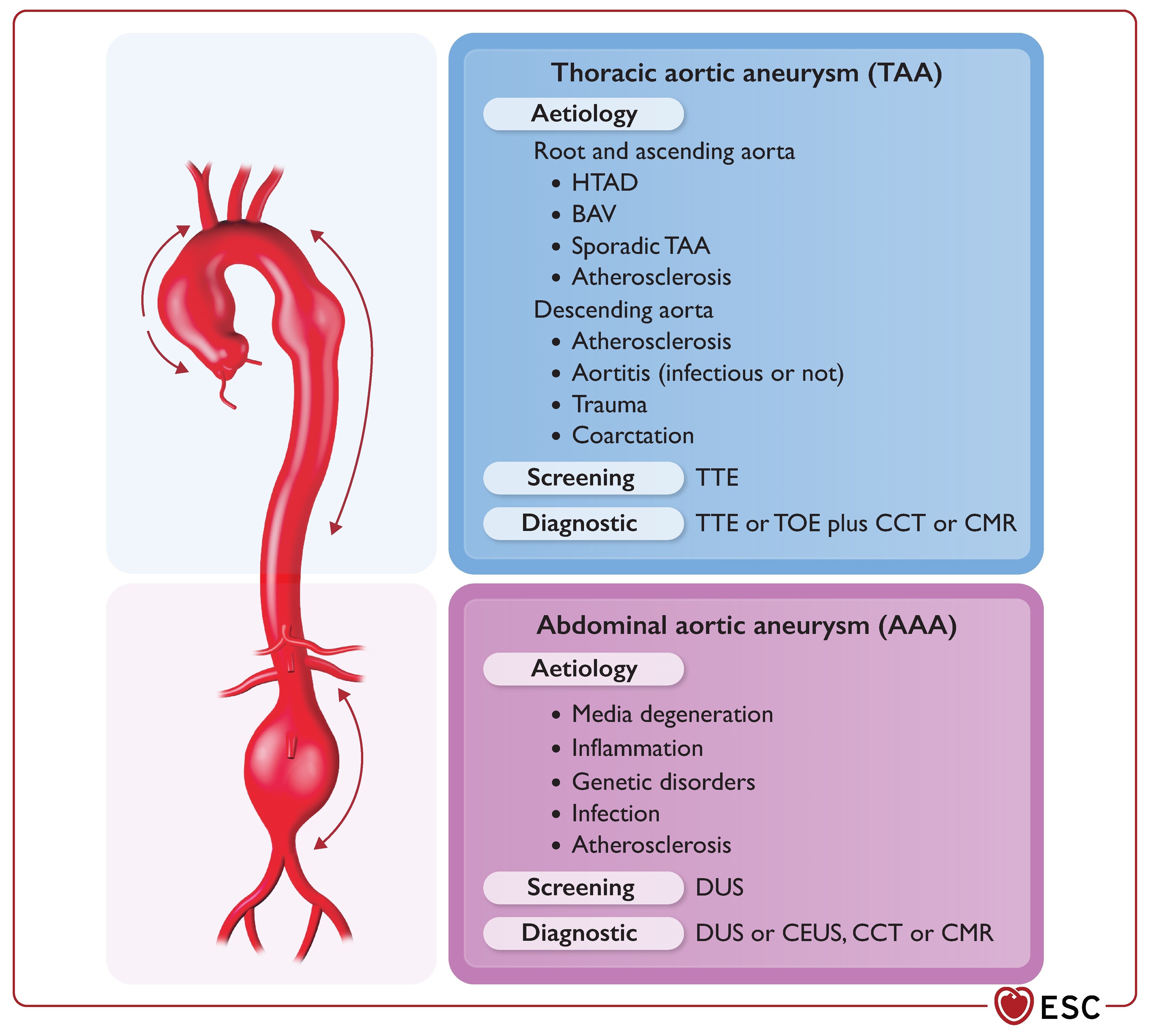
Anévrismes de l'aorte thoracique et abdominale : étiologie, dépistage et méthodes diagnostiques.
AAA, anévrisme de l'aorte abdominale ; BAV, valve aortique bicuspide ; CCT, tomodensitométrie cardiovasculaire ; CEUS, échographie Doppler avec contraste ; CMR, résonance magnétique cardiovasculaire ; DUS, échographie Doppler ; HTAD, maladie aortique thoracique héréditaire ; TAA, anévrisme de l'aorte thoracique ; ETO, échocardiographie transoesophagienne ; TTE, échocardiographie transthoracique.
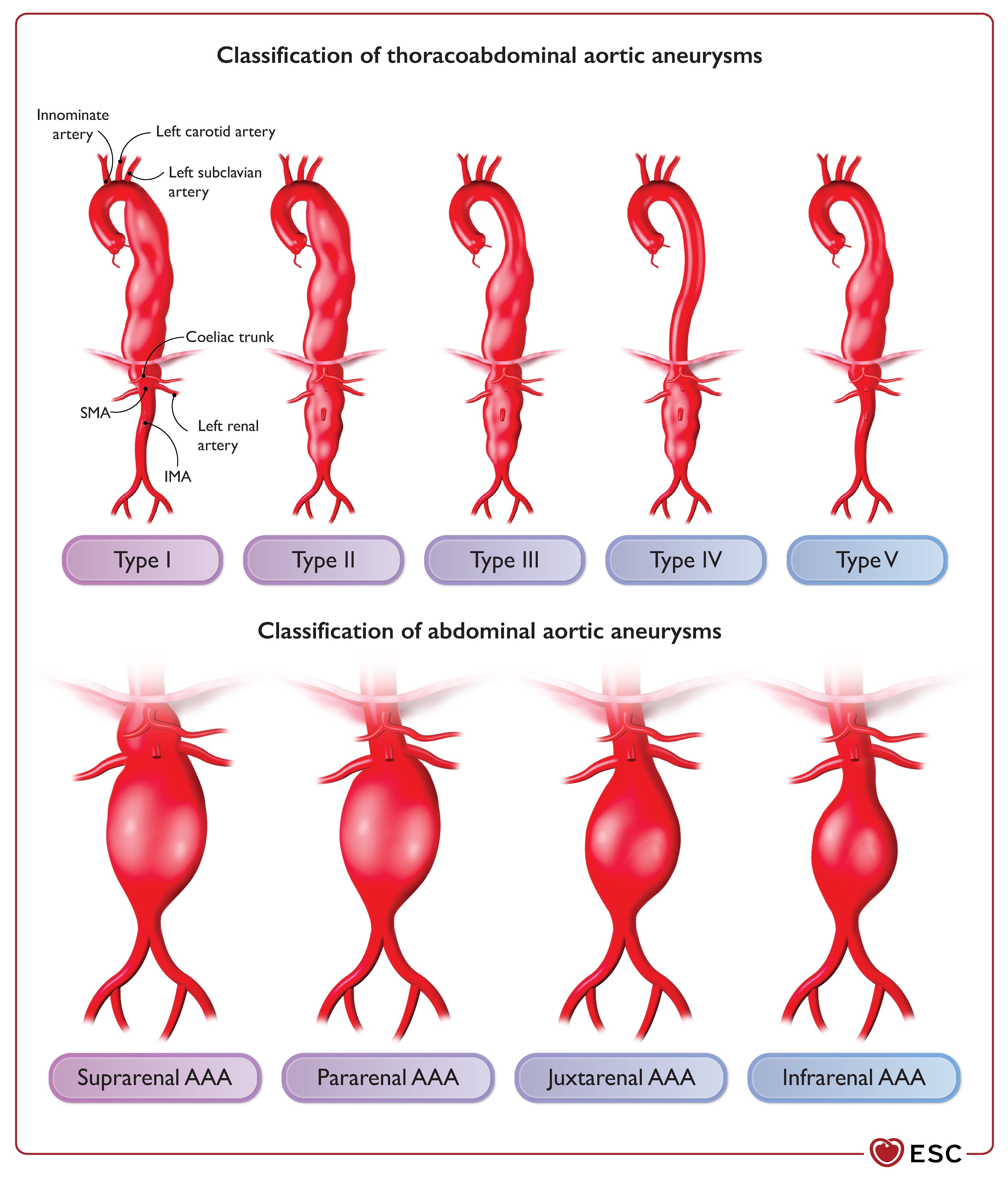
Classification des anévrismes de l'aorte thoraco-abdominale 900 et abdominale.
AAA, anévrisme de l'aorte abdominale ; IMA, artère mésentérique inférieure ; SMA, artère mésentérique supérieure.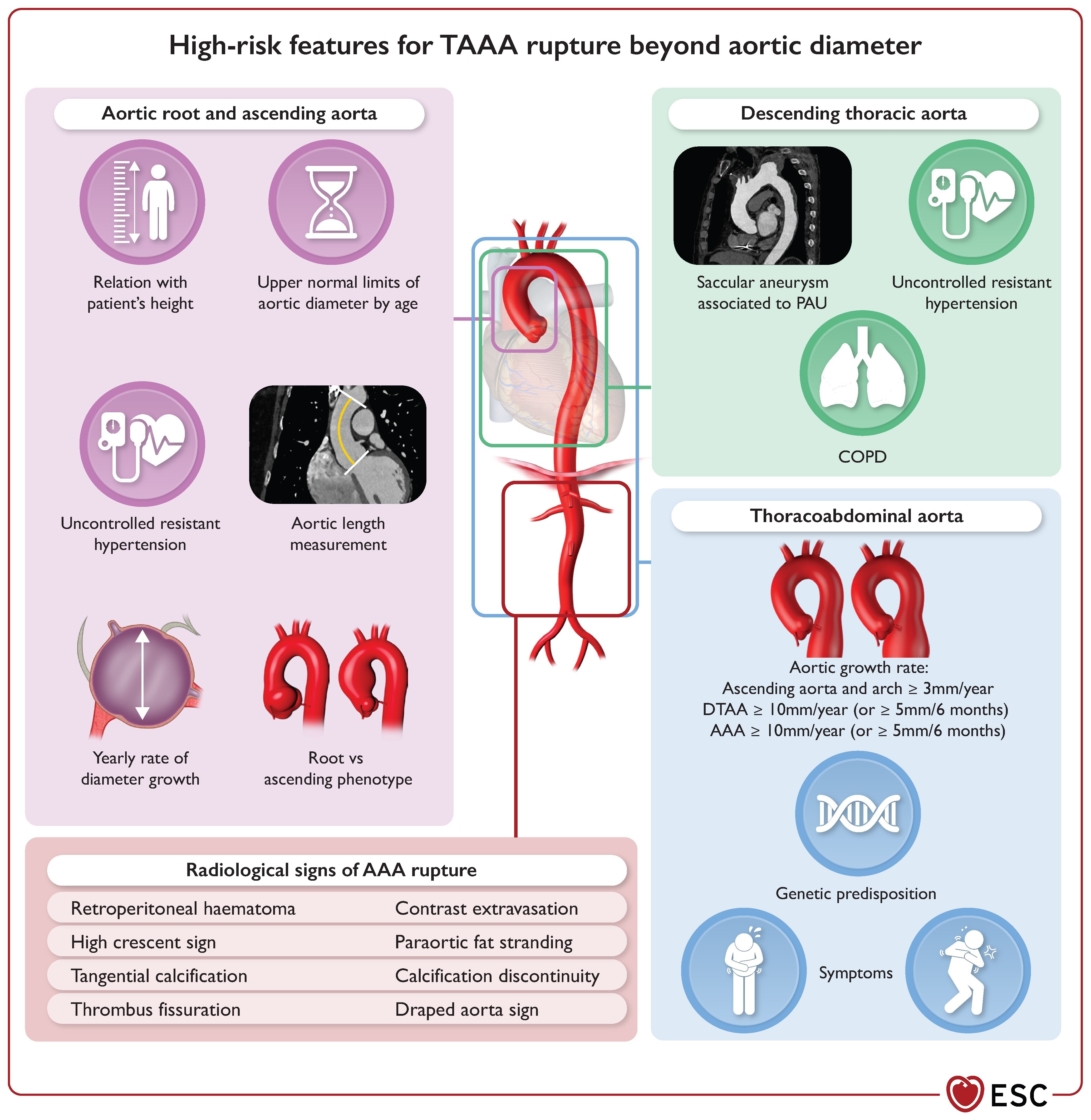
Facteurs de risque de rupture d'anévrisme thoracique et abdominal.
AAA, anévrisme de l'aorte abdominale ; BPCO, maladie pulmonaire obstructive chronique ; AATD, anévrisme de l'aorte thoracique descendante ; UAP, ulcère athéroscléreux pénétrant ; AAAT, anévrisme de l'aorte thoraco-abdominale
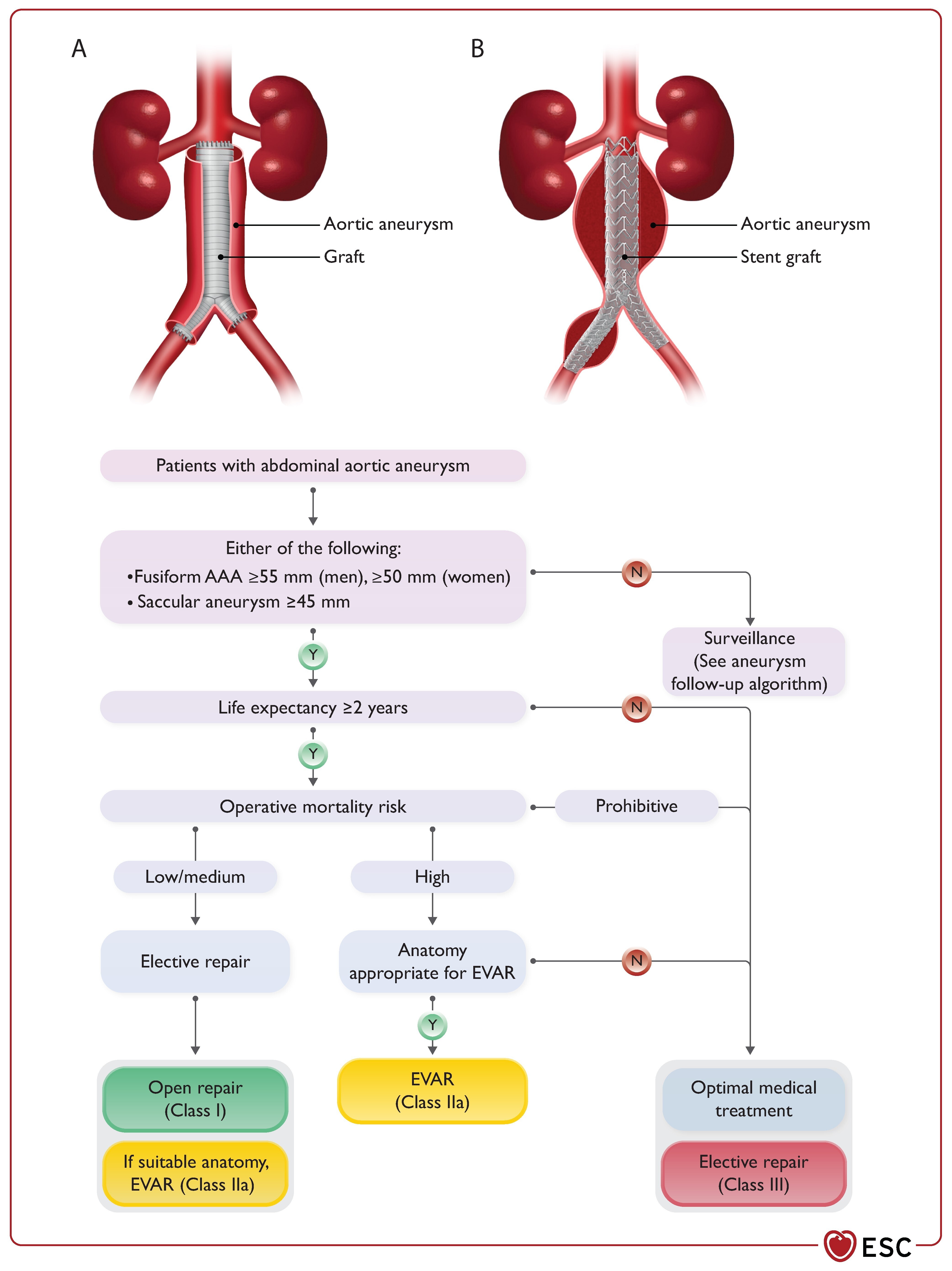
Algorithme pour le processus de prise de décision individuelle dans le traitement des patients atteints d'anévrisme de l'aorte abdominale.
( A ) Illustration d'une réparation ouverte (greffe). ( B ) Illustration d'un traitement endovasculaire (EVAR). AAA, anévrisme de l'aorte abdominale ; EVAR, réparation endovasculaire de l'anévrisme de l'aorte.
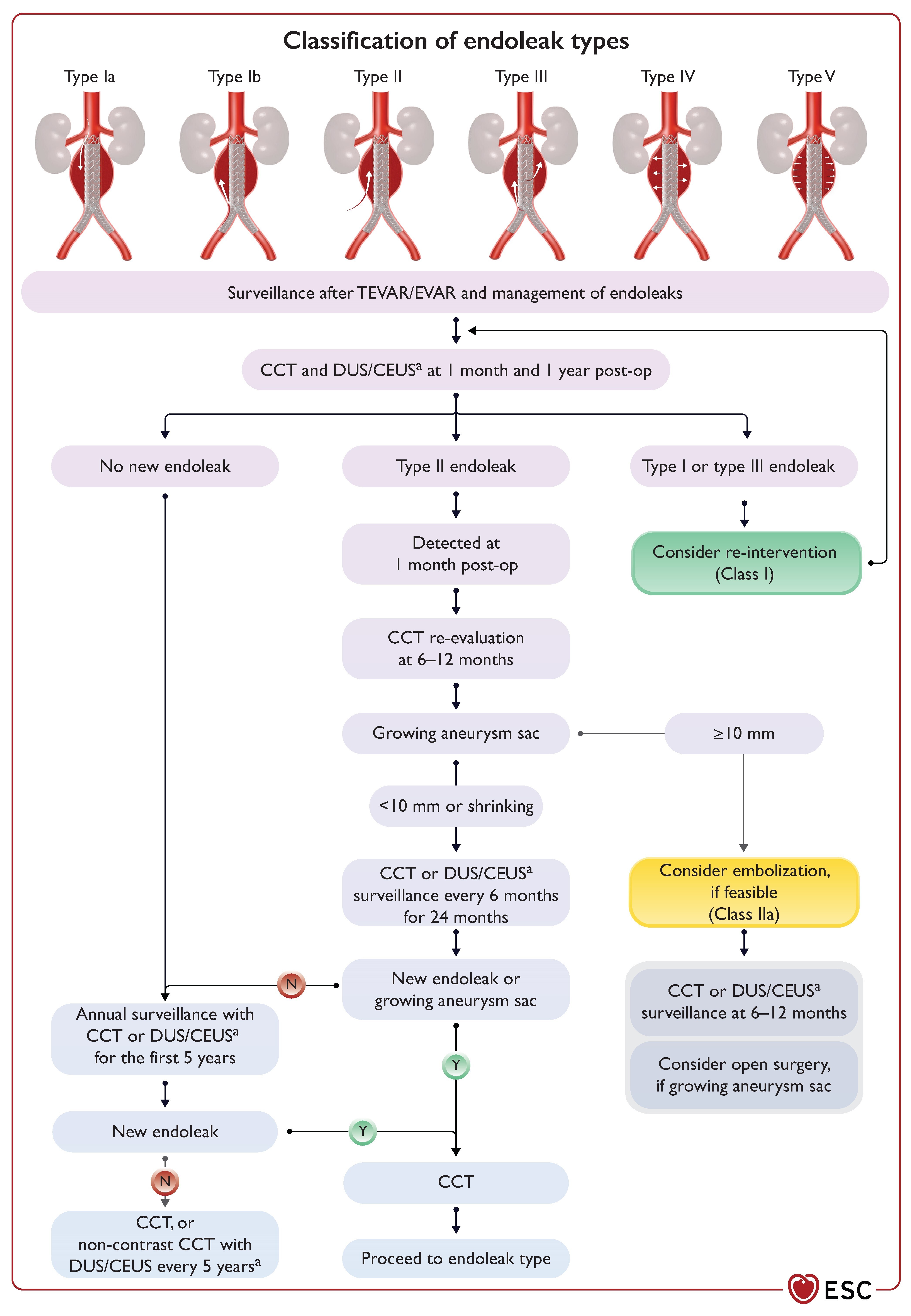
Algorithme de suivi après réparat ion endovasculaire d'un anévrisme de l'aorte thoracique, et gestion des endofuites et leur classification.
CEUS, échographie avec contraste ; CCT, tomodensitométrie cardiovasculaire ; DUS, échographie duplex ; TEVAR, réparation endovasculaire de l'anévrisme de l'aorte thoracique ; EVAR : réparation endovasculaire de l'aorte. a Dans les cas de TEVAR, la CCT est la technique d'imagerie préférée car la DUS/CEUS ne permet pas l'évaluation correcte de l'aorte thoracique. En cas d'insuffisance rénale, la CCT sans contraste est une bonne alternative pour surveiller la croissance du sac anévrismal et est associée à la DUS/CEUS pour la surveillance de l'EVAR. Les endofuites sont classées en cinq types : Type Ia, endofuite au site d'attache proximal ; Type Ib, endofuite au site d'attache distal ; Type II, remplissage du sac anévrismal par des vaisseaux ramifiés de l'aorte ; Type III, défaut de greffe ou mauvais alignement des composants ; Type IV, fuite à travers la paroi de la greffe attribuable à la porosité de l'endoprothèse ; et Type V ; causée par une « endotension », résultant peut-être de la pression aortique transmise par le greffon/thrombus au sac anévrismal. Adapté de Rokosh et al. avec permission
Les maladies artérielles périphériques et aortiques sont très répandues, souvent asymptomatiques et associées à une augmentation de la morbidité et de la mortalité. Un diagnostic précoce est essentiel pour de meilleurs résultats et la prise en charge nécessite une équipe multidisciplinaire. Le contrôle de la CVRF est essentiel pour prévenir la progression et les complications. Malgré les avantages du traitement médical, les changements de mode de vie, une alimentation saine, l'abstinence de tabac, l'exercice/la rééducation et l'éducation sont essentiels pour une prise en charge efficace. L'autonomisation des patients est essentielle pour améliorer l'observance et une surveillance étroite/régulière est essentielle pour améliorer le pronostic. L'utilisation de calculateurs en ligne ou sur application pour l'estimation du risque CV dans la prévention secondaire des ASCVD peut aider à motiver les patients à modifier leur mode de vie et à adhérer au traitement.
Artères périphériques
L’AOMI athéroscléreuse des membres inférieurs est une maladie chronique nécessitant un suivi à vie.
L’évaluation des troubles de la marche, de l’état fonctionnel et du risque d’amputation est essentielle dans la prise en charge de l’AOMI.
L'index cheville-bras doit être le test diagnostique initial pour le dépistage et le diagnostic de l'AOMI et sert de marqueur de substitution pour la mortalité CV et toutes causes confondues. L'imagerie par résonance magnétique (DUS) est la méthode d'imagerie de première intention pour confirmer les lésions de l'AOMI.
L'entraînement physique supervisé ou, à défaut, l'électrostimulation HBET, améliorent la marche et les performances fonctionnelles et réduisent le risque cardiovasculaire. L'entraînement physique reste sous-utilisé et une sensibilisation accrue est nécessaire.
Chez les patients atteints d'AOMI asymptomatique, la revascularisation n'est pas recommandée. Chez les patients atteints d'AOMI symptomatique, la nécessité d'un traitement interventionnel, après une période de traitement médical optimal et d'exercice, doit être discutée dans un cadre multidisciplinaire.
L'ischémie chronique menaçant les membres augmente le risque d'événements CV et nécessite un diagnostic précoce, une orientation rapide vers une équipe vasculaire multidisciplinaire et une revascularisation pour sauver le membre.
L'ischémie aiguë des membres nécessite une évaluation clinique rapide par une équipe vasculaire et une revascularisation urgente.
L'échographie duplex est la modalité diagnostique de première intention pour la sténose carotidienne. Une revascularisation systématique n'est pas recommandée en cas de sténose asymptomatique. Chez les patients symptomatiques, une évaluation multidisciplinaire est recommandée.
L'UEAD athérosclérotique est le plus souvent localisée dans l'artère sous-clavière et peut être suspectée en raison d'une différence absolue de PAS inter-bras > 10–15 mmHg. L'échographie endoscopique est l'imagerie de première intention et une revascularisation systématique n'est pas recommandée.
La clé du diagnostic précoce de l'ischémie mésentérique aiguë et chronique est un niveau élevé de suspicion clinique, les tests de laboratoire n'étant pas fiables pour le diagnostic. L'occlusion aiguë de l'AMS nécessite une revascularisation immédiate.
Aorte
Les anévrismes de l'aorte sont gérés en fonction de leur taille, de leur localisation et de leur taux de croissance. Les petits anévrismes sont surveillés régulièrement (les directives fournissent des algorithmes de suivi spécifiques à la maladie), tandis que les plus gros peuvent nécessiter une réparation chirurgicale/endovasculaire pour éviter leur rupture.
Dans les anévrismes de la racine aortique, le remplacement aortique peut être envisagé à > 52 mm chez les patients à faible risque et dans les centres expérimentés.
Le diamètre aortique est le principal facteur de risque des événements aortiques. Cependant, des données probantes soutiennent l'indexation du diamètre (en particulier dans les populations de BSA extrêmes) et l'utilisation de la longueur aortique (> 11 cm), de l'IAH (> 32,1 mm/m), du taux de croissance (≥ 3 mm par an pour l'aorte ascendante et l'arche ou > 5 mm tous les 6 mois dans l'aorte thoraco-abdominale) et de l'âge/sexe pour l'évaluation du risque.
La collaboration multidisciplinaire, les salles d’opération hybrides et la technologie avancée des stents ont augmenté l’adoption d’approches hybrides et de thérapies endovasculaires pour différentes maladies de l’aorte thoraco-abdominale.
La prise en charge du syndrome aortique aigu implique un traitement médical dans des unités de soins intensifs et une intervention chirurgicale sélective en fonction de la localisation et des complications. Le principal problème dans ces pathologies reste le retard dans le diagnostic des patients ou leur transfert vers un centre aortique. L'amélioration des algorithmes de diagnostic et la réduction des complications chirurgicales ont permis de réduire les taux de mortalité. Un traitement chirurgical/endovasculaire en phase subaiguë est recommandé pour les patients à haut risque atteints du syndrome aortique de type B.
Les pathologies génétiques aortiques suspectées doivent être évaluées dans des centres expérimentés afin d'évaluer à la fois le patient et ses FDR pour des études génétiques. Les pathologies génétiques aortiques doivent être envisagées en fonction des antécédents familiaux, des caractéristiques syndromiques, de l'âge < 60 ans et de l'absence de FRVC (les lignes directrices proposent un algorithme de dépistage des maladies de l'aorte thoracique). Une évaluation complète de l'ensemble de l'aorte et d'autres territoires vasculaires est recommandée dans le cadre du DHTA. Les progrès récents en génétique permettent une évaluation personnalisée et centrée sur le patient. Cela comprend l'utilisation de différents seuils de diamètre aortique pour indiquer une intervention chirurgicale et la mise en œuvre de divers algorithmes de surveillance.
Un manque importante , la place l'IA demain dans les pathologies décrites, il aurait été judicieux d'anticiper........
Ces recommandations sont cependant hypercomplètes à lire en prenant son temps, lecture passionnante
Bravo aux autrices et auteurs et à Lucia Mazzolai aux commandes
Références complètes : texte, slide set et appli
https://www.escardio.org/Guidelines/Clinical-Practice-Guidelines/Peripheral-Arterial-and-Aortic-Diseases
1598 références bibliographiques
A SUIVRE.......

