Spécial RPTH
“La science n'a pas de patrie " Louis Pasteur
ARTICLE 1
Patients with myeloproliferative neoplasms and COVID-19 have increased rates of arterial thrombosis, Orly Leiva et Coll, Res Pract Thromb Haemost.
Les patients atteints de néoplasmes myéloprolifératifs et de COVID-19 ont des taux accrus de thrombose artérielle
2022;6:e12752,https://onlinelibrary.wiley.com/doi/epdf/10.1002/rth2.12752
Article Libre d'Accès
L'Essentiel
Les néoplasmes myéloprolifératifs (MPN) sont associés à une inflammation et à un risque de coagulation.
Le COVID-19 est également associé à une augmentation de la coagulation et de l'inflammation.
Notre étude visait à comparer l'incidence de la coagulation et du décès chez les patients atteints de COVID-19 avec NMP.
Les anomalies de la coagulation et la coagulopathie sont reconnues comme des conséquences de l'infection par le coronavirus 2 du syndrome respiratoire aigu sévère et de la maladie à coronavirus 2019 (COVID-19) qui en résulte. Plus précisément, la thromboembolie veineuse (TEV) a été signalée comme une complication fréquente. Au 27 mai 2021, au moins 93 études originales et 25 méta-analyses portant sur l'incidence de la TEV chez les patients atteints de COVID-19 avaient été publiées, montrant une grande hétérogénéité dans l'incidence rapportée de la TEV allant de 0 % à 85 %. Cette grande variation complique l'interprétation des résultats des études individuelles ainsi que les comparaisons entre les études, par exemple, pour étudier les changements d'incidence au fil du temps, comparer les sous-groupes et effectuer des méta-analyses.
Les études originales de trois méta-analyses ont été examinées et une liste de sources d'hétérogénéité pouvant expliquer l'hétérogénéité observée entre les études a été composée.
Les sources d'hétérogénéité de l'incidence de la TEV ont été classées en sources cliniques et en sources méthodologiques. Les sources cliniques d'hétérogénéité comprennent les différences entre les études concernant les caractéristiques des patients qui affectent le risque initial de TEV et les protocoles utilisés pour les tests de TEV. Les sources méthodologiques d'hétérogénéité comprennent les différences dans les types d'inclusion de TEV, la qualité des données et les méthodes utilisées pour l'analyse des données.
Pour apprécier les estimations rapportées de l'incidence de la TEV chez les patients atteints de COVID-19 par rapport à son étiologie, sa prévention et son traitement, les chercheurs doivent signaler sans ambiguïté les sources cliniques et méthodologiques possibles d'hétérogénéité dans ces estimations. Cet article fournit des suggestions pour cela.
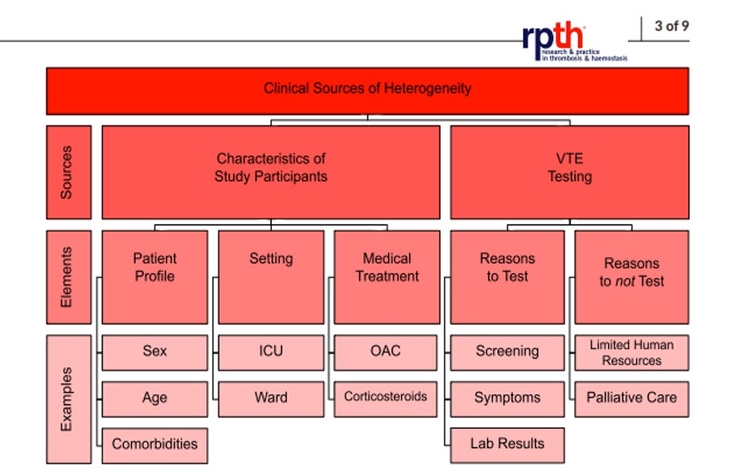
Sources cliniques d'hétérogénéité dans les études sur l'incidence de la thromboembolie veineuse pouvant expliquer l'hétérogénéité observée entre les études. Abréviations : USI, unité de soins intensifs ; OAC, anticoagulation orale ; TEV, thromboembolie veineuse
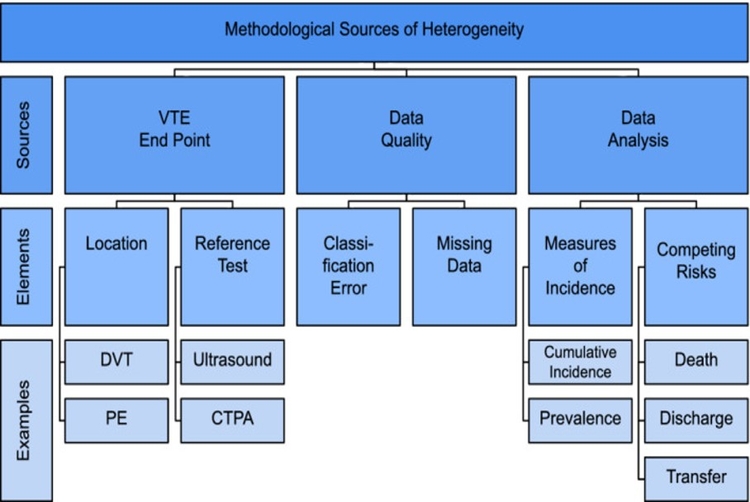
Sources méthodologiques d'hétérogénéité dans les études sur l'incidence de la thromboembolie veineuse pouvant expliquer l'hétérogénéité observée entre les études. Abréviations : CTPA, angiographie pulmonaire par tomodensitométrie ; TVP, thrombose veineuse profonde ; EP, embolie pulmonaire ; TEV, thromboembolie veineuse
Les études d'incidence de la thromboembolie veineuse chez les patients atteints de COVID-19 montrent une grande hétérogénéité.
Les sources cliniques et les sources méthodologiques d'hétérogénéité ont été identifiées et illustrées par des exemples.
La classification de ces sources d'hétérogénéité a éclairé les suggestions d'amélioration des rapports.
La description de ces éléments peut mieux isoler les différences importantes dans les déclarations d'incidences.
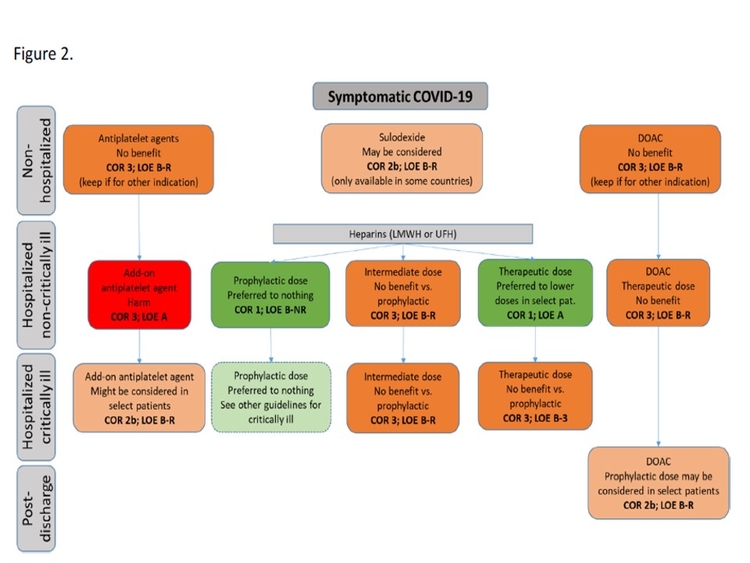
L'hétérogénéité des patients qui présentent une MTEV au décours de la Covid-19 explique la difficulté dans leur traitement préventif par HBPM. En effet la dose des HBPM fait débat . Aujourd'hui l'ISTH a fait des propositions mais rien de finaliser. L'étude française Covi-Dose pourra amener des réponses , nous l'espérons.
ARTICLE 4
Lidstrom, SC, Wiggins, KL, Harrington, LB, McKnight, B, Blondon, M, Smith, NL. Incident thrombus location and predicting risk of recurrent venous thromboembolism.
Localisation du thrombus veineux et risque prédictif de thromboembolie veineuse récurrente
Res Pract Thromb Haemost. 2022; 6:e12762. doi: 10.1002/rth2.12762
Article Libre d'Accès
Comprendre le risque de récidive de thromboembolie veineuse (TEV) est essentiel pour déterminer le traitement approprié. La question de savoir si ce risque varie après l'arrêt de l'anticoagulation ou globalement selon le type d'événement incident (embolie pulmonaire [EP] vs thrombose veineuse profonde [TVP]) et selon la localisation détaillée de la TVP doit être clarifiée.
Article Libre d'Accès
Contexte
La maladie à coronavirus 2019 (COVID-19) et les néoplasmes myéloprolifératifs (MPN) sont associés à une inflammation systémique et à un risque de thrombose. Le risque de thrombose chez les patients atteints de COVID avec et sans NMP n'a pas été largement étudié.
La maladie à coronavirus 2019 (COVID-19) et les néoplasmes myéloprolifératifs (MPN) sont associés à une inflammation systémique et à un risque de thrombose. Le risque de thrombose chez les patients atteints de COVID avec et sans NMP n'a pas été largement étudié.
Méthodes
Étude de cohorte rétrospective de 44 patients atteints de NMP et 1114 patients sans NMP positifs pour le SRAS-COV-2. Les résultats étaient la thrombose artérielle (TA), la thromboembolie veineuse (TEV), les saignements et la mort. L'analyse du délai jusqu'à l'événement a été réalisée à l'aide du modèle de régression des risques concurrents et des risques proportionnels de Cox.
Étude de cohorte rétrospective de 44 patients atteints de NMP et 1114 patients sans NMP positifs pour le SRAS-COV-2. Les résultats étaient la thrombose artérielle (TA), la thromboembolie veineuse (TEV), les saignements et la mort. L'analyse du délai jusqu'à l'événement a été réalisée à l'aide du modèle de régression des risques concurrents et des risques proportionnels de Cox.
Résultats
L'AT est survenue plus fréquemment chez les patients atteints de NMP (7 % contre 1 %, p = 0,03). Les taux de TEV (7 % contre 5 %, p = 0,73), de saignement (7 % contre 2 %, p = 0,06) et de décès (9 % contre 6 %, p = 0,32) étaient similaires. Les patients MPN étaient plus âgés et avaient plus de comorbidités cardiovasculaires. Après ajustement de la régression des risques concurrents sur le temps jusqu'à l'événement en fonction de l'âge, les patients atteints de NMP présentaient un risque plus élevé d'AT (risque relatif de subdivision 3,95, IC à 95 % 1,09–14,39), mais pas de TEV, d'hémorragie ou de décès.
L'AT est survenue plus fréquemment chez les patients atteints de NMP (7 % contre 1 %, p = 0,03). Les taux de TEV (7 % contre 5 %, p = 0,73), de saignement (7 % contre 2 %, p = 0,06) et de décès (9 % contre 6 %, p = 0,32) étaient similaires. Les patients MPN étaient plus âgés et avaient plus de comorbidités cardiovasculaires. Après ajustement de la régression des risques concurrents sur le temps jusqu'à l'événement en fonction de l'âge, les patients atteints de NMP présentaient un risque plus élevé d'AT (risque relatif de subdivision 3,95, IC à 95 % 1,09–14,39), mais pas de TEV, d'hémorragie ou de décès.
Conclusion
Parmi les patients atteints de COVID-19, les patients MPN avaient un risque plus élevé de thrombose artérielle mais pas de TEV, de saignement et de décès par rapport aux patients non MPN. Des études plus importantes sont nécessaires pour confirmer nos résultats compte tenu de la taille limitée de l'échantillon.
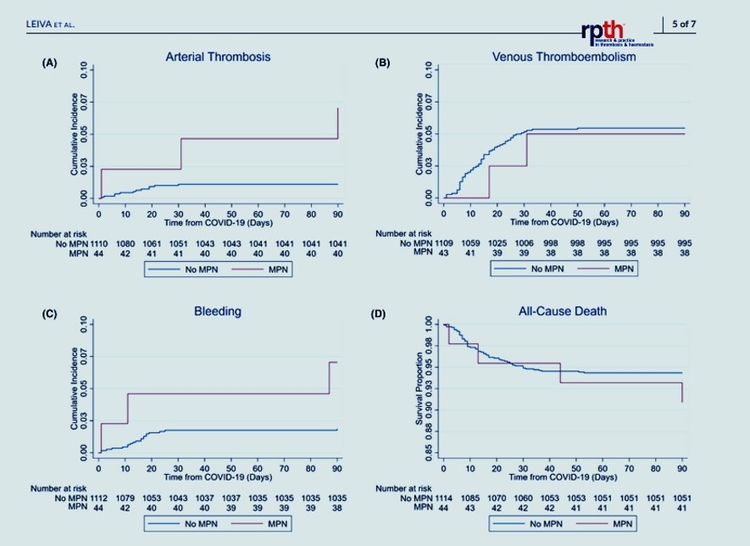
Incidence cumulée des résultats thrombotiques, hémorragiques et de survie chez les patients atteints de COVID‐19 avec et sans NMP. Graphiques d'incidence cumulée de la thrombose artérielle (A), de la TEV (B) et des saignements (C). Survie Courbe de Kaplan–Meier de la survie globale (D). Après régression du risque compétitif avec le décès comme risque concurrent et ajustement en fonction de l'âge, les patients atteints de NMP et de COVID‐19 ont une incidence accrue de thrombose artérielle par rapport aux patients non‐MPN atteints de COVID‐19 (Fine‐Gray SHR 3,95, IC à 95 % 1,09–14,39 ). Il n'y avait aucune différence dans le risque de TEV (Fine‐Gray SHR 0,62, IC à 95 % 0,15–2,60), d'hémorragie (Fine‐Gray SHR 2,32, IC à 95 % 0,71–7,59) ou de mortalité toutes causes confondues (Cox HR 0,53, 95). % IC 0,19–1,47)
Parmi les patients atteints de COVID-19, les patients MPN avaient un risque plus élevé de thrombose artérielle mais pas de TEV, de saignement et de décès par rapport aux patients non MPN. Des études plus importantes sont nécessaires pour confirmer nos résultats compte tenu de la taille limitée de l'échantillon.

Incidence cumulée des résultats thrombotiques, hémorragiques et de survie chez les patients atteints de COVID‐19 avec et sans NMP. Graphiques d'incidence cumulée de la thrombose artérielle (A), de la TEV (B) et des saignements (C). Survie Courbe de Kaplan–Meier de la survie globale (D). Après régression du risque compétitif avec le décès comme risque concurrent et ajustement en fonction de l'âge, les patients atteints de NMP et de COVID‐19 ont une incidence accrue de thrombose artérielle par rapport aux patients non‐MPN atteints de COVID‐19 (Fine‐Gray SHR 3,95, IC à 95 % 1,09–14,39 ). Il n'y avait aucune différence dans le risque de TEV (Fine‐Gray SHR 0,62, IC à 95 % 0,15–2,60), d'hémorragie (Fine‐Gray SHR 2,32, IC à 95 % 0,71–7,59) ou de mortalité toutes causes confondues (Cox HR 0,53, 95). % IC 0,19–1,47)
L'Essentiel
Les néoplasmes myéloprolifératifs (MPN) sont associés à une inflammation et à un risque de coagulation.
Le COVID-19 est également associé à une augmentation de la coagulation et de l'inflammation.
Notre étude visait à comparer l'incidence de la coagulation et du décès chez les patients atteints de COVID-19 avec NMP.
Cette étude suggère que les patients atteints de NMP et de COVID-19 courent un risque plus élevé de thrombose artérielle
NMP, Covid 19 sur risque de MTEV, la vaccination est le seul moyen de réduire ce risque, un message à rappeler encore et encore !
ARTICLE 2
Characteristics and predictors of venous thrombosis recurrence in patients with cancer and catheter-related thrombosis, Demis N Lipe et Coll, Res Pract Thromb Haemost. 2022;6:e12761
Caractéristiques et facteurs prédictifs de récidive de thrombose veineuse chez les patients atteints de cancer et de thrombose liée au cathéter
https://onlinelibrary.wiley.com/doi/full/10.1002/rth2.12761
Article Libre d'Accès
Sur les 257 personnes répondant aux critères d'inclusion, 80,2 % ont eu leur cathéter retiré ; parmi ceux-ci, 50,5 % n'ont pas reçu d'anticoagulation avant le prélèvement. Les patients qui n'ont pas reçu d'anticoagulation avant le retrait présentaient des risques accrus de récidive de TEV sur 3 mois et 1 an (rapport de cotes, 5,07 [intervalle de confiance à 95 % [IC], 1,53–23,18] ; et rapport de risque, 3,47 [IC à 95 % , 1.34–9.01]), respectivement.
Les cathéters veineux centraux augmentent le risque de thrombose liée au cathéter.
Des patients atteints de cancer et de thromboembolie veineuse associée à un cathéter veineux central (TEV) ont été étudiés.
Le retrait du cathéter avant l'anticoagulation a augmenté la récurrence de la TEV à 3 mois.
Cette étude soutient l'utilisation de l'anticoagulation avant le retrait du cathéter chez les patients atteints de cancer.
En ca de TVP sur PAC et anticoagulation, ne pas envisager l'ablation du PAC d'autant plus qu'il est fonctionnel. Par contre PAC avec thrombose septique = ablation,
Estimating incidence of venous thromboembolism in COVID-19: Methodological considerations, Lina Nab et Coll, Res Pract Thromb Haemost. 2022;6:e12776.
Estimation de l'incidence de la thromboembolie veineuse dans le COVID-19 : considérations méthodologiques
https://onlinelibrary.wiley.com/doi/10.1002/rth2.12776
Article Libre d'Accès
NMP, Covid 19 sur risque de MTEV, la vaccination est le seul moyen de réduire ce risque, un message à rappeler encore et encore !
ARTICLE 2
Characteristics and predictors of venous thrombosis recurrence in patients with cancer and catheter-related thrombosis, Demis N Lipe et Coll, Res Pract Thromb Haemost. 2022;6:e12761
Caractéristiques et facteurs prédictifs de récidive de thrombose veineuse chez les patients atteints de cancer et de thrombose liée au cathéter
https://onlinelibrary.wiley.com/doi/full/10.1002/rth2.12761
Article Libre d'Accès
Arrière plan
Les cathéters veineux centraux augmentent le risque de thrombose liée au cathéter (CRT) chez les patients atteints de cancer, affectant généralement le membre supérieur. La prise en charge de la CRT implique le retrait du cathéter et l'anticoagulation. Cependant, des preuves solides manquent sur le moment optimal de l'anticoagulation par rapport au retrait du cathéter.
Les cathéters veineux centraux augmentent le risque de thrombose liée au cathéter (CRT) chez les patients atteints de cancer, affectant généralement le membre supérieur. La prise en charge de la CRT implique le retrait du cathéter et l'anticoagulation. Cependant, des preuves solides manquent sur le moment optimal de l'anticoagulation par rapport au retrait du cathéter.
Objectifs
Notre objectif est de fournir une meilleure compréhension des facteurs qui augmentent le risque de thromboembolie veineuse récurrente (TEV) chez ces patients.
Notre objectif est de fournir une meilleure compréhension des facteurs qui augmentent le risque de thromboembolie veineuse récurrente (TEV) chez ces patients.
Patients et méthodes
Nous avons effectué un examen rétrospectif des dossiers de tous les patients consécutifs atteints de cancer dans notre hôpital touchés par la CRT entre le 1er janvier 2015 et le 31 décembre 2017. Nous avons mesuré la récidive de la TEV sous forme de thrombose dans n'importe quel lit vasculaire ou d'embolie pulmonaire, jusqu'à 2 ans. après diagnostic. Des analyses de régression des risques logistiques et concurrents ont été utilisées pour déterminer l'association entre différents facteurs cliniques et toute récidive de TEV chez les patients atteints de cancer et de CRT.
Nous avons effectué un examen rétrospectif des dossiers de tous les patients consécutifs atteints de cancer dans notre hôpital touchés par la CRT entre le 1er janvier 2015 et le 31 décembre 2017. Nous avons mesuré la récidive de la TEV sous forme de thrombose dans n'importe quel lit vasculaire ou d'embolie pulmonaire, jusqu'à 2 ans. après diagnostic. Des analyses de régression des risques logistiques et concurrents ont été utilisées pour déterminer l'association entre différents facteurs cliniques et toute récidive de TEV chez les patients atteints de cancer et de CRT.
Résultats
Sur les 257 personnes répondant aux critères d'inclusion, 80,2 % ont eu leur cathéter retiré ; parmi ceux-ci, 50,5 % n'ont pas reçu d'anticoagulation avant le prélèvement. Les patients qui n'ont pas reçu d'anticoagulation avant le retrait présentaient des risques accrus de récidive de TEV sur 3 mois et 1 an (rapport de cotes, 5,07 [intervalle de confiance à 95 % [IC], 1,53–23,18] ; et rapport de risque, 3,47 [IC à 95 % , 1.34–9.01]), respectivement.
Conclusion
Cette étude soutient l'utilisation d'anticoagulants avant le retrait du cathéter chez les patients avec CRT. Des essais cliniques randomisés sont recommandés pour établir des preuves plus solides concernant le risque à long terme de récidive de MTEV et l'effet de la réinsertion du cathéter.
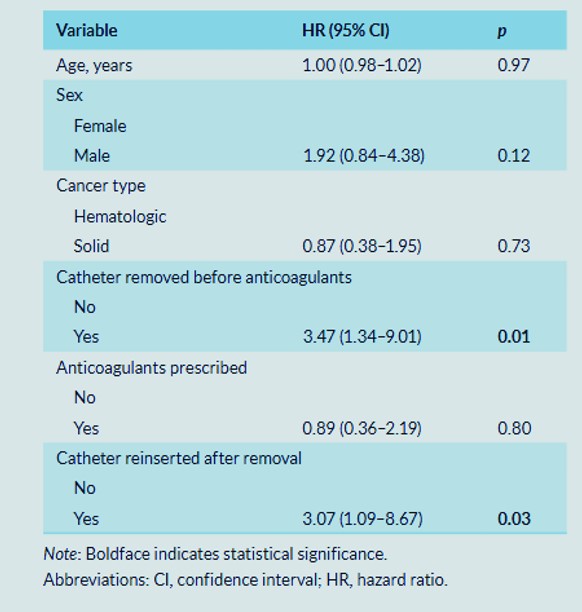
Analyse de régression des risques concurrents multivariés des facteurs cliniques et de la récidive thromboembolique veineuse à 1 an chez les patients atteints de cancer et de thrombose liée au cathéter
Cette étude soutient l'utilisation d'anticoagulants avant le retrait du cathéter chez les patients avec CRT. Des essais cliniques randomisés sont recommandés pour établir des preuves plus solides concernant le risque à long terme de récidive de MTEV et l'effet de la réinsertion du cathéter.

Analyse de régression des risques concurrents multivariés des facteurs cliniques et de la récidive thromboembolique veineuse à 1 an chez les patients atteints de cancer et de thrombose liée au cathéter
Essentiel
Les cathéters veineux centraux augmentent le risque de thrombose liée au cathéter.
Des patients atteints de cancer et de thromboembolie veineuse associée à un cathéter veineux central (TEV) ont été étudiés.
Le retrait du cathéter avant l'anticoagulation a augmenté la récurrence de la TEV à 3 mois.
Cette étude soutient l'utilisation de l'anticoagulation avant le retrait du cathéter chez les patients atteints de cancer.
En ca de TVP sur PAC et anticoagulation, ne pas envisager l'ablation du PAC d'autant plus qu'il est fonctionnel. Par contre PAC avec thrombose septique = ablation,
ARTICLE 3
,Estimating incidence of venous thromboembolism in COVID-19: Methodological considerations, Lina Nab et Coll, Res Pract Thromb Haemost. 2022;6:e12776.
Estimation de l'incidence de la thromboembolie veineuse dans le COVID-19 : considérations méthodologiques
https://onlinelibrary.wiley.com/doi/10.1002/rth2.12776
Article Libre d'Accès
Arrière plan
Les anomalies de la coagulation et la coagulopathie sont reconnues comme des conséquences de l'infection par le coronavirus 2 du syndrome respiratoire aigu sévère et de la maladie à coronavirus 2019 (COVID-19) qui en résulte. Plus précisément, la thromboembolie veineuse (TEV) a été signalée comme une complication fréquente. Au 27 mai 2021, au moins 93 études originales et 25 méta-analyses portant sur l'incidence de la TEV chez les patients atteints de COVID-19 avaient été publiées, montrant une grande hétérogénéité dans l'incidence rapportée de la TEV allant de 0 % à 85 %. Cette grande variation complique l'interprétation des résultats des études individuelles ainsi que les comparaisons entre les études, par exemple, pour étudier les changements d'incidence au fil du temps, comparer les sous-groupes et effectuer des méta-analyses.
Objectif
ise à fournir un aperçu des sources d'hétérogénéité dans les études d'incidence de TEV chez les patients atteints de COVID-19, illustrées à l'aide d'exemples.
Méthodes
Les études originales de trois méta-analyses ont été examinées et une liste de sources d'hétérogénéité pouvant expliquer l'hétérogénéité observée entre les études a été composée.
Résultats
Les sources d'hétérogénéité de l'incidence de la TEV ont été classées en sources cliniques et en sources méthodologiques. Les sources cliniques d'hétérogénéité comprennent les différences entre les études concernant les caractéristiques des patients qui affectent le risque initial de TEV et les protocoles utilisés pour les tests de TEV. Les sources méthodologiques d'hétérogénéité comprennent les différences dans les types d'inclusion de TEV, la qualité des données et les méthodes utilisées pour l'analyse des données.
Conclusion
Pour apprécier les estimations rapportées de l'incidence de la TEV chez les patients atteints de COVID-19 par rapport à son étiologie, sa prévention et son traitement, les chercheurs doivent signaler sans ambiguïté les sources cliniques et méthodologiques possibles d'hétérogénéité dans ces estimations. Cet article fournit des suggestions pour cela.

Sources cliniques d'hétérogénéité dans les études sur l'incidence de la thromboembolie veineuse pouvant expliquer l'hétérogénéité observée entre les études. Abréviations : USI, unité de soins intensifs ; OAC, anticoagulation orale ; TEV, thromboembolie veineuse

Sources méthodologiques d'hétérogénéité dans les études sur l'incidence de la thromboembolie veineuse pouvant expliquer l'hétérogénéité observée entre les études. Abréviations : CTPA, angiographie pulmonaire par tomodensitométrie ; TVP, thrombose veineuse profonde ; EP, embolie pulmonaire ; TEV, thromboembolie veineuse
Essentiel
Les études d'incidence de la thromboembolie veineuse chez les patients atteints de COVID-19 montrent une grande hétérogénéité.
Les sources cliniques et les sources méthodologiques d'hétérogénéité ont été identifiées et illustrées par des exemples.
La classification de ces sources d'hétérogénéité a éclairé les suggestions d'amélioration des rapports.
La description de ces éléments peut mieux isoler les différences importantes dans les déclarations d'incidences.

L'hétérogénéité des patients qui présentent une MTEV au décours de la Covid-19 explique la difficulté dans leur traitement préventif par HBPM. En effet la dose des HBPM fait débat . Aujourd'hui l'ISTH a fait des propositions mais rien de finaliser. L'étude française Covi-Dose pourra amener des réponses , nous l'espérons.
ARTICLE 4
Lidstrom, SC, Wiggins, KL, Harrington, LB, McKnight, B, Blondon, M, Smith, NL. Incident thrombus location and predicting risk of recurrent venous thromboembolism.
Localisation du thrombus veineux et risque prédictif de thromboembolie veineuse récurrente
Res Pract Thromb Haemost. 2022; 6:e12762. doi: 10.1002/rth2.12762
Article Libre d'Accès
Contexte
Comprendre le risque de récidive de thromboembolie veineuse (TEV) est essentiel pour déterminer le traitement approprié. La question de savoir si ce risque varie après l'arrêt de l'anticoagulation ou globalement selon le type d'événement incident (embolie pulmonaire [EP] vs thrombose veineuse profonde [TVP]) et selon la localisation détaillée de la TVP doit être clarifiée.
Méthodes
Dans cette cohorte initiale basée sur la population de cas incidents de TEV avec suivi par examen des dossiers de santé électroniques, la TVP incidente a été classée comme distale, poplitée ou iliofémorale. Nous avons utilisé le modèle de régression Fine-Gray pour décrire l'association prédictive de la localisation du thrombus avec le risque de récidive avant le décès.
Dans cette cohorte initiale basée sur la population de cas incidents de TEV avec suivi par examen des dossiers de santé électroniques, la TVP incidente a été classée comme distale, poplitée ou iliofémorale. Nous avons utilisé le modèle de régression Fine-Gray pour décrire l'association prédictive de la localisation du thrombus avec le risque de récidive avant le décès.
Résultats
Parmi les 2766 participants avec un événement incident de 2002 à 2010, 1713 (62%) ont cessé l'anticoagulation et ont été suivis pour des événements récurrents ; 301 événements ont été observés au cours des 4,5 années de suivi. Par rapport aux participants avec un thrombus incident dans une localisation ilio-fémorale et sans EP, ceux avec un thrombus dans une localisation poplitée et sans EP avaient un risque similaire de récidive (risque relatif de sous-distribution ajusté [aSHR], 0,82 [intervalle de confiance (IC) à 95 % , 0,57–1,19]), tandis que ceux avec un thrombus en position distale et sans EP et ceux avec un thrombus incluant un EP avaient un risque de récidive plus faible : aSHR, 0,34 (IC à 95 %, 0,20-0,57) ; et aSHR, 0,58 (IC à 95 % 0,45-0,76), respectivement.
Parmi les 2766 participants avec un événement incident de 2002 à 2010, 1713 (62%) ont cessé l'anticoagulation et ont été suivis pour des événements récurrents ; 301 événements ont été observés au cours des 4,5 années de suivi. Par rapport aux participants avec un thrombus incident dans une localisation ilio-fémorale et sans EP, ceux avec un thrombus dans une localisation poplitée et sans EP avaient un risque similaire de récidive (risque relatif de sous-distribution ajusté [aSHR], 0,82 [intervalle de confiance (IC) à 95 % , 0,57–1,19]), tandis que ceux avec un thrombus en position distale et sans EP et ceux avec un thrombus incluant un EP avaient un risque de récidive plus faible : aSHR, 0,34 (IC à 95 %, 0,20-0,57) ; et aSHR, 0,58 (IC à 95 % 0,45-0,76), respectivement.
Conclusion
Les résultats de cette cohorte initiale basée sur la population confirment que le risque de récidive de TEV après l'arrêt des anticoagulants est similaire après une TVP ilio-fémorale et poplitée, mais est plus faible après une TVP distale. La récidive peut être plus faible après une EP qu'une TVP proximale.
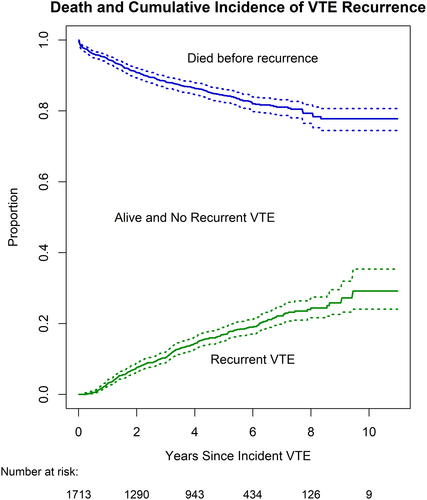
Décès sans récidive et incidence cumulée des récidives dans le temps. La distance verticale au-dessus de la ligne bleue représente la proportion d'individus décédés avant une TEV récurrente, la distance verticale en dessous de la ligne verte représente la proportion d'individus ayant subi une TEV récurrente et la distance verticale entre les lignes bleue et verte représente la proportion d'individus qui sont restés en vie sans TEV récurrente à ce nombre d'années depuis l'incident de TEV. Les lignes pointillées donnent des limites d'intervalles de confiance ponctuels à 95 %. TEV, thromboembolie veineuse
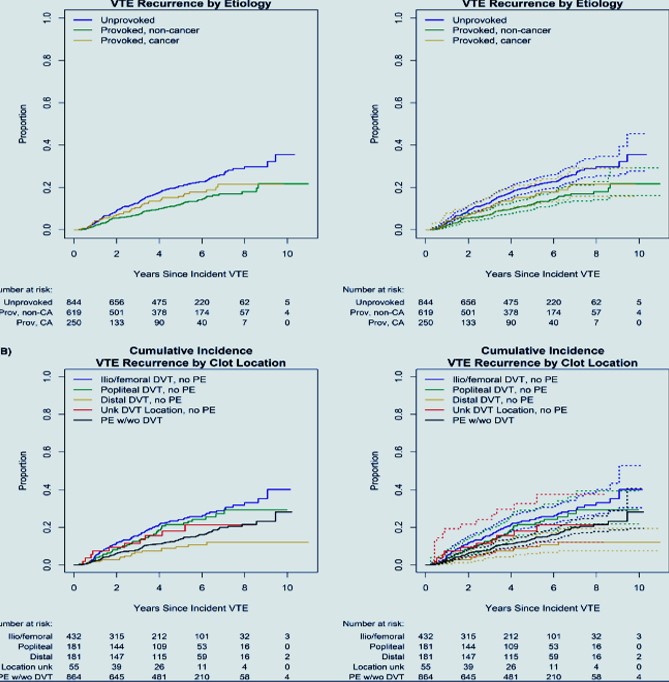
Incidence cumulée des récidives stratifiée par étiologie (A) et emplacement du thrombus (B), sans (gauche) et avec (droite) intervalles de confiance ponctuels à 95 % (lignes pointillées). AC, cancer ; TVP, thrombose veineuse profonde ; TEV, thromboembolie veineuse
Les résultats de cette cohorte initiale basée sur la population confirment que le risque de récidive de TEV après l'arrêt des anticoagulants est similaire après une TVP ilio-fémorale et poplitée, mais est plus faible après une TVP distale. La récidive peut être plus faible après une EP qu'une TVP proximale.

Décès sans récidive et incidence cumulée des récidives dans le temps. La distance verticale au-dessus de la ligne bleue représente la proportion d'individus décédés avant une TEV récurrente, la distance verticale en dessous de la ligne verte représente la proportion d'individus ayant subi une TEV récurrente et la distance verticale entre les lignes bleue et verte représente la proportion d'individus qui sont restés en vie sans TEV récurrente à ce nombre d'années depuis l'incident de TEV. Les lignes pointillées donnent des limites d'intervalles de confiance ponctuels à 95 %. TEV, thromboembolie veineuse

Incidence cumulée des récidives stratifiée par étiologie (A) et emplacement du thrombus (B), sans (gauche) et avec (droite) intervalles de confiance ponctuels à 95 % (lignes pointillées). AC, cancer ; TVP, thrombose veineuse profonde ; TEV, thromboembolie veineuse
Essentiel
L'emplacement d'un premier caillot dans les veines peut aider à identifier le risque d'un caillot récurrent.
Nous avons suivi des adultes avec une première thrombose dans différentes veines et identifié des thromboses récurrentes.
Les récidives sont plus probables chez les personnes ayant une première thrombose au-dessus du genou qu'une thrombose sous le genou.
Ils peuvent également être plus susceptibles d'avoir des thromboses récurrentes que ceux qui ont une embolie pulmonaire
Artucle comme les précédents passionnants. Rappelons qu'une TVP récidive par une TVP et une EP par une EP, ce qui confirme la gravité de l'EP. Les TVP proximales récidivent plus que les TVP distales. Endin plus de récidives des TVP proximales que les EP. Les EP non fatales, avec ou sans TVP diagnostiquée, présentaient un risque de récidive plus faible que ceux avec une TVP iliofémorale initiale. le risque de TVP proximale incidente était associé à un risque accru de 40 % de TEV récurrente, par rapport à l'EP isolée incidente, chez les patients présentant un premier événement TEV non provoqué. après arrêt de l'anticoagulation. Ces données suggèrent que, parmi tous les patients atteints de TEV, la TVP proximale comporte un plus grand risque de récidive de TEV que l'EP, a des implications cliniques potentiellement importantes et devrait être évaluée dans d'autres contextes de population. Est ce que les EP sous segmentaires récidivent comme les TVP distales, c'est à dire peu, la question reste posée. Une TVP proximale sans facteur déclenchant impose à priori une anticoagulation longue sutout si aucune étiologie n'est retrouvée comme les EP proximales. A discuter au cas par cas, as usual.......
A signaler que les articles publiés dans RPTH sont Libres d'Accès
L'emplacement d'un premier caillot dans les veines peut aider à identifier le risque d'un caillot récurrent.
Nous avons suivi des adultes avec une première thrombose dans différentes veines et identifié des thromboses récurrentes.
Les récidives sont plus probables chez les personnes ayant une première thrombose au-dessus du genou qu'une thrombose sous le genou.
Ils peuvent également être plus susceptibles d'avoir des thromboses récurrentes que ceux qui ont une embolie pulmonaire
Artucle comme les précédents passionnants. Rappelons qu'une TVP récidive par une TVP et une EP par une EP, ce qui confirme la gravité de l'EP. Les TVP proximales récidivent plus que les TVP distales. Endin plus de récidives des TVP proximales que les EP. Les EP non fatales, avec ou sans TVP diagnostiquée, présentaient un risque de récidive plus faible que ceux avec une TVP iliofémorale initiale. le risque de TVP proximale incidente était associé à un risque accru de 40 % de TEV récurrente, par rapport à l'EP isolée incidente, chez les patients présentant un premier événement TEV non provoqué. après arrêt de l'anticoagulation. Ces données suggèrent que, parmi tous les patients atteints de TEV, la TVP proximale comporte un plus grand risque de récidive de TEV que l'EP, a des implications cliniques potentiellement importantes et devrait être évaluée dans d'autres contextes de population. Est ce que les EP sous segmentaires récidivent comme les TVP distales, c'est à dire peu, la question reste posée. Une TVP proximale sans facteur déclenchant impose à priori une anticoagulation longue sutout si aucune étiologie n'est retrouvée comme les EP proximales. A discuter au cas par cas, as usual.......
A signaler que les articles publiés dans RPTH sont Libres d'Accès


