Entretien
-
Entretien Michel Dauzat : les ULTRASONS
 "Le véritable voyage de découverte ne consiste pas à chercher de nouveaux paysages, mais à avoir de nouveaux yeux."Marcel Proust
"Le véritable voyage de découverte ne consiste pas à chercher de nouveaux paysages, mais à avoir de nouveaux yeux."Marcel Proust
"L’époque de la prouesse technique est révolue ! Aujourd'hui ce qui compte avant tout c’est un diagnostic et une indication thérapeutique sous-tendus à la fois par un examen clinique et un examen paraclinique ultrasonique ou autre de qualité.Il s’agit d’une démarche métier qui s’inscrit dans un référentiel métier et de compétences en Médecine Vasculaire, avec toujours le souci de la QUALITE et de l'INNOVATION" JPL"En médecine, les dogmes ont, fort heureusement, une durée de vie plus courte que les malades". Michel Dauzat
Nous nous sommes rencontrés en 1980, nous sommes "jumeaux", même date de naissance. plus ou moins un an. Nous nous connaissons depuis 42 ans et nous avons travaillé ensemble pendant 42 ans en toute amitié. Michel m'a fait découvrir sa vision des ultrasons et découvrir l'angiosonologie. Il m'a appris à écrire un article , il m'a tout appris de ce que je connais des ultrasons. Michel est un médecin formidable , le "géotrouvetou "des ultrasons. Nous avons découvert ensemble en 1982 tout l'intérêt de l'échographie veineuse puis de l'écho Doppler pour le diagnostic des thromboses veineuses C'est un pédagogue hors pairs, c'est une référence mondiale . Il était donc naturel d'avoir avec lui un entretien sur les ultrasons, examen "échologique".
Merci Michel.
« Venant d’un ami, tout nous est précieux » Théocrite
Professeur Michel Dauzat
Professeur émérite - Université de Montpellier - UFR de Médecine de Montpellier-NîmesL'ensemble de l'iconographie : M Dauzat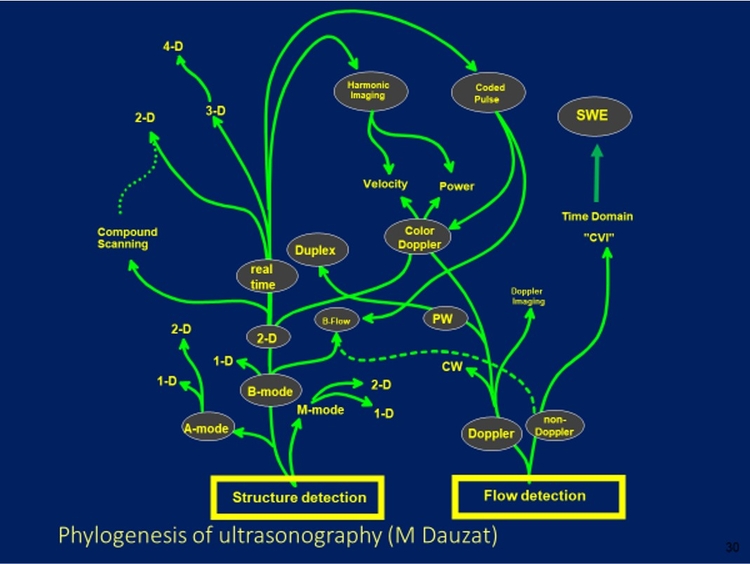 Parmi les explorations fonctionnelles vasculaires, les ultrasons font la course en tête depuis de nombreuses années. Michel, pourrais-tu nous retracer brièvement leur histoire sur le plan chronologique ?
Parmi les explorations fonctionnelles vasculaires, les ultrasons font la course en tête depuis de nombreuses années. Michel, pourrais-tu nous retracer brièvement leur histoire sur le plan chronologique ?
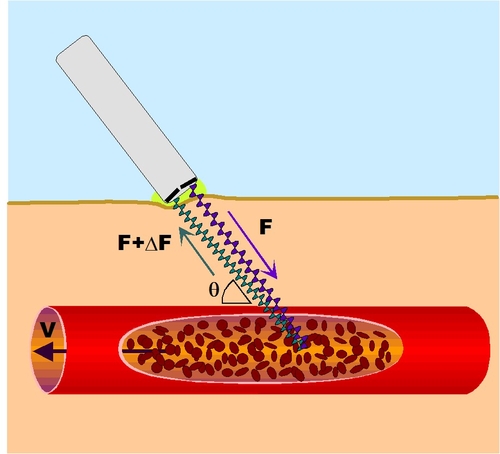
L’histoire de l’utilisation des ultrasons en diagnostic médical a commencé dans les années 1940 par des essais d’application clinique en mode « transmission », infructueux, puis, à l’instar du SONAR développé dans le contexte de la seconde guerre mondiale, en mode « réflexion » (écho), avec des résultats encourageants, notamment pour la détection des hématomes intracérébraux (mode A), de la cinétique des parois et valves cardiaques (mode TM), puis pour l’étude morphologique des organes, en particulier en obstétrique (mode bidimensionnel et mode B). Les années 1960 virent paraître les premiers travaux cliniques systématiques dans ces différents domaines, et les ultrasons commencèrent réellement à envahir la pratique clinique dans les années 1970, alors que les progrès techniques permettaient l’émergence de l’échographie « en temps réel », d’abord à l’aide de sondes mécaniques (transducteur mu par un moteur) puis électroniques (commutation électronique d’une série de transducteurs).L’utilisation du mode Doppler pour la détection par les ultrasons des mouvements tissulaires et de l’écoulement du sang date des années 1950, avec la mise au point du « Doppler à émission continue », puis, dès le début des années 1970, avec le « Doppler à émission pulsée » permettant d’obtenir une résolution spatiale.
Les fiançailles de l’échographie et du Doppler, au milieu des années 1970, mais leur mariage, c’est-à-dire de la disponibilité, sur le marché, d’appareils « écho-Doppler », ne furent célébrées que quelques années plus tard, à différents niveaux d’ergonomie selon que le couplage était réalisé avec des sondes échographiques mécaniques ou électroniques.
Le fruit de ce mariage fut, dans les années 1980, le « Doppler couleur » grâce auquel les flux sanguins purent être représentés en couleur par superposition à l’image échographique en échelle de gris.
L’échographie tridimensionnelle fit l’objet de travaux dès les années 1950, mais ne devint réellement exploitable, et disponible sur les appareils commerciaux, qu’à la fin des années 1980.Depuis, les progrès techniques n’ont cessé d’améliorer la qualité des images et signaux ultrasonographiques, permettant l’extension du champ des applications cliniques.De fait, l’évolution des techniques ultrasonographiques est indissociable des progrès thérapeutiques : dès lors qu’une affection ou une lésion peut être traitée, la technique qui en permet le diagnostic et l’évaluation devient incontournable.
L’écho-Doppler est donc devenu l’examen para-linique majeur en Médecine Vasculaire. Qu’est-ce qui fait ses forces et ses faiblesses ?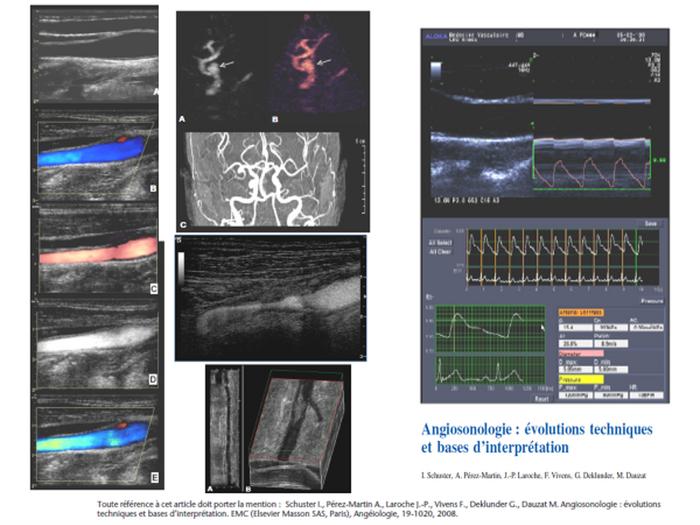
L’idée largement prévalente depuis la naissance de l’ultrasonographie est que cette technique est « opérateur-dépendante » et donc de fiabilité variable.Or, s’il s’agissait là d’une critique, elle s’adresserait aussi bien à l’ensemble des techniques et pratiques médicales et chirurgicales.La longueur des études médicales se justifie tout autant par la nécessité d’acquisition d’une expérience pratique que par la somme des connaissances à assimiler (d’autant que ces connaissances évoluent rapidement et sont régulièrement remises en question).La singularité de l’ultrasonographie, et particulièrement de l’écho-Doppler, est que son interprétation est réalisée au cours même de l’examen puisque c’est la lecture des images et signaux qui détermine la conduite de l’investigation elle-même. Interpréter un examen écho-Doppler sur des données enregistrées ne permet guère d’aller au-delà de ce que l’opérateur a pu lui-même déceler et a voulu montrer. Inversement, c’est ce « temps-réel » qui fait la principale force de l’ultrasonographie. Seule la radioscopie peut prétendre à une vision en temps réel, mais avec des images en projection et non en coupes.Les techniques modernes d’imagerie en coupes, pour aussi performantes qu’elles soient, ne permettent pas de véritable temps-réel, même si elles offrent une possibilité d’étude cinétique.
Dans le domaine cardiovasculaire, cette force est fondamentale, permettant l’observation de la cinétique des parois et des valves, mais aussi de l’écoulement sanguin et ses perturbations.Une autre caractéristique remarquable de l’échographie est sa résolution spatiale. Si celle-ci reste limitée pour les organes et tissus profonds, elle peut néanmoins atteindre, notamment pour les structures de profondeur moyenne ou superficielle, une résolution tout à fait excellente, loin devant les autres techniques d’imagerie.Certaines applications (ophtalmologie, dermatologie, exploration endocavitaire ou endovasculaire) parviennent ainsi à une résolution qui s’approche de la biomicroscopie.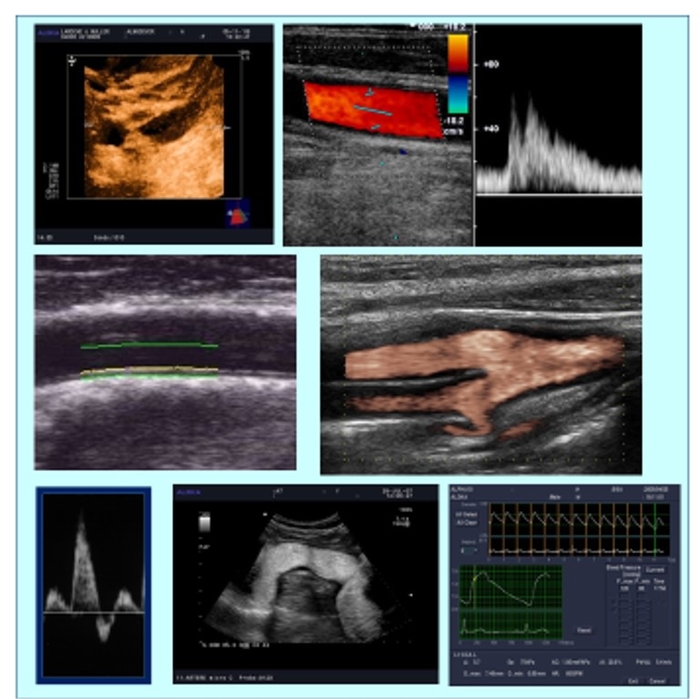
Inversement, l’importance et la diversité des artefacts constituent une limitation significative : les ultrasons ne peuvent franchir convenablement l’air ou les gaz de même que les structures fortement calcifiées.Divers phénomènes (atténuation, diffraction, réfraction, diffusion…) peuvent dégrader les images et altérer leur véracité géométrique. La qualité diagnostique d’une exploration ultrasonographique dépend donc de l’habileté de l’opérateur mais aussi de la morphologie du patient et de la présence éventuelle d’obstacles acoustiques.
Enfin, les ultrasons, dans des conditions d’utilisation raisonnables, sont inoffensifs car non-irradiants et non-vulnérant, ce qui confère à l’ultrasonographie une place de première ligne dans de nombreux domaines d’application clinique, et une place essentielle, naturellement, en obstétrique.
L’imagerie médicale scanner et IRM nous montre chaque jour des images en 3D et 4D. En obstétrique et en cardiologie cette technologie est disponible, en vasculaire périphérique nous en sommes toujours aux balbutiements, pourquoi ?
L’imagerie échographique en trois et quatre dimensions est très évoluée et performante.Techniquement, la reconstruction tridimensionnelle des images échographiques est beaucoup plus exigeante que pour le scanner ou l’IRM en raison de la très fine résolution spatiale et de la très haute résolution temporelle : le flux de données à traiter est donc considérable, mais les appareils actuels, dotés de calculateurs puissants, y parviennent très bien. Cependant, outre les artefacts et limites évoqués plus haut, se pose le problème de l’anisotropie : la résolution spatiale de l’échographie n’est pas identique dans les trois directions de l’espace, et les images reconstruites n’offrent donc pas une qualité homogène à cet égard.En d’autres termes, une coupe reconstruite ne peut offrir la même résolution qu’une coupe « native ».
Néanmoins, la raison principale du balbutiement que tu évoques est d’ordre clinique. La question centrale est : que peut apporter la reconstruction tridimensionnelle en plus des coupes échotomographiques usuelles ?Dans le domaine vasculaire, par exemple, il pourrait s’agir de volumétrie (plaques, anévrismes…), mais la qualité de mesure des volumes reste limitée par la qualité des images en coupes conventionnelles à partir desquelles est reconstruit le volume. Il peut s’agir aussi de la possibilité d’observation d’une lésion selon des incidences impossibles à obtenir de façon conventionnelle, mais la pratique de l’ultrasonographie repose en grande partie sur la multiplication des incidences pour bien « cerner » une éventuelle lésion.En d’autres termes, la plus-value du 3D et du 4D ne paraît pas toujours très significative dès lors que le champ d’exploration est, par nécessité, limité alors qu’il peut être très étendu avec le scanner et l’IRM.
L’écho- Doppler vasculaire et les produits de contraste. Quelles sont les bonnes indications ? Quelle est leur évolution potentielle : prise orale ?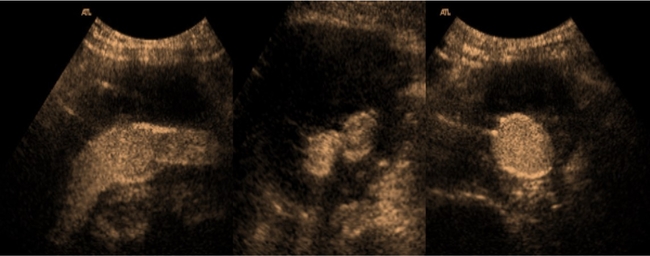 Clichés G Deklunder
Clichés G Deklunder
Les progrès spectaculaires de l’imagerie ultrasonographique sont tels que l’apport diagnostique des produits de contraste ne peut guère être autre que l’accroissement de sensibilité pour la détection des flux sanguins très lents et de la stase, donc, principalement, la détection des fuites (l’exemple le plus déterminant étant la surveillance des endoprothèses aortiques).Aider à surmonter les obstacles acoustiques est intéressant, notamment en Doppler transcrânien, mais les nouvelles modalités d’émission ultrasonore (codée, par exemple) et de traitement des signaux permettent d’obtenir une sensibilité toujours meilleure et donc de repousser toujours plus loin la limite.En outre, différentes approches techniques, notamment pour détecter et évaluer les flux sanguins sur d’autres principes que l’effet Doppler (comme le mode B-Flow), donnent des résultats spectaculaires en sensibilité et résolution. Du reste, nous devrons peu à peu (et peut-être à regret) abandonner le terme d’écho-Doppler puisque l’effet Doppler n'est plus le seul principe mis en œuvre pour la détection et l’analyse des flux sanguins.
L’utilisation des produits de contraste comme vecteurs d’agents thérapeutiques pour une délivrance ciblée et contrôlée par des séquences d’émission ultrasonore spécifiques est un objectif de très haut intérêt, faisant l’objet de nombreux travaux avec des résultats très prometteurs… mais une application clinique qui se fait encore attendre.
Quelles seraient les plateformes connectées à l’écho Doppler les plus utiles : écho-tracking etc. ?
Les plateformes connectées ont eu à jouer un rôle dans le développement des techniques d’analyse, traitement, et mesure des images et signaux ultrasonographiques avant leur intégration aux échographes eux-mêmes.Dès lors qu’une technique faisait la preuve de son utilité, elle pouvait alors être intégrée au logiciel de l’appareil écho-Doppler. Aujourd’hui, cela reste vrai mais les machines commerciales sont dotées de calculateurs d’une puissance telle que cette étape préalable n’est plus incontournable.
Par contre, la connexion des appareils ultrasonographiques à un réseau d’archivage et de communication (PACS) est essentielle, et l’ultrasonographie ne doit pas se désolidariser des autres techniques d’imagerie médicale à cet égard : ses données doivent être stockées et conservées sur les PACS et répondre aux mêmes normes et exigences de qualité. C’est à ce prix que l’écho-Doppler pourra pleinement tenir sa place dans une démarche diagnostique rationnelle et raisonnable.
C’est aussi dans cette mesure qu’elle pourra être parfaitement exploitée par les techniques avancées comme la « fusion » d’images qui permet le rapprochement des données fournies par les différentes modalités d’imagerie, chacune apportant ses caractéristiques spécifiques, cumulant donc les avantages.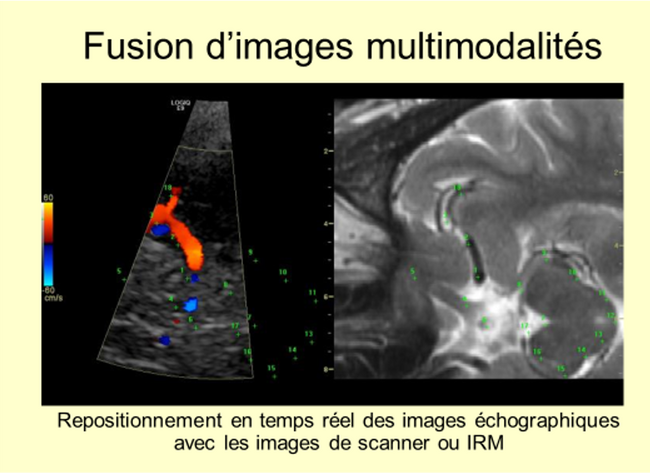
Comment vois-tu l’avenir, les développements à venir de l’écho-Doppler Vasculaire : très haute définition ? Elastographie ? Doppler vectorielle ? Echographie ultrarapide ? Doppler Ultrasensible ? Thérapie ultrasonore ?
La caractérisation des tissus à l’aide des ultrasons est un objectif majeur que de nombreux chercheurs ont poursuivi depuis le début de l’aventure ultrasonographique.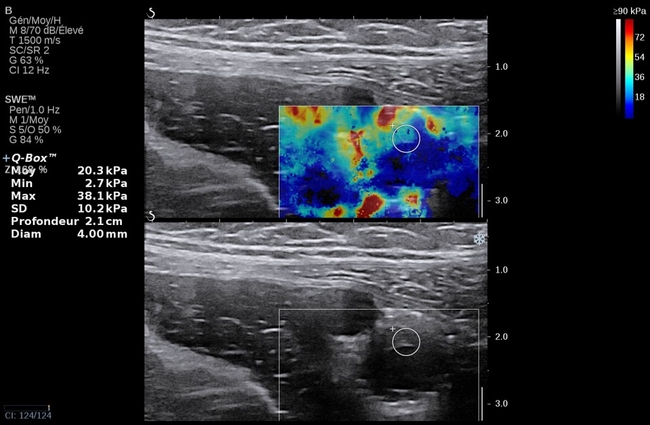 Elastographie : thrombus veineuxCependant, les écueils sont multiples du fait même de la nature des ultrasons et de leur interaction avec les tissus. L’un des problèmes est celui de la normalisation ou de l’étalonnage des données recueillies, préalables à toute quantification reproductible. L’élastographie a fait des progrès considérables ces dernières années et a commencé à porter ses fruits, particulièrement en oncologie. Les différentes techniques évoquées dans l’énoncé de la question sont mises à contribution, à des degrés divers, pour atteindre ces résultats.
Elastographie : thrombus veineuxCependant, les écueils sont multiples du fait même de la nature des ultrasons et de leur interaction avec les tissus. L’un des problèmes est celui de la normalisation ou de l’étalonnage des données recueillies, préalables à toute quantification reproductible. L’élastographie a fait des progrès considérables ces dernières années et a commencé à porter ses fruits, particulièrement en oncologie. Les différentes techniques évoquées dans l’énoncé de la question sont mises à contribution, à des degrés divers, pour atteindre ces résultats.
Cependant, avant même de parler de nouveaux développements, il reste beaucoup à faire pour améliorer l’image échographique, réduire l’impact des artefacts, homogénéiser la résolution, étendre la gamme dynamique et adapter le contraste aux objectifs diagnostiques…Il existe un foisonnement d’innovations, petites et grandes, dans ce domaine, mais elles sont parfois camouflées par des appellations commerciales pompeuses et trompeuses qui ne permettent pas de les identifier clairement.In fine, l’utilisateur juge sur le résultat global sans préjuger des techniques mises en œuvre pour l’obtenir.Dans certains cas, l’innovation surprend car elle heurte les habitudes. Par exemple, une image débarrassée de sa granularité habituelle peut être récusée par le clinicien tout simplement parce qu’il a été conditionné à une « cosmétique » d’image différente. Cet écueil existe depuis les débuts de l’échographie, et les « préréglages » des appareils ont parfois pour but de donner à l’image un aspect plaisant au détriment, par exemple, de la résolution temporelle : c’est ce qui se passe avec les techniques de lissage quand leur usage est excessif, de même que la réduction de la gamme dynamique peut donner naissance à des images plus « propres », avec une lumière vasculaire « bien noire », quitte à rendre invisibles des lésions endoluminales hypoéchogènes.
Pour le reste, c’est le bénéfice clinique apporté par les nouvelles techniques qui décidera de leur essor commercial. Par exemple, l’imagerie de la disposition dans l’espace des vecteurs de flux peut rendre de très grands services en cardiologie, notamment pour l’observation du fonctionnement des valves prothétiques, a fortiori si elles sont mises en place par voie endovasculaire. A partir d’une telle application, la technique correspondante peut diffuser dans d’autres domaines et s’imposer peu à peu. Les techniques permettant une identification automatique de la limite flux / paroi peuvent s’avérer extraordinairement utiles en pathologie cardiaque autant que vasculaire, mais les écueils sont nombreux et, dans tous les cas, seule l’expérience et la perspicacité de l’opérateur permettront d’en apprécier la fiabilité.
Carte blanche : l’Intelligence Artificielle et l’écho Doppler, mythe ou réalité ?
Tout ceci nous ramène à la question cruciale : celle de la formation des utilisateurs.Dans le domaine de la pathologie vasculaire, les angiologues, devenus médecins vasculaires, ont fait la preuve de leur compétence et sont reconnus comme les spécialistes de référence.D’un autre côté, en pathologie vasculaire comme dans tous les autres domaines cliniques d’application, l’ultrasonographie est devenue le prolongement naturel de l’examen clinique, s’imposant dans toutes les spécialités médicales mais aussi, et peut-être surtout, en médecine générale et d’urgence.Dès lors, le même niveau de compétence et d’expérience n’est pas envisageable, et le risque de mésusage de l’outil devient préoccupant.
L’intelligence artificielle est-elle une réponse ?
Oui dans la mesure ou peuvent être mises en œuvre dans les appareils ultrasonographiques des séquences de traitement des images et signaux permettant d’en améliorer la qualité et la lisibilité.Cependant, cela n’est pas encore de l’intelligence artificielle car celle-ci implique une possibilité d’apprentissage, donc de confrontation avec un verdict, ce qui signifie soit le recours à un examen de référence, soit l’observation de l’évolution clinique. Ceci ne peut se faire en temps réel et n’aurait guère de sens à l’échelle d’un seul appareil et d’un seul opérateur. Il faudrait donc que les données recueillies par un grand nombre d’appareils soient collectées et analysées, permettant alors l’amélioration progressive des procédures de traitement, analyse, et interprétation.Bien souvent, on parle à tort d’intelligence artificielle pour décrire la simple transposition en « langage machine » des procédures, « raisonnements » et analyses mis au point par des opérateurs humains. Il y donc encore beaucoup de chemin à faire dans ce domaine.
Non, parce que, dans tous les cas, le facteur limitant reste l’opérateur qui manipule la sonde et recueille les images. Les meilleurs algorithmes, et les meilleurs ordinateurs, ne peuvent analyser et interpréter que les données qui leur sont fournies. Si celles-ci sont de médiocre ou mauvaise qualité, l’interprétation ne peut être correcte (sinon par pur hasard).Pour l’heure, former les utilisateurs reste une tâche essentielle, et cette formation comporte en premier lieu la prise de conscience des questions auxquelles il leur est ou non possible de répondre, en fonction de l’appareillage qu’ils utilisent, mais aussi de leur compétence et de leur expérience. Dans le futur, on peut imaginer des sondes manipulées par des robots recherchant, sur un certain nombre de critères, les meilleures images et les meilleurs signaux.
Mais cela est-il vraiment souhaitable ? Après quelques décennies d’utilisation de l’ultrasonographie, j’en suis arrivé à la conclusion qu’il s’agit de la plus merveilleuse méthode d’exploration clinique, au contact du malade que l’on peut interroger et écouter, à qui l’on peut parler et fournir des explications, dont on peut percevoir les douleurs et les angoisses, et que l’on peut rassurer.Cette dimension humaine n’est pas négligeable et distingue l’ultrasonographie de la plupart des autres techniques d’imagerie pour lui donner une place à part, une place qu’il importe de lui conserver.« Le présent est indéfini, le futur n’a de réalité qu’en tant qu’espoir présent, le passé n’a de réalité qu’en tant que souvenir présent. » Jorge Luis Borges
Après quelques décennies d’utilisation de l’ultrasonographie, j’en suis arrivé à la conclusion qu’il s’agit de la plus merveilleuse méthode d’exploration clinique, au contact du malade que l’on peut interroger et écouter, à qui l’on peut parler et fournir des explications, dont on peut percevoir les douleurs et les angoisses, et que l’on peut rassurer.Cette dimension humaine n’est pas négligeable et distingue l’ultrasonographie de la plupart des autres techniques d’imagerie pour lui donner une place à part, une place qu’il importe de lui conserver.« Le présent est indéfini, le futur n’a de réalité qu’en tant qu’espoir présent, le passé n’a de réalité qu’en tant que souvenir présent. » Jorge Luis Borges
Page 2 sur 2
- 1
- 2

