“Chercher n'est pas une chose et trouver une autre, mais le gain de la recherche, c'est la recherche même.” Saint Grégoire de Nysse
-
" Il y a dans la recherche contre le cancer une volonté collective d'innover, de dépasser les dogmes établis pour transformer chaque découverte en espoir concret", a proposé la Fondation ARC, inspirée lors de la remise des prix Griffuel 2025.
La plus grande étude sur un test sanguin de détection précoce de plusieurs cancers
Examen des nouvelles données et du domaine de la « biopsie liquide »
Eric TOPOL
21 octobre 2025
https://mail.google.com/mail/u/0/?ogbl#inbox/FMfcgzQcqQxHMDwGrFkrLvrPpbpHKdWV
Article en libre d'accès
Lors du congrès de la Société européenne d'oncologie médicale (ESMO) la semaine dernière, la plus vaste étude sur le test sanguin de détection précoce de cancers multiples (TMD) a été présentée pour la première fois. J'ai déjà abordé ce sujet dans SUPER AGERS, mais cet essai, portant sur près de 36 000 participants, constitue une avancée significative. Dans ce numéro de Ground Truths, j'aborderai les données, les implications et l'avenir de ce domaine.
Essai et résultats de PATHFINDER 2
Cette nouvelle étude a évalué le test sanguin GRAIL, appelé Galleri , qui analyse les marqueurs de méthylation de l'ADN (chaînes latérales d'ADN) dans le plasma à partir de fragments cancéreux acellulaires, appelés « signaux cancéreux ».
Ce nouvel essai a été précédé par PATHFINDER, une étude portant sur 6 602 participants, publiée dans The Lancet , et dont j'ai fait la revue ici dans Ground Truths au moment de sa publication en 2023.
Pour ce nouvel essai, 35 878 participants ont été recrutés dans 50 centres aux États-Unis et au Canada.
Les principaux critères d'inclusion étaient les suivants :
* être âgé de 50 ans et plus
* sans antécédents de cancer lors des trois dernières années.
Pour plus de détails sur les critères d'inclusion et d'exclusion, ainsi que sur le plan d'analyse, consultez le formulaire d'inscription sur clinicaltrials.gov ici . Les participants ont été encouragés à effectuer leurs examens de dépistage habituels, tels que la mammographie ou la coloscopie.
Sur les près de 36 000 personnes inscrites, 23 161 étaient analysables avec un suivi de 12 mois, qui a servi de base à la présentation des résultats.
Voici les principales conclusions :
* Un « signal de cancer » a été identifié dans 216 cas, soit 0,93 %, ce qui correspond à 9,3 cas pour 1 000 participants.
* Le test de Galleri a confirmé un cancer chez 133 cas, soit 5,7 cas pour 1 000 participants. La valeur prédictive positive était de 61,6 % (figure ci-dessous).
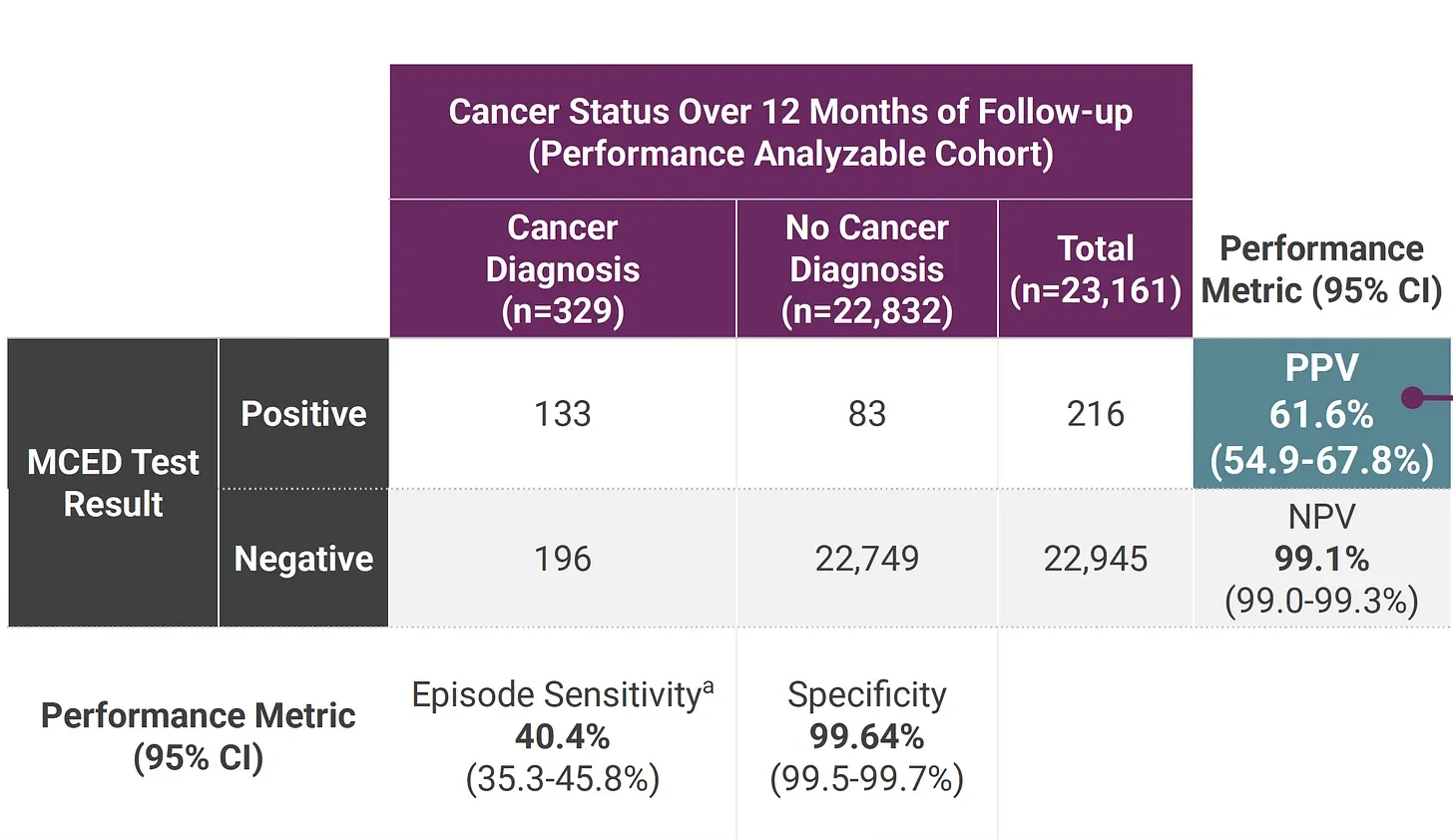
* Un cancer précoce (stade 1 ou 2) a été détecté chez 61 participants, soit 3 cas pour 1 000 participants, dont près de la moitié (N = 133) présentaient un cancer confirmé. Il est à noter que l'objectif principal du test est de détecter un cancer précoce et non métastatique.
* Il y a eu 196 faux négatifs : le MCED était négatif, mais le participant s'est avéré avoir un cancer au cours du suivi de 12 mois, soit une sensibilité de 40 %.
- Les types de cancers (plus de 50) détectés par Galleri étaient divers, comme indiqué ci-dessous, la plupart d'entre eux n'étant pas détectés par la mammographie de dépistage de masse recommandée, la coloscopie ou le scanner thoracique (pour les personnes à haut risque de cancer du poumon), tous les 3 indiqués en bleu ci-dessous.
- * Le dépistage de masse ( hors MCED ) a permis de détecter 67 cancers (sein, col de l'utérus, côlon, poumon et prostate). Hors prostate, le dépistage de masse n'a détecté que 20 cancers.
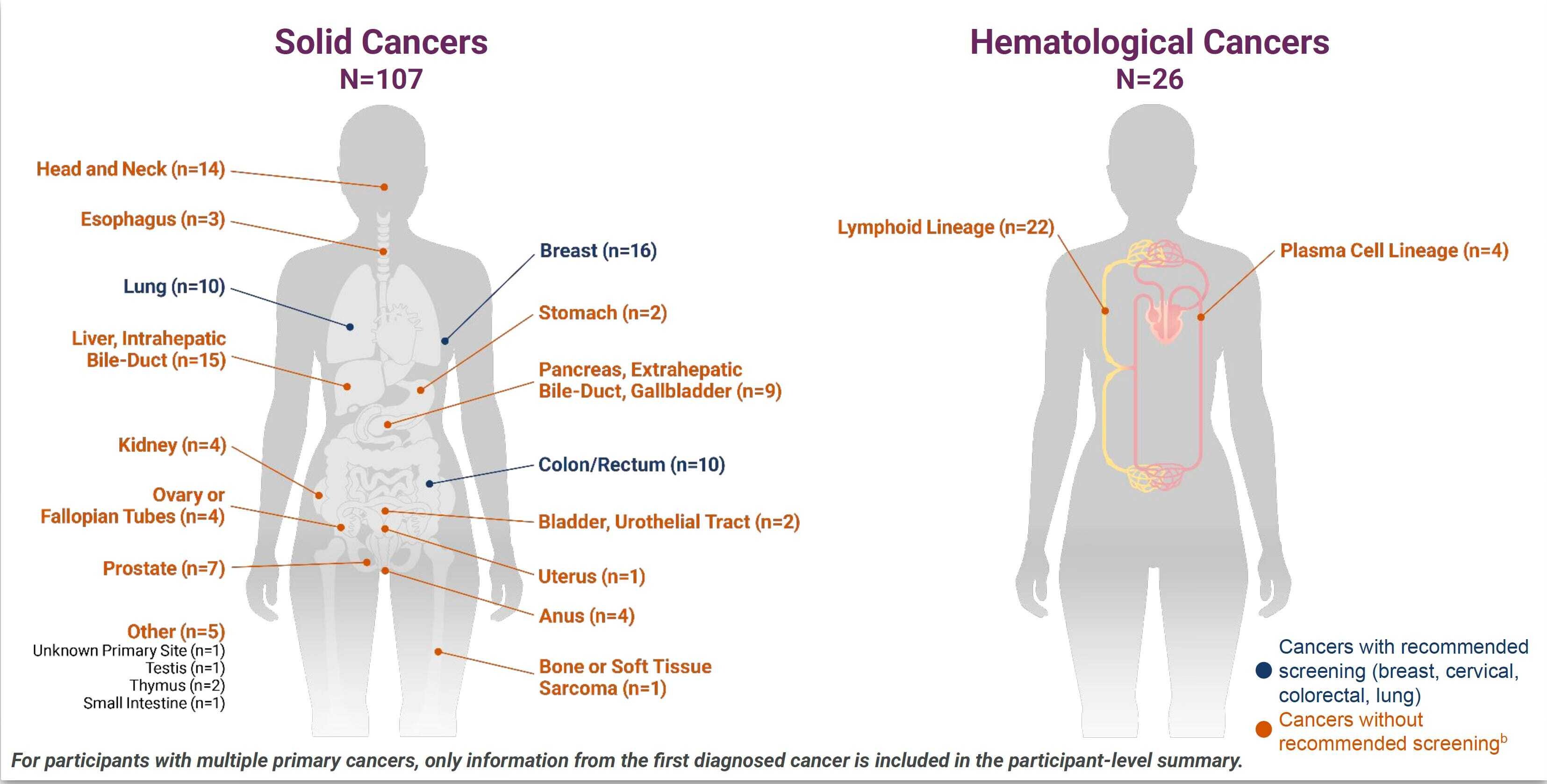
* L'IA du modèle de marqueur de méthylation a correctement identifié le site d'origine chez presque tous les participants (92,7 %) atteints de cancer, comme confirmé ultérieurement par des analyses de laboratoire, une imagerie, une biopsie ou une intervention chirurgicale.
Critique
Le taux de détection précoce du cancer, soit 3 cas pour 1 000 personnes évaluées, est dérisoire.
En incluant des personnes en bonne santé âgées de 50 ans et plus, le test de Galleri a été appliqué à une cohorte à très faible risque.
Ce résultat est supérieur à celui de 1 ou 2 cas de cancer précoce détectés lors de l'essai précédent, probablement grâce à l'inclusion de participants plus âgés (comme stipulé dans le protocole, et 29 % d'entre eux étaient effectivement âgés de 70 ans et plus).
Au-delà du faible rendement, il existe un problème de faux négatifs. Comme le montre la figure du haut, le test de Galleri a enregistré plus de faux négatifs (N = 196) que de vrais positifs (N = 133) .
Dans son communiqué de presse, la société GRAIL a présenté les résultats de l'essai comme détectant le cancer plus de sept fois le dépistage de masse recommandé par l'USPSTF (US Preventive Services Task Force). Cette affirmation est trompeuse pour de nombreuses raisons. Ce n'était pas le critère d'évaluation principal de l'essai . Ce taux de sept fois exclut les diagnostics de cancer de la prostate détectés lors du dépistage. Le protocole n'imposait pas aux participants de suivre les recommandations de dépistage de masse. De plus, il n'est pas du tout rassurant de considérer les recommandations de l'USPSTF comme une référence absolue, car elles présentent un dénominateur commun : un rendement remarquablement faible, l'âge étant le seul critère de dépistage.
La couverture médiatique était tout aussi inégale, comme en témoignent certains exemples ci-dessous. Les résultats pouvaient difficilement être qualifiés de « transformateurs » et n'étaient pas contextualisés par le faible rendement ou les cancers manqués. Certes, le Galleri a détecté plus de 50 types de cancer, ce qui constitue assurément un grand pas dans la bonne direction. De plus, la capacité à localiser le site d'origine de la tumeur grâce à l'apprentissage automatique chez presque tous les participants est tout à fait impressionnante.
Aller de l'avant
Nous pouvons faire bien mieux.
La première étape consiste à recruter des personnes à haut risque, que l'on peut distinguer de plusieurs manières : antécédents familiaux de cancers fréquents, cancer antérieur, score de risque polygénique pour les cancers courants (voir article précédent), séquençage du génome entier, réalisable à faible coût et permettant de détecter systématiquement 5 % ou plus de personnes présentant des mutations pathogènes cancérigènes non suspectées , utilisation du test CHIP (hématopoïèse clonale à potentiel indéterminé ; voir article précédent) , et une horloge du système immunitaire présentant un décalage significatif par rapport à l'âge chronologique de la personne.
Il existe des dizaines de tests multi-âges émergents, dont beaucoup font l'objet d'essais cliniques en cours. Ces tests mesurent différents facteurs sanguins, comme je l'ai mentionné dans SUPER AGERS, tels que l'ARN acellulaire, la fragmentation de l'ADN, les exosomes circulants, les éléments répétés d'ADN, les protéines et les métabolites. Il existe de nombreuses façons d'amplifier la faible quantité d'ADN tumoral acellulaire, grâce à des agents d'amorçage améliorant le rapport signal/bruit et la précision. Cependant, tous ces tests, divers et perfectionnés, gagneraient également à être évalués chez les personnes à risque élevé, plutôt que de se limiter à l'âge comme méthode de sélection, imitant ainsi les pratiques défaillantes et inefficaces de nos politiques actuelles de dépistage de masse.
Le test GRAIL Galleri est en tête, approchant le million de personnes testées au total (commercialement et dans le cadre d'essais de recherche). L'entreprise peut être félicitée pour sa recherche rigoureuse, qui inclut de nombreux essais, dont un essai randomisé en cours au Royaume-Uni, portant sur plus de 140 000 participants dont le recrutement est désormais terminé. Cependant, le test coûte 949 $ et n'est pas pris en charge par l'assurance maladie. C'est un prix très élevé pour un taux de détection précoce aussi faible (3 sur 1 000) et un taux de faux négatifs élevé. Je ne recommanderais pas le test Galleri tel qu'il est pratiqué aujourd'hui (à partir de 50 ans). Cependant, chez une personne présentant un risque élevé, cela mérite d'être considéré, et ce de plus en plus à mesure que les tests MCED continuent de s'améliorer.
Ce qui est manqué, c'est l'opportunité de privilégier la prévention du cancer , et pas seulement la détection précoce. S'il serait bien plus efficace de détecter le cancer au microscope avec un test comme Galleri ou d'autres MCED qu'avec une IRM corps entier, compte tenu de la nécessité de milliards de cellules tumorales avant qu'une masse ne soit détectée par imagerie, mieux encore serait de prévenir complètement le cancer .
Nous disposons du nouveau potentiel de la prévention primaire, principe de base des SUPER AGERS, et évoqué dans ce récent article de Ground Truths.
L'utilisation des méthodes de définition du risque élevé (risque polygénique, score, CHIP, séquençage du génome entier, évaluation du système immunitaire) permettrait, grâce à l'analyse multimodale par IA, d'identifier les patients à haut risque qui permettent la prévention primaire, comme cela contribuerait à accroître considérablement le rendement et la précision des tests de détection précoce multicancer.
Comment révolutionner le dépistage du cancer
La chance d'être beaucoup plus intelligent T
Eris TOPOL / 2023
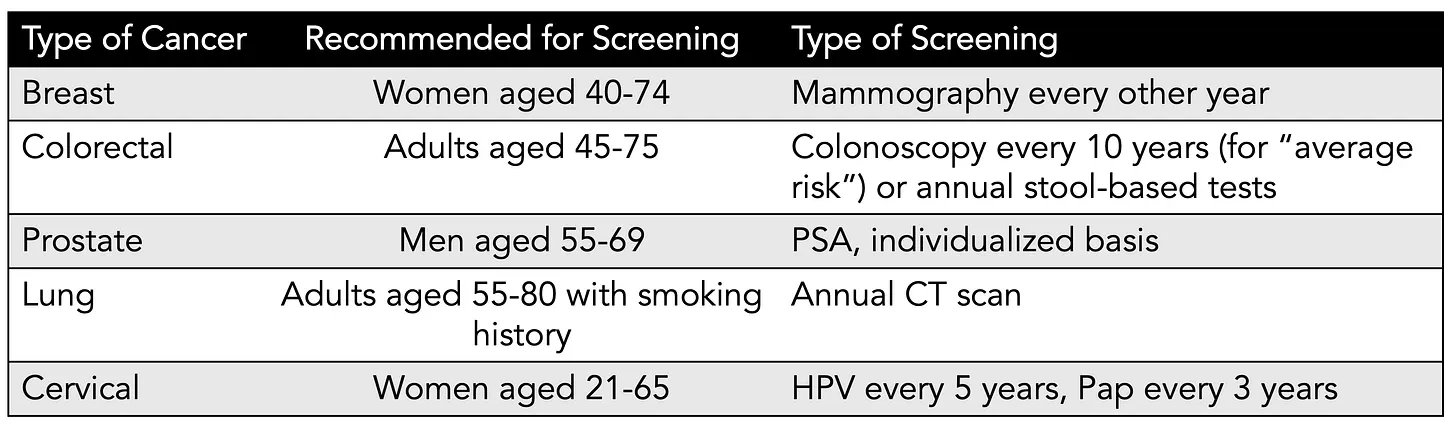
Âge. C'est le critère majeur des recommandations de dépistage du cancer pour tous les cancers courants.
Les recommandations actuelles du Groupe de travail des services de prévention des États-Unis (USPSTF) sont résumées ci-dessous (version simplifiée, sans classement ni détails), l'âge étant le critère de base du dépistage en population.
Le coût de ce dépistage de masse, basé sur l'âge, en soi, hors examens et procédures de suivi ni surdiagnostic, est estimé entre 40 et 80 milliards de dollars par an . Pourtant, par exemple, 88 % des femmes ne développeront jamais de cancer du sein au cours de leur vie , bien que la mammographie soit recommandée tous les deux ans pour les femmes de 40 ans et plus (la date d'âge ayant récemment été abaissée de 50 ans par l'USPSTF). Récemment, ces seuils d'âge ont été remis en question par la tendance émergente à la survenue du cancer chez les jeunes . À cela s'ajoute un taux de faux positifs d'environ 10 % pour de nombreux tests, comme la mammographie, à chaque fois qu'ils sont réalisés. En ce qui concerne la mammographie, environ la moitié des femmes auront un faux positif au cours d'une décennie (5 examens). Actuellement, aux États-Unis, seulement 14 % des cancers diagnostiqués sont détectés grâce à un test de dépistage recommandé.
Commentaire
La biopsie liquide, ou la détection des cancers par une simple prise de sang, pose plus de questions qu'elle n'a de réponses.
C'est au seul médecin de décider de la réalisation ou non d'un tel test.
La prescription devra être encadrée, donc justifiée, mais halte à la multiplication de ce type de test.
Ainsi, il y a une restriction immédiate concernant le dépistage sanguin du cancer.
Prenons l'exemple de la MTEV sans facteur déclenchant après 50 ans, test sanguin de dépistage du cancer systématique. On sait que c'est seulement 5 à 7% des patients qui ont un cancer.
Si un jour le test devient fiable à 100%, en particulier avec une valeur prédictive négative de 100%, nous changerons d'avis.
Donc PATIENCE, concentrons-nous sur les dépistages des cancers, les dépistages validés.
Ce type de test peut rendre le patient et le médecin très anxieux.
Tous les hypochondriaques vont adorer ce type de test, ce qui risque de les rendre encore plus anxieux.
COMPLEMENT d'ENQUETE
PATHFINDER 2: a Multi-Cancer Early Detection Study
https://www.clinicaltrials.gov/study/NCT05155605?term=pathfinder%202&rank=2
Les résultats de GRAIL PATHFINDER 2 montrent que le test sanguin de détection précoce multicancers Galleri® a multiplié par plus de sept la détection du cancer lorsqu'il est ajouté aux dépistages recommandés par l'USPSTF A et B.
I"l est important de prendre en compte les informations sur la sécurité du test Galleri.
Le test Galleri est recommandé chez les adultes présentant un risque élevé de cancer, notamment les personnes de 50 ans et plus. Ce test ne détecte pas tous les cancers et doit être utilisé en complément des tests de dépistage de la maladie de routine recommandés par un professionnel de santé. Le test Galleri est destiné à détecter les signaux cancéreux et à prédire leur localisation dans l'organisme. Son utilisation est déconseillée aux femmes enceintes, aux personnes âgées de 21 ans ou moins ou aux personnes suivant un traitement anticancéreux actif.
Les résultats doivent être interprétés par un professionnel de santé en tenant compte des antécédents médicaux, des signes cliniques et des symptômes. Un résultat de test indiquant « Aucun signal cancéreux détecté » n'exclut pas la possibilité d'un cancer. Un résultat de test indiquant « Signal cancéreux détecté » nécessite une évaluation diagnostique de confirmation par des procédures médicales établies (par exemple, imagerie) pour confirmer le cancer.
Si le cancer n'est pas confirmé par des examens complémentaires, cela pourrait signifier qu'il n'est pas présent ou que les examens n'ont pas été suffisants pour le détecter, notamment en raison d'une localisation différente du cancer. Des faux positifs (signal cancéreux détecté alors qu'il n'est pas présent) et des faux négatifs (signal cancéreux non détecté alors qu'il y est) peuvent survenir. Sur ordonnance uniquement.
Informations sur le laboratoire/les tests :
Le laboratoire clinique GRAIL est certifié conformément aux modifications de 1988 relatives à l'amélioration des laboratoires cliniques (CLIA) et accrédité par le College of American Pathologists. Le test Galleri a été développé et ses caractéristiques de performance ont été déterminées par GRAIL. Ce test n'a pas été homologué par la Food and Drug Administration (FDA). Le laboratoire clinique GRAIL est réglementé par la CLIA pour réaliser tests de haute complexité. Le test Galleri est destiné à des fins cliniques. "
https://grail.com/press-releases/grail-pathfinder-2-results-show-galleri-multi-cancer-early-detection-blood-test-increased-cancer-detection-more-than-seven-fold-when-added-to-uspstf-a-and-b-recommended-screenings/
À LIRE
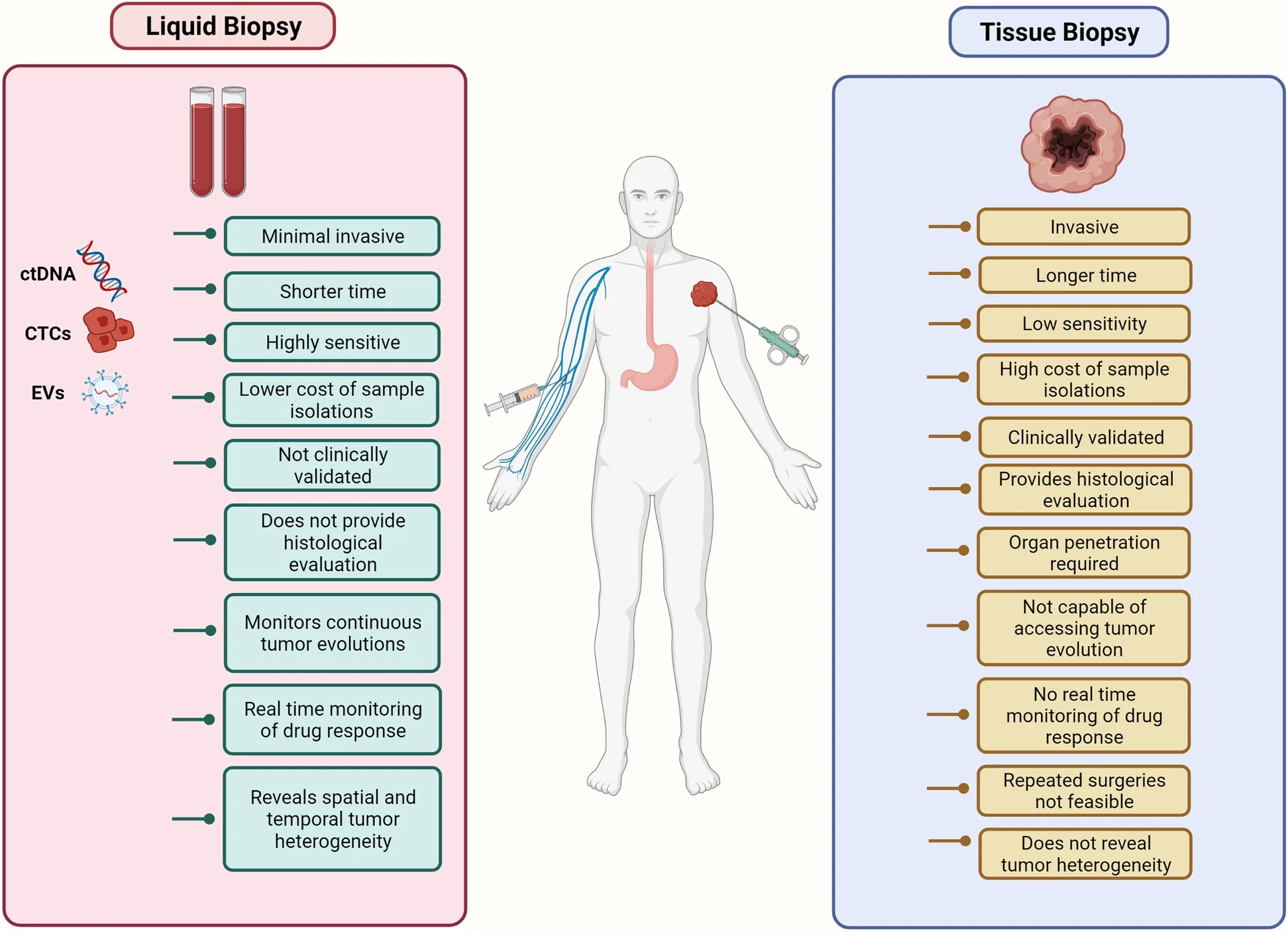
BIOPSIE LIQUIDE
Comparaison de la biopsie tissulaire traditionnelle et de la biopsie liquide. Le schéma illustre les avantages que les biopsies liquides ont acquis par rapport aux méthodes chirurgicales invasives traditionnelles au cours de la dernière décennie. Montré ici sont des méthodes d'extraction d'un échantillon de test qui comprend généralement un petit fragment de tissu en cas de biopsies tissulaires et de sang dans les LB. Les analytes qui sont isolés et surveillés dans les LB comprennent l'ADNct, les CTC et les véhicules électriques tumoraux
https://molecular-cancer.biomedcentral.com/articles/10.1186/s12943-022-01543-7/figures/1
https://medvasc.info/archives-blog/biopsie-liquide-1
BIOPSIE LIQUIDE 2 : PANDORE REVISITÉE
Question à PERPLEXITY/IA, que penser de la BIOPSIE LIQUIDE ?
Voici un tableau comparatif résumant les points clés à connaître sur la biopsie liquide, présentant ses avantages, limites et indications principales:
Ce résumé en tableau montre que la biopsie liquide représente un outil complémentaire innovant en cancérologie, avec des bénéfices marqués pour le suivi et le confort du patient, mais certaines limites persistent en routine clinique.
La suite avec GEMINI /IA
La biopsie liquide est une avancée majeure dans le domaine de l'oncologie, offrant une alternative moins invasive à la biopsie tissulaire traditionnelle pour la détection et le suivi des cancers. Établie sur une simple prise de sang, cette technique promet de transformer la prise en charge des patients atteints de cancer. Voici un aperçu complet pour vous forger une opinion éclairée sur le sujet.
Qu'est-ce qu'une biopsie liquide ?
Une biopsie liquide est un test qui vise à détecter des marqueurs tumoraux circulants, tels que des cellules cancéreuses intactes (CTC) ou des fragments d'ADN tumoral (ADNtc) libérés par la tumeur dans la circulation sanguine. L'analyse de ces éléments permet d'obtenir des informations précieuses sur les caractéristiques génétiques de la tumeur.
Les multiples applications en oncologie
La biopsie liquide a un large éventail d'applications à différents stades de la maladie cancéreuse :
-
* Diagnostic précoce : elle offre la possibilité de détecter un cancer à un stade précoce, parfois même avant l'apparition des premiers symptômes.
-
* Choix du traitement : en identifiant des mutations génétiques spécifiques dans l'ADN tumoral, la biopsie liquide aide les médecins à choisir les thérapies ciblées les plus appropriées pour un patient donné. Par exemple, la recherche de mutations du gène EGFR dans le cancer du poumon non à petites cellules ou de ESR1 dans celui du sein.
-
* Suivi de l'efficacité du traitement : des analyses répétées permettent de surveiller la réponse de la tumeur au traitement. Une diminution de la quantité d'ADN tumoral circulant est un signe d'efficacité, tandis qu'une augmentation peut indiquer une progression de la maladie.
-
* Détection des résistances : les tumeurs peuvent évoluer et développer des résistances aux traitements. La biopsie liquide peut identifier l'apparition de nouvelles mutations responsables de ces résistances, permettant ainsi d'adapter la stratégie thérapeutique.
-
* Surveillance des récidives : après la fin du traitement, la biopsie liquide peut être utilisée pour détecter une éventuelle récidive de manière précoce, avant même qu'elle ne soit visible à l'imagerie.
Avantages et limites à considérer
La biopsie liquide présente des avantages significatifs mais aussi des limites qu'il est important de connaître.
| Avantages | Limites |
| Moins invasive et moins risquée qu'une biopsie tissulaire (qui peut nécessiter une intervention chirurgicale ou une endoscopie). | La quantité de matériel tumoral dans le sang peut être minuscule, rendant la détection ardue, surtout aux stades précoces de la maladie. |
| Permet une analyse dynamique et répétée de l'évolution de la tumeur. | La fiabilité et la précision peuvent varier en fonction des technologies utilisées et nécessitent une standardisation des techniques. |
| Accès à l'information génétique de la tumeur lorsque la biopsie tissulaire est difficile ou impossible à réaliser (tumeur inaccessible, patient fragile). | Ne remplace pas encore la biopsie tissulaire qui reste la référence pour le diagnostic initial et l'analyse du microenvironnement tumoral. |
| Permet d'avoir une vision plus globale de l'hétérogénéité de la tumeur en capturant l'ADN de différentes localisations tumorales (tumeur primaire et métastases). | Le coût peut être élevé et la disponibilité pas encore généralisée pour toutes les indications. |
Fiabilité et précision : où en est-on ?
La fiabilité des biopsies liquides s'est considérablement améliorée grâce aux avancées technologiques telles que le séquençage à haut débit (NGS) et la PCR digitale. Cependant, la sensibilité du test (sa capacité à détecter la maladie quand elle est présente) peut être limitée par la faible concentration d'ADN tumoral dans le sang.
La spécificité (la capacité du test à être négatif quand la maladie est absente) est généralement élevée, mais des faux positifs peuvent survenir, entraînant une anxiété et des examens complémentaires inutiles pour les patients. Des recherches actives sont en cours pour standardiser les méthodes et améliorer la performance globale de ces tests.
L'avenir prometteur de la biopsie liquide
Le futur de la biopsie liquide est très prometteur. Les chercheurs travaillent à améliorer la sensibilité des tests pour une détection encore plus précoce des cancers. L'intégration de l'intelligence artificielle et de l'apprentissage automatique devrait permettre d'analyser plus finement les données complexes issues de ces études pour des prédictions plus précises.
À terme, la biopsie liquide pourrait devenir un outil de dépistage de routine pour certains cancers, permettant une prise en charge plus rapide et plus personnalisée, et améliorant ainsi significativement le pronostic des patients.
Des partenariats entre des institutions de recherche de premier plan, comme Gustave Roussy en France, et des entreprises spécialisées visent à accélérer l'intégration de ces technologies innovantes dans la pratique clinique courante.
QUE PENSE ERIC TOPOL DE LA BIOPSIE LIQUIDE ? interview de PERPLEXITY
"Eric Topol considère la biopsie liquide comme une révolution en oncologie, permettant une approche moins invasive du suivi et du diagnostic du cancer grâce à un prélèvement sanguin banal. Il souligne que cette technologie ouvre la voie à une médecine plus personnalisée, notamment dans la gestion du cancer colorectal où la biopsie liquide (par ADN tumoral circulant, ctDNA) peut réduire le recours à la chimiothérapie sans diminuer les chances de survie. Topol évoque également les premiers tests de dépistage par biopsie liquide (par exemple Galleri), capables de détecter une cinquantaine de cancers dans le sang et de localiser l'origine tumorale dans 89% des cas détectés, mais restant moins sensibles pour les stades précoces.
Dans ses prises de parole récentes, Topol affirme que le potentiel de la biopsie liquide dans le dépistage précoce et le suivi tumoral est immense. Il rappelle toutefois que cette méthode, encore émergente, n'est pas encore un substitut complet aux diagnostics traditionnels, notamment pour certains cancers hématologiques. Il voit la biopsie liquide comme un outil central pour améliorer la personnalisation des traitements et limiter les effets indésirables inutiles, tout en anticipant d'innombrables progrès dans les 10 à 20 prochaines années."
BONUS PERPLEXITY, BIBLIOGRAPHIE 2024 et 2025 sur la BIOPSIE LIQUIDE
Voici une bibliographie commentée sur la biopsie liquide rassemblant des articles de 2024 et 2025 récents, incluant des revues, des avancées technologiques, des essais cliniques et des analyses de l'impact en oncologie :
Articles et revues scientifiques internationales (2024-2025)
-
Wan JCM, Sasieni P, Rosenfeld N. "Promesses et pièges de la détection précoce de plusieurs cancers à l'aide de tests basés sur la biopsie liquide." Nature Reviews Oncologie Clinique. juin 2025 ; 22(6):345-357. Revue analysant les défis et perspectives des tests de dépistage multicancer par biopsie liquide, avec discussion sur la sensibilité, la spécificité et la trajectoire future du secteur.
-
Perachino M, Di Lella FA, Severi S et al. "Élargir le dépistage grâce à l'utilisation de la biopsie liquide pour la détection précoce du cancer." Médecine des communications. 2025 mai;5(1):e885. Revue détaillant les enjeux du dépistage précoce via la biopsie liquide, avec discussions sur les différents biomarqueurs (ctDNA, CTCs, exosomes).
-
Maheswaran S, Haber DA. « Cancer in a Drop : aperçus de la biopsie liquide de l'AACR 2025. » PMC12223554. 9 juin 2025. Synthèse des dernières recherches et communications du congrès AACR 2025 sur les multiples technologies et applications cliniques de la biopsie liquide.
-
Aredo JV, Kris MG, Paweletz C. «Approches de biopsie liquide pour la caractérisation et la surveillance du cancer». Livre éducatif ASCO 2025 ; EDBK-25-481114. Revue sur l'utilisation de la biopsie liquide pour le profilage moléculaire et la surveillance des cancers avancés ou métastatiques.
-
Shen F et coll. "Biopsie liquide - une revue narrative avec une mise à jour sur les applications actuelles et futures." 2025. Discussion sur les applications actuelles : suivi de maladie résiduelle, détection précoce, réponse au traitement, innovations méthodologiques.
Études, innovations et applications cliniques récentes
-
ASCO 2024 et 2025 : Études issues de l'Institut Curie et d'autres centres français sur l'application de la biopsie liquide dans le suivi du cancer du sein, la résistance aux traitements, et l'extension du profilage génomique à grande échelle.
-
Gustave Roussy a présenté le "profilage génomique sanguin par biopsie liquide". 2024-2025. Déploiement de la technologie à grande échelle en France avec le laboratoire Fresh, permettant l'analyse de milliers d'échantillons pour le suivi génomique.
-
Recherche mondiale M3. "Biopsies liquides : l'avenir de la détection précoce du cancer." 2025. Point sur les principaux essais cliniques en cours (PATHFINDER, NHS-Galleri), nouvelles approches microfluidiques, techniques à base de nanoparticules et CRISPR.
Synthèses de vulgarisation et applications en population générale
-
Curie.fr, "Octobre Rose 2025 : Les biomarqueurs circulants, un espoir sur tous les fronts." Article grand public sur l'apport de la biopsie liquide pour le diagnostic, la personnalisation des soins et la surveillance, en particulier dans le cancer du sein métastatique.
-
Ouest-France Santé, « Biopsie liquide : comment une simple prise de sang pourrait changer la lutte contre le cancer du sein. » Discussion sur les progrès et essais français.
-
Roche Diagnostics, "Qu'est-ce qu'une biopsie liquide" (2025). Cette présentation met en avant les avantages de la biopsie liquide pour le diagnostic et la gestion du cancer, ainsi que ses intérêts par rapport à la biopsie tissulaire classique.
Liens vers d'autres synthèses et états des lieux
-
Continentalhospitals.com. "Comment la biopsie liquide va-t-elle changer le diagnostic du cancer en 2025 ?" Description des nouvelles méthodes et impact sur le suivi en temps réel.
-
Inoviegroup.com. "Biopsie liquide : une avancée stratégique en oncogénétique, portée par IMAGENOME." Mise à jour sur les plateformes françaises, innovations et intégration en oncogénétique.
Cette sélection intègre des sources académiques et de vulgarisation, couvrant à la fois les avancées technologiques, les essais cliniques en population générale, les impacts pratiques en oncologie et les enjeux de dépistage multicancer.
Copyright : Dr Jean-Pierre Laroche/2025