« Il y a toujours de l'espoir au-delà de ce que l'on voit. »
— Cora Connor , soignante d'une personne atteinte d'un cancer du rein
« Il est possible non seulement de survivre, mais aussi de s'épanouir et de vivre à nouveau une vie saine et merveilleuse. »
— Erika Evans , survivante de la leucémie
« La vie, c'est 10 % ce qui nous arrive et 90 % la façon dont nous y réagissons. »
— Leslie Medley-Russell , survivante du cancer de l'ovaire
« Le cancer, c'est comme une balançoire. Parfois, il faut descendre pour remonter. »
— John Kennedy , survivant d'un cancer du côlon
Saad M, Batool RM, Waqas SA, Sohail MU, Mohan A, Kumar V, Hameed I, Ahmed R, Alraies MC. Unveiling the trends: Growing cancer and venous thromboembolism mortality in older adults in the United States, 1999-2020.
Dévoiler les tendances : Croissance de la mortalité due au cancer et à la thromboembolie veineuse chez les personnes âgées aux États-Unis, 1999-2020
Thromb Res. 2025 Mar;247:109259. doi: 10.1016/j.thromres.2025.109259. Epub 2025 Jan 23. PMID: 39874686.Contexte : Bien que la mortalité par cancer ait diminué aux États-Unis grâce aux progrès de la chimiothérapie, les personnes âgées atteintes de cancer présentent un risque accru de thromboembolie veineuse (TEV). Cette étude analyse les tendances de la mortalité par TEV associée au cancer chez les personnes âgées aux États-Unis.
Méthodes : À l’aide de la base de données CDC WONDER sur les causes multiples de décès (MCD), nous avons examiné les certificats de décès de 1999 à 2020 afin d’évaluer la mortalité par thrombose veineuse (TEV) associée au cancer chez les personnes âgées (≥ 65 ans). Nous rapportons les taux de mortalité ajustés selon l’âge (TMAA) pour 100 000 personnes, ainsi que la variation annuelle moyenne en pourcentage (VAM) à l’aide de la régression Joinpoint.
Résultats : Au cours de la période d'étude, 175 811 décès par thrombose veineuse (TEV) associés au cancer ont été enregistrés. Le taux de mortalité annuel moyen (TMA) est passé de 16,8 en 1999 à 22,8 en 2020, avec un CPAM de +1,4 % (IC à 95 % : 1,2-1,6 ; p < 0,001). Les hommes avaient un TMA plus élevé (22,2) que les femmes (17,0). Les personnes noires non hispaniques (NH) avaient le TMA le plus élevé (28,3), suivies des Blancs du NH (19,3), des Hispaniques (12,0) et des Asiatiques du NH (7,9). Les TMA étaient plus élevés dans les zones non métropolitaines (19,4) que dans les zones urbaines (19,1). Au niveau régional, le Midwest a enregistré le TMA le plus élevé, soit 20,9. Les États du 90e percentile supérieur ont signalé des TMA deux fois plus élevés que ceux du 10e percentile inférieur.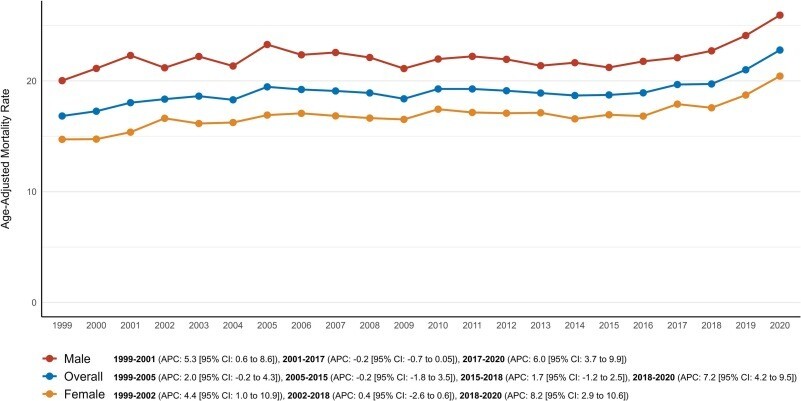
Taux globaux et stratifiés par sexe de thromboembolie veineuse associée au cancer pour 100 000 personnes âgées aux États-Unis de 1999 à 2020.
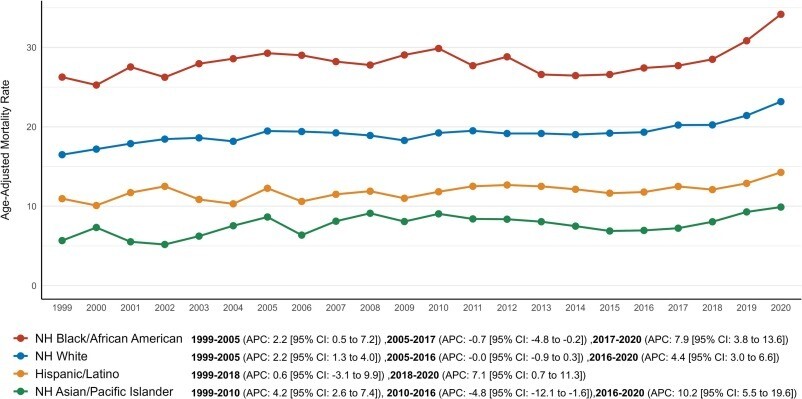
AAMR liés à la thromboembolie veineuse associée au cancer pour 100 000 personnes stratifiées par race chez les personnes âgées aux États-Unis de 1999 à 2020.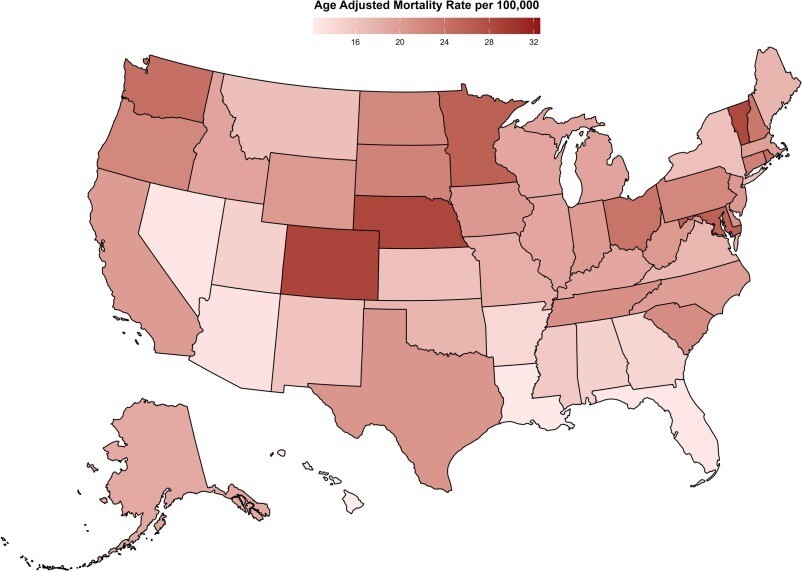
AAMR liés à la thromboembolie veineuse associée au cancer pour 100 000 personnes stratifiées par État chez les personnes âgées aux États-Unis de 1999 à 2020.
Conclusion
Points forts
Le taux de croissance annuel moyen (TAAM) global a augmenté de +1,4 % par an.
Les hommes et les personnes noires du New Hampshire présentaient les AAMR les plus élevés.
La région du Midwest avait le taux de mortalité infantile le plus élevé parmi toutes les régions des États-Unis.
"Article important montrant une augmentation de la mortalité liée au cancer/TEV chez les personnes âgées, ajustée en fonction de l'âge, au fil du temps et selon le lieu aux États-Unis."
"Les recherches futures devraient prioriser le développement de modèles personnalisés de stratification du risque qui intègrent les prédispositions génétiques, les comorbidités, les sous-types de cancer et les schémas thérapeutiques spécifiques afin de mieux prédire et atténuer le risque de TEV chez les patients atteints de cancer. Des études supplémentaires sont nécessaires pour mieux comprendre les voies thrombogéniques associées à différentes tumeurs malignes, ce qui pourrait conduire à des interventions spécifiques au cancer ciblant ces voies. Des essais cliniques se concentrant sur la durée et la posologie optimales de l'anticoagulation chez les patients atteints de cancer en rémission sont nécessaires pour fournir des recommandations fondées sur des données probantes pour la prise en charge des MTEV. Il est crucial d'élargir l'accès à la prophylaxie des MTEV dans les populations rurales et mal desservies. De même, des études de mise en œuvre évaluant l'adhésion aux protocoles de prophylaxie des MTEV dans divers milieux de soins pourraient affiner les recommandations actuelles. Des changements de politique visant à accroître la couverture d'assurance et à améliorer l'accès aux traitements anticoagulants joueraient également un rôle essentiel dans la réduction de la mortalité parmi les populations à haut risque. D'autres études devraient mettre l'accent sur la déclaration standardisée de la race et de l'origine ethnique, en veillant à ce que les diverses populations soient représentées avec précision Enfin, une approche interdisciplinaire combinant les soins cliniques, la défense des politiques et l’éducation des patients contribuera à réduire la mortalité par thrombose veineuse (MTEV) liée au cancer et à améliorer les résultats dans l’ensemble des populations "
L'avis de PERPLEXITY/IA
La prévention de la maladie thromboembolique veineuse (MTEV) chez les patients cancéreux présente des défis complexes, expliquant son application souvent suboptimale.
Plusieurs facteurs interdépendants contribuent à cette situation :
Facteurs liés aux risques cliniques
Risque hémorragique accru : Les anticoagulants réduisent de 59 % les événements thromboemboliques , mais doublent le risque d’hémorragies majeures. Cette balance bénéfice-risque incite à la prudence, surtout chez les patients avec un cancer avancé ou des comorbidités.
Hétérogénéité des profils de risque : Le risque de MTEV varie selon le type de cancer (pancréas, poumon), le stade, les traitements (chimiothérapie, hormonothérapie) et les facteurs individuels (obésité, antécédents thrombotiques. L’absence de stratification systématique par des outils comme le score de Khorana entraîne une sous-identification des patients éligibles à une prophylaxie primaire.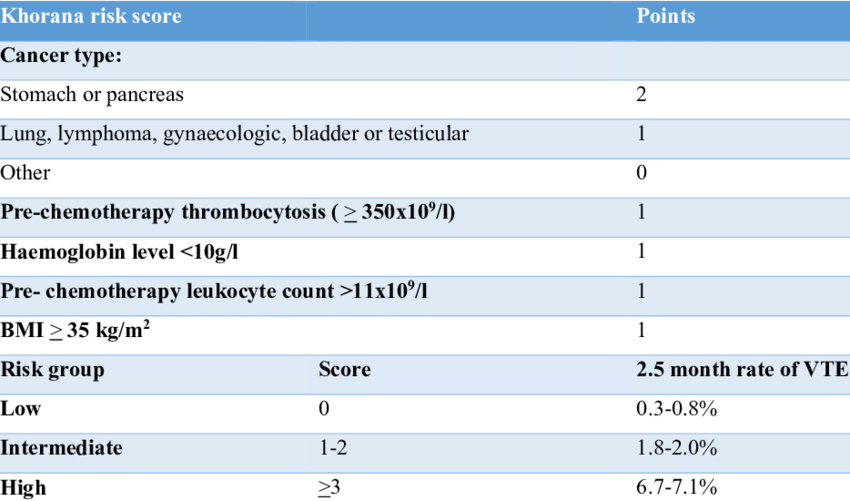
SCORE DE KHORANA
https://www.researchgate.net/figure/The-Khorana-venous-thromboembolism-risk-score_tbl4_334646882
Défis pratiques et organisationnels
Application inconstante des recommandations : Bien que les HBPM soient recommandées en postopératoire pour une durée de 7 à 30 jours selon le risque, leur utilisation reste limitée par la complexité des protocoles (doses ajustées au poids, fonction rénale) et la préférence pour les bas de contention.
Méconnaissance des guidelines : Les études soulignent une adoption insuffisante des directives, notamment dans la sélection des patients à haut risque ou la gestion des cathéters centraux. Par exemple, seuls 13 % des patients hospitalisés sans prophylaxie présentaient un cancer, contre 22 % dans le groupe traité
Limites des stratégies préventives
Efficacité partielle des anticoagulants : Même avec une prophylaxie optimale, le risque résiduel de MTEV persiste en raison de l’hypercoagulabilité induite par la tumeur. Les filtres de veine cave, bien que parfois utilisés, n’ont pas prouvé leur efficacité préventive.
Dilemmes thérapeutiques : Les anticoagulants oraux directs (AOD), bien que prometteurs, ont une place encore limitée en contexte cancéreux en raison d’études contradictoires sur leur sécurité à long terme. L’apixaban réduit les thromboses mais augmente les saignements majeurs, tandis que le rivaroxaban nécessite des validations supplémentaires.
En résumé, l’optimisation de la prévention nécessite une évaluation dynamique des risques, une meilleure formation des praticiens aux recommandations, et le développement de stratégies personnalisées intégrant les avancées pharmacologiques.
RECOMMANDATIONS / FRANCE
En milieu chirurgical
L’utilisation des HBPM en 1 injection par jour ou de l’héparine calcique en 3 injections par jour est recommandée à la dose prophylactique la plus élevée pour prévenir la MTEV post opératoire. Cette prophylaxie doit être débutée 2 à 12 heures avant l’intervention et être poursuivie au moins 7 à 10 jours. La pose de filtre cave n’est pas recommandée.
En milieu médical
La prophylaxie par HBPM, héparine calcique ou fondaparinux est recommandée chez les patients atteints de cancer hospitalisés et à mobilité réduite. Chez les patients traités par chimiothérapie, la prophylaxie systématique n’est pas recommandée. Une prophylaxie primaire pharmacologique peut être indiquée chez les patients avec un cancer du pancréas localement avancé ou métastatique ayant un faible risque hémorragique. Chez les patients atteints de myélome multiple et traités par thalidomide ou lenalidomide en association avec des corticoïdes et/ou une chimiothérapie (doxorubicine), une prophylaxie de la MTEV est recommandée.
Prophylaxie de la thrombose veineuse sur cathéter central
L’utilisation d’anticoagulants n’est pas recommandée dans la prophylaxie de la thrombose veineuse sur cathéter central. Le cathéter doit être inséré du côté droit, dans la veine jugulaire, l’extrémité distale du cathéter doit se situer à la jonction veine cave supérieure-oreillette droite.
https://www.portailvasculaire.fr/prevention-de-la-mtev-et-cancer#:~:text=L'utilisation%20des%20HBPM%20en,moins%207%20%C3%A0%2010%20jours.
Commentaire
La réalité US est-elle la nôtre en France ?
Cet article est important il doit nous interpeller surtout actuellement où les retards diagnostiques se multiplient du fait de délais de rendez-vous inadmissibles. La prévention est- elle optimale en matière de MTEV , pas si sûr. Une partie de la population renonce aux soins , les dépistages des cancers sont en panne.La prévention de la MTEV en médecine et notamment en cancérologie n'est pas optimale , elle l'est en chirurgie. Le score de KHORANA n'est pas souvent évalué, par défaut le score de PADOUE ou le score IMPROVE validé en prévention en médecine est adaptable en cancérologie, ils sont représentatifs en cancérologie . Par contre la prévention de la MTEV en chirurgie oncologique est une réalité. Mais il faut penser aussi à la prévention de la MTEV au décours des chimiothérapies et autres traitements du cancer.
Les cancers sont des affections graves, mais pourqoui les rendre plus graves en négligrabnt par exemple la prévention de MTEC au déciours des cancers ?
Quand on connaît les bienfaits du dépistage des cancers, pourquoi hésiter voire les refuser ?

A LIRE
Les chiffres du cancer en France
https://www.fondation-arc.org/cancer/le-cancer-en-chiffres-france-et-monde#:~:text=Les%20d%C3%A9c%C3%A8s%20li%C3%A9s%20au%20cancer,constante%20diminution%20depuis%2025%20ans.
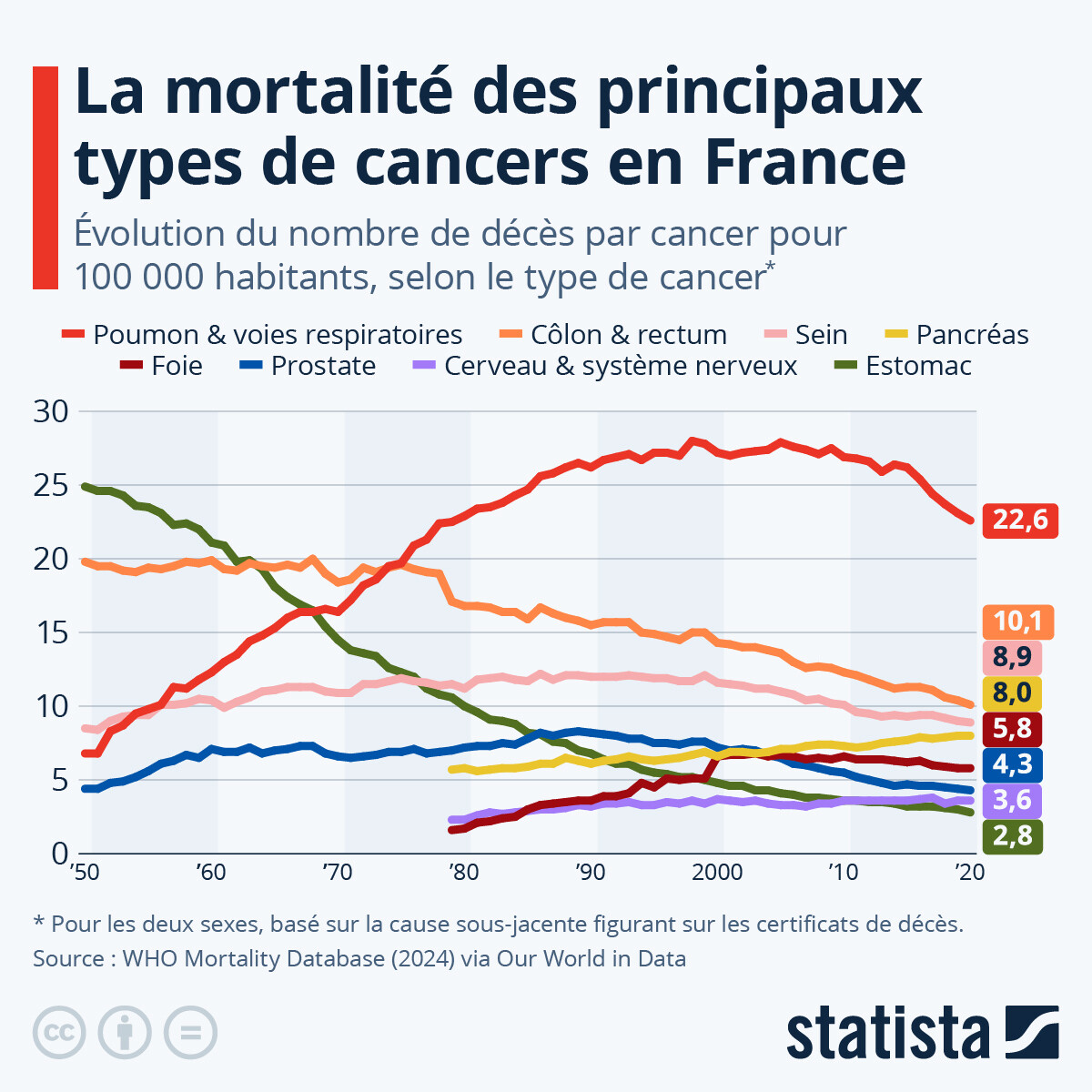
https://fr.statista.com/infographie/33252/taux-de-mortalite-des-principaux-types-de-cancer-en-france-evolution-depuis-1950/
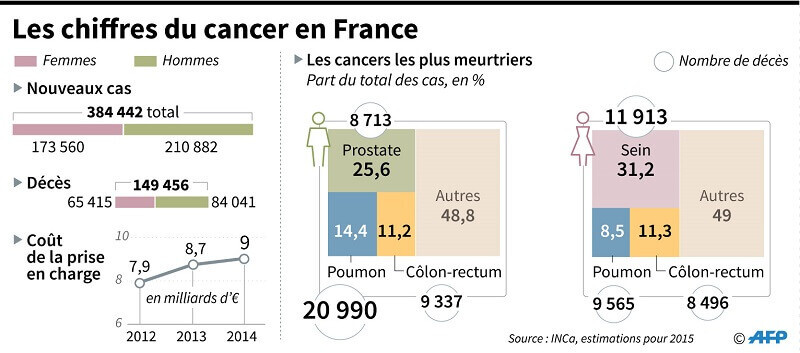 https://lymphomeetcompagnieblog.fr/2017/04/26/les-chiffres-du-cancer-en-france/
https://lymphomeetcompagnieblog.fr/2017/04/26/les-chiffres-du-cancer-en-france/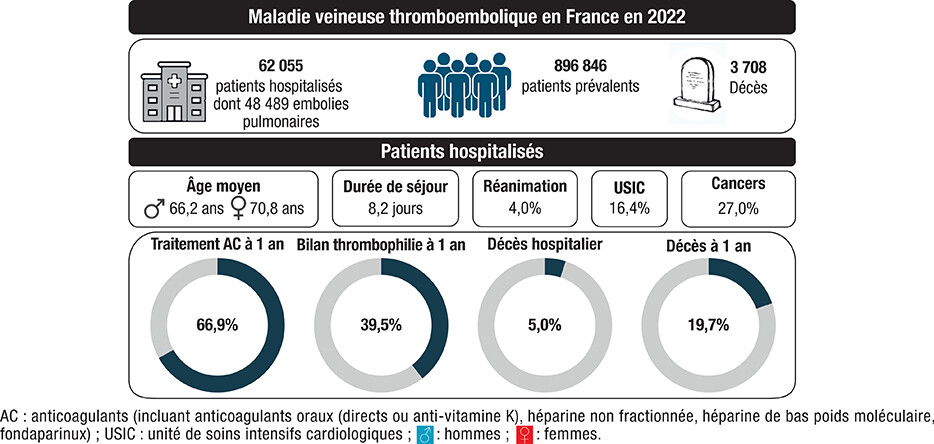
MTEV et CANCER : 10 messages et plus (2022)
Certaines études vont jusqu'à 9
2. En cas de maladie thromboembolique veineuse sans facteurs de risque connus, la prévalence d’un cancer occulte est de 5 à 10 % ; la plupart de ces cancers se révèlent au cours de la première année suivant le diagnostic de thrombose.
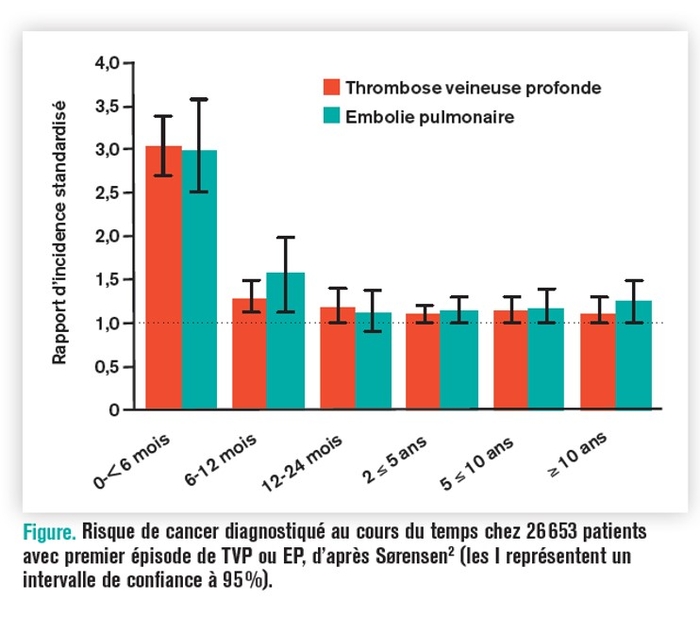
3. En cas de maladie thromboembolique veineuse récemment diagnostiquée, en l’absence de facteur déclenchant majeur, la recherche d’un cancer comporte un interrogatoire et un examen clinique soigneux, un bilan biologique minimal et la mise à jour des dépistages prévus en population générale. Des stratégies plus extensives sont encore en cours d’évaluation.
La CLINIQUE reste le point de départ, elle est incontournable et elle évite des fausses pistes.
4. Les héparines de bas poids moléculaire (HBPM) sont plus efficaces que les antivitamines K Les anticoagulants oraux directs ont une efficacité au moins comparable aux HBPM....voire plus
5. Le choix du type d’anticoagulant pour le traitement d’une maladie thromboembolique veineuse récente associée au cancer dépend du risque hémorragique, du type de cancer et de l’éventuel traitement antitumoral associé. Il est recommandé de prendre un avis d’expert en cas de doute.
6. Après six mois, s’il est bien toléré, le traitement anticoagulant curatif par héparines de bas poids moléculaire ou anticoagulants oraux directs à pleine dose est poursuivi tant que le cancer est actif ou traité, y compris par traitement hormonal.
7. Une thrombose veineuse du membre supérieur survient chez 2 à 6 % des patients atteints dé cancer porteurs d’un cathéter veineux central. En cas d’embolie pulmonaire au moment du diagnostic, le risque de récidive de l’événement thrombotique veineux est majoré.
8. Une thrombose veineuse profonde du membre supérieure proximale associée au cancer doit bénéficier d’un traitement anticoagulant à dose curative pendant au moins trois mois par héparines de bas poids moléculaire ou anticoagulants oraux directs. Le retrait du cathéter n’est pas systématique.
9. En dehors des périodes d’hospitalisation pour une affection aiguë ou pour une chirurgie carcinologique, il n’y a pas d’indication à un traitement prophylactique de la maladie thromboembolique veineuse systématique pour les patients ambulatoires ayant un cancer actif. Il ne doit se discuter qu’en cas de haut risque de thrombose, sans risque hémorragique majeur, au début de traitement et au cours de l’évolution.
10. L’indication d’une prophylaxie pour les patients ambulatoires recevant une chimiothérapie reste à l’étude, de même que la place des anticoagulants oraux directs dans cette situation.
Je rajouterai que les RCP ONCO THROMBOSE sont très importantes pour les cas difficiles, en cas d'association MTEV et CANCER

