" Si vous traversez l’enfer, continuez" Winston Churchill
https://academic.oup.com/eurheartj/advance-article/doi/10.1093/eurheartj/ehaf167/8107983?login=false
Les personnes atteintes d'insuffisance rénale chronique (IRC) présentent un risque accru de développer une maladie cardiovasculaire (MCV) avec ses manifestations : coronaropathie, accident vasculaire cérébral, insuffisance cardiaque, arythmies et mort subite d'origine cardiaque. (ne pas oublier l'artériopathie des MI)
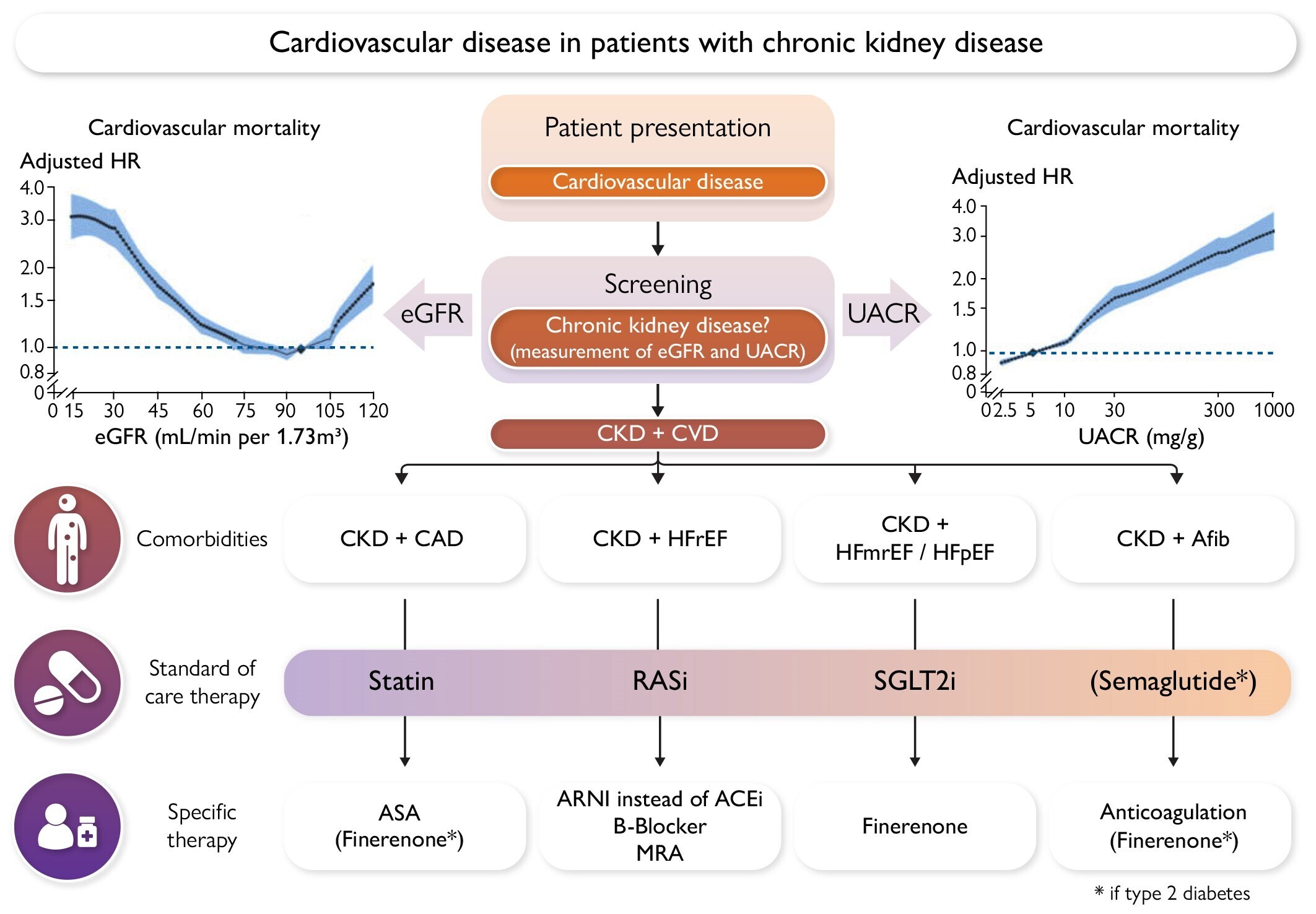
Les patients atteints d'insuffisance rénale chronique (IRC) présentent un risque accru de développer une maladie cardiovasculaire (MCV) avec ses différentes manifestations : coronaropathie, accident vasculaire cérébral (AVC), insuffisance cardiaque (IC), arythmies et mort subite d'origine cardiaque. De plus, la présence d'IRC a un impact majeur sur le pronostic des patients atteints de MCV, entraînant une augmentation de la morbidité et de la mortalité en présence des deux comorbidités.
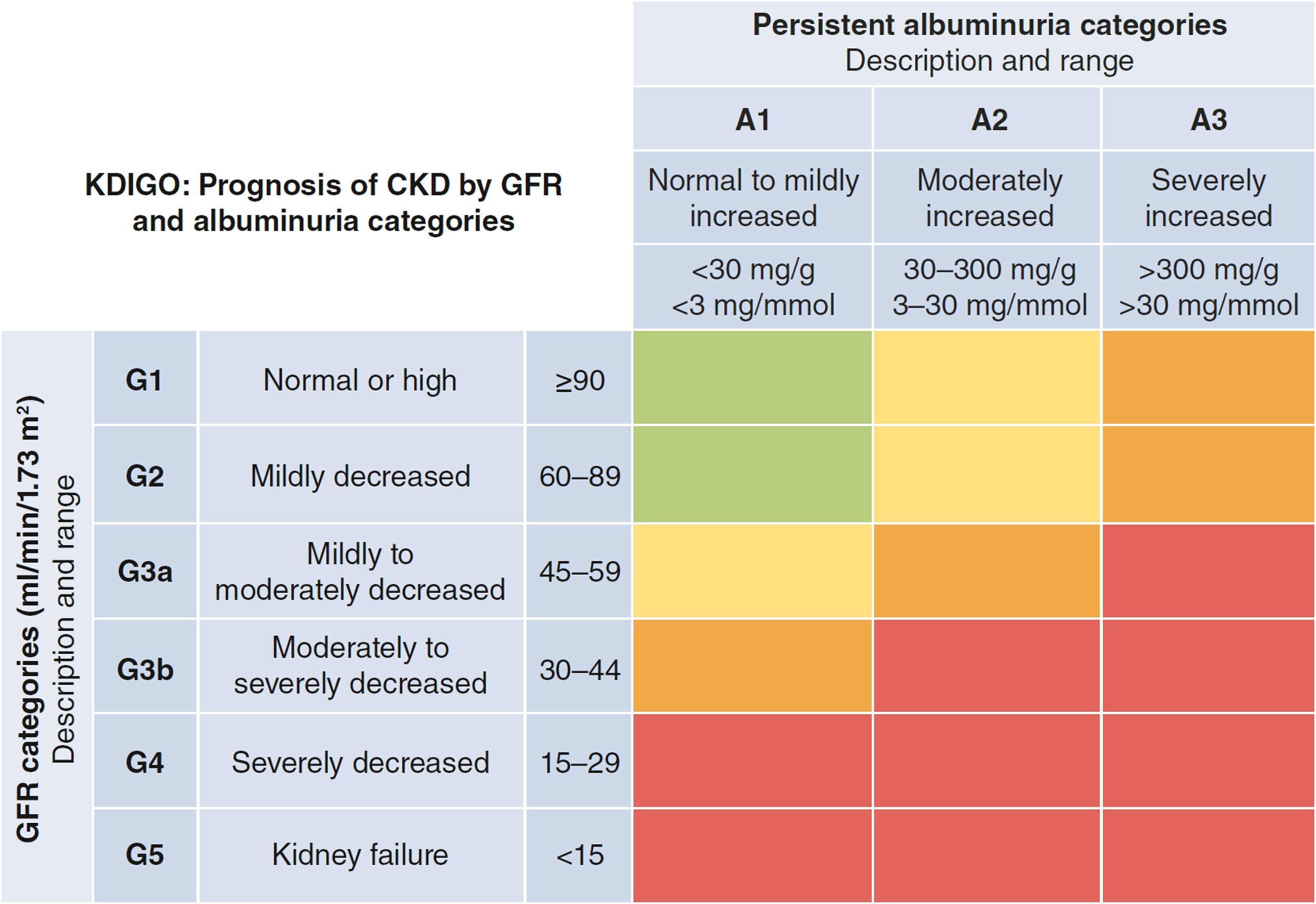
Nomenclature actuelle des maladies rénales chroniques utilisée par KDIGO. Système de stadification KDIGO pour les maladies rénales chroniques basé sur les catégories de débit de filtration glomérulaire et de rapport albumine/créatinine urinaire. Les couleurs représentent le risque de développer un besoin de dialyse ou d'autres résultats pertinents, y compris les maladies cardiovasculaires. Le vert indique un faible risque (et représente l'absence de maladie rénale chronique en l'absence de preuve structurelle ou histologique de maladie rénale). Comparé à un faible risque (estimé à 0,04/1 000 patients-années), le jaune indique une maladie rénale chronique avec un risque modérément accru (au moins ∼5 fois), l'orange indique une maladie rénale chronique avec un risque élevé (au moins ∼20 fois) et le rouge indique une maladie rénale chronique avec un risque très élevé (au moins ∼150 fois).
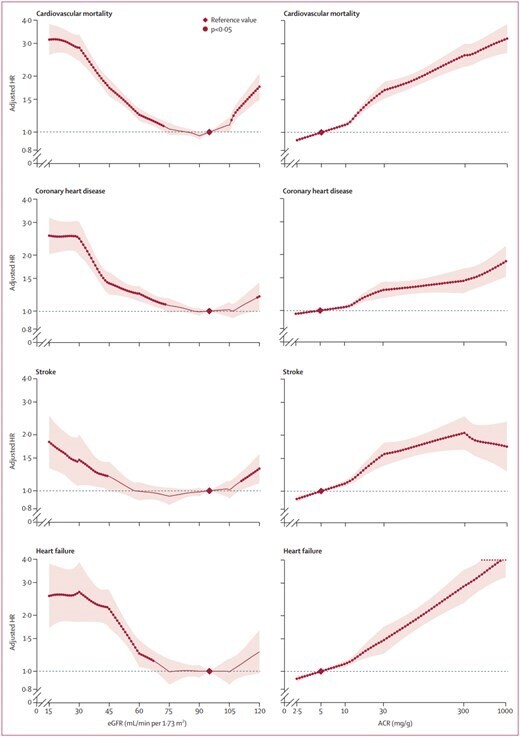
Rapports de risque ajustés et IC à 95 % (zones ombrées ou graphiques à moustaches) de mortalité cardiovasculaire (rangée supérieure), de maladie coronarienne (deuxième rangée), d'accident vasculaire cérébral (troisième rangée) et d'insuffisance cardiaque (rangée inférieure) selon le débit de filtration glomérulaire estimé (colonne de gauche) et le rapport albumine/créatinine (colonne de droite) dans la population générale combinée et les cohortes à haut risque. La référence est un débit de filtration glomérulaire estimé de 95 mL/min/1,73 m² et un rapport albumine/créatinine de 5 mg/g (losange). Les points représentent la signification statistique ( p < 0,05). *Les ajustements ont été effectués en fonction de l'âge, du sexe, de la race/origine ethnique, du tabagisme, de la pression artérielle systolique, des médicaments antihypertenseurs, du diabète, des concentrations de cholestérol total et de cholestérol des lipoprotéines de haute densité, et de l'albuminurie (rapport albumine/créatinine ou bandelette réactive) ou du débit de filtration glomérulaire estimé, selon le cas. Les analyses du débit de filtration glomérulaire estimé ont révélé 629 776 décès cardiovasculaires, 144 874 cas de coronaropathie, 137 658 cas d'accident vasculaire cérébral et 105 127 cas d'insuffisance cardiaque. Les analyses du rapport albumine/créatinine ont révélé 120 148 décès cardiovasculaires, 91 185 cas de coronaropathie, 82 646 cas d'accident vasculaire cérébral et 55 855 cas d'insuffisance cardiaque. Figure de Matsushita
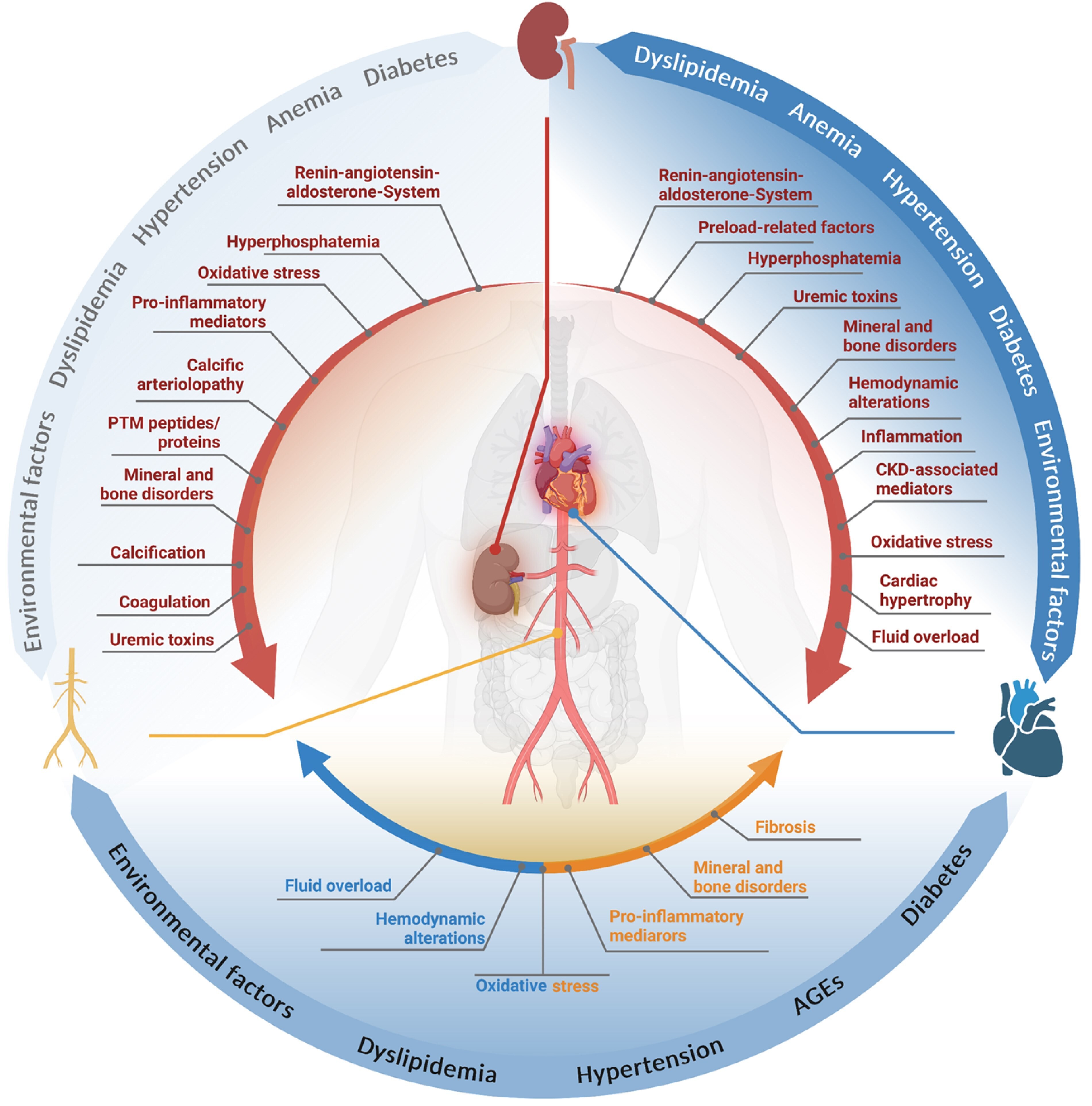
Interactions organiques entre le rein et le système cardiovasculaire dans l'insuffisance rénale chronique. Divers médiateurs et mécanismes contribuent au développement et à la progression des maladies cardiovasculaires chez les patients atteints d'insuffisance rénale chronique, et une interaction complexe de facteurs caractérise les interactions organiques multiformes entre le système cardiovasculaire et le rein dans le contexte de l'insuffisance rénale chronique. AGE : produits finaux de glycation avancée ; PTM : modification post-traductionnelle.
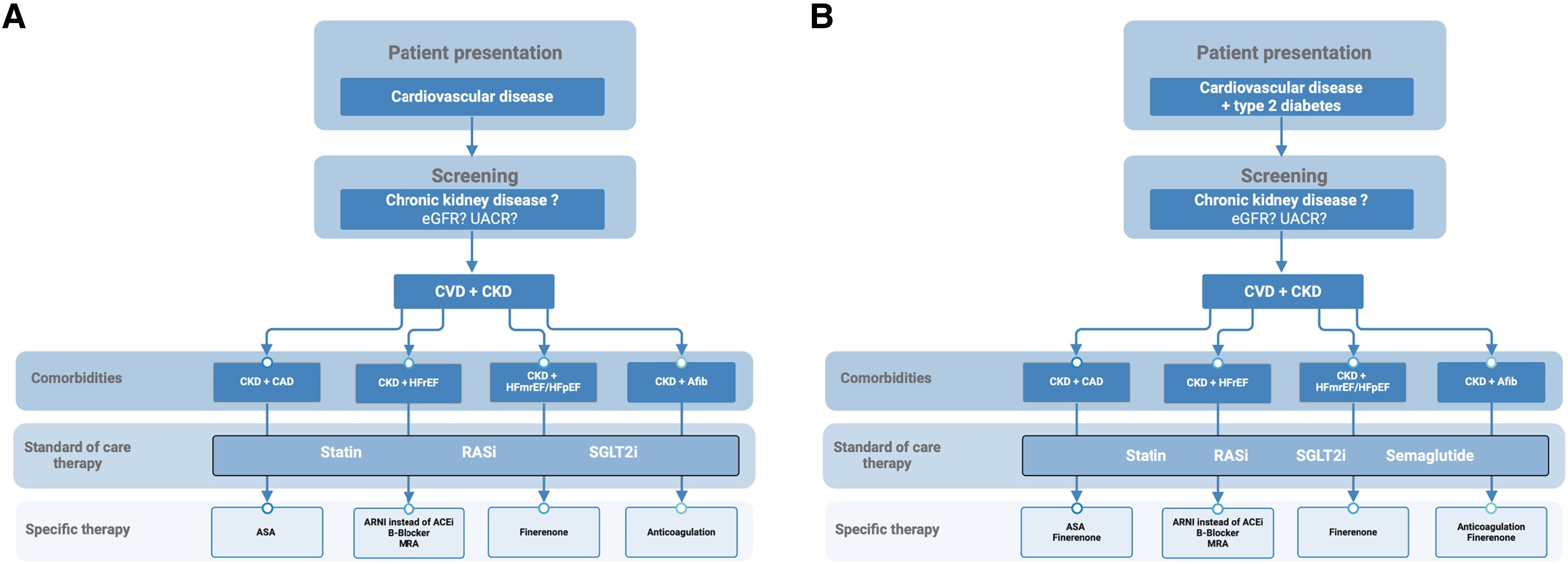
Approche clinique pour la prise en charge des maladies cardiovasculaires chez les patients atteints d'insuffisance rénale chronique non hémodialysés. A , Tous les patients atteints d'une maladie cardiovasculaire doivent être dépistés pour la présence d'une maladie rénale chronique par la mesure du débit de filtration glomérulaire estimé (DFGe) ainsi que par l'évaluation du rapport albumine/créatinine urinaire (RACU) dans l'urine ponctuelle. Les patients atteints à la fois d'une maladie cardiovasculaire et d'une maladie rénale chronique bénéficient d'un traitement standard par statine, inhibiteur du SRA (inhibiteur de l'enzyme de conversion de l'angiotensine ou antagoniste des récepteurs de l'angiotensine II) ainsi qu'un inhibiteur du cotransporteur sodium-glucose-2, en plus d'un contrôle strict de la pression artérielle avec une pression artérielle systolique < 130 mmHg. De plus, selon la manifestation de la maladie cardiovasculaire (coronaropathie, insuffisance cardiaque avec fraction d'éjection réduite (ICFEr), insuffisance cardiaque avec fraction d'éjection légèrement réduite/fraction d'éjection préservée (ICFEmr/ICFEp) ou fibrillation auriculaire, des traitements spécifiques supplémentaires doivent être mis en œuvre). B , Tous les patients atteints de maladie cardiovasculaire et de diabète de type 2 doivent être dépistés pour la présence d'une maladie rénale chronique par la mesure du DFGe ainsi que par l'évaluation du RACU dans l'urine ponctuelle. Les patients atteints de maladie cardiovasculaire, de diabète de type 2 et d'une maladie rénale chronique bénéficient d'un traitement standard par statine, sémaglutide, inhibiteur du SRA (inhibiteur de l'enzyme de conversion de l'angiotensine ou antagoniste des récepteurs de l'angiotensine II) ainsi qu'un inhibiteur du cotransporteur sodium-glucose 2 en plus d'un contrôle strict de la pression artérielle (pression artérielle systolique < 130 mmHg). De plus, en fonction de la manifestation de la maladie cardiovasculaire (maladie rénale chronique, ICFEr, ICFEmr/ICFEp ou fibrillation auriculaire), des traitements spécifiques supplémentaires doivent être mis en œuvre. FA, fibrillation auriculaire ; AAS, acide acétylsalicylique ; B-bloquant, bêtabloquant ; ARM, antagoniste des récepteurs des minéralocorticoïdes.
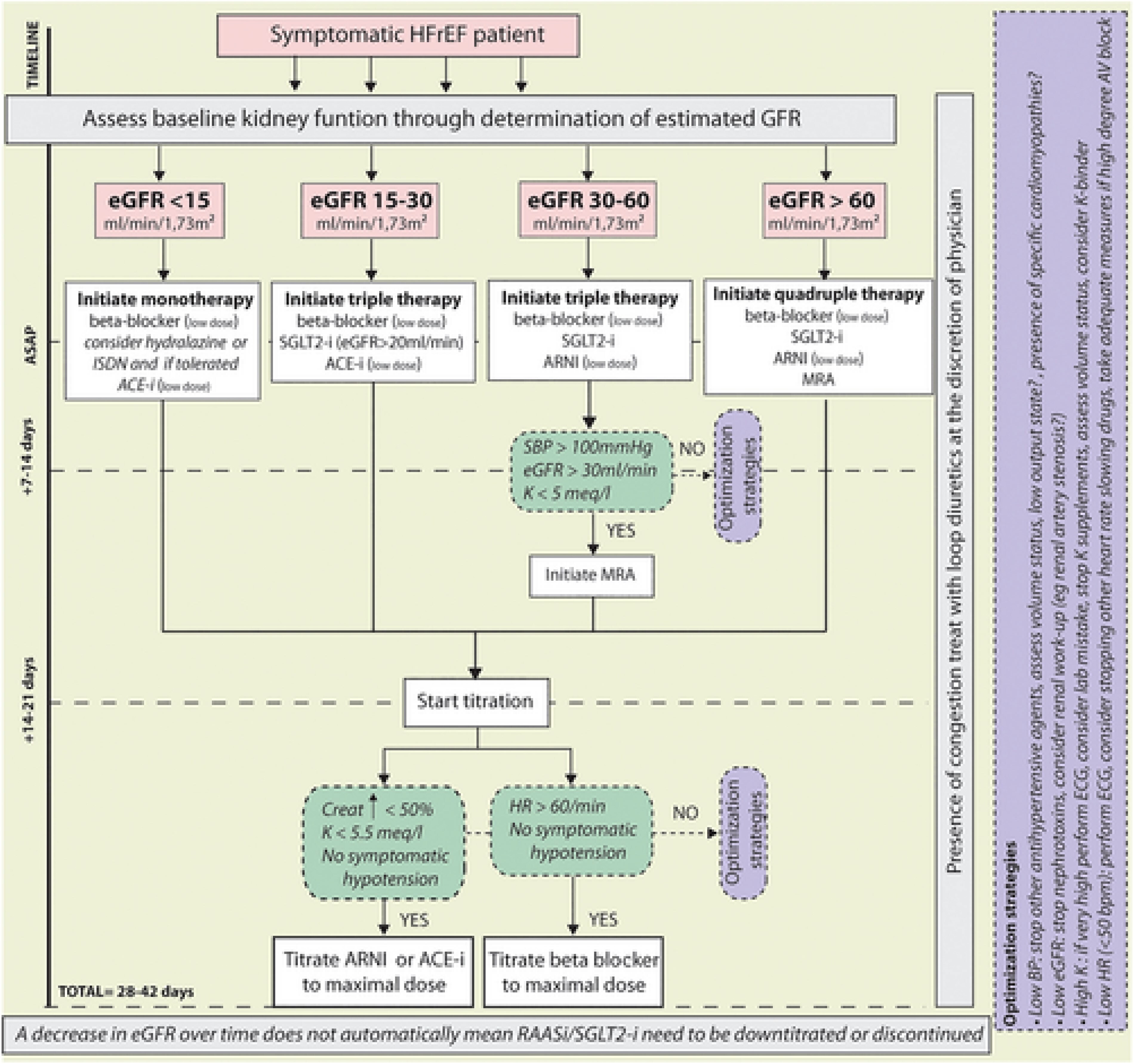
Approche rénale pour l'instauration et la titration d'un traitement médical multiniveaux, basé sur les recommandations. Organigramme proposé pour la titration d'un traitement médical basé sur les recommandations dans le contexte de l'insuffisance rénale chronique. Lors de la titration, le seuil tensionnel inférieur doit être individualisé en fonction de la présence d'une hypotension limitant l'activité plutôt que des valeurs tensionnelles pures. IEC, inhibiteur de l'enzyme de conversion de l'angiotensine ; ARNI, inhibiteur du récepteur de l'angiotensine-néprilysine ; AV, auriculo-ventriculaire ; PA, pression artérielle ; Creat, créatinine ; ECG, électrocardiogramme ; DFGe, débit de filtration glomérulaire estimé ; FC, fréquence cardiaque ; ISDN, dinitrate d'isosorbide ; K, potassium ; ARM, antagoniste des récepteurs des minéralocorticoïdes ; RAASi, inhibiteur du système rénine-angiotensine-aldostérone ; PAS, pression artérielle systolique ; SGLT2-i, inhibiteur du cotransporteur sodium-glucose de type
Messages clés de conclusion pour le clinicien pour la prise en charge des maladies cardiovasculaires dans l'IRC
Dépistage de tous les patients atteints de maladies cardiovasculaires pour détecter la présence d'IRC
Tous les patients atteints de MCV doivent être dépistés pour la présence d'IRC en évaluant le DFGe défini par CKD-EPI et UACR dans l'urine ponctuelle, car la présence de ces deux comorbidités a un impact majeur sur le pronostic ainsi que sur la mise en œuvre de thérapies supplémentaires réduisant le risque de MCV.
Réduction du risque CV chez les patients atteints de maladies cardiovasculaires et d'IRC
Les patients atteints de MCV et d'IRC doivent recevoir le traitement standard suivant pour réduire le risque de MCV : contrôle strict de la pression artérielle (PAS < 130 mmHg), traitement par statines, traitement par inhibiteurs de la recapture de la sérotonine (IRA) avec IEC ou ARA, ainsi qu'un traitement par inhibiteur du SGLT2. Chez les patients atteints de MCV, d'IRC et de diabète de type 2, un traitement complémentaire par finérénone et sémaglutide est indiqué pour réduire davantage le risque de MCV et d'insuffisance rénale.
Gestion interdisciplinaire centrée sur le patient
Globalement, la prise en charge des maladies cardiovasculaires chez les patients atteints d'IRC nécessite une approche interdisciplinaire incluant cardiologues, néphrologues, médecins généralistes et autres professionnels de santé afin de mettre en œuvre des stratégies fondées sur des données probantes et centrées sur la personne, afin de réduire le fardeau de la maladie pour chaque patient et d'améliorer le pronostic. De plus, l'éducation et la sensibilisation des patients sont essentielles à une prise en charge réussie de ce groupe de personnes à haut risque.
Insuffisance rénale et maladies cardiovasculaires
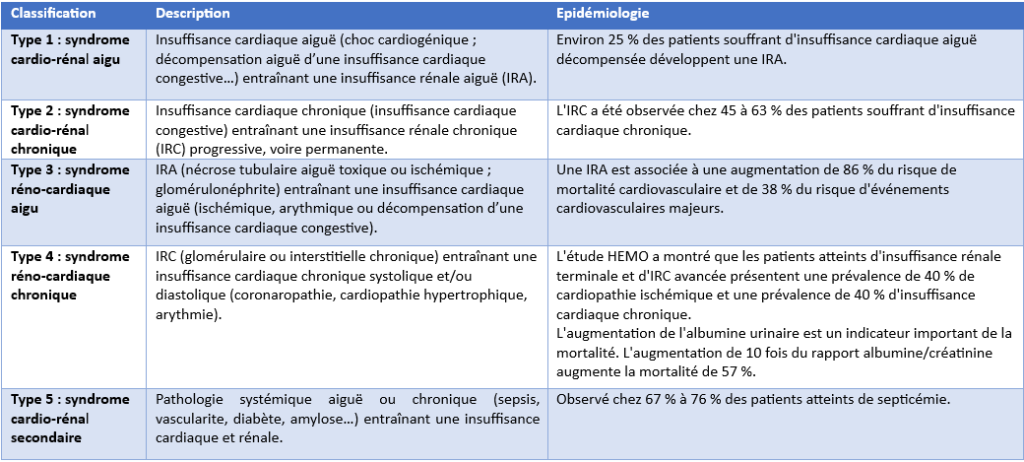
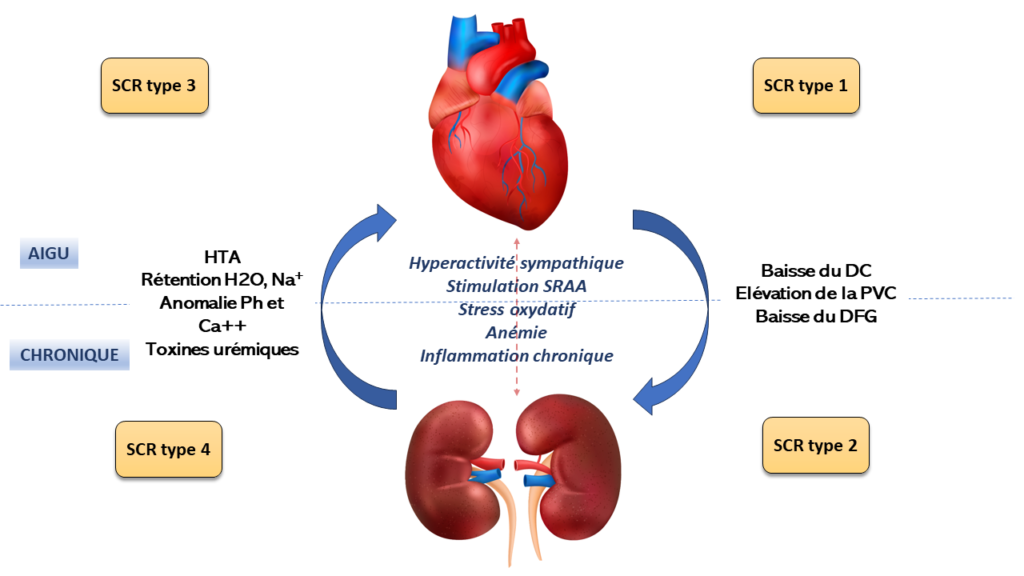
Résumé des mécanismes physiopathologiques des différents syndromes cardio-rénaux (SCR). HTA : hypertension artérielle ; SRAA : système rénine–angiotensine–aldostérone ; DC : débit cardiaque ; PVC : pression veineuse centrale ; DFG : débit de filtration glomérulaire
https://sitegpr.com/fr/rein/en-savoir-plus/cardiologie-et-insuffisance-renale/ https://maux-croises.fr/les-maux-croises/maladie-renale-chronique-et-maladie-coronarienne/
https://maux-croises.fr/les-maux-croises/maladie-renale-chronique-et-maladie-coronarienne/
SYNTHESE
Cette revue de l'état de l'art parue dans l'European Heart Journal en 2025 examine en profondeur le lien complexe entre la maladie cardiovasculaire et la maladie rénale chronique. Elle met en lumière la prévalence accrue des problèmes cardiaques chez les patients atteints de troubles rénaux et explore les mécanismes physiopathologiques communs qui sous-tendent cette association. L'article offre également un aperçu des stratégies actuelles de réduction du risque cardiovasculaire adaptées à cette population spécifique, incluant la gestion des facteurs de risque traditionnels et les traitements pharmacologiques récents. Enfin, il aborde la prise en charge des manifestations spécifiques de la maladie cardiovasculaire, telles que les pathologies coronariennes, l'insuffisance cardiaque et la fibrillation auriculaire, chez les patients souffrant de maladie rénale chronique. (NoteBookLM)
Commentaire par PERPLEXITY /IA
Les mécanismes expliquant l'impact de l'insuffisance rénale chronique (IRC) sur le système cardiovasculaire impliquent des interactions complexes entre les deux systèmes. Voici les principaux facteurs pathophysiologiques :
1. Dysrégulation tensionnelle et surcharge volumique
-
La rétention hydrosodée réduit l'excrétion rénale de sodium et d'eau, augmentant la volémie et la pression artérielle.
-
L'activation excessive du système rénine-angiotensine-aldostérone (SRAA) provoque une vasoconstriction et une hypertrophie ventriculaire gauche.
-
Ces mécanismes entraînent une hypertension artérielle dans 80 à 85 % des cas d'IRC, forçant le cœur à travailler contre une résistance accrue
2. Altérations métaboliques et hormonales
-
Les déséquilibres calciques et phosphatés (hyperphosphatémie, hypocalcémie) induisent une calcification vasculaire et une rigidité artérielle
-
L'anémie fréquente en IRC (par déficit en érythropoïétine) réduit la capacité de transport d'oxygène, provoquant une tachycardie compensatrice et une hypertrophie cardiaque.
-
L'acidose métabolique chronique altère la contractilité myocardique et favorise l'hyperkaliémie arythmogène
3. Inflammation et stress oxydatif
-
L'accumulation de toxines urémiques (comme la parathormone et les produits de glycation avancée) active des voies pro-inflammatoires26.
-
Le stress oxydatif endommage l'endothélium vasculaire et accélère l'athérogenèse26.
-
Ces processus favorisent la dysfonction endothéliale et la formation de plaques d'athérome coronarienne
4. Remodelage cardiaque
-
La surcharge pressionnelle (HTA) et volumique (rétention hydrique) conduit à une hypertrophie ventriculaire gauche, présente chez 75 % des patients dialysés.
-
La fibrose myocardique résultant de l'activation du SRAA et de l'inflammation altère la compliance ventriculaire.
5. Facteurs de risque partagés
-
Les comorbidités communes (diabète, dyslipidémie) potentialisent les lésions vasculaires.
-
L'hyperparathyroïdie secondaire aggrave la calcification des artères coronaires.
Ces mécanismes s'entretiennent mutuellement, créant un cercle vicieux où chaque atteinte organique aggrave l'autre. Les maladies cardiovasculaires représentent ainsi 50 % des décès chez les patients IRC, avec un risque relatif multiplié par 10 à 30 comparé à la population générale
Impact des thérapies récentes
-
Les inhibiteurs du SGLT2 réduisent la mortalité cardiovasculaire en agissant sur la réabsorption tubulaire du glucose et la diminution de la pression intraglomérulaire.
-
Les agonistes du GLP-1 améliorent le contrôle glycémique tout en réduisant l’inflammation et le stress oxydatif systémique
La finérénone représente une avancée importante dans le traitement des patients atteints de MRC et DT2, en offrant une double protection rénale et cardiovasculaire. Bien que son efficacité soit prometteuse, sa place exacte dans l'arsenal thérapeutique doit encore être clarifiée, notamment en comparaison avec les gliflozines
Commentaire
Quand le rein est malade , le coeur et les vaisseaux le sont aussi ! Un résumé simpliste qui colle à la réalité. Si on rajoute le diabète de type 2 on peut affirmer que cette traide est à sur risque sur le plan de la morbi-mortalité
Copyright : Dr Jean Pierre Laroche / 2025

