"Rivières: hémorragie des montagnes" Sylvain Tesson

Sen L, Kangpin X, Yihui L. Research progress on bleeding risk assessment models in anticoagulant therapy. Progrès de la recherche sur les modèles d'évaluation du risque hémorragique sous traitement anticoagulant
Front Cardiovasc Med. 2025 Nov 11;12:1645823. doi: 10.3389/fcvm.2025.1645823. PMID: 41306267; PMCID: PMC12644015.
https://pmc.ncbi.nlm.nih.gov/articles/PMC12644015/
Article en accès libre
L'équilibre entre la prévention des thromboembolies et la prise en charge des complications hémorragiques demeure un enjeu majeur du traitement anticoagulant.
Si les modèles d'évaluation du risque hémorragique (MER) établis, tels que HAS-BLED et HEMORR 2 HAGES, ont été initialement développés pour les patients traités par warfarine, leur applicabilité aux patients sous anticoagulants oraux non antagonistes de la vitamine K (AOD) et aux populations atteintes de thromboembolie veineuse (TEV) restait incertaine.
Cette revue synthétise les avancées récentes en matière de stratification du risque hémorragique chez les patients atteints de fibrillation auriculaire (FA) et de TEV, en s'intéressant à la performance des modèles, aux adaptations spécifiques à chaque médicament et aux nouvelles approches établies sur les biomarqueurs.
Chez les patients atteints de FA, les MER traditionnels (HAS-BLED, HEMORR 2 HAGES, ATRIA) ont démontré une précision prédictive modérée (AUC : 0,55-0,74) dans les cohortes sous AOD, HEMORR 2 HAGES présentant une discrimination supérieure dans certaines études. L'ABC intégrant des biomarqueurs (GDF-15, troponine et hémoglobine) et le score DOAC spécifique aux AOD ont permis une meilleure stratification du risque, ce dernier présentant une aire sous la courbe (C) supérieure à celle du HAS-BLED.
Chez les patients atteints de MTEV, l'IMPROVE (AUC : 0,62-0,73) a permis d'identifier efficacement les patients hospitalisés à haut risque, tandis que le RIETE (incidence des hémorragies majeures : 0,1 %-6,2 %) et l'EINSTEIN (C : 0,68-0,74) ont pris en compte les risques dynamiques sous anticoagulation.
Cependant, l'hétérogénéité des cohortes de validation, des définitions des critères d'évaluation (par exemple, critères ISTH vs TIMI) et des facteurs de risque statiques sélectionnés a limité la généralisation des résultats. Les modèles d'évaluation du risque (RAM) actuels ont présenté des performances variables selon les schémas anticoagulants et les contextes cliniques, soulignant la nécessité de modèles de nouvelle génération intégrant des modificateurs de risque dynamiques (par exemple, anémie transitoire, utilisation d'antiagrégants plaquettaires) et des approches basées sur les biomarqueurs.
Bien que les outils spécifiques aux AOD, tels que l'AOD, puissent être plus appropriés pour les patients atteints de fibrillation auriculaire, les modèles adaptés au contexte, comme IMPROVE et RIETE, sont mieux adaptés aux populations atteintes de thromboembolie veineuse. Les recherches futures devraient privilégier la validation en conditions réelles, l'intégration de l'apprentissage automatique et la standardisation des définitions des saignements afin de perfectionner les stratégies d'anticoagulation de précision.
RESUME GEBERATIF
Ce document traite des progrès de la recherche sur les modèles d'évaluation du risque de saignement dans le cadre de la thérapie anticoagulante.
Modèles d'évaluation du risque de saignement
L'évaluation du risque de saignement est essentielle dans la thérapie anticoagulante pour prévenir les événements thromboemboliques.
- * Les modèles d'évaluation du risque de saignement (RAM) comme HAS-BLED et HEMORR2HAGES ont été initialement développés pour les patients sous warfarine.
- * L'applicabilité de ces modèles aux utilisateurs de NOAC et aux populations de thromboembolie veineuse (VTE) reste incertaine.
- * Les modèles traditionnels montrent une précision prédictive modérée (AUC : 0,55–0,74) pour les patients AF sous NOAC.
- * Des modèles spécifiques aux NOAC, comme le score DOAC, ont montré une meilleure stratification des risques.
Évaluation du risque de saignement chez les patients AF
L'évaluation du risque de saignement chez les patients atteints de fibrillation auriculaire (AF) est cruciale pour la gestion des anticoagulants.
- * Le modèle HAS-BLED inclut des facteurs de risque tels que l'hypertension et l'âge avancé, un score ≥3 indiquant un risque élevé.
- * Le modèle ORBIT évalue l'anémie et l'historique de saignement, avec un score ≥4 indiquant un risque élevé.
- * Le modèle ATRIA attribue des points pour l'anémie et l'âge, avec un score de 5-10 indiquant un risque élevé.
- * Le modèle ABC intègre des biomarqueurs pour une prédiction dynamique et individualisée du risque de saignement.
Comparaison des modèles de risque de saignement
La comparaison des modèles de risque de saignement aide à identifier le meilleur outil pour les patients sous anticoagulants.
- Les valeurs AUC pour HAS-BLED, HEMORR2HAGES et ATRIA chez les utilisateurs de warfarine étaient respectivement de 0,72, 0,69 et 0,74.
- Pour les utilisateurs de NOAC, les AUC étaient plus faibles, avec HEMORR2HAGES montrant la meilleure performance.
- Le modèle ABC a montré un rapport de risque plus élevé pour identifier les patients à haut risque par rapport à HAS-BLED.
Évaluation du risque de saignement chez les patients VTE
L'évaluation du risque de saignement chez les patients atteints de thromboembolie veineuse (VTE) est essentielle pour la prévention des complications.
- Le modèle IMPROVE a été développé spécifiquement pour la prévention de la VTE, avec un score ≥7 indiquant un risque élevé.
- Des études ont montré que le modèle IMPROVE a une sensibilité de 34,0% et une spécificité de 81,5% pour prédire les saignements.
- Le modèle HAS-BLED a également été utilisé chez les patients VTE, montrant une incidence de saignement cliniquement pertinent de 2,1% dans le groupe à faible risque.
Modèles spécifiques pour évaluer risque de saignement
Des modèles spécifiques ont été développés pour mieux évaluer le risque de saignement dans différents contextes cliniques.
- * Le modèle Kuijer inclut des facteurs simples comme l'âge et le sexe, avec un score ≥3 indiquant un risque élevé.
- * Le modèle ACCP couvre 18 facteurs de risque, mais a une capacité prédictive limitée pour les événements de saignement prolongés.
- * Le modèle RIETE a identifié six facteurs de risque associés à des saignements majeurs, avec une incidence de 6,2% dans le groupe à haut risque.
Évaluation du risque de saignement chez les patients âgés
Le score de risque de saignement Seiler a été développé pour prédire le risque de saignement chez les patients âgés sous anticoagulation prolongée.
- * Le score Seiler est basé sur l'étude SWITCO65+ et inclut sept variables.
- * Les catégories de risque sont : faible (0-1 point), intermédiaire (2-3 points), et élevé (≥4 points).
- Incidence de saignement majeur : 1,4 % (faible), 5,0 % (intermédiaire), 12,2 % (élevé) par an.
- * C-statistique pour prédire le risque de saignement : 0,78 à 3 mois et 0,71 à 36 mois.
- * Comparé à d'autres scores, le Seiler a montré une meilleure performance prédictive.
Comparaison des modèles de risque de saignement
Différents modèles de risque de saignement ont été évalués pour leur efficacité dans divers scénarios cliniques.
- * Les lignes directrices actuelles ne recommandent pas de modèle spécifique, mais le score HAS-BLED est suggéré par les directives NICE.
- * Le score VTE-BLEED a montré une incidence cumulative de saignement majeur de 13,2 % dans le groupe à haut risque.
- * Cinq modèles (Seiler, Kuijer, RIETE, HEMORR2HAGES, ATRIA) identifient un groupe à haut risque avec un taux de saignement annuel de 6,5 %.
Modèles de risque de saignement pour populations spéciales
Les patients atteints de cancer et ceux à risque de saignement gastro-intestinal nécessitent des modèles spécifiques.
- * Les patients atteints de CAVTE ont un risque de saignement 2 à 6 fois plus élevé que les patients non cancéreux.
- * Le score IMPROVE est utilisé pour évaluer le risque de saignement chez les patients atteints de CAVTE.
- * Le modèle Alfalfa-DOAC-GIB a été développé pour prédire le risque de saignement gastro-intestinal chez les patients sous NOAC, avec un AUC de 0,778.
Évaluation du risque d'hémorragie intracrânienne
Plusieurs modèles sont utilisés pour prédire le risque d'hémorragie intracrânienne chez les patients subissant une thrombolyse.
- * Le modèle HAT évalue le risque d'hémorragie intracrânienne symptomatique avec un score allant de 0 à 5 points.
- * Le modèle SITS a une large applicabilité et un bon pouvoir prédictif (C-statistique = 0,70).
- * Le modèle SEDAN ne prend pas en compte les fluctuations de la pression artérielle, un facteur important pour le risque de saignement.
Conclusion sur les modèles de risque de saignement
Les modèles de risque de saignement montrent une performance variable et nécessitent des améliorations pour une meilleure application clinique.
- * La variabilité dans les conceptions d'études et les définitions de saignement complique la comparaison des modèles.
- * Les modèles traditionnels ont souvent une performance sous-optimale dans les populations traitées par NOAC.
- * L'intégration de facteurs dynamiques et l'utilisation de l'intelligence artificielle sont nécessaires pour améliorer la gestion des risques de saignement.
SYNTHÈSE / NOTEBOOKLM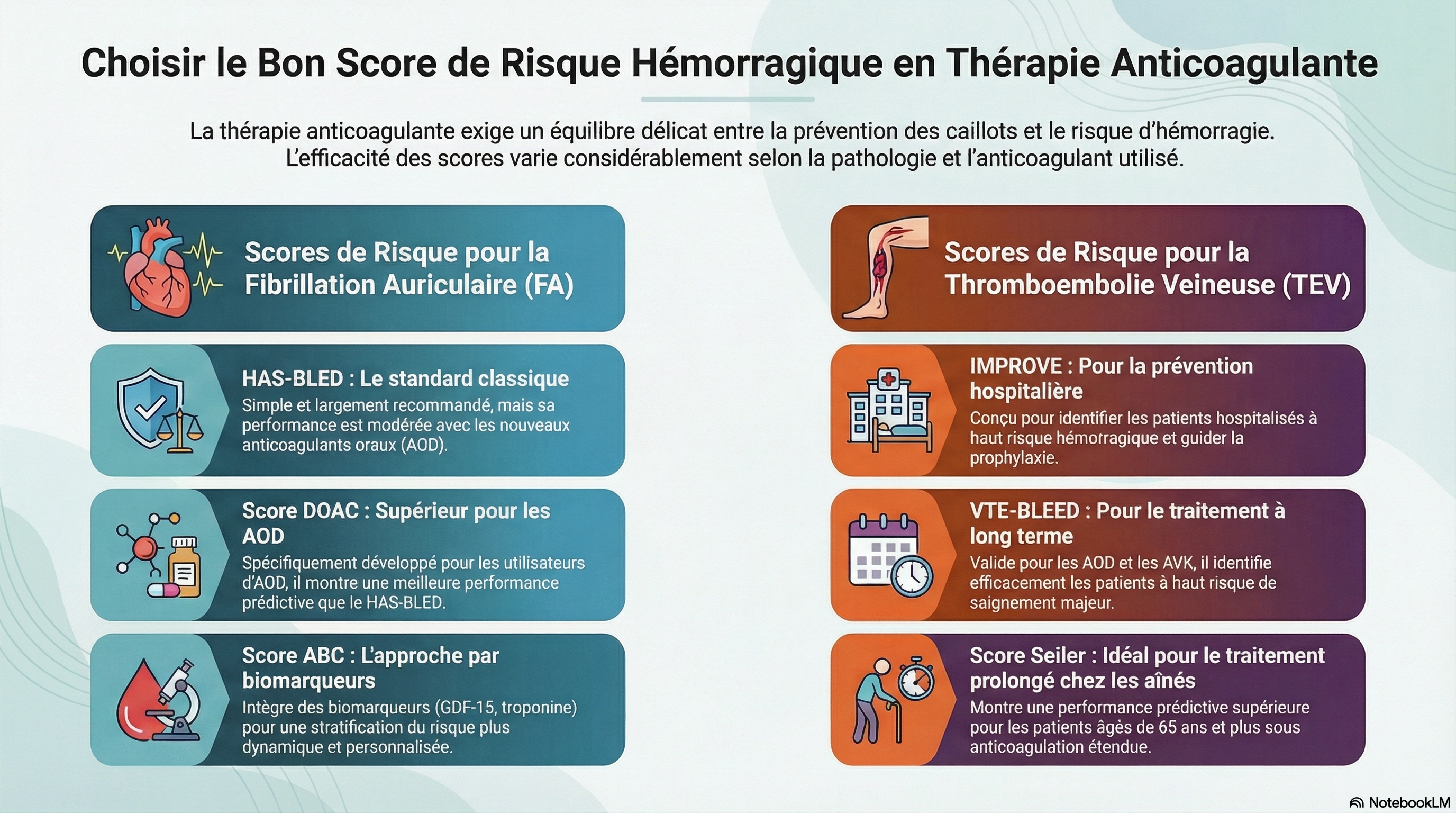 Cette revue scientifique analyse les modèles d'évaluation du risque hémorragique pour les patients sous traitement anticoagulant, particulièrement ceux souffrant de fibrillation atriale ou de thromboembolie veineuse. L'étude compare l'efficacité des scores traditionnels comme HAS-BLED avec de nouveaux outils adaptés aux anticoagulants oraux directs et aux approches basées sur les biomarqueurs. Les auteurs soulignent que l'application de ces modèles varie selon le contexte clinique, notamment pour les populations cancéreuses ou les cas d'hémorragies intracrâniennes. Le texte conclut sur la nécessité de développer des outils de prédiction dynamiques et personnalisés utilisant l'apprentissage automatique. Cette synthèse vise ainsi à améliorer la sécurité des patients en équilibrant la prévention des caillots et le risque de saignement.
Cette revue scientifique analyse les modèles d'évaluation du risque hémorragique pour les patients sous traitement anticoagulant, particulièrement ceux souffrant de fibrillation atriale ou de thromboembolie veineuse. L'étude compare l'efficacité des scores traditionnels comme HAS-BLED avec de nouveaux outils adaptés aux anticoagulants oraux directs et aux approches basées sur les biomarqueurs. Les auteurs soulignent que l'application de ces modèles varie selon le contexte clinique, notamment pour les populations cancéreuses ou les cas d'hémorragies intracrâniennes. Le texte conclut sur la nécessité de développer des outils de prédiction dynamiques et personnalisés utilisant l'apprentissage automatique. Cette synthèse vise ainsi à améliorer la sécurité des patients en équilibrant la prévention des caillots et le risque de saignement.
Le DIAPORAMA / NOTEBOOKLM

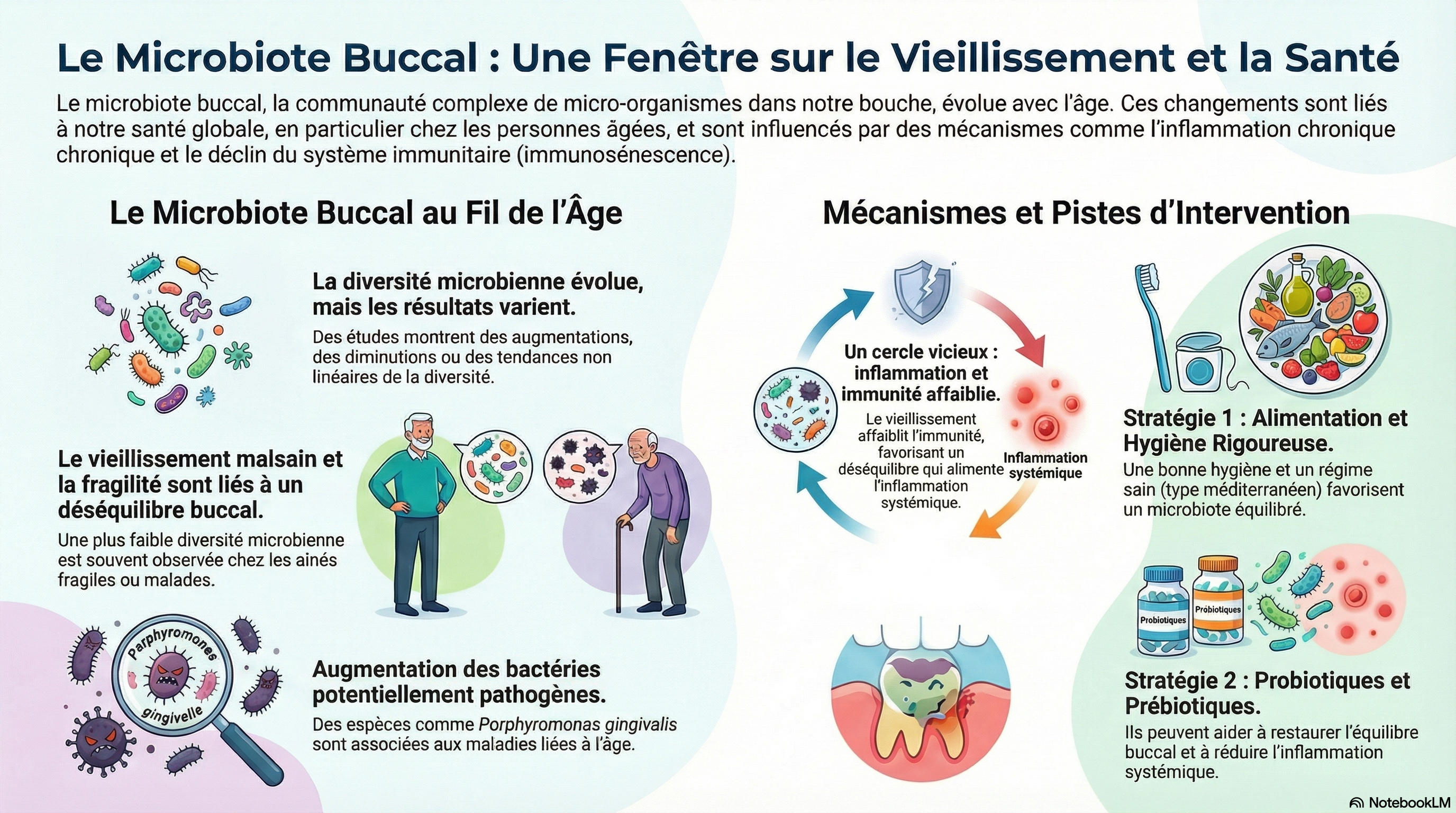






Le risque hémorragique chez les patients anticoagulés reste difficile à évaluer, que ce soit pour la FA ou la MTEV
Cette étude conclut à la nécessité d'utiliser l'IA (Machine Learning) pour évaluer ce risque.
En attendant, chaque cas est différent, les scores peuvent être une aide mais le plus souvent c'est le médecin qui doit décider dans la VRAIE VIE.
Pour les sujets âgés, ne pas oublier les 5 C.
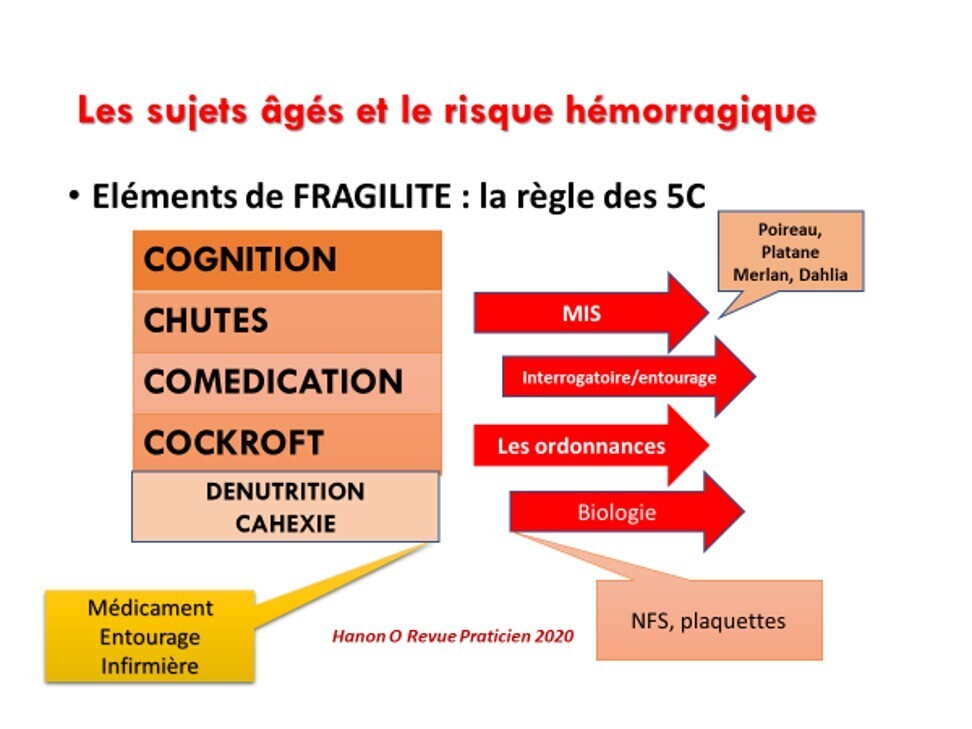
Les responsables du risque hémorragique
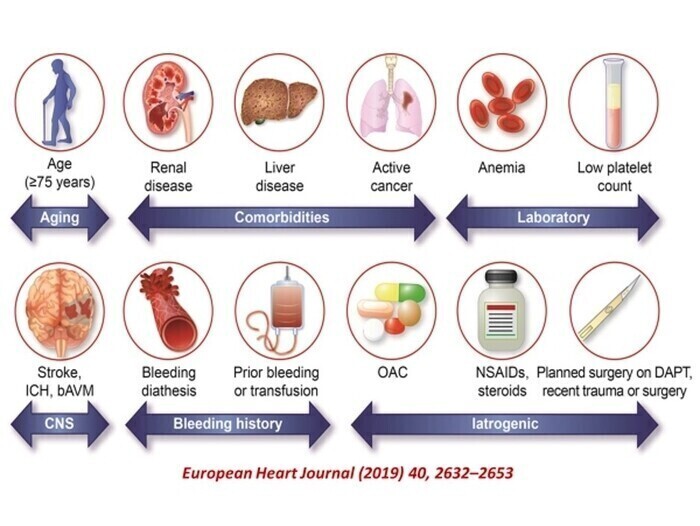 Le SCORE HEMORRAGIQUE de SEILER
Le SCORE HEMORRAGIQUE de SEILERThe clinical score is based on seven clinical factors (previous bleeding, active cancer, low physical activity, anemia, thrombocytopenia, antiplatelet drugs/NSAIDs, and poor INR control).
- Éthique de la décision médicale
- Réflexion philosophique
- Jacques Ricot
- Dans Laennec 2014/4 (Tome 62), pages 40 à 50
https://www.cairn.info/revue-laennec-2014-4-page-40.htm#:~:text=Issu%20de%20la%20loi%20du,les%20d%C3%A9cisions%20concernant%20sa%20sant%C3%A9.%20%C2%BB

