"Langue. Greffe d'un sens commun dans le cerveau de chacun, qui permet à chacun d'être un pays, de faire partie d'un peuple.” Jacques Ferron
Jean Pierre LAROCHE
Clics : 2325
IA : Rejet greffe rénale "made in France"
"Je me permets de dire que les problèmes vraiment difficiles de la morale ne sont pas de choisir entre le Bien et le Mal. Les cas bien plus difficiles sont ceux où l’on doit choisir entre le gris et le gris". Paul RICŒUR, « L’éthique, entre le Mal et le Pire »
« Ces vingt dernières années, la progression des connaissances de la maladie, le rejet du greffon, nous a fait découvrir qu’elle [était] beaucoup plus complexe qu’on le pensait », explique Alexandre Loupy.
« Ces vingt dernières années, la progression des connaissances de la maladie, le rejet du greffon, nous a fait découvrir qu’elle [était] beaucoup plus complexe qu’on le pensait », explique Alexandre Loupy.
Préambule
Quelques chiffres
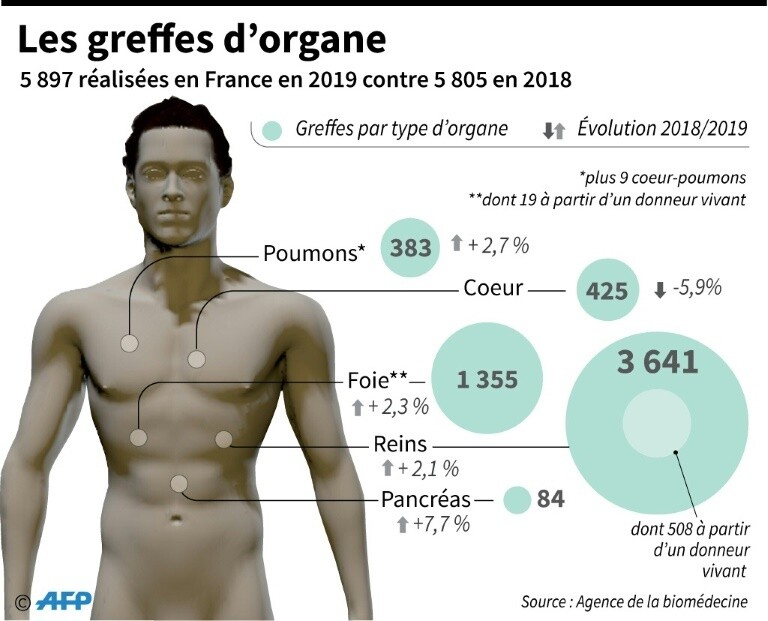
https://www.sciencesetavenir.fr/sante/les-greffes-d-organes-repartent-a-la-hausse-en-2019-en-france_140673
 https://fondation-du-rein.org/le-don-dorganes/
https://fondation-du-rein.org/le-don-dorganes/
Quel que soit l’âge du patient, la greffe de rein est considérée comme le traitement de suppléance dechoix des patients en insuffisance rénale terminale car :
En 2020, 2 595 greffes rénales ont été réalisées en France et environ 8 619 patients étaient en liste d’attente active au 1er janvier 2020 selon l’Agence de la biomédecine. Le taux de survie du greffon rénal à 10 ans tous facteurs confondus (origine du donneur, âge du donneur et du receveur, statut immunitaire du receveur, etc.) est d’environ 59,8 %, plus élevé lorsque l’organe greffé est issu d’un donneur vivant par rapport à un organe issu d’un donneur décédé.
https://www.has-sante.fr/upload/docs/evamed/CT-19602_IDEFIRIX_PIC_INS_AvisDef_CT19602.pdf
Yoo, D., Goutaudier, V., Divard, G. et al. An automated histological classification system for precision diagnostics of kidney allografts. Nat Med (2023). https://doi.org/10.1038/s41591-023-02323-6
 https://fondation-du-rein.org/le-don-dorganes/
https://fondation-du-rein.org/le-don-dorganes/Transplantation rénale
La transplantation rénale (TR) et la dialyse constituent les deux options possibles pour le traitement
de suppléance de la maladie rénale terminale (stade 5 : DFG < 15 mL/min/1,73 m2 ), maladie
gravement invalidante et potentiellement mortelle.
La transplantation rénale (TR) et la dialyse constituent les deux options possibles pour le traitement
de suppléance de la maladie rénale terminale (stade 5 : DFG < 15 mL/min/1,73 m2 ), maladie
gravement invalidante et potentiellement mortelle.
Quel que soit l’âge du patient, la greffe de rein est considérée comme le traitement de suppléance dechoix des patients en insuffisance rénale terminale car :
- le plus efficace en termes d'espérance de vie (12,4 ans contre 5,4 ans pour les patients dialysés),
- et le plus efficace en termes de qualité de vie (proche de celle de la population générale, contrairement aux patients dialysés).
En 2020, 2 595 greffes rénales ont été réalisées en France et environ 8 619 patients étaient en liste d’attente active au 1er janvier 2020 selon l’Agence de la biomédecine. Le taux de survie du greffon rénal à 10 ans tous facteurs confondus (origine du donneur, âge du donneur et du receveur, statut immunitaire du receveur, etc.) est d’environ 59,8 %, plus élevé lorsque l’organe greffé est issu d’un donneur vivant par rapport à un organe issu d’un donneur décédé.
Yoo, D., Goutaudier, V., Divard, G. et al. An automated histological classification system for precision diagnostics of kidney allografts. Nat Med (2023). https://doi.org/10.1038/s41591-023-02323-6
Un système de classification histologique automatisé pour le diagnostic de précision des allogreffes rénales
Pendant trois décennies, la classification internationale de Banff a été la référence en matière de diagnostic de rejet d'allogreffe rénale, mais ce système s'est complexifié au fil du temps avec l'intégration de données et de règles multimodales, entraînant des erreurs de classification pouvant avoir des conséquences thérapeutiques délétères pour les patients.
Classification de Banff
https://cuen.fr/cuen.mars.2021/pdf/2-RABANT-%20Banff-CUEN%20TR%202021.pdf
Pour améliorer le diagnostic, les auteurs développé un système d'aide à la décision, basé sur un algorithme couvrant toutes les règles de classification et les scénarios de diagnostic, qui attribue automatiquement des diagnostics d'allogreffe rénale.
L 'équipe a testé sa capacité à reclasser les diagnostics de rejet chez les greffés rénaux adultes et pédiatriques dans trois cohortes multicentriques internationales et deux grands essais cliniques prospectifs, incluant 4 409 biopsies de 3 054 patients (62,05 % d'hommes et 37. 95 % de femmes) suivies dans 20 centres de référence pour les greffes en Europe et en Amérique du Nord. Dans la population adulte de transplantation rénale, le système d'automatisation de Banff a reclassé 83 cas de rejet à médiation par les anticorps sur 279 (29,75 %) et 57 cas de rejet à médiation par les lymphocytes T sur 105 (54,29 %), tandis que 237 sur 3 239 (7,32 %) les biopsies diagnostiquées comme non-rejet par les pathologistes ont été reclassées comme rejet. Dans la population pédiatrique, les taux de reclassification étaient de 8 sur 26 (30,77 %) pour le rejet médié par les anticorps et de 12 sur 39 (30,77 %) pour le rejet médié par les lymphocytes T. Enfin, nous avons constaté que la reclassification des diagnostics initiaux par le Banff Automation System était associée à une meilleure stratification des risques des résultats à long terme des allogreffes.
Enregistrement ClinicalTrials.gov : NCT05306795 .
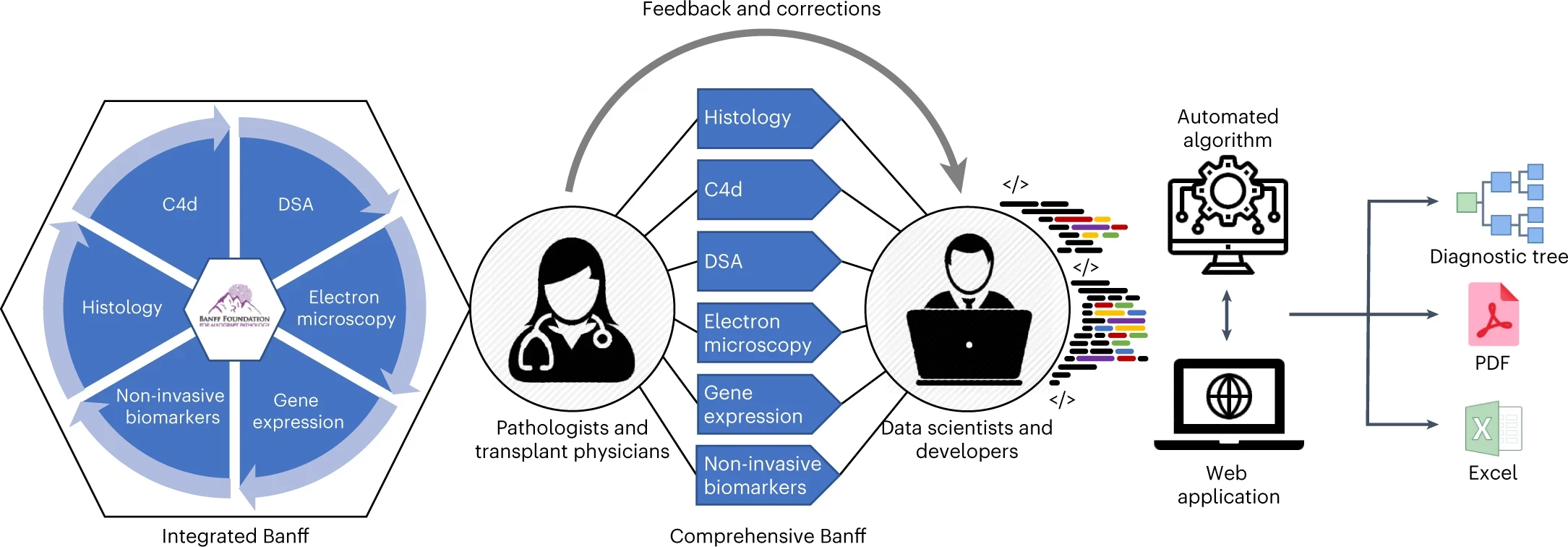 Diagramme schématique illustrant les processus de décodage, de codage et de rectification utilisés pour construire le système d'automatisation de Banff. Au cours du processus de développement, le consortium multidisciplinaire (pathologistes, médecins transplanteurs, data scientists et développeurs) a travaillé en étroite collaboration et a amélioré l'application à de nombreuses reprises. Les sorties de l'application sont un arbre de décision pour une meilleure visualisation du processus qui génère le diagnostic et des rapports automatisés au format PDF ou Excel. C4d, coloration du composant du complément C4d ; DSA, anticorps spécifique du donneur.
Diagramme schématique illustrant les processus de décodage, de codage et de rectification utilisés pour construire le système d'automatisation de Banff. Au cours du processus de développement, le consortium multidisciplinaire (pathologistes, médecins transplanteurs, data scientists et développeurs) a travaillé en étroite collaboration et a amélioré l'application à de nombreuses reprises. Les sorties de l'application sont un arbre de décision pour une meilleure visualisation du processus qui génère le diagnostic et des rapports automatisés au format PDF ou Excel. C4d, coloration du composant du complément C4d ; DSA, anticorps spécifique du donneur.
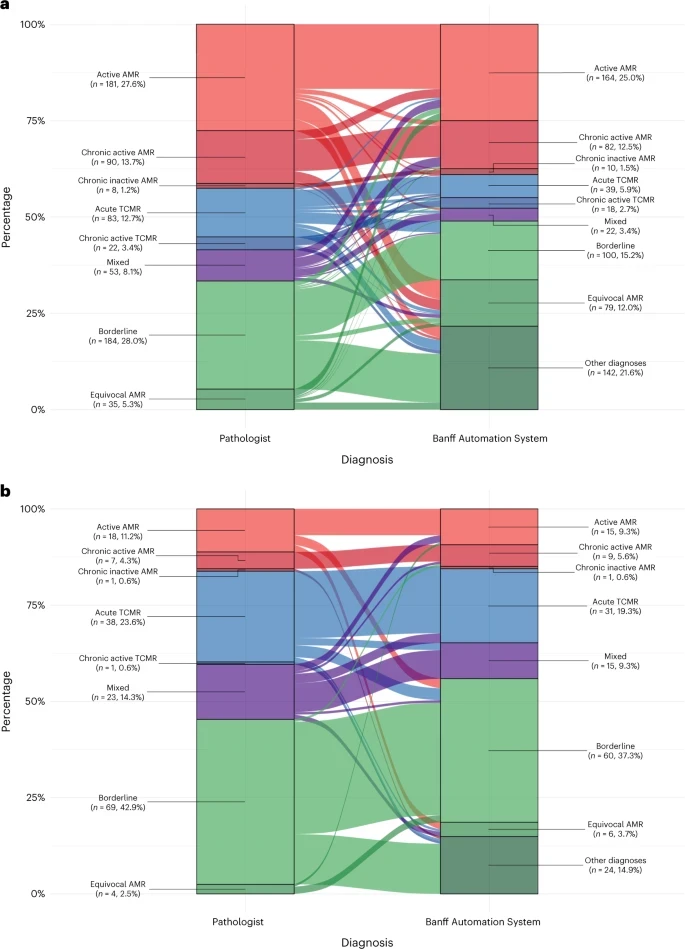
a , b , diagrammes de Sankey illustrant le flux des réévaluations des diagnostics liés au rejet par le Banff Automation System. Les proportions des diagnostics par les pathologistes et le système d'automatisation de Banff sont indiquées respectivement sur les côtés gauche et droit de chaque diagramme. Réévaluation des diagnostics de 3 895 biopsies de la cohorte Paris Transplant Group, de la cohorte University of Wisconsin-Madison, de l'étude KTD-Innov (NCT03582436) et de l'étude EU -TRAIN ( NCT03652402 ), réalisées entre janvier 2016 et mars 2021 ( une). Réévaluation des diagnostics de 514 biopsies d'une cohorte multicentrique de greffés rénaux pédiatriques (projet National Institutes of Health (NIH) 1R21DK122229-01) réalisées entre janvier 2016 et mars 2021 dans six centres nord-américains et deux centres français ( b). La catégorie « RAM équivoque » désigne les biopsies présentant des lésions évocatrices de RAM mais ne remplissant pas tous les critères de diagnostic de RAM (inflammation microvasculaire modérée (g + ptc ≥ 2 en l'absence de glomérulonéphrite récurrente ou de novo et au moins g ≥ 1 en présence de TCMR aigu, infiltrat borderline ou infection) sans DSA circulante ou substitut (complément coloration C4d ou expression de marqueurs moléculaires validés) et ATI C4d+ sans DSA circulante). La catégorie « autres diagnostics » comprend l'IFTA, l'ATI, la microangiopathie thrombotique, la toxicité CNI et les biopsies sans diagnostic spécifique. Les diagnostics de néphropathies à polyomavirus, de maladie récurrente, de glomérulonéphrite de novo, de PTLD, de pyélonéphrite et de néphrite interstitielle d'origine médicamenteuse ont été exclus car leur attribution reposait sur la saisie de l'utilisateur dans l'application.
"Le consortium a dans un premier temps conduit une revue systématique de la littérature scientifique afin de colliger l’ensemble des règles diagnostiques de la classification du rejet publiées au cours des 30 dernières années. Les médecins et les pathologistes ont ensuite travaillé avec les data scientists, développeurs et programmeurs informatiques, afin que ces derniers puissent traduire ces règles diagnostiques en un algorithme informatique couvrant l’ensemble des scénarios possibles de rejets. Ils ont ensuite créé un assistant informatique automatisé disponible en ligne et facile d’utilisation, qui interprète instantanément grâce à l’algorithme les données médicales complexes renseignées par les médecins, afin de fournir aux patients un diagnostic en appliquant scrupuleusement les règles de la classification internationale."
 Diagramme schématique illustrant les processus de décodage, de codage et de rectification utilisés pour construire le système d'automatisation de Banff. Au cours du processus de développement, le consortium multidisciplinaire (pathologistes, médecins transplanteurs, data scientists et développeurs) a travaillé en étroite collaboration et a amélioré l'application à de nombreuses reprises. Les sorties de l'application sont un arbre de décision pour une meilleure visualisation du processus qui génère le diagnostic et des rapports automatisés au format PDF ou Excel. C4d, coloration du composant du complément C4d ; DSA, anticorps spécifique du donneur.
Diagramme schématique illustrant les processus de décodage, de codage et de rectification utilisés pour construire le système d'automatisation de Banff. Au cours du processus de développement, le consortium multidisciplinaire (pathologistes, médecins transplanteurs, data scientists et développeurs) a travaillé en étroite collaboration et a amélioré l'application à de nombreuses reprises. Les sorties de l'application sont un arbre de décision pour une meilleure visualisation du processus qui génère le diagnostic et des rapports automatisés au format PDF ou Excel. C4d, coloration du composant du complément C4d ; DSA, anticorps spécifique du donneur.
a , b , diagrammes de Sankey illustrant le flux des réévaluations des diagnostics liés au rejet par le Banff Automation System. Les proportions des diagnostics par les pathologistes et le système d'automatisation de Banff sont indiquées respectivement sur les côtés gauche et droit de chaque diagramme. Réévaluation des diagnostics de 3 895 biopsies de la cohorte Paris Transplant Group, de la cohorte University of Wisconsin-Madison, de l'étude KTD-Innov (NCT03582436) et de l'étude EU -TRAIN ( NCT03652402 ), réalisées entre janvier 2016 et mars 2021 ( une). Réévaluation des diagnostics de 514 biopsies d'une cohorte multicentrique de greffés rénaux pédiatriques (projet National Institutes of Health (NIH) 1R21DK122229-01) réalisées entre janvier 2016 et mars 2021 dans six centres nord-américains et deux centres français ( b). La catégorie « RAM équivoque » désigne les biopsies présentant des lésions évocatrices de RAM mais ne remplissant pas tous les critères de diagnostic de RAM (inflammation microvasculaire modérée (g + ptc ≥ 2 en l'absence de glomérulonéphrite récurrente ou de novo et au moins g ≥ 1 en présence de TCMR aigu, infiltrat borderline ou infection) sans DSA circulante ou substitut (complément coloration C4d ou expression de marqueurs moléculaires validés) et ATI C4d+ sans DSA circulante). La catégorie « autres diagnostics » comprend l'IFTA, l'ATI, la microangiopathie thrombotique, la toxicité CNI et les biopsies sans diagnostic spécifique. Les diagnostics de néphropathies à polyomavirus, de maladie récurrente, de glomérulonéphrite de novo, de PTLD, de pyélonéphrite et de néphrite interstitielle d'origine médicamenteuse ont été exclus car leur attribution reposait sur la saisie de l'utilisateur dans l'application.
L’équipe de recherche a eu une idée originale pour résoudre ce problème.
« La médecine de précision a besoin d’outils d’aide au diagnostic qui soient fiables, robustes, précis, largement validés et démontrant un bénéfice réel et mesurable pour les patients.
Il est également capital que ces systèmes digitaux soient éthiques et bénéficient d’une transparence complète tant dans leur construction que dans l’interprétation et le rendu des résultats. Dans notre étude nous avons pu démontrer qu’un assistant informatique automatisé permettait aux médecins de poser des diagnostics plus précis », indique le Professeur Alexandre Loupy.
Il est également capital que ces systèmes digitaux soient éthiques et bénéficient d’une transparence complète tant dans leur construction que dans l’interprétation et le rendu des résultats. Dans notre étude nous avons pu démontrer qu’un assistant informatique automatisé permettait aux médecins de poser des diagnostics plus précis », indique le Professeur Alexandre Loupy.
« Notre principal défi était d’établir un consortium réunissant des experts en transplantation, néphrologie, anatomopathologie mais aussi en sciences des données, épidémiologie, biostatistiques, programmation informatique et intelligence artificielle, capables de développer ce système informatique et de recruter des patients dans le monde entier afin de tester s’il était capable de correctement diagnostiquer les rejets. Les résultats sont sans appel, puisque plus de 40 % des diagnostiques sont corrigés et requalifiés par la machine. Cet outil permettra de mieux traiter les patients et également d’améliorer les essais cliniques et le développement de traitements immunosuppresseurs"
"Il s’agit d’une avancée majeure vers une médecine de précision accompagnée par des systèmes informatiques automatisés, et de la première étude, toutes spécialités médicales confondues, à démontrer qu’un assistant informatique peut aider les médecins à poser un meilleur diagnostic".
Mode d'emploi IA en Médecine
"Il s’agit d’une avancée majeure vers une médecine de précision accompagnée par des systèmes informatiques automatisés, et de la première étude, toutes spécialités médicales confondues, à démontrer qu’un assistant informatique peut aider les médecins à poser un meilleur diagnostic".
Mode d'emploi IA en Médecine
"Le consortium a dans un premier temps conduit une revue systématique de la littérature scientifique afin de colliger l’ensemble des règles diagnostiques de la classification du rejet publiées au cours des 30 dernières années. Les médecins et les pathologistes ont ensuite travaillé avec les data scientists, développeurs et programmeurs informatiques, afin que ces derniers puissent traduire ces règles diagnostiques en un algorithme informatique couvrant l’ensemble des scénarios possibles de rejets. Ils ont ensuite créé un assistant informatique automatisé disponible en ligne et facile d’utilisation, qui interprète instantanément grâce à l’algorithme les données médicales complexes renseignées par les médecins, afin de fournir aux patients un diagnostic en appliquant scrupuleusement les règles de la classification internationale."
"Cet assistant informatique, qui permet d’améliorer la performance diagnostique des phénomènes de rejet, a été validé par toutes les sociétés internationales de transplantation, et sera donc prochainement utilisé par les équipes de transplantation du monde entier pour améliorer la prise en charge des patients.
Il permettra également de standardiser les diagnostics de rejet dans les essais cliniques de nouvelle génération, afin de faciliter le développement de nouveaux traitements immunosuppresseurs.
Il permettra également de standardiser les diagnostics de rejet dans les essais cliniques de nouvelle génération, afin de faciliter le développement de nouveaux traitements immunosuppresseurs.
La transplantation n’est pas la seule spécialité médicale à être confrontée à des données de plus en plus complexes. D’autres spécialités, telles que l’oncologie et l’immunologie, où des données variées et complexes sont de plus de plus utilisées, pourraient se tourner vers l’automatisation des classifications des maladies pour améliorer la prise en charge des patients."
https://presse.inserm.fr/un-assistant-informatique-automatise-specialise-dans-le-diagnostic-du-rejet-de-greffe/66978/#:~:text=Cet%20assistant%20informatique%2C%20qui%20permet,prise%20en%20charge%20des%20patients.
Commentaire
Voici un article très important pour les patients, les médecins et pour l'Intelligence Artificielle C'est un exemple plus que démonstratif de l'utilité de l'IA.
Ce consotium par ses travaux va donner de la vie à la vie des greffés rénaux !
Bravo au Pr Alexandre Loupy à l'origine de ce travail exceptionnel, si important pour tous les greffés rénaux.
Pr Alexandre Loupy : En 2017, il reçoit le Prix de la Société Américaine de Transplantation pour la recherche clinique. En 2018, il est lauréat du Prix de l'Académie nationale de médecine et Vanity Fair France le place dans la liste des 50 Français les plus influents du monde cette année-là. En 2020, il reçoit le Prix des Innovateurs de la Région Ile-de-France. (Wikipédia)
Un nobélisable en puissance !
Voici donc une concrétisation démontrée du rôle puissant de l'IA, ici pour les greffés rénaux.
Tout cela nous ouvre des portes dans d'autres spécialités....notamment en médecine vasculaire .....jeune spécialité qui ne pourra se passer de l'IA !
A LIRE
L’intelligence artificielle au service de la personnalisation du suivi post-transplantation
Alors que 20 % des patients perdent leur greffe au bout de 5 ans, le suivi post-transplantation constitue un vrai enjeu de santé publique.
Pour mieux comprendre et évaluer le risque individuel de rejet après une transplantation rénale pour adapter le suivi des patients, l’intelligence artificielle offre de nouveaux espoirs.
Alors que 20 % des patients perdent leur greffe au bout de 5 ans, le suivi post-transplantation constitue un vrai enjeu de santé publique.
Pour mieux comprendre et évaluer le risque individuel de rejet après une transplantation rénale pour adapter le suivi des patients, l’intelligence artificielle offre de nouveaux espoirs.
Le nombre de facteurs pouvant expliquer le rejet d’un rein greffé est trop important pour qu’un médecin puisse les analyser et en tirer des indications thérapeutiques. Les recherches en transplantation s’intéressent d’ailleurs à une ou deux variables à la fois, pas plus. Or, prises individuellement, elles ne permettent pas d’établir des corrélations fortes. En revanche, la combinaison de plusieurs facteurs donne des résultats fiables, grâce à l’utilisation de l’intelligence artificielle via des algorithmes.
Certains d’entre eux peuvent ainsi calculer les probabilités de survie d’un greffon à 3, 5, 7 et 10 ans, en indiquant un niveau de certitude de la prédiction réalisée, voire de prédire la réponse d’un patient à un traitement anti-rejet. Une vraie aide à la décision, en éclairant au mieux le choix des professionnels de santé qui peuvent ainsi savoir si un changement thérapeutique induit une réponse positive ou négative sur le long terme.
https://www.sanofi.fr/fr/nos-domaines-therapeutiques/greffedorgane
https://www.sanofi.fr/fr/nos-domaines-therapeutiques/greffedorgane
Commentaire
Voici un article très important pour les patients, les médecins et pour l'Intelligence Artificielle C'est un exemple plus que démonstratif de l'utilité de l'IA.
Ce consotium par ses travaux va donner de la vie à la vie des greffés rénaux !
Bravo au Pr Alexandre Loupy à l'origine de ce travail exceptionnel, si important pour tous les greffés rénaux.
Pr Alexandre Loupy : En 2017, il reçoit le Prix de la Société Américaine de Transplantation pour la recherche clinique. En 2018, il est lauréat du Prix de l'Académie nationale de médecine et Vanity Fair France le place dans la liste des 50 Français les plus influents du monde cette année-là. En 2020, il reçoit le Prix des Innovateurs de la Région Ile-de-France. (Wikipédia)
Un nobélisable en puissance !
Voici donc une concrétisation démontrée du rôle puissant de l'IA, ici pour les greffés rénaux.
Tout cela nous ouvre des portes dans d'autres spécialités....notamment en médecine vasculaire .....jeune spécialité qui ne pourra se passer de l'IA !
A LIRE
https://www.arcagy.org/infocancer/traitement-du-cancer/greffes/les-lois-de-la-transplantation.html/
https://www.inserm.fr/dossier/transplantation-organes-greffe/
https://www.revmed.ch/revue-medicale-suisse/2018/revue-medicale-suisse-595/retour-en-dialyse-apres-transplantation-renale-une-etude-retrospective-dans-le-canton-de-vaud
https://www.has-sante.fr/jcms/c_2576220/fr/greffe-renale-assurer-un-acces-equitable-a-la-liste-d-attente
https://www.youtube.com/watch?v=HE9zEgYYtBU&ab_channel=CampusSant%C3%A9RouenNormandie
https://www.ktdinnov.fr/blog/letat-et-les-enjeux-de-la-transplantation-renale-en-chiffres
https://www.inserm.fr/dossier/transplantation-organes-greffe/
https://www.revmed.ch/revue-medicale-suisse/2018/revue-medicale-suisse-595/retour-en-dialyse-apres-transplantation-renale-une-etude-retrospective-dans-le-canton-de-vaud
https://www.has-sante.fr/jcms/c_2576220/fr/greffe-renale-assurer-un-acces-equitable-a-la-liste-d-attente
https://www.youtube.com/watch?v=HE9zEgYYtBU&ab_channel=CampusSant%C3%A9RouenNormandie
https://www.ktdinnov.fr/blog/letat-et-les-enjeux-de-la-transplantation-renale-en-chiffres

