" Le défi majeur de l’intelligence artificielle est de parvenir à aligner les objectifs des systèmes intelligents avec les valeurs et les préférences de l’humanité, afin d’assurer leur utilité et leur sécurité à long terme. " Stuart J. Russell
" L’intelligence artificielle est l’électricité de demain : omniprésente, indispensable. Nous avons donc une lourde responsabilité : l’utiliser pour le bien de l’humanité – en créant des emplois, en faisant progresser la médecine, en révolutionnant la production industrielle, en généralisant l’accès à une éducation de qualité ou en mettant au point de petites et grandes inventions qui nous facilitent la vie au quotidien " Kaï-Fu Lee
Rinehart S, Raible SJ, Ng N, Mullen S, Huey W, Rogers C, Pursnani A. Utility of Artificial Intelligence Plaque Quantification: Results of the DECODE Study. J Soc Cardiovasc Angiogr Interv. 2024 Mar 26;3(3Part B):101296. doi: 10.1016/j.jscai.2024.101296. PMID: 39131216; PMCID: PMC11308844.
Contexte
L'analyse des plaques par intelligence artificielle (AI-QCPA, HeartFlow) fournit, à partir d'un CCTA (scanner) , des informations quantitatives sur la gravité de la plaque, y compris les volumes totaux de la plaque et du sous-type de plaque.
Nous avons cherché à évaluer l'utilité clinique de l'AI-QCPA dans la prise de décision clinique.
Méthodes
Cent cas ont été examinés par 3 cardiologues praticiens très expérimentés qui sont des lecteurs de CCTA de niveau 3 de SCCT. Les patients avaient des niveaux variables de calcium (CACS médian : 99,5) et des scores CAD-RADS. Le plan de gestion initial pour chaque cas était une décision majoritaire basée sur les données démographiques du patient, des antécédents cliniques et du rapport CCTA. L'AI-QCPA a ensuite été fourni pour chaque patient, et le plan a été reconsidéré. Le critère d'évaluation principal était le taux de reclassement (RR). Dans une analyse secondaire de 40 cas, le processus ci-dessus a été répété, mais le plan initial était basé sur l'examen des images CCTA réelles.
Résultats
Le RR après examen AI-QCPA était de 66 % (66/100) des cas (IC de 95 %, 56,72 % à 75,28 %). Le RR allait de 47 % dans les cas avec CACS 0 à 96 % dans les cas avec CACS >400, et de 40 % dans les cas CAD-RADS 1 à 94 % dans les cas CAD-RADS 4. Le RR était plus élevé dans les cas avec des sténoses coronariennes ≥50 % (89,5 %) par rapport aux cas avec des sténoses <50 % (51,6 %). Le RR était de 39 % dans les cas de LDL <70 mg/dL contre 70 % dans les LDL ≥70 mg/dL. Après examen des images de la CCTA plutôt que du rapport de la CCTA, le RR était de 50 % (IC de 95 % sur 34,51 % - 65,49 %).
Le principal effet de reclassement était d'intensifier la thérapie médicale préventive.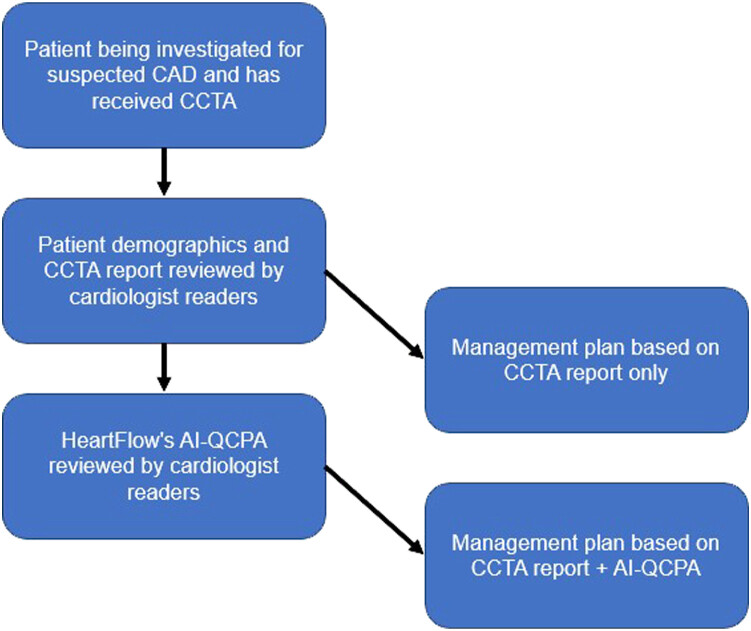
Conception de l'étude. AI-QCPA, analyse quantifiée de la plaque coronaire par intelligence artificielle ; CAD, maladie coronarienne ; CCTA, angiographie coronarienne par
tomodensitométrie.

Stadification de la prise en charge médicale .
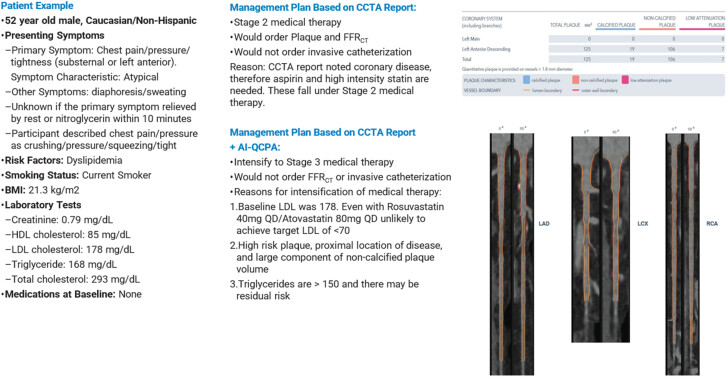
Exemple de patient. AI-QCPA, analyse quantifiée de la plaque coronaire par intelligence artificielle ; CCTA, angiographie coronarienne par tomodensitométrie.
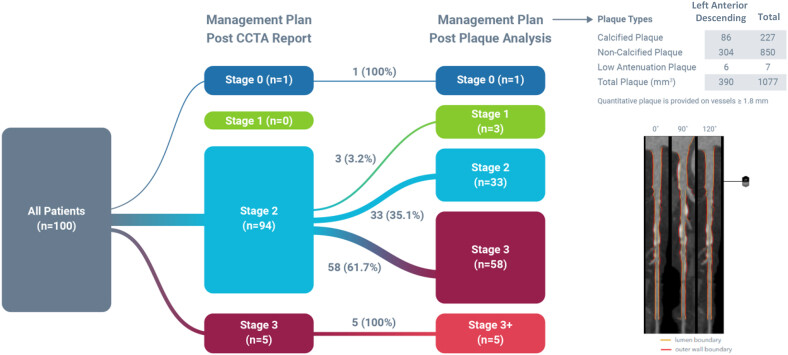
Taux de reclassification suite à une analyse quantifiée de plaque coronaire par intelligence artificielle. CCTA, angiographie coronaire par tomodensitométrie.
Conclusion
L'ajout de l'IA-QCPA à la seule CCTA entraîne un changement dans les soins cliniques chez les deux tiers des patients.
"L’étude DECODE était axée sur le changement de comportement dans la gestion clinique des prestataires et cherchait à être généralisable au-delà des cardiologues ayant suivi une formation à l’interprétation de l’ECT.
Par conséquent, pour l’analyse principale, les chercheurs ont utilisé uniquement le rapport structuré de l’ECT plutôt qu’un examen direct des images de l’ECT. Il est intéressant de noter que dans une analyse exploratoire où les chercheurs (qui étaient en fait également formés à l’interprétation de l’ECT) ont vu les images de l’ECT en même temps que le rapport structuré pour chaque patient, il n’y a eu qu’une réduction modeste du RR (de 66 % à 50 % de reclassification). Cette observation suggère que, que ce soit avec le rapport anatomique par CAD-RADS 2.0 ou l’inspection directe de l’ECT par des médecins formés, il existe une sous-estimation de la charge totale et des types de plaque. Ainsi, les informations supplémentaires sur la VTP ainsi que les images de l’ECT ont été progressivement bénéfiques dans les décisions de gestion.
Plusieurs raisons peuvent expliquer que l’intégration de l’IA-QCPA dans la prise de décision puisse conduire à des changements fréquents dans la prise en charge, notamment les efforts visant à aligner les thérapies médicales préventives sur la charge réelle de plaque.
Les paradigmes de rapport CCTA conventionnels ne permettent pas d’obtenir des informations détaillées sur le type et la quantité de plaque chez chaque patient. Bien que l’impact de ces facteurs soit bien décrit, il n’existait pas auparavant la capacité de les connaître et donc d’agir sur eux. Dans l’essai écossais de tomodensitométrie cardiaque, la charge de plaque à faible atténuation était le meilleur prédicteur d’infarctus du myocarde, indépendamment du score de risque cardiovasculaire, de la CAC ou de la gravité de la sténose : les patients présentant une charge de plaque à faible atténuation supérieure à 4 % étaient presque 5 fois plus susceptibles de subir un infarctus du myocarde ultérieur.
Dans l'étude cas-témoin des syndromes coronariens incidents identifiés par tomodensitométrie du registre Coronary CT Angiography Evaluation for Clinical Outcomes: An International Multicenter, 65 % des patients ayant développé un syndrome coronarien aigu avaient une angio-scanner coronaire de base montrant une athérosclérose coronaire non obstructive, avec un volume de plaque non calcifiée et une plaque à haut risque et nécrotique identifiant les patients à risque plus élevé. De plus, dans une analyse secondaire de la cohorte Prospective Multicenter Imaging Study for Evaluation of Chest Pain, la présence de plaque à haut risque, y compris la plaque à faible atténuation, était fortement associée à des événements cardiovasculaires ultérieurs qui persistaient après ajustement du score de risque de maladie cardiovasculaire d'athérosclérose et de la gravité de la sténose.
Récemment, des nomogrammes spécifiques à l'âge et au sexe ont été développés à partir des données de 11 808 patients adressés pour CCTA et ayant subi une AI-QCPA. Ces nomogrammes peuvent s'avérer particulièrement utiles chez les patients plus jeunes chez qui les valeurs absolues de la charge de plaque peuvent être faibles, mais peuvent refléter un percentile plus élevé pour l'âge et le sexe. Ces nomogrammes peuvent aider à identifier les patients qui sont sur une trajectoire défavorable et qui peuvent bénéficier d'une modification agressive du risque avec des thérapies médicales
Étant donné l’indication relativement récente de classe IA des lignes directrices pour la CCTA pour l’évaluation des syndromes de douleur thoracique stables et aigus, on s’attend à ce que cette modalité d’imagerie soit de plus en plus utilisée par les prestataires de soins primaires.
De la même manière que les prestataires de soins primaires ont adopté l’utilisation des scores de calcium coronaire pour évaluer le risque cardiovasculaire et guider le traitement médical, la description quantitative par IA de la charge de plaque sur la CCTA est une évaluation plus précise de la charge et de la composition de plaque que celle qui peut être vérifiée sur la base d’images, sans parler d’un rapport clinique de CCTA. Certaines études ont suggéré que certains seuils de VTP sont associés à un risque plus élevé d’événements cardiovasculaires. 13 , 14 Ces informations pourraient permettre aux prestataires d’obtenir une évaluation plus précise du risque cardiovasculaire et d’identifier des seuils plus appropriés pour les soins préventifs qui sont actuellement sous-estimés par les scores d’évaluation des risques. En outre, la quantification numérique de la charge de plaque non calcifiée et à faible atténuation pourrait être un moyen intéressant pour les prestataires et les patients d’évaluer objectivement la réponse aux interventions thérapeutiques et d’identifier potentiellement les patients présentant des facteurs de risque résiduels à un stade plus précoce de leur évolution pathologique.
Commentaire
Etude intéressante, la question : pourrions nous faire de même avec les plaques carotidiennes analysées par un écho-Doppler boosté par l'IA pour une quantification très précise des sténoses carotidiennes asymptomatiques.
Cette IA intégrerait l'anatomie de la plaque , sa vulnérabilté, le degré de sténose dont l'anatomie et l'hémodynamique et tout cela en temps réel !
Cela n'a rien à voir avec ce qui est décrit dans cet article mais c'est une porte d'entrée à l'IA et les ultrasons
Le score CAD-RADS carotides devra être impliqué
On peut rêver. Les industriels qui fabriquent les écho-Doppler n'ont pas encore pris conscience de ce que l'IA pourrait apporter aux médecins en général et vasculaires en particulier et indirectement aux patients
Cahier des charges IA/US/Carotides
- * Une sonde 3D/4D haute fréquence
* Un calculateur en temps réel : structure plaque (GSM), vulnérabilté (RADS), degré de sténose NASCET, volumétrie plaque,.......pour débuter !
A LIRE
CAROTIDE - RADS
Classification à intégrer dans l'IA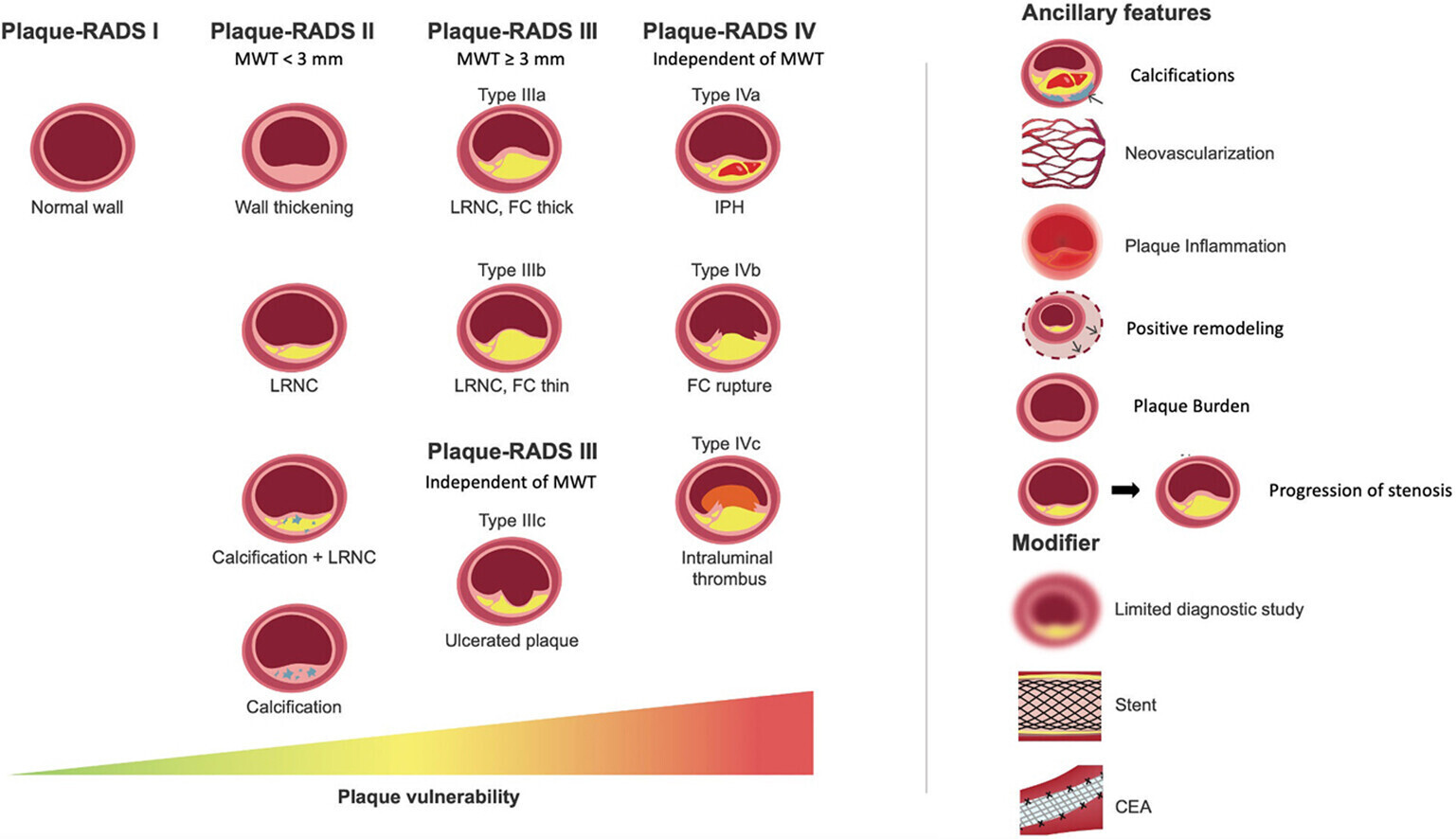
Un exemple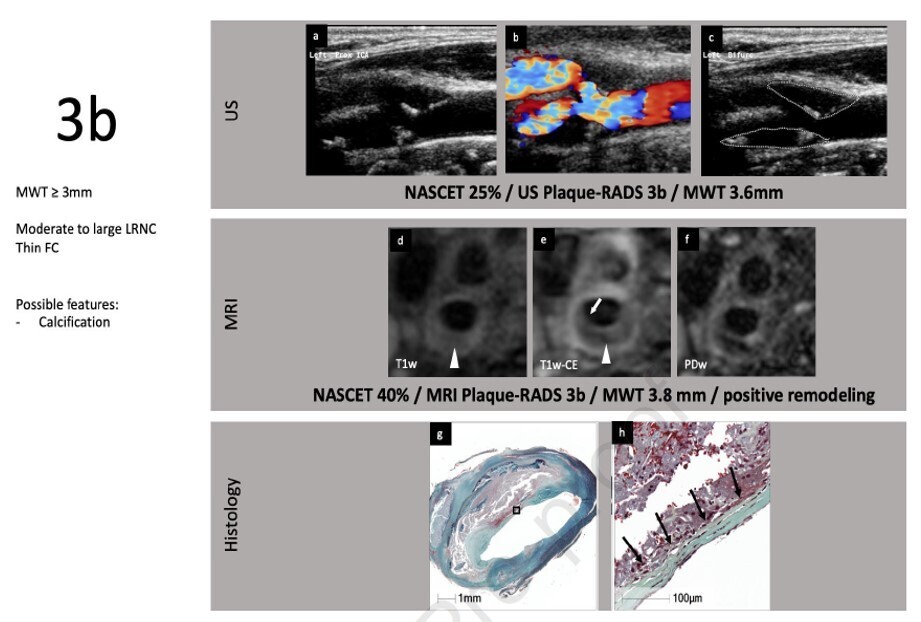
https://medvasc.info/archives-blog/carotide-rads?highlight=WyJjYXJvdGlkZSJd
Copyright : Dr Jean Pierre Laroche / 2024

