https://academic.oup.com/eurheartj/advance-article/doi/10.1093/eurheartj/ehaf054/8045293?login=false
Article libre d'accès
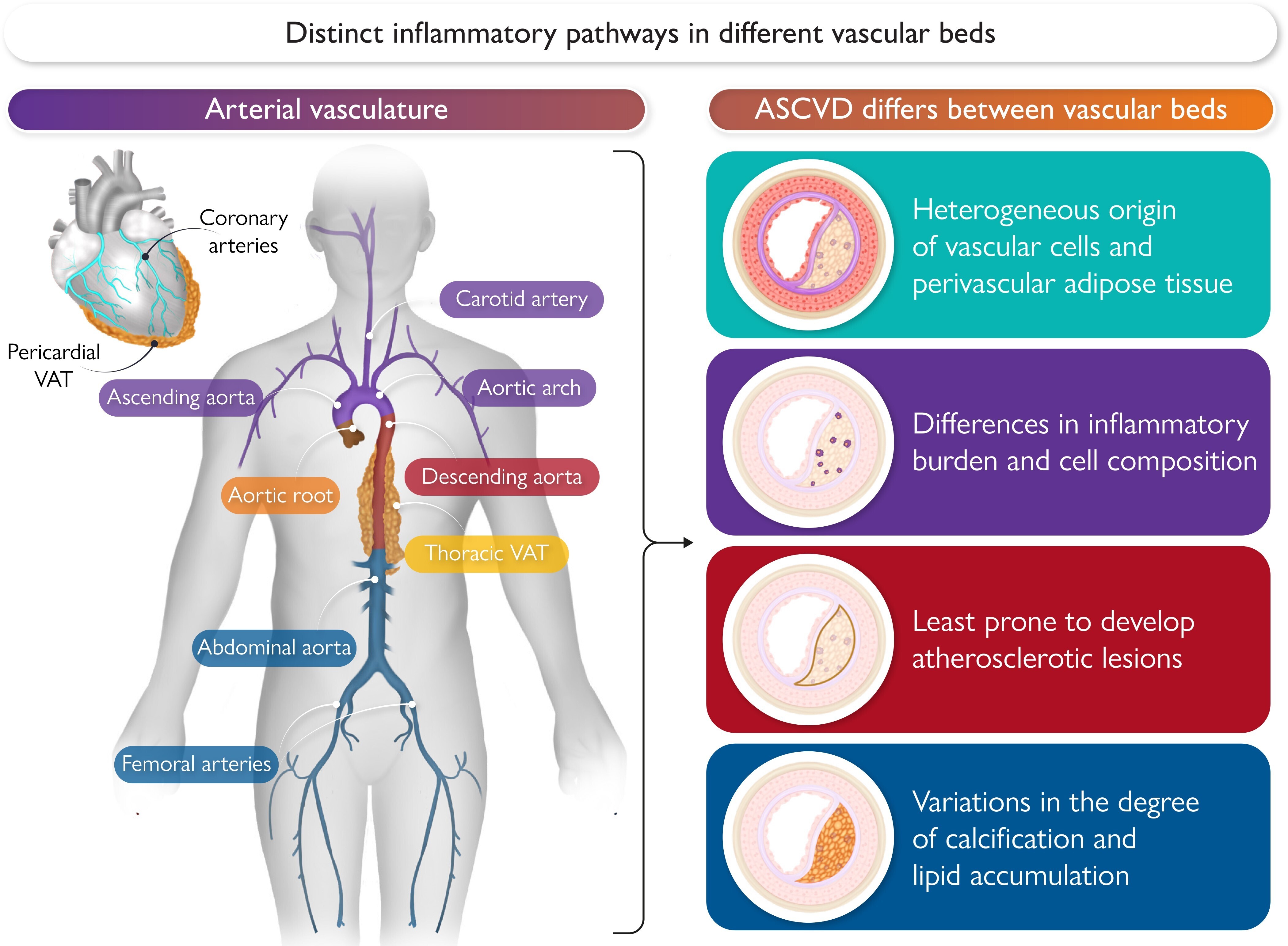
Origine embryonnaire diverse et lésions athéroscléreuses hétérogènes dans différents territoires vasculaires. VAT, tissu adipeux vasculaire.
Ensemble, elles représentent l'arbre artériel qui peut être sujet au développement d'une maladie cardiovasculaire athéroscléreuse (MCVA).
Les plaques athéroscléreuses se développent à partir d'une paroi vasculaire artérielle bien définie pour former un conglomérat de cellules stromales et immunitaires de type tumoral bénin. Ces lésions athéroscléreuses se forment dans la couche interne des grosses artères au niveau de sites de prédilection tels que les courbures et les points de ramification. Les athéromes avancés sont morphologiquement caractérisés par un noyau riche en lipides avec des cellules nécrotiques protégées par une coque fibreuse et une seule couche de cellules endothéliales (EC).
Le développement de lésions athéroscléreuses est déclenché par un certain nombre de facteurs de risque, notamment l'hypertension, le tabagisme et les troubles métaboliques qui alimentent finalement le dysfonctionnement endothélial et l'exsudation et la rétention de lipides plasmatiques dans l'espace sous-endothélial. En conséquence de l'activation endothéliale, les chimiokines guident les cellules myéloïdes, notamment les neutrophiles et les monocytes, pour infiltrer la paroi vasculaire. Ces cellules oxydent les lipoprotéines, les engloutissent et finissent par s'activer et sécrètent des cytokines pro-inflammatoires. La production de cytokines et la mort cellulaire qui s'ensuit déclenchent un cercle vicieux qui transforme les plaques en lésions hyper-enflammées complexes, qui, une fois rompues, apparaissent cliniquement comme un infarctus du myocarde ou un accident vasculaire cérébral.
Bien qu'une telle pathogénèse soit largement applicable aux différents lits vasculaires, il existe des indications de processus immunitaires et inflammatoires distincts dans les artères carotides, l'aorte, les artères coronaires et fémorales.
Ces différences dans les lésions athéroscléreuses entre les différents lits artériels sont censées être le résultat d'une interaction complexe de forces hémodynamiques, d'environnements cellulaires locaux (par exemple, différences dans l'origine des cellules musculaires lisses vasculaires [CMLV] et le phénotype ou le contenu en cellules spumeuses et le phénotype des macrophages et moléculaires, de caractéristiques structurelles des parois artérielles, de facteurs génétiques et épigénétiques et d'influences externes.
Cependant, les études comparatives concluantes évaluant en particulier les différences spécifiques aux terrtoires vasculaires sont rares à ce stade.
Cette revue résume la compréhension actuelle des différences dans la biologie des lésions athéroscléreuses selon les lits vasculaires en accordant une attention particulière à la composition des cellules lésionnelles, aux biomarqueurs inflammatoires potentiels et aux informations issues des études de séquençage de cellules uniques ( Figure 1 , Tableau 1 , Résumé graphique ). Notamment, nous n'avons pas abordé l'athérosclérose intra-stent, l'athérosclérose de transplantation, les maladies valvulaires et les anévrismes de quelque nature que ce soit dans cette revue.
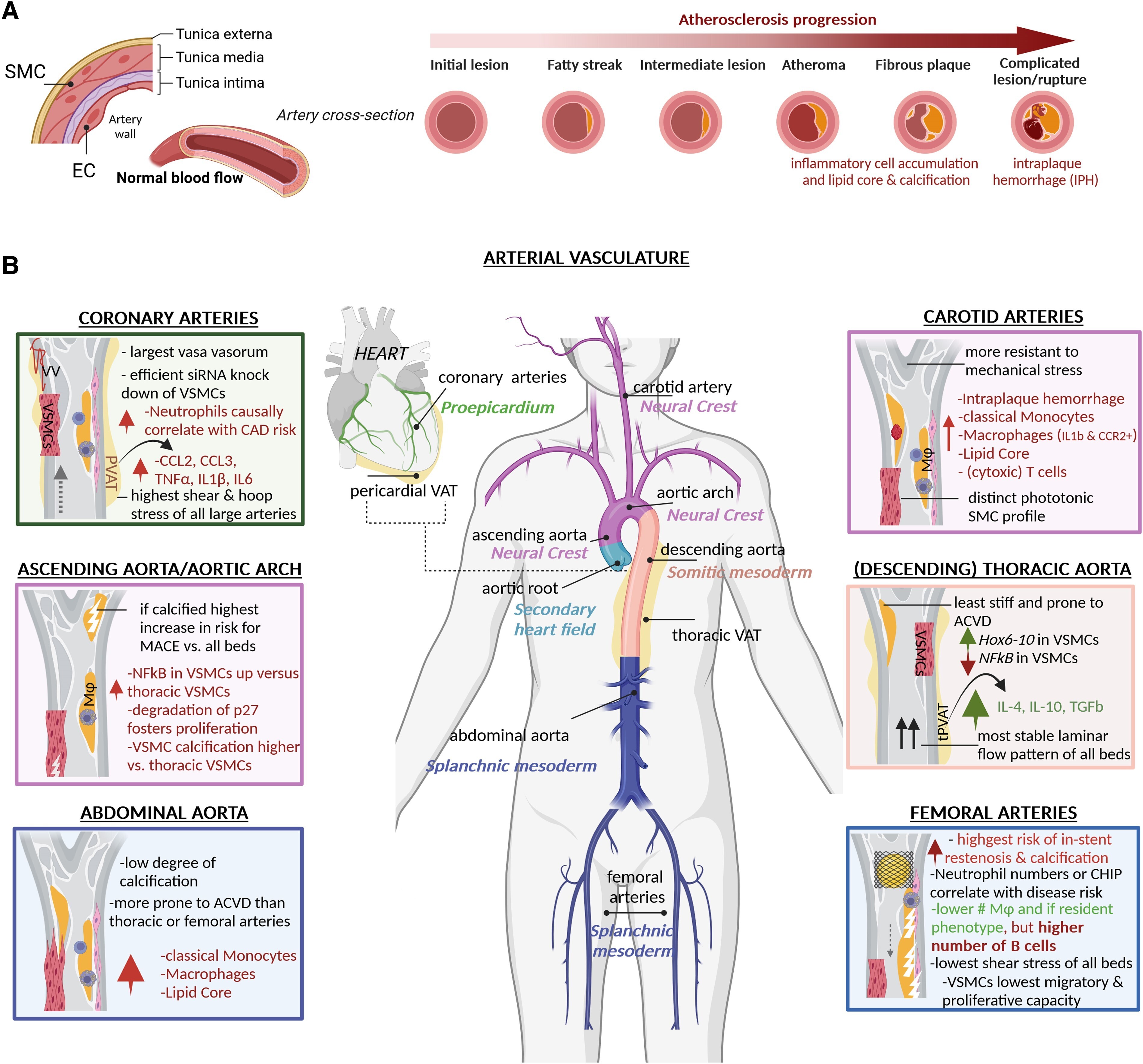
Aperçu des différences les plus importantes dans les lésions athéroscléreuses humaines dans différents lits vasculaires. ( A ) Dessin schématique d'une paroi artérielle et caractéristiques générales d'une maladie cardiovasculaire athéroscléreuse évolutive dans des coupes transversales d'un vaisseau artériel. ( B ) Un être humain avec un arbre artériel et un cœur. Les artères individuelles sont nommées en noir tandis que l'origine embryonnaire des cellules musculaires lisses vasculaires est ajoutée en couleur en dessous et correspond à la couleur de la section artérielle respective de l'arbre. Les cases à gauche et à droite résument les caractéristiques individuelles des lésions de chaque lit et sont encadrées dans la couleur de l'origine des cellules musculaires lisses vasculaires. De plus, les tissus adipeux vasculaires thoraciques et péricardiques sont indiqués. ASCVD, maladie cardiovasculaire athéroscléreuse ; CAD, maladie coronarienne ; EC, cellule endothéliale ; IL, interleukine ; MACE, événements cardiovasculaires indésirables majeurs ; NF-κB facteur nucléaire-κB ; siRNA, petit ARN interférent, SMC, cellule musculaire lisse ; TNF, facteur de nécrose tumorale ; tPVAT, tissu adipeux vasculaire périaortique thoracique ; VAT, tissu adipeux vasculaire ; VSMC, cellule musculaire lisse vasculaire ; Mϕ, macrophage. La figure a été réalisée avec Biorender.com
Bien que ces études confirment les différences de composition cellulaire et de transcriptomes unicellulaires dans les plaques athéroscléreuses à différents endroits de l'arbre artériel, des analyses unicellulaires supplémentaires approfondies comparant les données unicellulaires des plaques à différents endroits artériels sont nécessaires pour comprendre pleinement les différents mécanismes qui déterminent la pathogénèse divergente à différents endroits de l'arbre artériel. L'application de la transcriptomique spatiale, comme celle qui a été réalisée dans les plaques d'endartériectomie carotidienne par Sun et al. , s'avérera inestimable à cette fin, car cette technique permet une analyse unicellulaire de zones précises de plaques athéroscléreuses obtenues de différents côtés de l'arbre artériel par autopsie ou chirurgie à partir d'une seule section de tissu.
Perspectives et conclusion
Les connaissances actuelles sur les mécanismes de l’ASCVD spécifiques au lit vasculaire sont limitées, principalement en raison d’un manque d’études de cohorte standardisées à grande échelle.
Les principaux défis comprennent l’hétérogénéité des patients, la traduction limitée des modèles animaux, les exigences d’imagerie variées, la focalisation du financement sur les types d’ASCVD les plus courants et les obstacles logistiques et éthiques à la collaboration et à l’intégration des données.
Surmonter ces défis pourrait fournir des informations précieuses pour des traitements personnalisés.
Outre ces raisons plus structurelles, on ne sait pas non plus pourquoi certains patients présentent une maladie coronarienne monovasculaire, tandis que d’autres présentent une maladie multivasculaire, avec une distribution et une gravité de la charge de plaque variées.
Des résultats similaires ont été décrits dans la circulation carotidienne, la majorité des patients présentant une maladie unilatérale contre une minorité présentant une maladie bilatérale.
Selon l’origine embryonnaire et d’autres aspects de la variation locale, on pourrait s’attendre à ce qu’au moins pour le même type d’artère, la susceptibilité soit comparable. Actuellement, on ne sait pas pourquoi ce n’est pas le cas.
À l’heure actuelle, des études transcriptomiques unicellulaires et spatiales bien conçues sont très prometteuses pour éclaircir les détails mécanistiques sous-jacents à l’énorme hétérogénéité du développement et de la progression des lésions selon leterritoire.
De plus, il est tentant de spéculer que des analyses omiques approfondies de l’aorte thoracique pourraient introduire des cibles qui, lorsqu’elles sont activées de manière appropriée, pourraient générer un phénotype résistant à l’athérosclérose.
De plus, et ce n’est pas couvert dans cette revue en raison d’un manque de données originales, de telles analyses devraient également aborder les effets spécifiques au sexe qui introduisent un autre niveau de complexité dans l’ASCVD dans différents territoires vasculaires.
Article passionnant qui interpelle.
Beaucoup de questions , peu de réponses surtout térapeutiques
A l'heure actuelle la prise en charge des atteintes vasculaires est univoque : corrections des FDRC, antiagrégant et statine, voire colchicine, alors que les mécanismes des atteintes dans les territoires vasculaires sont très différents.
Le "coeur" de ces lésions reste caché : anatomie, hémodynamique, génétique, épigénétique, exposome, endothélium, génomique , embryologie.....sont à l'origine de différents mécanismes , qui devraient nécessiter des traitements différents,...en théorie !
La PREVENTION CV PRIMAIRE ne devrait-elle pas débuter par cette nouvelle perception des lésions vasculaires?
"Cette revue de la littérature scientifique explore comment différentes voies inflammatoires contribuent à l'athérosclérose dans divers lits vasculaires, tels que les artères carotides, coronaires et fémorales. Elle met en lumière les disparités dans la composition des lésions athérosclérotiques, les profils cellulaires immunitaires et les mécanismes sous-jacents entre ces régions. L'article examine également le rôle de facteurs hémodynamiques, des phénotypes endothéliaux et de l'origine embryonnaire des cellules musculaires lisses dans ces différences. Enfin, il discute du potentiel des biomarqueurs et des études de séquençage unicellulaire pour améliorer la compréhension et le traitement de l'athérosclérose spécifique aux sites vasculaires."
By GEMINI IA
L'athérosclérose, une maladie caractérisée par l'accumulation de plaques dans les artères, présente des caractéristiques distinctes selon les territoires vasculaires affectés. Cette variabilité est due à une combinaison de facteurs complexes, notamment :
1. Différences hémodynamiques :
- Flux sanguin : Les artères sont soumises à des forces de cisaillement variables, liées au flux sanguin. Les zones de turbulence, souvent situées aux bifurcations artérielles, favorisent l'accumulation de lipides et l'inflammation.
- Pression artérielle : Les variations de pression artérielle, notamment l'hypertension, exercent un stress mécanique sur la paroi artérielle, induisant des lésions et une réponse inflammatoire.
2. Facteurs de risque locaux :
- Exposition aux facteurs de risque : Les cellules endothéliales, qui tapissent la paroi artérielle, peuvent être exposées à des concentrations variables de facteurs de risque tels que le cholestérol LDL oxydé, le tabac ou le glucose, selon le territoire vasculaire.
- Microenvironnement vasculaire : La composition du microenvironnement vasculaire, notamment la présence de cellules inflammatoires et de facteurs de croissance, peut varier selon les territoires, influençant la progression de l'athérosclérose.
3. Réponse inflammatoire spécifique :
- Hétérogénéité des cellules immunitaires : Les populations de cellules immunitaires présentes dans la paroi artérielle peuvent différer selon les territoires, entraînant des réponses inflammatoires variables.
- Expression de molécules d'adhésion : L'expression de molécules d'adhésion, qui régulent le recrutement des cellules inflammatoires, peut varier selon les territoires, modulant l'intensité de la réponse inflammatoire.
4. Génétique et épigénétique :
- Prédisposition génétique : Des variations génétiques peuvent influencer la susceptibilité à l'athérosclérose dans différents territoires vasculaires.
- Modifications épigénétiques : Les modifications épigénétiques, qui régulent l'expression des gènes, peuvent être influencées par des facteurs environnementaux et contribuer à la variabilité de l'athérosclérose.
En résumé :
La diversité des voies inflammatoires qui façonnent l'athérosclérose dans différents territoires vasculaires résulte d'une interaction complexe entre des facteurs hémodynamiques, des facteurs de risque locaux, une réponse inflammatoire spécifique et des facteurs génétiques et épigénétiques. Comprendre ces mécanismes est crucial pour développer des stratégies de prévention et de traitement personnalisées de l'athérosclérose.
Copyright : De Jean Pierre Laroche / 2025

