Swan D, Turner R, Franchini M, Mannucci PM, Thachil J. Air pollution and venous thromboembolism: current knowledge and future perspectives.
Pollution atmosphérique et thromboembolie veineuse : connaissances actuelles et perspectives d'avenir
Lancet Haematol. 2024 Dec 6:S2352-3026(24)00291-6. doi: 10.1016/S2352-3026(24)00291-6. Epub ahead of print. PMID: 39653046.ABSTRACT
La pollution de l’air, composée d’un mélange variable de particules gazeuses et solides, représente un problème de santé mondial grave et non résolu. L’étude Global Burden of Disease a révélé que 12 % de tous les décès survenus en 2019 étaient liés à la pollution de l’air ambiant, les particules étant souvent considérées comme la principale cause de préjudice.
En 2024, plus de 90 % de la population mondiale est exposée à des quantités excessives de particules, selon les directives de l’OMS sur les niveaux d’exposition maximum. De nombreuses preuves étayent l’existence d’un lien entre la pollution de l’air et les maladies cardiovasculaires, environ la moitié des décès liés à la pollution ambiante étant considérés comme secondaires à des causes cardiovasculaires.
Une éventuelle association entre les particules et la thromboembolie veineuse est moins claire, mais au cours de la dernière décennie, plusieurs études ont enrichi la littérature disponible.
Dans cette revue, nous examinons les preuves épidémiologiques actuelles reliant la pollution de l’air au développement d’événements thrombotiques veineux.
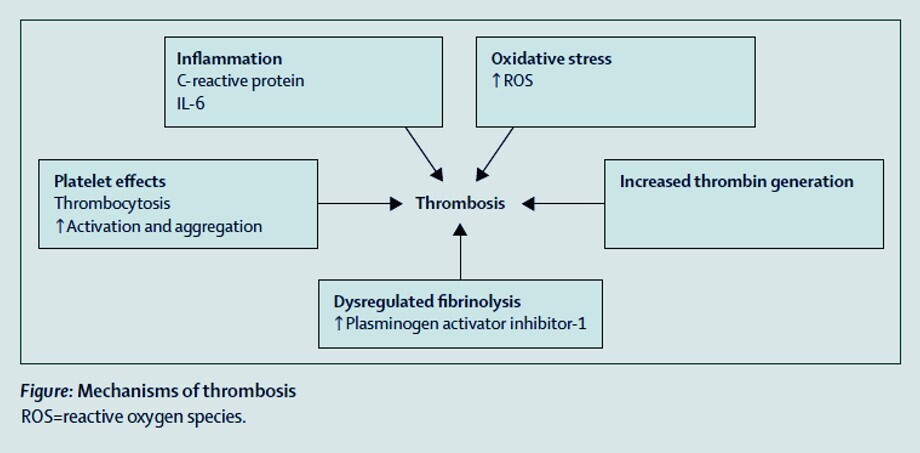
Nous étudions les mécanismes favorisant un phénotype thrombo-inflammatoire chez ces individus, notamment le dysfonctionnement plaquettaire, la fibrinolyse dysrégulée et la production accrue de thrombine.
Compte tenu de l'importance de la pollution atmosphérique pour la santé mondiale, nous discutons également des stratégies possibles nécessaires pour atténuer l'impact de la pollution atmosphérique sur la santé humaine dans le monde entier.
Introduction
La composition de la pollution atmosphérique variera donc en fonction de plusieurs facteurs, notamment l’emplacement, le degré d’urbanisation, le statut de développement économique et l’heure de la journée.
Plus récemment, l’étude GBD de 2021 a déterminé que 8 % du total des années de vie mondiales ajustées en fonction de l’incapacité cette année-là étaient attribuables à la pollution atmosphérique par les particules (PM).
Exposition de la population mondiale aux particules2·5 a atteint un sommet en 2011 (38,9 μg/m3), avec une réduction en 2019 (34,7 μg/m3), ce qui s’explique principalement par la baisse des concentrations en Chine et en Inde, et le ralentissement de la croissance de l’exposition en Asie du Sud, au Moyen-Orient et en Afrique.
Cependant, ces concentrations sont bien supérieures aux niveaux d’exposition maximaux recommandés par l’OMS (5 μg/m3), l’Agence américaine de protection de l’environnement (9 μg/m3) et les normes de qualité de l’air de l’Union européenne (25 μg/m3En fait, plus de 90 % de la population mondiale vit dans des zones qui ne répondent pas aux critères de l’OMS, ce qui représente environ 7 milliards de personnes.9
En 2010, l’American Heart Association a publié une déclaration scientifique décrivant les mécanismes sous-jacents les plus probables.
En 2021, l’American Heart Association, la Fédération mondiale du cœur, l’American College of Cardiology et la Société européenne de cardiologie ont publié une déclaration appelant à une augmentation de la recherche et de l’éducation dans ce domaine de besoin mondial.9 Ces revues et les déclarations connexes ont porté en particulier sur les maladies cardiovasculaires athérothrombotiques, tandis que les événements thrombotiques veineux ont été moins fréquemment abordés.
En 2016, Franchini et ses collègues a réalisé la première revue systématique des études sur la thromboembolie veineuse, suggérant une association entre la pollution de l’air et la thromboembolie veineuse, mais leurs conclusions ont été entravées par l’hétérogénéité de l’étude. Cependant, des études publiées au cours des 8 dernières années ont ajouté de nouvelles connaissances importantes à ce domaine.
Dans cette revue, nous examinons les preuves actuellement disponibles, y compris les publications antérieures et postérieures à l’article fondateur de Franchini et de ses collègues. Nous nous sommes concentrés principalement sur la gestion de projet2·5 et PM10, car la plupart des preuves se rapportent à ces composantes de la pollution ambiante. Cependant, nous abordons également d’autres facteurs tels que l’impact des oxydes d’azote (NONX) et l’ozone, entre autres
Pollution de l’air et thromboembolie veineuse
Mécanismes
Modifications du système hémostatique
Changements inflammatoires
Stress oxydatif
Limites de l’étude
Perspectives
Responsabilités des cliniciens et des professionnels de santé
Éducation et conseil aux patients concernant les risques liés à la pollution atmosphérique
Discussion sur les effets de la pollution de l'air ambiant sur la santé
- Expliquer le lien entre la pollution atmosphérique et divers problèmes de santé
- Informer sur les impacts à court et long terme de l'exposition à la pollution de l'air
- Moyens de transport : privilégier les modes de déplacement moins polluants
- Exposition aux routes à forte circulation : limiter le temps passé près des axes routiers très fréquentés
- Utilisation de sources domestiques de pollution et alternatives : sensibiliser aux polluants intérieurs et promouvoir de bonnes pratiques d'aération
- Évitement de l'exposition aux feux ouverts et au tabagisme passif
Considération de l'utilisation de masques FFP2 ou N95
- Recommander leur usage pour les patients dans les zones urbaines polluées lors des pics de mauvaise qualité de l'air
Plaidoyer
Adhésion à des groupes de défense- Exemples : Réseau de pratiques vertes (Royaume-Uni), Médecins pour l'environnement (Australie), Médecins pour des soins de santé plus écologiques (Europe), Soins de santé sans danger (Mondial)
- Participer aux débats sur la qualité de l'air et les politiques de santé environnementale
- Promouvoir des mesures visant à réduire la pollution atmosphérique à long terme
Recherche et financement
Initiatives de recherche- Étude de l'impact de la réduction de l'exposition
- Identification des groupes à risque
- Local et international
- Subventions des assurances
Réduction des niveaux de pollution atmosphérique
- Utilisation de sources d'énergie renouvelables
- Amélioration des réseaux de transport public
- Végétalisation urbaine
- Méthodes agricoles propres et améliorées, avec accent sur l'utilisation de produits locaux
Réduction de l'exposition à la pollution atmosphérique
- Systèmes de filtration et de ventilation de l'air
- Choix individuels en matière de transport
- Arrêt du tabagisme
- Utilisation de masques FFP2 ou N95
Conclusions
Une explication possible de ces données contradictoires, par opposition à l’association claire avec l’athérothrombose, pourrait être que la thromboembolie veineuse est moins fréquente ..............................

Commentaire
La MTEV est-elle liée "en partie" à la pollution ?
Rien de très solide à ce jour à la différence du risque cardio vasculaire.
Existe- t'il une interaction avec l'athérothrombose pour laquelle la pollution est en cause ? Indirectement si on considère que l'athérothrombose est un possible FDRCV induit par la pollution, un effet cascade pourait impacter la MTEV.
Un nouvel article publié ,le 12/12/2024 apporte enfin des réponses
Pamela L Lutsey, Jeffrey R Misialek, Michael T Young, Jesse David Berman, Claire Leiser, Zachary C Pope, Mary Cushman, Aaron R. Folsom, Joel D Kaufman; Air pollution is associated with increased risk of venous thromboembolism: the Multi-Ethnic Study of Atherosclerosis. Blood 2024; blood.2024026399. doi:https://doi.org/10.1182/blood.2024026399
Article libre d'accès
Points clés
-
L’exposition à la pollution de l’air est courante et peut augmenter le risque de développer des caillots sanguins.
-
Une exposition prolongée à la pollution atmosphérique (c.-à-d. PM2,5, NOxNO2) était associée à un risque plus élevé de développer une thromboembolie veineuse.

L'exposition à la pollution atmosphérique peut induire des effets procoagulants et l'exposition chronique peut être liée à un risque accru de thromboembolie veineuse (TEV). Nous avons testé l'hypothèse selon laquelle la pollution atmosphérique est associée à un risque accru de TEV dans l'étude prospective multiethnique sur l'athérosclérose (MESA), qui dispose de mesures bien caractérisées de la pollution atmosphérique et d'informations sur les facteurs de confusion potentiels. Nous avons inclus 6 651 participants recrutés en 2000-2002 (tranche d'âge de référence : 45-84 ans ; 53 % de femmes). La pollution atmosphérique a été évaluée à l'aide d'un modèle spatio-temporel validé qui intègre une surveillance spécifique à la cohorte. Quatre indices de pollution atmosphérique mis à jour tous les quinze jours pendant le suivi ont été moyennés pour estimer l'exposition chronique au niveau des participants : particules fines ≤ 2,5 micromètres de diamètre aérodynamique (PM2,5), oxydes d'azote (NOx), dioxyde d'azote (NO2) et ozone (O3). Français La moyenne ± ET de PM2,5 était de 13,5 ± 3,0 µg/m3, NO2 de 17,9 ± 8,2 ppb, NOx de 36,1 ± 19,6 ppb et O3 de 22,2 ± 3,7 ppb. Les incidents de TEV ont été identifiés à l'aide des codes de sortie d'hospitalisation jusqu'en 2018. Au total, 248 événements de TEV se sont produits sur une période de suivi médiane de 16,7 ans. Après ajustement pour les données démographiques de base, les comportements de santé et l'indice de masse corporelle, le rapport de risque (IC à 95 %) pour les incidents de TEV associés à une concentration de PM2,5 supérieure de 3,6 µg/m3 était de 1,39 (1,04-1,86) ; pour une concentration de NO2 supérieure de 13,3 ppb était de 2,74 (1,57-4,77) ; et pour une concentration de NOx supérieure de 30 ppb était de 2,21 (1,42-3,44). L'O3 n'était pas lié. Dans cette cohorte prospective communautaire avec estimation individuelle de l'exposition chronique à la pollution atmosphérique, des concentrations ambiantes moyennes plus élevées de PM2,5, NO2 et NOX étaient associées à un risque plus élevé de développer une thrombose veineuse. Ces résultats s'ajoutent aux preuves accumulées des effets néfastes sur la santé attribués à l'exposition à la pollution atmosphérique.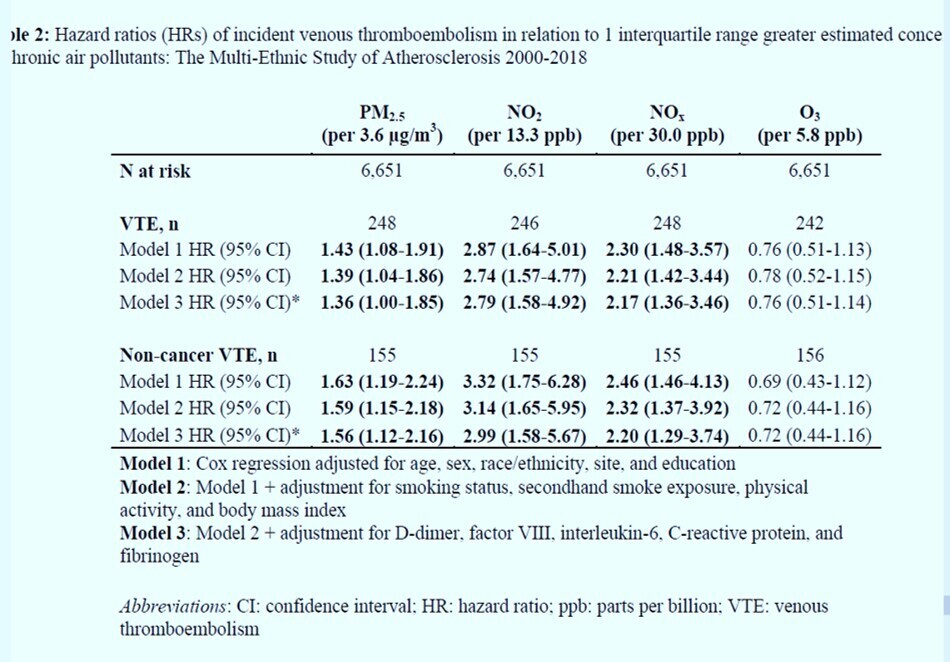
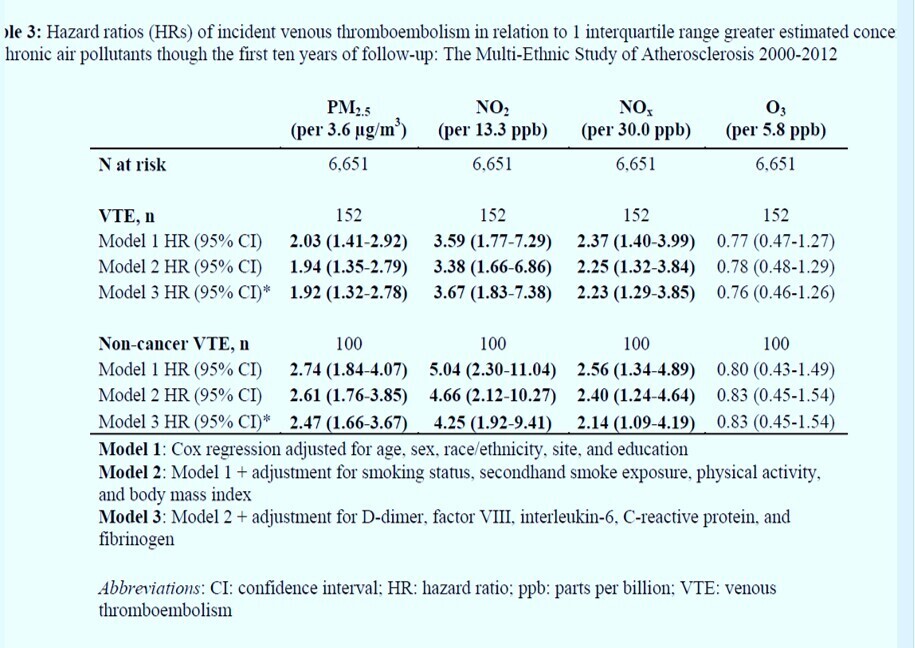
Dans cette étude, une exposition plus importante aux PM2.5 au cours de la décennie précédant l'événement TEV (modélisée comme une moyenne mobile) était associée à un risque accru de TEV [HR : 1,17 (IC 95% : 1,01-1,37) par intervalle interquartile de 1,2 μg/m3 d'exposition]. L'ampleur de ce résultat est comparable à celui de l'étude actuelle lorsqu'une échelle similaire est considérée [HR de 1,10 (1,01-1,19) pour une augmentation de 1 μg/m3].La cohorte MDC n'a pas observé d'association significative entre d'autres polluants (PM10, NOx, carbone noir) et l'incidence de TEV. De même, il n'y avait pas d'association avec les PM2.5 lorsqu'elles étaient modélisées comme une exposition moyenne au cours de l'année précédente
Une analyse de la cohorte coréenne National Health Insurance Service-National Health Screening (NHIS-HEALS) a rapporté un risque accru de TEV associé aux PM10 [HR : 1,06 (IC 95% : 1,05-1,07) par 1 μg/m3], au SO2 [HR : 1,12 (IC 95% : 1,08-1,16) par 1 ppb], et à l'O3 [HR : 1,04 (IC 95% : 1,03-1,05) par 1 ppb]. Dans l'étude MESA, des associations défavorables ont été identifiées entre le NO2 et les NOX et l'incidence de TEV, mais pas avec l'O3.
Cette étude est l'une des rares à évaluer l'exposition chronique à la pollution atmosphérique et la TEV aux États-Unis, un pays présentant d'importantes inégalités raciales et géographiques en matière d'exposition à la pollution atmosphérique
Une analyse menée dans le nord-est des États-Unis a révélé que l'exposition estimée aux PM2.5 au sein d'un code postal (moyenne mobile annuelle) était associée à un taux plus élevé d'admissions hospitalières pour TEV dans la même région.
Bien que cette étude ait porté sur un grand nombre d'événements TEV, contrairement à MESA AIR, elle disposait d'une évaluation moins complète de la pollution atmosphérique individuelle, manquait d'informations sur les facteurs de confusion ou de médiation potentiels, et n'était pas une cohorte fermée. Une autre étude de cohorte prospective basée aux États-Unis a évalué l'exposition à la pollution atmosphérique en fonction de la proximité des routes, ne trouvant aucune association avec l'incidence de TEV, mais manquait de puissance statistique pour détecter des associations de taille raisonnable." Traduction by PERPLEXITY
Qu'il faille controler la pollution pour mieux prtotéger la santé, une évidence . Mais il reste très difficile de faire la relation directe avec les affections chroniques.
Cependant on doit prendre conscience de cet impact et donc réduire le plus possible nos conduites "polluantes" .
Affaire à suivre.....................
Copyright : Dr Jean Pierre Laroche /2024

