"En culture tous les progrès pour le pays sont des bienfaits." Proverbe Catalan
" Apprendre à douter, c'est apprendre à penser. " Octavio Paz
Javier Trujillo-Santos, Cihan Ay, Behnood Bikdeli, David Jiménez, Aurora Villalobos, Luciano López-Jiménez, Montserrat Pérez-Pinar, Javier Pagán-Escribano, Maurizio Ciammaichella, Manuel Monreal, Variation in Venous Thromboembolism Outcomes Based on Primary Cancer Site: A RIETE Registry Analysis, Variation des résultats de la thromboembolie veineuse en fonction du site du cancer primaire : analyse du registre RIETE
JACC: Advances, Volume 4, Issue 9, 2025, 102101, ISSN 2772-963X,
https://doi.org/10.1016/j.jacadv.2025.102101.
https://www.sciencedirect.com/science/article/pii/S2772963X25005265
Contexte
Objectifs
Méthodes
Résultats
Le risque thrombotique le plus élevé a été observé dans les cancers du poumon (aHR : 4,03 ; IC à 95 % : 3,38-4,81) et du pancréas (aHR : 3,85 ; IC à 95 % : 3,04-4,88), suivis des cancers gastro-intestinaux (aHR : 1,95 ; IC à 95 % : 1,53-2,48) et du sein (aHR : 1,63 ; IC à 95 % : 1,27-2,09).
Le risque de saignement majeur était le plus élevé dans les cancers gastro-intestinaux (aHR : 1,66 ; IC à 95 % : 1,37-2,00), génito-urinaires (aHR : 1,66 ; IC à 95 % : 1,38-2,00) et du pancréas (aHR : 1,43 ; IC à 95 % : 1,05-1,95). Les résultats étaient cohérents dans la cohorte appariée par propension.
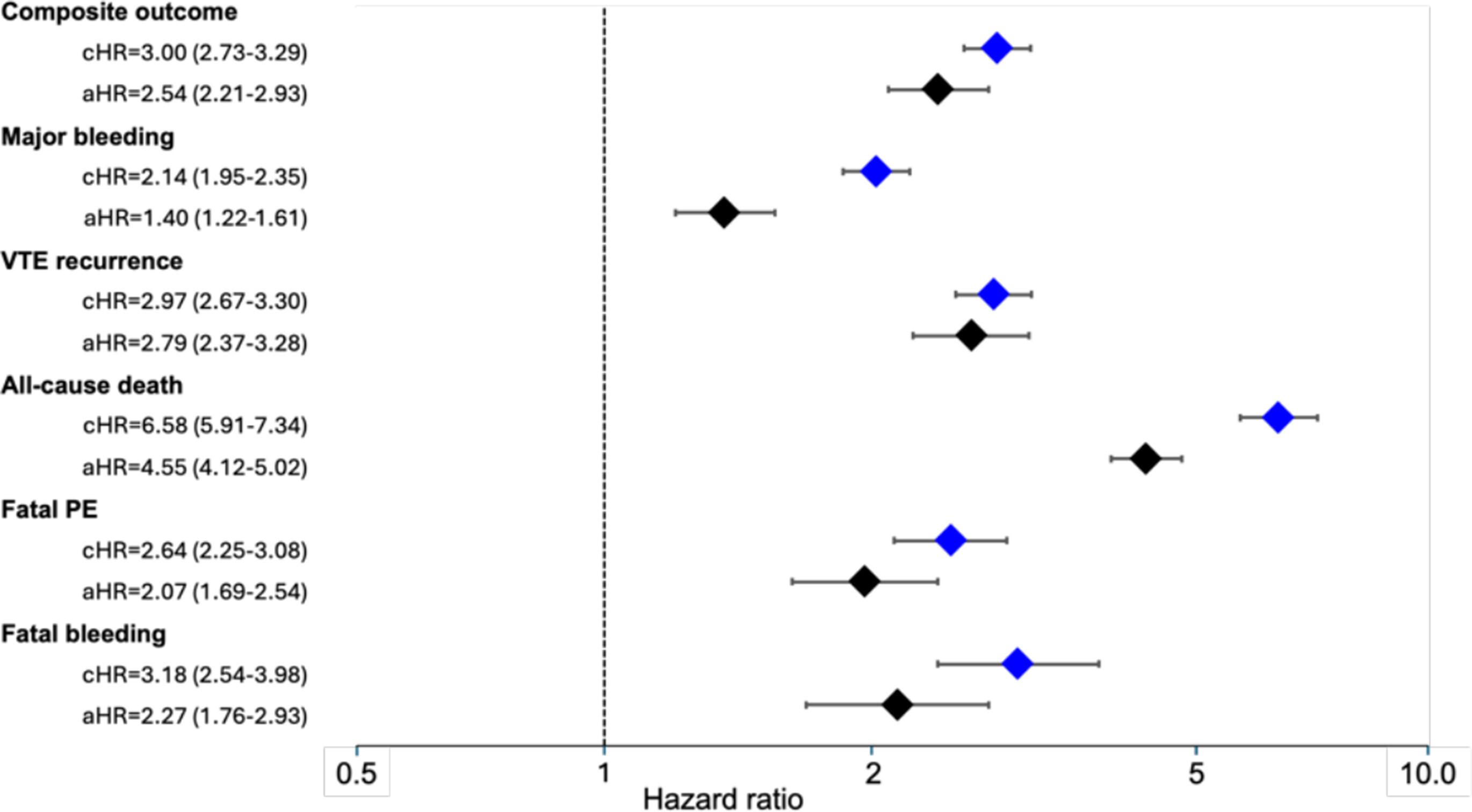
Risques ajustés pour les résultats de la thromboembolie veineuse selon le statut du cancer
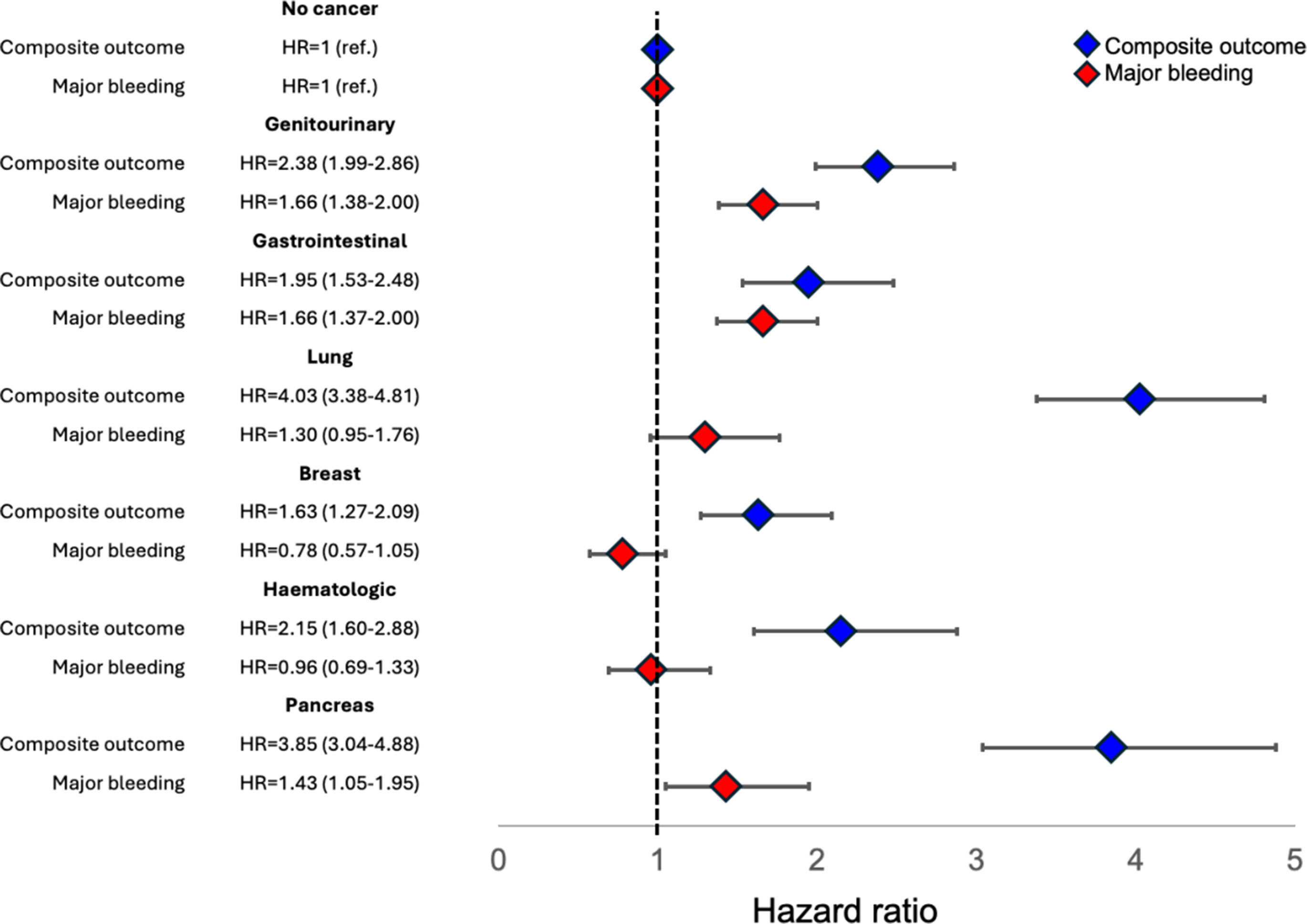
Thromboembolie veineuse et risque de saignement chez les patients atteints de cancer
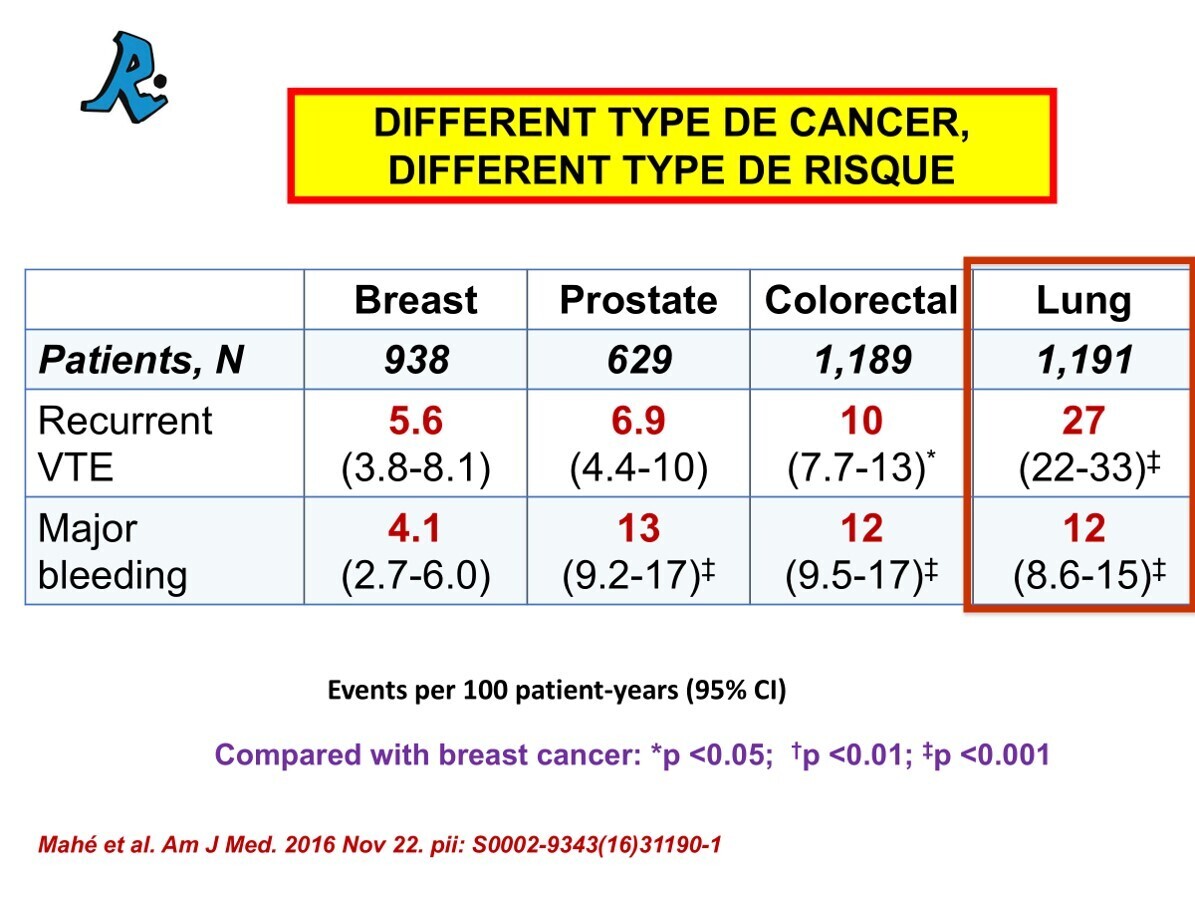
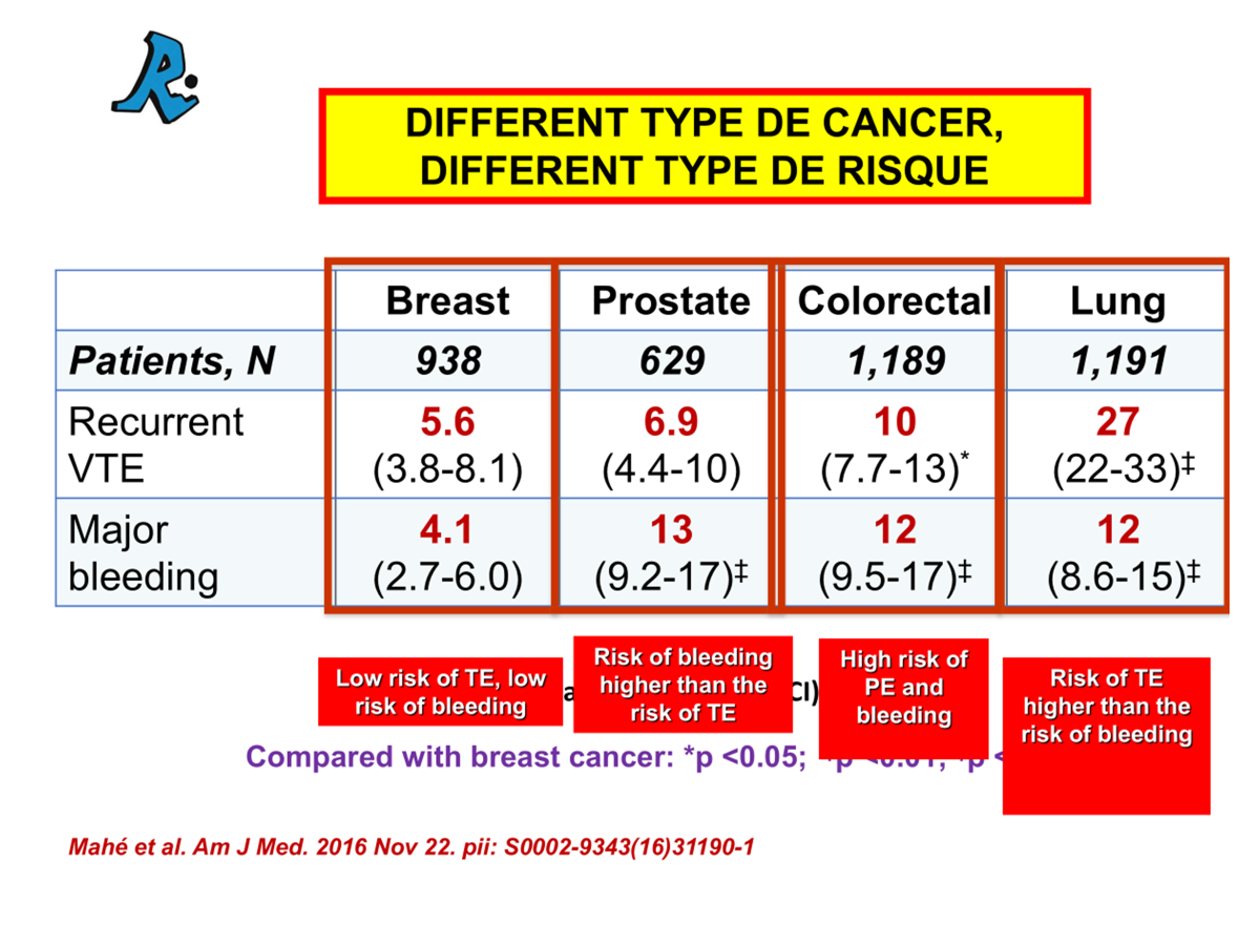
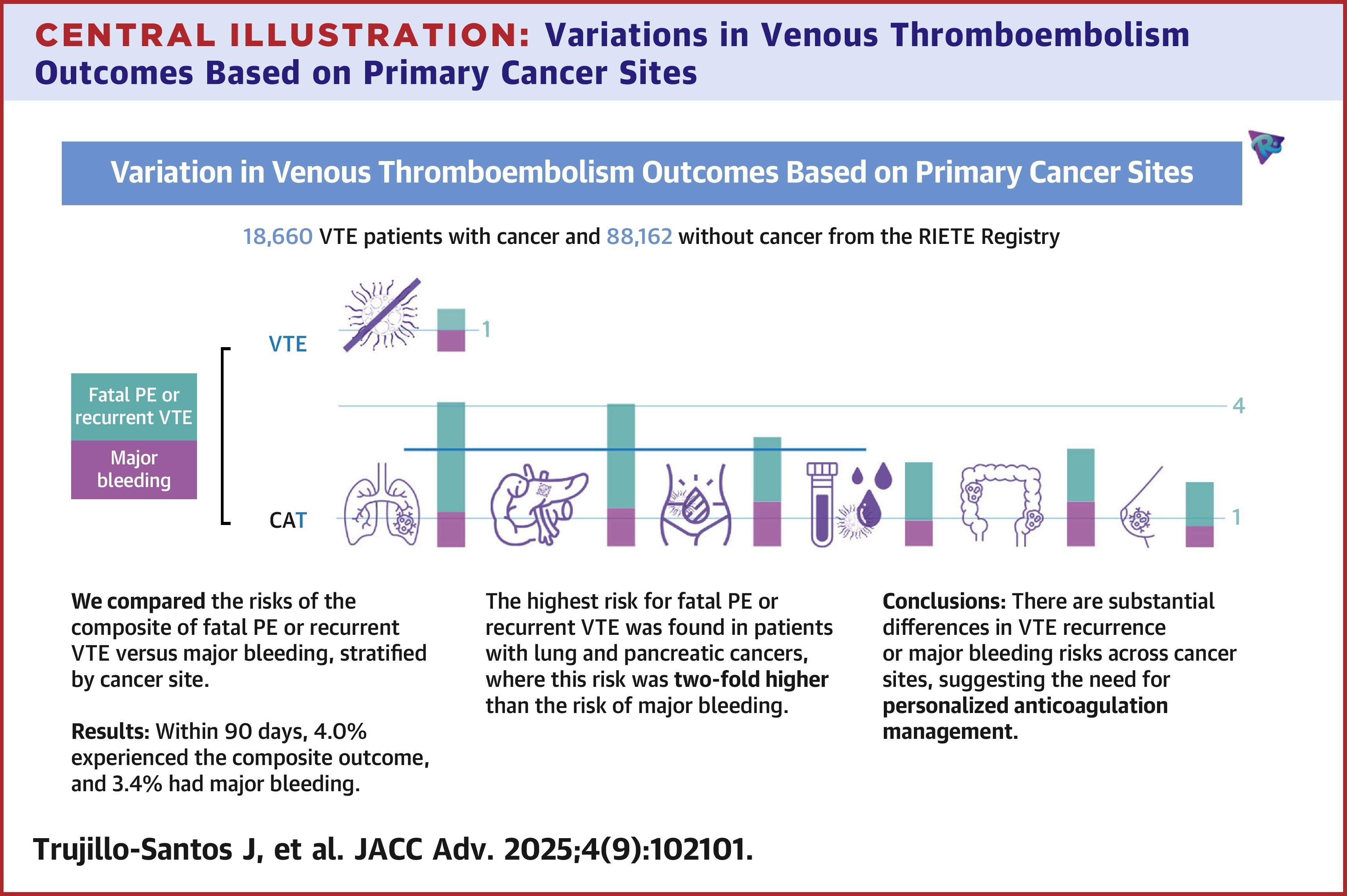
Conclusions
SYNTHESE
Cette étude de recherche explore comment les résultats des thromboembolies veineuses (TEV) varient selon le type de cancer primaire. En analysant les données de plus de 18 000 patients atteints de cancer et de TEV, ainsi que de plus de 88 000 patients sans cancer issus du registre RIETE, les chercheurs ont comparé les risques de TEV récurrente, de décès lié à la TEV et d'hémorragie majeure sur 90 jours. Les résultats révèlent des différences significatives entre les sites de cancer, soulignant par exemple que les cancers du poumon et du pancréas présentent les risques thrombotiques les plus élevés, tandis que les cancers gastro-intestinaux et génito-urinaires sont associés aux risques hémorragiques les plus importants. Ces constatations plaident en faveur d'une approche individualisée de l'anticoagulation pour les patients atteints de cancer, s'éloignant des traitements uniformes.
Commentaire
Les rasultats de cette étude amplifie et consolide les résultats de 2016 d'Isabelle Mahé
J'avais réalisé un entretien avec avec le Pr Manuel Monreal Bosch, en 2021
"Quelle est votre conception sur la durée de l'anticoagulation ?
Nous devons mieux identifier les patients à risque accru de récidive de MTEV (en particulier les récidives d'EP) après l'arrêt de l'anticoagulation. Nous devons également mieux identifier quels patients atteints de MTEV présentent un risque accru d'hémorragie majeure au-delà des 3 premiers mois de traitement. Ce n'est qu'alors que nous serons en mesure de fournir quelques recommandations (peut-être seulement suggestions) sur la durée optimale du traitement anticoagulant pour chaque patient. Mais la quantité de variables qui peuvent influencer chacun de ces résultats est importante. Mon sentiment est que nous avons actuellement des recommandations trop simples (3 mois de thérapeutique si facteurs de risque transitoires, indéterminée si cancer ou événement secondaire), et que nous avons besoin de scores pronostiques plus précis (et sophistiqués), accessibles via internet, pour ajuster la durée du traitement anticoagulant aux nombreuses variables : âge, poids corporel, fonction rénale, traitements concomitants, troubles sous-jacents, MTEV initiale , mode de présentation de la MTEV qui peuvent influencer les résultats."
Le cancer associé à la MTEV est un sujet très important et nos connaissances ont évolué mois après mois.Pour vous,quels sont les développements les plus importants pour le les patients?
Dans une étude portant sur 10 962 patients atteints d'un cancer actif et d'une MTEV, 2,2 % sont décédés d'EP et 1,6 % sont morts d'hémorragie au cours des 12 premiers mois. Fait intéressant les patients présentant initialement une EP mortelle, l’EP était 3 fois plus fréquente que l'hémorragie mortelle.
A contrario chez ceux qui ne présentaient qu'une TVP, l'EP fatale était 3 fois moins fréquente qu’une hémorragie. Il y a donc des raisons de croire que les patients cancéreux atteints de TVP bénéficient probablement d'un traitement différent de celui des patients cancéreux atteints d'EP. Des doses plus faibles, des anticoagulants plus sûrs, des durées de traitement plus courtes ? Seuls des essais randomisés pourraient apporter une réponse à ces questions.
Dans une autre étude, le taux de récidives de MTEV pendant l'anticoagulation était similaire au taux d'hémorragie majeure chez les patientes atteintes d'un cancer du sein ou colorectal. Cependant, chez les patients atteints d'un cancer de la prostate, le taux de récidive était la moitié du taux d’hémorragie, alors que chez les patients atteints de cancer du poumon, le taux de récidive était supérieur à 2 fois plus élevé que le taux de saignement majeur. Encore une fois, il y a des raisons de suggérer que les patients cancéreux atteints de MTEV pourraient probablement bénéficier de thérapies adaptées en fonction du siège du cancer. Les oncologues ont appris il y a plus de 20 ans que l'adaptation du traitement oncologique selon un certain nombre de variables chez leurs patients atteints de cancer a été associée à de meilleurs résultats. En attendant, nous continuons à traiter nos patients avec cancer et MTEV avec les mêmes médicaments, mêmes doses et mêmes durées."
On retrouvait déjà l'essence même de l'article cité : le "formatage anticoagulant" des patients avec MTEV et cancer devra s'arrêter répidement. Chaque cancer a une histoire de MTEV différente : risque de récidive, risque hémorragique.
L'IA devrait une fois pour toute régler ce probléme et RIETE devra le faire compte tenu des données "faramineuses" en matière de MTEV. Les antiXI(a) devrient apporter un début de réponse ou pas ...
Cpoyright : Dr Jean Pierre Laroche / 2025


