Anti XI : du nouveau !
“Journalisme. La névrose du scoop.”Pierre Assouline et Philippe Dampenon
RAPPELS
L’étude sur la fibrillation auriculaire avec l’abélacimab a été interrompue prématurément par le comité de surveillance des données en raison d’une réduction écrasante des saignements par rapport à un AOD (anticoagulant oral direct)
L’abénacimab, un inhibiteur du facteur XI / XIa à double action, a démontré une réduction sans précédent des saignements dans la plus grande et la plus longue étude en tête-à-tête comparant un inhibiteur du facteur XI à un AOD
L'abélacimab est le premier et le seul inhibiteur du facteur XI à démontrer une réduction des saignements majeurs par rapport à un AOD
La dose d’abélacimab de 150 mg assure une inhibition quasi complète du facteur XI, récapitulant le profil hémorragique bénin des patients déficients en facteur XI génétique
Les patients du bras rivaroxaban peuvent passer à l’abénacimab dans le cadre d’une étude de prolongation
CAMBRIDGE, Massachusetts--(BUSINESS WIRE)--Anthos Therapeutics, Inc.,
une société au stade clinique développant des thérapies innovantes pour les maladies cardiovasculaires, fondée par Blackstone Life Sciences, a annoncé aujourd’hui que l’étude de phase 71 AZALEA-TIMI 2 menée auprès de 1 287 patients atteints de fibrillation auriculaire présentant un risque modéré à élevé d’AVC avait atteint son critère d’évaluation principal.
L’étude a été arrêtée prématurément par le comité de surveillance des données en raison d’une réduction écrasante de la combinaison de saignements majeurs et cliniquement pertinents non majeurs chez les patients prenant de l’abénacime par rapport aux patients prenant du rivaroxaban, un AOD standard de premier plan.
De plus, l’abélacimab est le premier et le seul inhibiteur du facteur XI à démontrer une réduction sans précédent des saignements majeurs par rapport à une AOD, qui est le type de saignement le plus grave. Les résultats complets d’AZALEA-TIMI 71 seront présentés lors d’un prochain congrès scientifique
« Compte tenu de la réduction importante eds saignements d’AZALEA-TIMI 71, ainsi que d’une réduction de 80 % de la thrombose démontrée dans notre étude antérieure sur la TEV,1 l ’abélacimab incarne sa promesse en tant qu’anticoagulant épargnant l’hémostase et représente un changement de paradigme dans la prévention des accidents vasculaires cérébraux et d’autres affections thrombotiques.
« L’étude AZALEA-TIMI 71 est la plus grande et la plus longue étude directe sur un inhibiteur du facteur XI à fournir des preuves définitives d’une réduction très significative des saignements par rapport à l’anticoagulant standard. Avec une médiane de suivi de 21 mois, couvrant plus de 2 000 années-patients, AZALEA-TIMI 71 représente une étude historique confirmant la promesse de l’inhibition du facteur XI comme causant beaucoup moins de saignements qu’une norme de soins actuelle
L’abélacimab est un nouvel anticorps monoclonal hautement sélectif entièrement humain ayant une double activité inhibitrice contre le facteur XI et sa forme active, le facteur XIa.
L’abélacimab 150 mg maintient une inhibition de ~98 % sur l’intervalle posologique, récapitulant le profil hémorragique bénin des patients présentant un déficit génétique en facteur XI. Avant AZALEA-TIMI 71, l’abélacimab a permis de réduire de ~80 % la thromboembolie veineuse (MTEV) par rapport à un comparateur standard dans une étude de preuve de concept de référence publiée dans le New England Journal of Medicine.1
« Compte tenu de la réduction majeure des saignements d’AZALEA-TIMI 71, ainsi que d’une réduction de 80 % de la thrombose démontrée dans notre étude antérieure sur la TEV,1 l’abélacimab incarne sa promesse en tant qu’anticoagulant épargnant l’hémostase et représente un changement de paradigme dans la prévention des accidents vasculaires cérébraux et d’autres affections thrombotiques », a déclaré Dan Bloomfield, MD, médecin en chef d’Anthos Therapeutics. « S’il est approuvé, davantage de patients atteints de fibrillation auriculaire pourraient être traités efficacement et en toute sécurité, avec un risque beaucoup plus faible de saignement avec l’abélacimab par rapport à un AOD. »
Le Center for Disease Control and Prevention (CDC) estime que 12,1 millions de personnes aux États-Unis souffriront de fibrillation auriculaire d’ici 2030.2 Malheureusement, 40% à 60% des patients atteints de fibrillation auriculaire ne se voient pas prescrire d’anticoagulants aujourd’hui. Cette sous-utilisation d’anticoagulants pour la prévention des accidents vasculaires cérébraux a été citée comme l’un des plus grands problèmes de santé publique auxquels sont confrontés les patients cardiovasculaires.3 Dans une enquête auprès des médecins, le principal obstacle à la prise d’anticoagulants oraux par les patients était lié aux saignements.4
« L’abélacimab a le potentiel de fournir une option thérapeutique révolutionnaire pour tous les patients qui vivent avec la peur quotidienne de saigner tout en prenant les anticoagulants actuels. Nous pouvons maintenant imaginer un avenir où ces patients pourront reprendre et profiter d’activités qu’ils sont actuellement forcés d’abandonner en raison de préoccupations associées aux saignements », a déclaré Leslie Lake, président de la National Blood Clot Alliance. « Nous sommes ravis qu’AZALEA-TIMI 71 ait démontré un résultat aussi positif et enthousiasmés par les promesses qu’il offre aux patients. »
Anthos Therapeutics a lancé une étude d’extension pour permettre aux patients de passer du rivaroxaban à l’abélacimab afin de bénéficier de l’amélioration du profil hémorragique. De plus, une désignation accélérée pour l’abélacimab a déjà été accordée par la Food and Drug Administration des États-Unis pour la prévention des accidents vasculaires cérébraux et de l’embolie systémique chez les patients atteints de fibrillation auriculaire.
À propos de l’abélacimab
L’abélacimab est un nouvel anticorps monoclonal hautement sélectif entièrement humain qui verrouille le facteur XI à l’état inactif, entraînant une double activité inhibitrice contre le facteur XI et sa forme activée, le facteur XIa. En dissociant la thrombose de l’hémostase, un inhibiteur du facteur XI à double activité peut fournir une voie à suivre pour les patients qui bénéficieraient de la protection que les anticoagulants peuvent fournir.
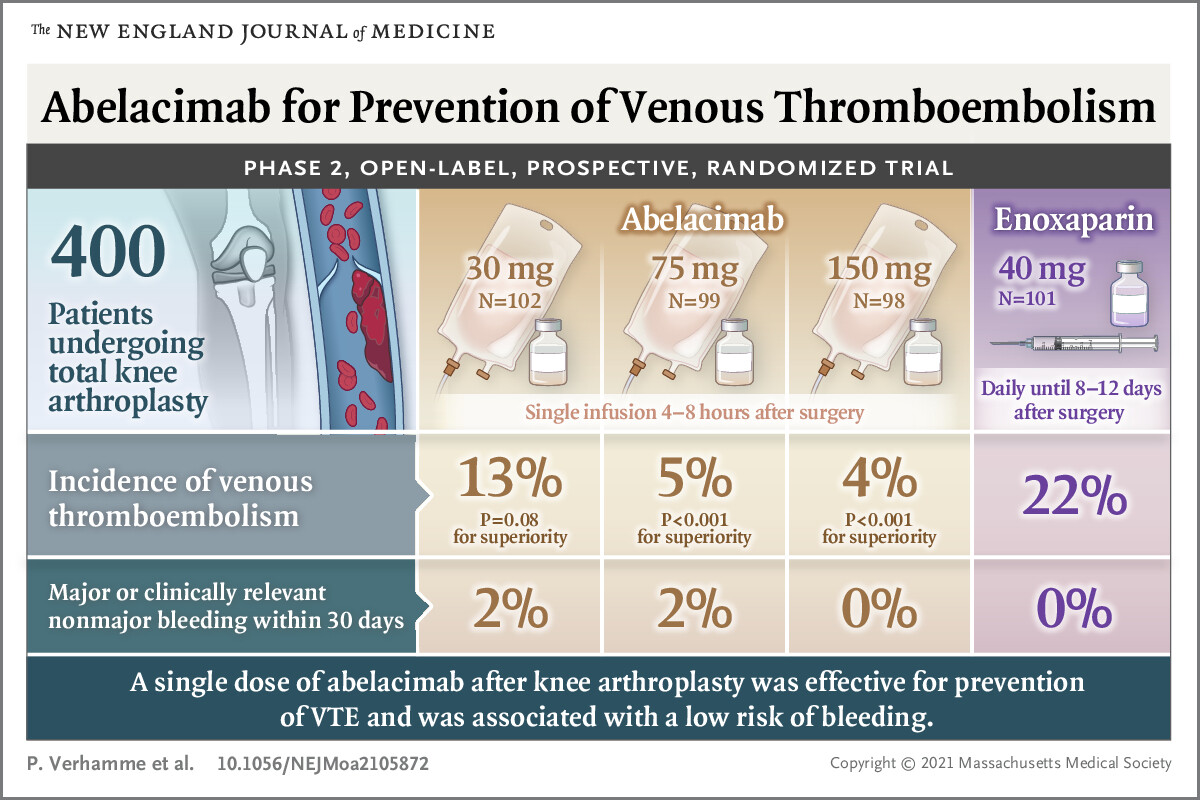
Dans une étude PK /, l’abénacime administré par voie IV a entraîné une suppression profonde du facteur XI dans l’heure suivant le début du traitement et a maintenu une inhibition presque maximale jusqu’à 30 jours.5 Dans une étude de phase 2 publiée dans le New England Journal of Medicine en 2021, une dose intraveineuse unique d’abélacimab après une chirurgie du genou a réduit le taux de thromboembolie veineuse de 80%, mesurée 10 jours après la chirurgie, par rapport à l’énoxaparine.1 L’inhibition du facteur XI offre la promesse d’une anticoagulation épargnant l’hémostase pour la prévention et le traitement des événements thromboemboliques artériels et veineux.6
L’abénacime est un agent expérimental et n’est approuvé pour aucune indication dans aucun pays.
À propos de l’étude de phase 71 AZALEA-TIMI 2
L’étude AZALEA-TIMI 71 est une étude en groupes parallèles, randomisée, contrôlée activement, à insu et axée sur les événements, dont le critère d’évaluation principal évalue l’effet de deux doses en aveugle d’abénacime par rapport au rivaroxaban ouvert chez des patients atteints de fibrillation auriculaire (FA) présentant un risque modéré à élevé d’AVC. Le critère d’évaluation principal de l’étude AZALEA-TIMI 71 est le taux composite d’événements hémorragiques majeurs ou cliniquement significatifs non majeurs. Un critère d’évaluation secondaire est une hémorragie majeure en soi. Les patients ont été randomisés 1:1:1 et ont reçu 150 mg d’abélacimab par voie sous-cutanée (SC) une fois par mois, 90 mg d’abélacimab une fois par mois ou 20 mg de rivaroxaban par jour. Le recrutement de cette étude événementielle s’est achevé en décembre 2021, avec 1 287 patients répartis dans 95 sites d’étude mondiaux, notamment aux États-Unis et au Canada, en Europe et en Asie.
À propos de l’étude de phase 76 LILAC-TIMI 3
L’étude LILAC-TIMI 76 est une étude événementielle, randomisée, contrôlée par placebo, en double aveugle, en groupes parallèles visant à évaluer l’efficacité et l’innocuité de l’abélacimab par rapport au placebo sur le taux d’AVC ischémique ou d’embolie systémique chez les patients atteints de fibrillation auriculaire (FA) qui ont été jugés inappropriés pour le traitement anticoagulant actuellement disponible. Les patients de l’étude seront randomisés pour recevoir de l’abélacimab 150 mg SC ou un placebo correspondant une fois par mois. L’étude vise à recruter environ 1 900 patients de plus de 400 sites en Amérique du Nord, en Europe, en Amérique latine, au Moyen-Orient et en Asie.
À propos d’Anthos Therapeutics
Anthos Therapeutics a été lancé par Blackstone Life Sciences en 2019 et a obtenu de Novartis Pharma les droits mondiaux exclusifs de développement, de fabrication et de commercialisation de l’abélacimab. Anthos Therapeutics est une société biopharmaceutique au stade clinique axée sur le développement et la commercialisation de thérapies innovantes génétiquement et pharmacologiquement validées pour faire progresser les soins aux patients cardiovasculaires à haut risque. Pour plus d’informations, visitez le site Web de l’entreprise et suivez-nous sur Twitter et LinkedIn.
Déclarations prospectives
Ce communiqué de presse contient des « déclarations prospectives » au sens de la loi Private Securities Litigation Reform Act de 1995 qui impliquent des risques et des incertitudes substantiels, y compris des déclarations concernant le lancement et le calendrier des futurs essais cliniques et de leurs activités de recherche et développement. Tous les énoncés, autres que les énoncés de faits historiques, contenus dans le présent communiqué de presse, y compris les énoncés concernant la stratégie de la société, ses activités futures, sa situation financière future, ses perspectives, ses plans et ses objectifs de direction, sont des énoncés prospectifs. Les mots « anticiper », « devenir », « croire », « continuer », « pourrait », « estimer », « s’attendre à », « avoir l’intention de », « pouvoir », « planifier », « potentiel », « prédire », « projeter », « devrait », « cibler », « sera », « serait » et d’autres expressions similaires sont destinés à identifier les énoncés prospectifs, bien que tous les énoncés prospectifs ne contiennent pas ces mots d’identification. Tous les énoncés prospectifs sont fondés sur les attentes actuelles de la direction à l’égard d’événements futurs et sont assujettis à un certain nombre de risques et d’incertitudes qui pourraient faire en sorte que les résultats réels diffèrent sensiblement et défavorablement de ceux énoncés ou sous-entendus dans ces énoncés prospectifs. De plus, les énoncés prospectifs inclus dans le présent communiqué de presse représentent les opinions de la société à la date des présentes et ne doivent pas être considérés comme représentant les opinions de la société à toute date postérieure à la date des présentes. La société prévoit que les événements et développements ultérieurs entraîneront un changement de point de vue de l’entreprise. Cependant, bien que la société puisse choisir de mettre à jour ces énoncés prospectifs à un moment donné dans le futur, la société décline spécifiquement toute obligation de le faire.
Références
1 Verhamme P et al. New Engl J Med Juillet 2021 (https://www.nejm.org/doi/full/10.1056/NEJMoa2105872)
2 Site Web du Centre de contrôle et de prévention des maladies; Page sur la fibrillation auriculaire (https://www.cdc.gov/heartdisease/atrial_fibrillation.htm)
3 Pokorney et al, American Heart Journal, avril 2019 (https://www.sciencedirect.com/science/article/abs/pii/S0002870318302989?via%3Dihub)
4 Yao C et al PEC Innov 2022;1:100062. (https://www.sciencedirect.com/science/article/pii/S2772628222000474)
5 Yi BA et al. J Thromb Haemost. oct. 2021 (https://pubmed.ncbi.nlm.nih.gov/34714969/)
6 Hsu et coll. J Am Coll Cardiol. août 2021 (https://www.sciencedirect.com/science/article/abs/pii/S0735109721053213?via%3Dihub)
https://www.businesswire.com/news/home/20230918829025/en/Atrial-Fibrillation-Study-with-Abelacimab-Stopped-Early-by-the-Data-Monitoring-Committee-Due-to-an-Overwhelming-Reduction-in-Bleeding-as-Compared-to-a-DOAC-Direct-Oral-Anticoagulant
Commentaire
Une avancée thérapeutique incontestable
Affaire à suivre de très prés, la MTEV devrait pourvoir bénéficier de l'ABELACIMAB
Une injection mensuelle représente une autre avancée thérapeutique, l'ABELACIMAB
Commentaire
Une avancée thérapeutique incontestable
Affaire à suivre de très prés, la MTEV devrait pourvoir bénéficier de l'ABELACIMAB
Une injection mensuelle représente une autre avancée thérapeutique, l'ABELACIMAB
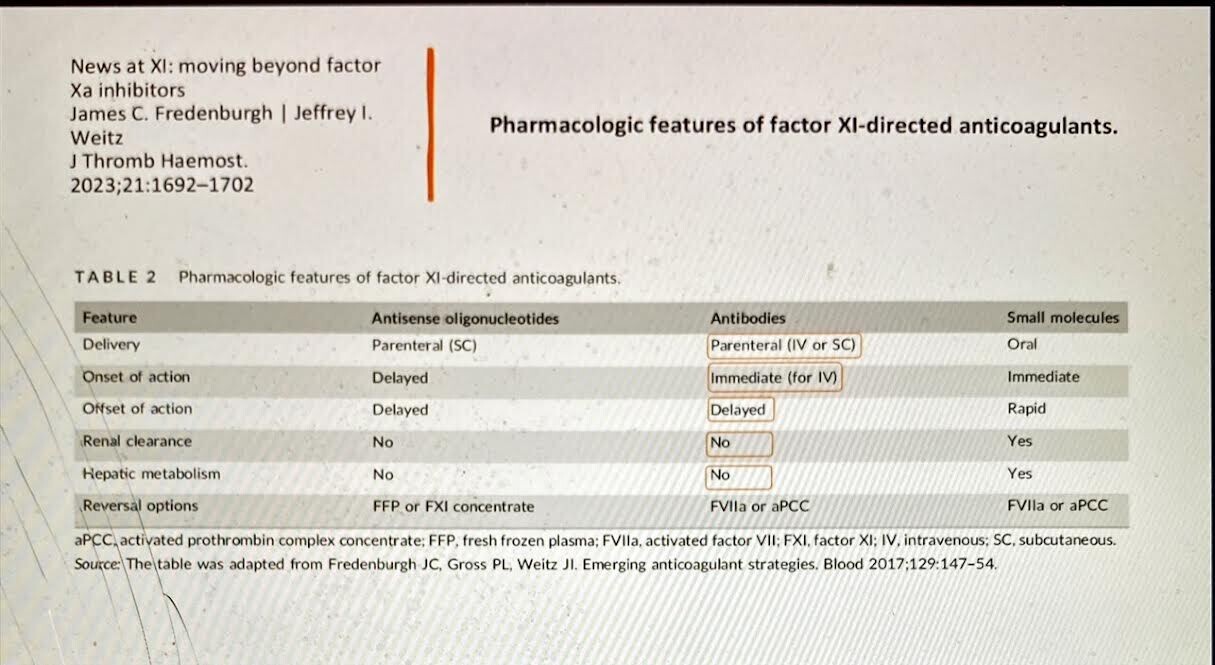
ANTIDOTE FACT VIIa ou APCC......as usual mais le risque hémorragique est si faible......
A RELIRE
https://medvasc.info/archives-blog/isth-2021-abelacimab
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC9191224/R
A RELIRE
https://medvasc.info/archives-blog/isth-2021-abelacimab
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC9191224/R
RAPPELS

D'après A ELIAS

