iconographie : thrombose
"L'incertitude est notre pire ennemi en terme de microbes. On peut prédire la trajectoire d'un astéroïde, la durée d'une éclipse solaire, or une pandémie est imprévisible. Et complètement invisible..." Franck Thilliez
Influence of sex on development of thrombosis in patients with COVID-19: From the CLOT-COVID study, Yugo Yamashita et Coll, Thrombosis Research 213 (2022) 173–178, https://www.thrombosisresearch.com/article/S0049-3848(22)00118-9/fulltext, Libre d'Accès
Influence du sexe sur le développement de la thrombose chez les patients atteints de COVID-19 : extrait de l'étude CLOT-COVID
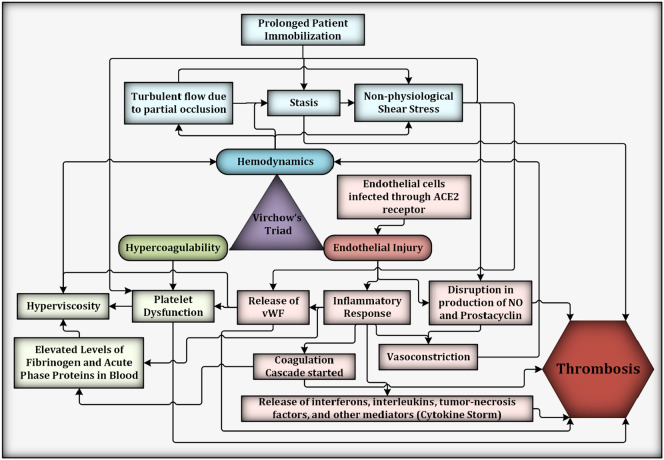 La triade de Virchow et quelques voies interconnectées contribuant à la thrombose dans les cas graves de COVID-19. Selon la triade de Virchow, l'hypercoagulabilité, les lésions endothéliales et l'hémodynamique sont les facteurs qui contribuent à la thrombose. Bien que de nombreuses voies biologiques entraînent une thrombose, il y a ici des sous-facteurs qui influencent directement (par exemple, l'immobilisation prolongée du patient, qui conduit à une thrombose induite par la stase) ou indirectement l'hémodynamique (par exemple, l'augmentation des taux de fibrinogène contribue à une plus grande résistance à l'écoulement en augmentant la viscosité du sang ). La production d'éléments antithrombotiques (par exemple, NO et prostacycline) initiée par une lésion endothéliale est également perturbée par une contrainte de cisaillement non physiologique. Certains facteurs ont un effet en cascade, tels que la libération de vWF après une lésion endothéliale entraînant un dysfonctionnement plaquettaire.
La triade de Virchow et quelques voies interconnectées contribuant à la thrombose dans les cas graves de COVID-19. Selon la triade de Virchow, l'hypercoagulabilité, les lésions endothéliales et l'hémodynamique sont les facteurs qui contribuent à la thrombose. Bien que de nombreuses voies biologiques entraînent une thrombose, il y a ici des sous-facteurs qui influencent directement (par exemple, l'immobilisation prolongée du patient, qui conduit à une thrombose induite par la stase) ou indirectement l'hémodynamique (par exemple, l'augmentation des taux de fibrinogène contribue à une plus grande résistance à l'écoulement en augmentant la viscosité du sang ). La production d'éléments antithrombotiques (par exemple, NO et prostacycline) initiée par une lésion endothéliale est également perturbée par une contrainte de cisaillement non physiologique. Certains facteurs ont un effet en cascade, tels que la libération de vWF après une lésion endothéliale entraînant un dysfonctionnement plaquettaire.
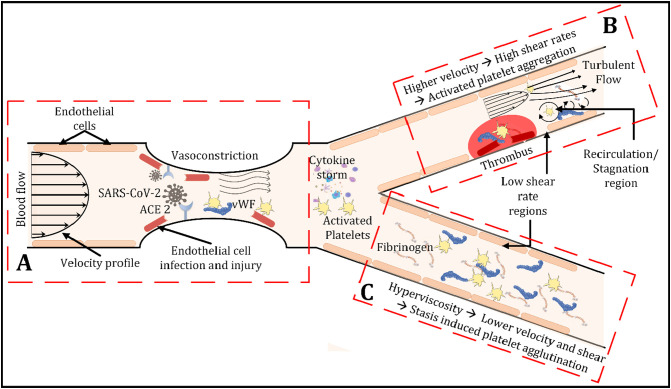 Schémas des paramètres hémodynamiques dans un vaisseau sanguin pour une éventuelle formation de thrombus chez les patients COVID-19. A) Le SRAS-CoV-2 se lie aux récepteurs ACE2, provoquant une lésion des cellules endothéliales qui initie diverses voies thrombotiques pour former un caillot sanguin dans différents environnements. La lésion des cellules endothéliales expose le facteur tissulaire, le vWF, le collagène et d'autres facteurs thrombotiques dans la circulation sanguine qui initient à la fois les voies intrinsèques et extrinsèques de la cascade de coagulation. De plus, la lumière du vaisseau se réduit en raison de la vasoconstriction induite par la blessure. Dans les petits vaisseaux et capillaires, tels que les capillaires alvéolaires, la vasoconstriction peut avoir un impact significatif, entraînant une congestion capillaire massive, des microthrombus diffus et des lésions organiques. B) Dans les petites artères, il y a une réduction de la lumière du vaisseau en raison de la formation de caillots sanguins et de la vasoconstriction, conduisant à une vitesse plus élevée et à un taux de cisaillement plus élevé. L'augmentation du taux de cisaillement induit des changements morphologiques du vWF, activant les plaquettes et augmentant la formation de thrombus. En aval du thrombus, des zones de recirculation/stagnation sont susceptibles de se présenter, et ces zones sont associées au dépôt de plaquettes. C) Une augmentation de la viscosité du plasma est observée chez les patients COVID-19, ce qui, dans les veines et les capillaires plus petits, entraîne des vitesses plus faibles et des taux de cisaillement plus faibles. De faibles valeurs non physiologiques de cisaillement influencent l'agglutination des plaquettes. C) Une augmentation de la viscosité du plasma est observée chez les patients COVID-19, ce qui, dans les veines et les capillaires plus petits, entraîne des vitesses plus faibles et des taux de cisaillement plus faibles. De faibles valeurs non physiologiques de cisaillement influencent l'agglutination des plaquettes. C) Une augmentation de la viscosité du plasma est observée chez les patients COVID-19, ce qui, dans les veines et les capillaires plus petits, entraîne des vitesses plus faibles et des taux de cisaillement plus faibles. De faibles valeurs non physiologiques de cisaillement influencent l'agglutination des plaquettes.
Schémas des paramètres hémodynamiques dans un vaisseau sanguin pour une éventuelle formation de thrombus chez les patients COVID-19. A) Le SRAS-CoV-2 se lie aux récepteurs ACE2, provoquant une lésion des cellules endothéliales qui initie diverses voies thrombotiques pour former un caillot sanguin dans différents environnements. La lésion des cellules endothéliales expose le facteur tissulaire, le vWF, le collagène et d'autres facteurs thrombotiques dans la circulation sanguine qui initient à la fois les voies intrinsèques et extrinsèques de la cascade de coagulation. De plus, la lumière du vaisseau se réduit en raison de la vasoconstriction induite par la blessure. Dans les petits vaisseaux et capillaires, tels que les capillaires alvéolaires, la vasoconstriction peut avoir un impact significatif, entraînant une congestion capillaire massive, des microthrombus diffus et des lésions organiques. B) Dans les petites artères, il y a une réduction de la lumière du vaisseau en raison de la formation de caillots sanguins et de la vasoconstriction, conduisant à une vitesse plus élevée et à un taux de cisaillement plus élevé. L'augmentation du taux de cisaillement induit des changements morphologiques du vWF, activant les plaquettes et augmentant la formation de thrombus. En aval du thrombus, des zones de recirculation/stagnation sont susceptibles de se présenter, et ces zones sont associées au dépôt de plaquettes. C) Une augmentation de la viscosité du plasma est observée chez les patients COVID-19, ce qui, dans les veines et les capillaires plus petits, entraîne des vitesses plus faibles et des taux de cisaillement plus faibles. De faibles valeurs non physiologiques de cisaillement influencent l'agglutination des plaquettes. C) Une augmentation de la viscosité du plasma est observée chez les patients COVID-19, ce qui, dans les veines et les capillaires plus petits, entraîne des vitesses plus faibles et des taux de cisaillement plus faibles. De faibles valeurs non physiologiques de cisaillement influencent l'agglutination des plaquettes. C) Une augmentation de la viscosité du plasma est observée chez les patients COVID-19, ce qui, dans les veines et les capillaires plus petits, entraîne des vitesses plus faibles et des taux de cisaillement plus faibles. De faibles valeurs non physiologiques de cisaillement influencent l'agglutination des plaquettes.
Les complications découlant de la COVID-19 grave, en particulier les incidents thromboemboliques, entraînent des conséquences fatales chez les patients. Il existe une interaction significative entre les lésions endothéliales, l'hypercoagulabilité et les voies hémodynamiques conduisant aux événements thromboemboliques. Sur la base de la littérature disponible, nous émettons l'hypothèse que différents paramètres hémodynamiques pourraient aggraver les complications observées chez les patients atteints de COVID-19 sévère par divers mécanismes tels que l'état d'hypercoagulabilité, la stase, le flux turbulent et l'activation et l'agrégation plaquettaires médiées par le cisaillement. Bien que certaines options de diagnostic et de traitement soient disponibles, des recherches supplémentaires sont nécessaires pour comprendre la physiopathologie sous-jacente du COVID-19 et ses ramifications dans la progression de la maladie, y compris son impact sur l'hémodynamique systémique.
Il existe une interaction significative entre les lésions endothéliales, l'hypercoagulabilité et les voies hémodynamiques conduisant aux événements thromboemboliques.
COVID-19 vaccine dilemmas, AVK Lee, Public Health. 2022 Jan; 202: 10–11.
"L'incertitude est notre pire ennemi en terme de microbes. On peut prédire la trajectoire d'un astéroïde, la durée d'une éclipse solaire, or une pandémie est imprévisible. Et complètement invisible..." Franck Thilliez
Influence of sex on development of thrombosis in patients with COVID-19: From the CLOT-COVID study, Yugo Yamashita et Coll, Thrombosis Research 213 (2022) 173–178, https://www.thrombosisresearch.com/article/S0049-3848(22)00118-9/fulltext, Libre d'Accès
Influence du sexe sur le développement de la thrombose chez les patients atteints de COVID-19 : extrait de l'étude CLOT-COVID
Introduction
Il existe des données limitées sur l'influence du sexe sur le développement de la thrombose chez les patients atteints de la maladie à coronavirus 2019 (COVID-19).
matériaux et méthodes
L'étude CLOT-COVID était une étude de cohorte rétrospective multicentrique recrutant 2894 patients hospitalisés consécutifs atteints de COVID-19 dans 16 centres au Japon d'avril 2021 à septembre 2021. Nous avons divisé l'ensemble de la cohorte en hommes ( N = 1885) et femmes ( N = 1009) groupes.
Résultats
Il n'y avait pas de différences significatives dans les niveaux de D-dimères à l'admission entre les hommes et les femmes. Les hommes présentaient un état de COVID-19 plus sévère à l'admission que les femmes (léger : 57 % contre 66 %, modéré : 34 % contre 29 % et sévère : 9,1 % contre 5,7 %, P < 0,001). Les hommes recevaient plus souvent une thromboprophylaxie pharmacologique que les femmes (47 % versus 35 %, P < 0,001). Au cours de l'hospitalisation, les hommes ont plus souvent développé une thrombose que les femmes (2,5 % [IC 95 %, 1,9–3,3 %] versus 0,8 % [IC 95 %, 0,4–1,6 %], P = 0,001). Les hommes avaient des incidences de thrombose numériquement plus élevées que les femmes dans tous les sous-groupes de la pire gravité de COVID-19 pendant l'hospitalisation (légère : 0,3 % contre 0,0 %, modérée : 1,6 % contre 1,0 % et grave : 11,1 % contre 4,3 %). Même après ajustement des facteurs de confusion dans le modèle de régression logistique multivariable, l'excès de risque des hommes par rapport aux femmes est resté significatif pour la thrombose (OR ajusté, 2,51 ; IC à 95 %, 1,16 à 5,43, P = 0,02).
Conclusion
Dans la grande étude observationnelle actuelle de patients atteints de COVID-19, les hommes avaient un statut plus grave du COVID-19 que les femmes, et le risque de développement de thrombose était plus élevé chez les hommes que chez les femmes, ce qui pourrait être utile pour déterminer le patient- stratégies de gestion optimale spécifiques pour COVID-19.
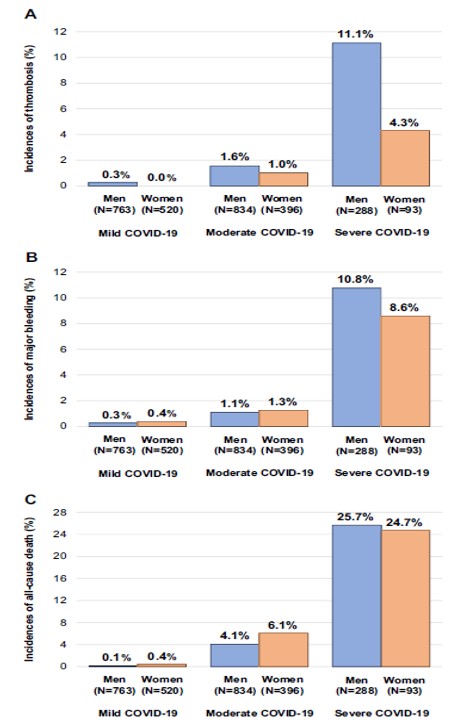
Incidences des thromboses (A), des hémorragies majeures (B) et des décès toutes causes confondues (C) comparant les hommes et les femmes selon la pire sévérité du COVID-19 au cours de l'hospitalisation.
COVID-19 is associated with higher risk of venous thrombosis, but not arterial thrombosis, compared with influenza: Insights from a large US cohort,Quartier André et Coll, PLOS ONE | https://doi.org/10.1371/journal.pone.0261786 January 12, 2022, Libre d'Accès
Le COVID-19 est associé à un risque plus élevé de thrombose veineuse, mais pas de thrombose artérielle, par rapport à la grippe : aperçu d'une grande cohorte américaine

Incidences des thromboses (A), des hémorragies majeures (B) et des décès toutes causes confondues (C) comparant les hommes et les femmes selon la pire sévérité du COVID-19 au cours de l'hospitalisation.
Les hommes avaient un statut plus grave du COVID-19 que les femmes, et le risque de développement de thrombose était plus élevé chez les hommes que chez les femmes,
COVID-19 is associated with higher risk of venous thrombosis, but not arterial thrombosis, compared with influenza: Insights from a large US cohort,Quartier André et Coll, PLOS ONE | https://doi.org/10.1371/journal.pone.0261786 January 12, 2022, Libre d'Accès
Le COVID-19 est associé à un risque plus élevé de thrombose veineuse, mais pas de thrombose artérielle, par rapport à la grippe : aperçu d'une grande cohorte américaine
Introduction
L'infection par le SRAS-CoV-2 est généralement comparée à la grippe pour contextualiser ses risques pour la santé. Le SRAS-CoV-2 a été associé à des troubles de la coagulation, notamment la thrombose artérielle, ce qui a suscité un intérêt considérable pour le traitement antithrombotique de la maladie à coronavirus 2019 (COVID-19). Cependant, le risque thromboembolique indépendant de l'infection par le SRAS-CoV-2 par rapport à la grippe reste incomplètement compris. Nous avons évalué les risques ajustés d'événements thromboemboliques après un diagnostic de COVID-19 par rapport à la grippe dans une large cohorte rétrospective.
L'infection par le SRAS-CoV-2 est généralement comparée à la grippe pour contextualiser ses risques pour la santé. Le SRAS-CoV-2 a été associé à des troubles de la coagulation, notamment la thrombose artérielle, ce qui a suscité un intérêt considérable pour le traitement antithrombotique de la maladie à coronavirus 2019 (COVID-19). Cependant, le risque thromboembolique indépendant de l'infection par le SRAS-CoV-2 par rapport à la grippe reste incomplètement compris. Nous avons évalué les risques ajustés d'événements thromboemboliques après un diagnostic de COVID-19 par rapport à la grippe dans une large cohorte rétrospective.
Méthodes
Nous avons utilisé un ensemble de données de dossiers de santé électroniques (DSE) basé aux États-Unis lié à des réclamations d'assurance pour identifier les adultes diagnostiqués avec le COVID-19 entre le 1er avril 2020 et le 31 octobre 2020. Nous avons identifié les patients atteints de grippe diagnostiqués entre le 1er octobre 2018 et le 31 avril. 2019. Principaux résultats [composite veineux d'embolie pulmonaire (EP) et de thrombose veineuse profonde aiguë (TVP) ; composite artériel d'AVC ischémique et d'infarctus du myocarde (IM)] et les résultats secondaires ont été évalués 90 jours après le diagnostic. Les scores de propension (PS) ont été calculés à l'aide de variables démographiques, cliniques et médicamenteuses. Les rapports de risque (RR) ajustés par PS ont été calculés à l'aide de la régression des risques proportionnels de Cox.
Nous avons utilisé un ensemble de données de dossiers de santé électroniques (DSE) basé aux États-Unis lié à des réclamations d'assurance pour identifier les adultes diagnostiqués avec le COVID-19 entre le 1er avril 2020 et le 31 octobre 2020. Nous avons identifié les patients atteints de grippe diagnostiqués entre le 1er octobre 2018 et le 31 avril. 2019. Principaux résultats [composite veineux d'embolie pulmonaire (EP) et de thrombose veineuse profonde aiguë (TVP) ; composite artériel d'AVC ischémique et d'infarctus du myocarde (IM)] et les résultats secondaires ont été évalués 90 jours après le diagnostic. Les scores de propension (PS) ont été calculés à l'aide de variables démographiques, cliniques et médicamenteuses. Les rapports de risque (RR) ajustés par PS ont été calculés à l'aide de la régression des risques proportionnels de Cox.
Résultats
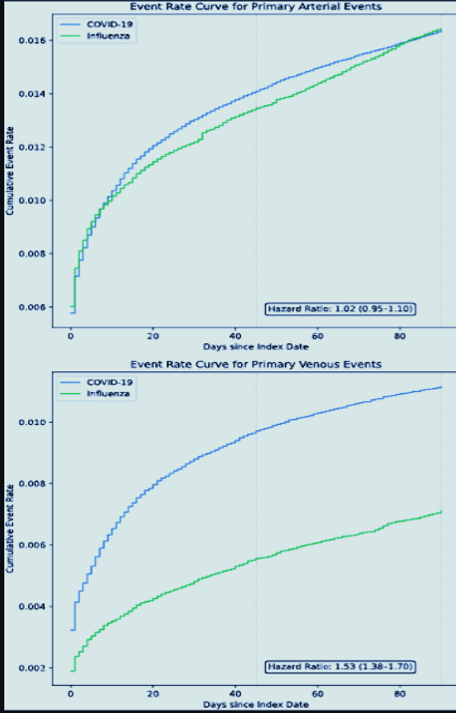
Il y avait 417 975 patients COVID-19 (âge médian 57 ans, 61 % de femmes) et 345 934 patients atteints de grippe (âge médian 47 ans, 66 % de femmes). Par rapport à la grippe, les patients atteints de COVID-19 présentaient un risque thromboembolique veineux plus élevé (HR 1,53, IC à 95 % 1,38–1,70), mais pas de risque thromboembolique artériel (HR 1,02, IC à 95 % 0,95–1,10). Des analyses secondaires ont démontré un risque similaire d'AVC ischémique (HR 1,11, IC à 95 % 0,98-1,25) et d'IM (HR 0,93, IC à 95 % 0,85-1,03) et un risque plus élevé de TVP (HR 1,36, IC à 95 % 1,19-1,56) et d'EP (HR 1,82, IC à 95 % 1,57–2,10) chez les patients atteints de COVID-19.
Il y avait 417 975 patients COVID-19 (âge médian 57 ans, 61 % de femmes) et 345 934 patients atteints de grippe (âge médian 47 ans, 66 % de femmes). Par rapport à la grippe, les patients atteints de COVID-19 présentaient un risque thromboembolique veineux plus élevé (HR 1,53, IC à 95 % 1,38–1,70), mais pas de risque thromboembolique artériel (HR 1,02, IC à 95 % 0,95–1,10). Des analyses secondaires ont démontré un risque similaire d'AVC ischémique (HR 1,11, IC à 95 % 0,98-1,25) et d'IM (HR 0,93, IC à 95 % 0,85-1,03) et un risque plus élevé de TVP (HR 1,36, IC à 95 % 1,19-1,56) et d'EP (HR 1,82, IC à 95 % 1,57–2,10) chez les patients atteints de COVID-19.
Conclusion
Dans une grande cohorte américaine rétrospective, le COVID-19 était indépendamment associé à un risque plus élevé de thrombose veineuse à 90 jours, mais pas de thrombose artérielle, par rapport à la grippe. Ces résultats peuvent éclairer des lacunes cruciales dans les connaissances concernant les risques thromboemboliques spécifiques de COVID-19.
Dans une grande cohorte américaine rétrospective, le COVID-19 était indépendamment associé à un risque plus élevé de thrombose veineuse à 90 jours, mais pas de thrombose artérielle, par rapport à la grippe. Ces résultats peuvent éclairer des lacunes cruciales dans les connaissances concernant les risques thromboemboliques spécifiques de COVID-19.

Courbes de taux d'événements cumulés pour les critères de jugement principaux.
Courbes de taux d'événements cumulés pondérés par la propension stratifiée dans les populations COVID-19 et grippales. Les rapports de risque avec des intervalles de confiance à 95 % sont indiqués. Après pondération, les cohortes ont été équilibrées sur 49 covariables, y compris la démographie, l'utilisation de médicaments et les comorbidités cliniques associées à la thromboembolie artérielle et veineuse.
https://doi.org/10.1371/journal.pone.0261786.g002
La COVID-19 était indépendamment associé à un risque plus élevé de thrombose veineuse à 90 jours, mais pas de thrombose artérielle, par rapport à la grippe
COVID-19 and thrombosis: The role of hemodynamics , Sudeep Sastry et Coll, Trends in Cardiovascular MedicineVolume 31, Issue 3, April 2021, Pages 143-160, Libre d'Accès, https://www.sciencedirect.com/science/article/pii/S1050173820301572?via%3Dihub
COVID-19 et thrombose : le rôle de l'hémodynamique
La COVID-19 était indépendamment associé à un risque plus élevé de thrombose veineuse à 90 jours, mais pas de thrombose artérielle, par rapport à la grippe
COVID-19 and thrombosis: The role of hemodynamics , Sudeep Sastry et Coll, Trends in Cardiovascular MedicineVolume 31, Issue 3, April 2021, Pages 143-160, Libre d'Accès, https://www.sciencedirect.com/science/article/pii/S1050173820301572?via%3Dihub
COVID-19 et thrombose : le rôle de l'hémodynamique

 Schémas des paramètres hémodynamiques dans un vaisseau sanguin pour une éventuelle formation de thrombus chez les patients COVID-19. A) Le SRAS-CoV-2 se lie aux récepteurs ACE2, provoquant une lésion des cellules endothéliales qui initie diverses voies thrombotiques pour former un caillot sanguin dans différents environnements. La lésion des cellules endothéliales expose le facteur tissulaire, le vWF, le collagène et d'autres facteurs thrombotiques dans la circulation sanguine qui initient à la fois les voies intrinsèques et extrinsèques de la cascade de coagulation. De plus, la lumière du vaisseau se réduit en raison de la vasoconstriction induite par la blessure. Dans les petits vaisseaux et capillaires, tels que les capillaires alvéolaires, la vasoconstriction peut avoir un impact significatif, entraînant une congestion capillaire massive, des microthrombus diffus et des lésions organiques. B) Dans les petites artères, il y a une réduction de la lumière du vaisseau en raison de la formation de caillots sanguins et de la vasoconstriction, conduisant à une vitesse plus élevée et à un taux de cisaillement plus élevé. L'augmentation du taux de cisaillement induit des changements morphologiques du vWF, activant les plaquettes et augmentant la formation de thrombus. En aval du thrombus, des zones de recirculation/stagnation sont susceptibles de se présenter, et ces zones sont associées au dépôt de plaquettes. C) Une augmentation de la viscosité du plasma est observée chez les patients COVID-19, ce qui, dans les veines et les capillaires plus petits, entraîne des vitesses plus faibles et des taux de cisaillement plus faibles. De faibles valeurs non physiologiques de cisaillement influencent l'agglutination des plaquettes. C) Une augmentation de la viscosité du plasma est observée chez les patients COVID-19, ce qui, dans les veines et les capillaires plus petits, entraîne des vitesses plus faibles et des taux de cisaillement plus faibles. De faibles valeurs non physiologiques de cisaillement influencent l'agglutination des plaquettes. C) Une augmentation de la viscosité du plasma est observée chez les patients COVID-19, ce qui, dans les veines et les capillaires plus petits, entraîne des vitesses plus faibles et des taux de cisaillement plus faibles. De faibles valeurs non physiologiques de cisaillement influencent l'agglutination des plaquettes.
Schémas des paramètres hémodynamiques dans un vaisseau sanguin pour une éventuelle formation de thrombus chez les patients COVID-19. A) Le SRAS-CoV-2 se lie aux récepteurs ACE2, provoquant une lésion des cellules endothéliales qui initie diverses voies thrombotiques pour former un caillot sanguin dans différents environnements. La lésion des cellules endothéliales expose le facteur tissulaire, le vWF, le collagène et d'autres facteurs thrombotiques dans la circulation sanguine qui initient à la fois les voies intrinsèques et extrinsèques de la cascade de coagulation. De plus, la lumière du vaisseau se réduit en raison de la vasoconstriction induite par la blessure. Dans les petits vaisseaux et capillaires, tels que les capillaires alvéolaires, la vasoconstriction peut avoir un impact significatif, entraînant une congestion capillaire massive, des microthrombus diffus et des lésions organiques. B) Dans les petites artères, il y a une réduction de la lumière du vaisseau en raison de la formation de caillots sanguins et de la vasoconstriction, conduisant à une vitesse plus élevée et à un taux de cisaillement plus élevé. L'augmentation du taux de cisaillement induit des changements morphologiques du vWF, activant les plaquettes et augmentant la formation de thrombus. En aval du thrombus, des zones de recirculation/stagnation sont susceptibles de se présenter, et ces zones sont associées au dépôt de plaquettes. C) Une augmentation de la viscosité du plasma est observée chez les patients COVID-19, ce qui, dans les veines et les capillaires plus petits, entraîne des vitesses plus faibles et des taux de cisaillement plus faibles. De faibles valeurs non physiologiques de cisaillement influencent l'agglutination des plaquettes. C) Une augmentation de la viscosité du plasma est observée chez les patients COVID-19, ce qui, dans les veines et les capillaires plus petits, entraîne des vitesses plus faibles et des taux de cisaillement plus faibles. De faibles valeurs non physiologiques de cisaillement influencent l'agglutination des plaquettes. C) Une augmentation de la viscosité du plasma est observée chez les patients COVID-19, ce qui, dans les veines et les capillaires plus petits, entraîne des vitesses plus faibles et des taux de cisaillement plus faibles. De faibles valeurs non physiologiques de cisaillement influencent l'agglutination des plaquettes.Les complications découlant de la COVID-19 grave, en particulier les incidents thromboemboliques, entraînent des conséquences fatales chez les patients. Il existe une interaction significative entre les lésions endothéliales, l'hypercoagulabilité et les voies hémodynamiques conduisant aux événements thromboemboliques. Sur la base de la littérature disponible, nous émettons l'hypothèse que différents paramètres hémodynamiques pourraient aggraver les complications observées chez les patients atteints de COVID-19 sévère par divers mécanismes tels que l'état d'hypercoagulabilité, la stase, le flux turbulent et l'activation et l'agrégation plaquettaires médiées par le cisaillement. Bien que certaines options de diagnostic et de traitement soient disponibles, des recherches supplémentaires sont nécessaires pour comprendre la physiopathologie sous-jacente du COVID-19 et ses ramifications dans la progression de la maladie, y compris son impact sur l'hémodynamique systémique.
Il existe une interaction significative entre les lésions endothéliales, l'hypercoagulabilité et les voies hémodynamiques conduisant aux événements thromboemboliques.
COVID-19 vaccine dilemmas, AVK Lee, Public Health. 2022 Jan; 202: 10–11.
Published online 2021 Feb 1. doi: 10.1016/j.puhe.2021.01.009
Les dilemmes du vaccin COVID-19
Il y a aussi une dimension morale – est-il juste de vacciner un grand nombre d'individus principalement à faible risque dans les pays à revenu élevé plutôt que d'autres individus vulnérables ailleurs ? En effet, l'accès aux vaccins ne devrait-il pas être déterminé par les besoins plutôt que par la richesse et l'influence nationales ? C'est peut-être pourquoi l'initiative COVAX est essentielle pour garantir l'équité d'accès aux vaccins.
Les dilemmes du vaccin COVID-19
L'arrivée des vaccins COVID-19 a déclenché une course aux vaccins entre les pays pour immuniser leurs populations dans l'espoir qu'elle puisse restaurer un semblant de normalité par la suite. Cette course favorise les pays à revenu élevé, et il existe de réelles inquiétudes quant au fait que le nationalisme vaccinal pourrait saper les efforts de coopération pour contrôler la pandémie à l'échelle mondiale. Cela créera des perdants et creusera les inégalités mondiales.
La vaccination de masse dans les pays à revenu élevé ne confère pas nécessairement la sécurité car il subsiste un risque de réimportation d'infections en provenance de pays à faible revenu où le virus est endémique.
Il y a aussi une dimension morale – est-il juste de vacciner un grand nombre d'individus principalement à faible risque dans les pays à revenu élevé plutôt que d'autres individus vulnérables ailleurs ? En effet, l'accès aux vaccins ne devrait-il pas être déterminé par les besoins plutôt que par la richesse et l'influence nationales ? C'est peut-être pourquoi l'initiative COVAX est essentielle pour garantir l'équité d'accès aux vaccins.
Dans un monde globalisé et interconnecté, tous nos destins sont liés. La solidarité mondiale est nécessaire pour protéger notre santé nationale, notre richesse et nos droits humains.
Essentiellement, nous ne sommes pas en sécurité tant que nous ne le sommes pas tous.
Essentiellement, nous ne sommes pas en sécurité tant que nous ne le sommes pas tous.
Un point essentiel, qui s'en soucie ?