Maladie artérielle périphérique : mécanismes moléculaires et nouvelles thérapies
https://pubmed.ncbi.nlm.nih.gov/38776386/
Pour explorer la collection complète du Centenaire, visitez : https://www-ahajournals-org.proxy.insermbiblio.inist.fr/centennial
L'AOMI touche plus de 200 millions de personnes dans le monde.
1 Alors que les cas bénins se manifestent généralement uniquement par une claudication (du latin claudicatio , signifiant boiter), l'AOMI est désormais reconnue comme l'une des formes les plus morbides de maladie cardiovasculaire et un facteur majeur d'amputation, d'invalidité cardiovasculaire et de décès.
2 L'AOMI était historiquement considérée comme une manifestation extracardiaque de l'athérosclérose, mais de nouvelles études génétiques et mécanistiques suggèrent qu'il s'agit peut-être d'une simplification excessive.
En effet, des études récentes indiquent des rôles spécifiques pour les défauts calciques, inflammatoires et angiogéniques, au-delà de ceux liés aux facteurs de risque établis depuis longtemps liés à la maladie coronarienne.
Dans ce bref aperçu de la Collection Centenaire, nous commençons par résumer les mécanismes connus et émergents sous-jacents à l'AP ( Figure ci dessous ), puis mettons en évidence de nouvelles thérapies translationnelles qui promettent d'améliorer les résultats pour les personnes souffrant de cette maladie hautement morbide.
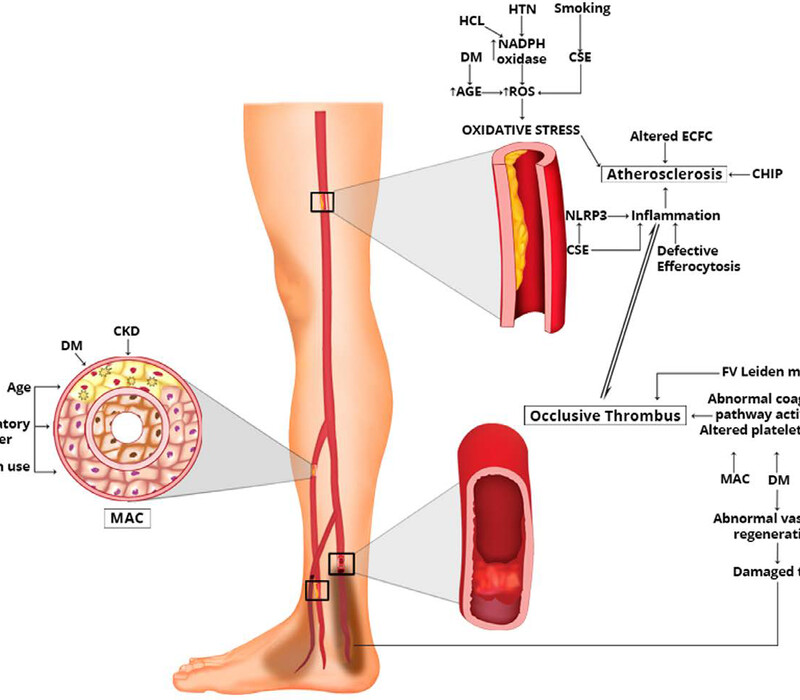
Mechanisms contributing to PAD.
AGE indicates advanced glycation end product; AS, atherosclerosis; CHIP, clonal hematopoiesis of indeterminate potential; CKD, chronic kidney disease; CSE, cigarette smoking extract; DM, diabetes mellitus; ECFC, endothelial colony forming cell; FV, factor 5; HCL, hypercholesterolemia; HTN, hypertension; MAC, medial arterial calcification; NADPH, nicotinamide adenine dinucleotide phosphate hydrogen; NLRP3, nucleotide-binding domain, leucine-rich–containing family, pyrin domain–containing-3 inflammasome; and ROS, reactive oxygen species.
Diabète sucré, tabagisme, hypertension et hypercholestérolémie
Ces conditions cliniques comptent parmi les facteurs de risque les plus importants de l'AOPMI un mécanisme commun qu’ils partagent comprend le stress oxydatif, provoqué par un déséquilibre des espèces réactives de l’oxygène et des défenses antioxydantes.
Ces processus conduisent à un dysfonctionnement endothélial, une vasoconstriction, un remodelage des cellules musculaires lisses, une transformation phénotypique des macrophages, une inflammation et, finalement, le développement de l'athérosclérose.
Le stress oxydatif résulte de la surproduction de produits finaux de glycation avancée et de leurs récepteurs dans le diabète sucré (DM), de l'expression accrue de la nicotinamide adénine dinucléotide phosphate hydrogénooxydase et de l'activation du système rénine-angiotensine dans l'hypertension, via la xanthine oxydase et la nicotinamide adénine dinucléotide phosphate hydrogène. oxydase dans l'hypercholestérolémie et extraits de fumée de cigarette chez les fumeurs.
Cependant, ces 3 facteurs de risque favorisent également l'AOMI via des mécanismes indépendants.
Outre le dysfonctionnement endothélial direct, l'état métabolique altéré du diabète semble contribuer à une activation anormale des plaquettes et de la coagulation, favorisant ainsi l'athérothrombose.
Dans les modèles animaux, la DM entrave également le développement du flux sanguin collatéral par régénération vasculaire, tandis que la résistance à l'insuline et les changements métaboliques liés à l'hyperglycémie nuisent à la capacité du muscle squelettique à se remettre d'une blessure.
La dérégulation médiée par le DM des processus épigénétiques tels que la modification des histones et la méthylation de l'ADN peut avoir des effets profonds sur la régulation des gènes dans les vaisseaux sanguins.
Ces effets néfastes sur la macro vascularisation et la micro vascularisation contribuent au développement de plaies, à une cicatrisation altérée et à la morbidité liée à l'AOMI. Il a été rapporté que le tabagisme est un facteur de risque plus important de MAP que de maladie coronarienne.
Des études d'association à l'échelle du génome ont identifié des variantes dans le locus CHRNA3 , qui sont associées à la maladie pulmonaire obstructive chronique et à la dépendance à la nicotine et sont uniquement liées à l'AOMI
Des études in vitro ont montré que les extraits de fumée de cigarette réduisent la synthèse des protéines en induisant un mauvais repliement des protéines dans le réticulum endoplasmique, ce qui contribue au stress du réticulum endoplasmique, à l'activation des voies de l'autophagie et, éventuellement, au dysfonctionnement endothélial. Le tabagisme peut affecter la différenciation des monocytes en macrophages, la transformation phénotypique des cellules musculaires lisses vasculaires, la migration et la dégradation de la matrice extracellulaire. Les extraits de fumée de cigarette contribuent également à un état pro-inflammatoire en induisant la production de chimiokines, de cytokines et de dommages mitochondriaux.
Ensemble, ces changements contribuent à l’athérosclérose.
Une gamme de lipoprotéines athérogènes ont également été causalement liées à l'AOMI
Les études d'épidémiologie générale et celles réalisées chez des sujets présentant des formes familiales d'hypercholestérolémie ont mis en évidence un lien fort entre les LDL (lipoprotéines de basse densité) et l'athérosclérose périphérique.
Les niveaux de lipoprotéines (a; Lp[a]) auraient également été associés à un risque accru d' AOMIet d'événements indésirables majeurs au niveau des membres, tout comme les cibles émergentes créées via le métabolisme des triglycérides, telles que le cholestérol résiduel. Klarin et al ont rapporté que les variations héréditaires du LDLR , du LPL et du LPA sont chacune associées à l'AOMI dans des études d'association pangénomiques et dans l'essai ODYSSEY OUTCOMES (Evaluation of Cardiovascular Outcomes After an Acute Coronary Syndrome Pendant Treatment With Alirocumab ) ont signalé une corrélation entre la concentration initiale de Lp(a) et le risque d''AOMI
Beaucoup de ces lipides athérogènes s'oxydent et sont piégés dans l'espace sous-endothélial, où ils s'accumulent non seulement pour favoriser la formation de cellules spumeuses et l'agrandissement de la plaque, mais servent également de facteurs d'inflammation et de thrombogénicité, deux facteurs essentiels de l'AOMI, comme indiqué ci-dessous.
Calcification artérielle médiale
La calcification au sein de la tunique média a été impliquée en tant que moteur de la MAP.
Les maladies rénales, le diabète, les troubles inflammatoires, l'utilisation de warfarine et l'âge ont chacun été signalés comme des facteurs de risque de MAC. 1
La calcification vasculaire est médiée par des voies régulées qui contribuent à la formation osseuse, à la différenciation ostéogénique des cellules souches et à la transdifférenciation des cellules musculaires lisses vasculaires en cellules de type ostéochondrocyte en réponse à des signaux environnementaux.
Des leçons ont également été tirées des troubles génétiques de calcification qui se manifestent par une maladie vasculaire extracoronaire, comme la calcification artérielle due à un déficit en CD73. La calcification artérielle due à un déficit en CD73 est causée par des mutations du gène NT5E , qui diminuent l'expression de CD73, augmentent la TNAP (phosphatase alcaline non spécifique des tissus) et favorisent la minéralisation ectopique, conduisant à une calcification artérielle. Une étude évaluant les artères fémoro-poplitées explantées a montré que l'expression de CD73 était plus faible dans les artères calcifiées malgré l'absence de mutation du gène NT5E, soulevant la possibilité que cet axe puisse jouer un rôle général dans la pathogenèse de la MAP, même chez celles sans formes mendéliennes de PAD.
Une activation plaquettaire altérée et un milieu prothrombotique peuvent contribuer à une obstruction luminale, en particulier dans le système vasculaire distal des personnes atteintes de MAP.
Narula et al ont rapporté que parmi les artères infrapoplitées présentant une sténose luminale >=70 %, moins de la moitié présentaient une athérosclérose significative.
Dans ces vaisseaux, la présence de thrombus expliquait la sténose ou l'obstruction malgré leur intima normale ou leur épaississement adaptatif de l'intima. De plus, l’athérosclérose et la calcification peuvent déclencher une thrombose, ce qui suggère l’existence d’une possible boucle de rétroaction positive pour les personnes atteintes de plaque.
Une activation plaquettaire altérée et un milieu pro thrombotique peuvent également favoriser le développement de l'AOMI.
Dans de petites études, il a été constaté que les patients atteints d'une MAP présentaient une activation plaquettaire accrue, comme l'ont évalué les études d'agrégation et la cyrtométrie en flux, ainsi que le degré d'activité plaquettaire corrélé à la gravité de la MAP. 9 En outre, il a été rapporté que, malgré l'utilisation d'aspirine, les personnes souffrant de claudication ont des propriétés d'activation plaquettaire comparables à celles des sujets témoins (non traités par antiplaquettaire) et que [presque égal à] 35 % des patients souffrant d'ischémie critique des membres peuvent avez une résistance à l’aspirine ou au clopidogrel.
Des études d'association pangénomiques ont également rapporté que la variante du facteur V Leiden ( F5 p.R506Q) est un facteur de risque unique d'AOMI.
Les mécanismes exacts par lesquels la thrombose favorise le développement de l'MAP n'ont pas encore été entièrement élucidés. Cependant, on émet l'hypothèse que le TF (facteur tissulaire) et d'autres facteurs de coagulation activés pourraient être signalés via les PAR (récepteurs activés par la protéase), le système immunitaire inné ou la cascade du complément. Ces cascades peuvent déclencher des événements cellulaires tels que la prolifération, la migration, l’adhésion, l’apoptose et l’inflammation, en plus de l’obstruction physique provoquée par le thrombus lui-même. Les microparticules et les pièges extracellulaires des neutrophiles ont également été impliqués dans la thrombose et l'inflammation ; cependant, leur pertinence clinique dans l'AOMI reste encore à élucider.
Inflammation
L'inflammation est de plus en plus reconnue comme un facteur de risque important de l'AOMI. Des niveaux élevés de CRP (protéine C-réactive) ont été associés de manière indépendante à l'MAP incidente9, tout comme le complexe inflammatoire pro inflammatoire NLRP3 (domaine de liaison aux nucléotides, famille contenant de la leucine, inflammasome contenant le domaine 3 de la pyrine). 23 NLRP3 s'assemble en réponse à des agents pathogènes envahissants ou à un stress endogène, induit la conversion de la famille de cytokines pro inflammatoires IL (interleukine)-1 en leurs formes bioactives, IL-1[bêta] et IL-18, et aboutit finalement à une pyroptose et à une prolifération cellulaire. la mort. Un autre mécanisme qui peut contribuer à un état inflammatoire accru est l’efférocytose défectueuse (élimination programmée des cellules), qui permet l’accumulation de cellules apoptotiques, la nécrose et la libération de contenus intracellulaires proinflammatoires dans la plaque athéroscléreuse en développement.
Hématopoïèse clonale à potentiel indéterminé
L'hématopoïèse clonale de potentiel indéterminé fait référence à la présence d'une cellule souche hématopoïétique à expansion clonale résultant d'une mutation leucémogène chez des individus sans signe d'hémopathie maligne, de dysplasie ou de cytopénie. Ce phénomène se manifeste par une inflammation des macrophages et est indépendamment associé à un risque cardiovasculaire accru chez les patients atteints d'AOMI. Buttner et al . ont signalé la présence d'une hématopoïèse clonale de mutations potentielles indéterminées dans le sang périphérique et dans des lésions athéroscléreuses chez des individus atteints d'une MAP, ce qui donne du crédit à l'hypothèse selon laquelle une hématopoïèse clonale de potentiel indéterminé pourrait contribuer à l'AOMI.
Modification de l'abondance et de la fonction des cellules endothéliales formant des colonies
On a également émis l'hypothèse qu'un déficit relatif en angiogenèse et en artériogenèse favoriserait la MAP. Les cellules circulantes qui donnent naissance à des cellules endothéliales matures et favorisent la régénération vasculaire, les cellules endothéliales formant des colonies, sont réduites et ont une fonction altérée chez les patients atteints de diabète. On suppose que cela crée un déséquilibre entre les dommages vasculaires et la réparation, contribuant finalement à l'athérosclérose et à une perfusion distale réduite.
Enquêtes mécanistiques en cours
Bien qu'ils sortent du cadre de cette brève revue, de nombreux autres facteurs génétiques et processus biologiques ont été récemment liés à la pathogenèse de la PAD 29 , y compris ceux de la première vague d'études d'association pangénomique spécifiques à la PAD 10 et d'études épigénétiques.
Les modifications du microbiote intestinal associées à la maladie (dysbiose), et éventuellement à leurs métabolites bioactifs, ont également été associées à des maladies cardiovasculaires, notamment la MAP.
Les différences raciales dans la prévalence de l’AOMI qui persistent même après l’ajustement des facteurs de risque traditionnels suggèrent une biologie supplémentaire, qui n’a pas encore été découverte, notamment des différences possibles dans le potentiel thrombogène, les profils lipoprotéiques, la propension au vieillissement vasculaire ou l’état sous-jacent d’inflammation.
Une meilleure compréhension de ces processus permettra de mieux comprendre les causes profondes de l’AOMI, de nous apprendre en quoi elle diffère des autres formes de maladies vasculaires et d’étoffer notre arsenal thérapeutique croissant, comme indiqué ci-dessous.
CIBLES DE TRAITEMENT ÉTABLIE ET ÉMERGENTE POUR L'AOMI
La prise en charge médicale conventionnelle de l'AOMI comprend la réduction du cholestérol, le traitement antiplaquettaire, l'anticoagulation, les vasodilatateurs périphériques, le contrôle de la tension artérielle, la thérapie par l'exercice et l'arrêt du tabac.
La réduction des LDL, généralement grâce à l'utilisation de statines à haute intensité, est le pilier du traitement et produit des effets bénéfiques sur les taux d'amputation et les complications systémiques liées à l'AOMI.
Inverser l’état prothrombotique de l’AOMI est un autre objectif majeur, en particulier à la lumière des résultats frappants des études COMPASS (Cardiovascular Outcomes for People Using Anticoagulation Strategies) et VOYAGER PAD (Vascular Outcomes Study of ASA [acetylsalicylic acid] Along With Rivaroxaban in Endovascular or Revascularisation chirurgicale des membres pour les essais de MAP [maladie artérielle périphérique]). Ces essais ont démontré que le rivaroxaban à faible dose réduisait de manière significative les événements indésirables majeurs au niveau des membres et les événements cardiovasculaires indésirables majeurs lorsqu'il était ajouté à l'aspirine chez les patients atteints d'AOMI et présentait un bénéfice comparable à celui des statines.
L'orientation vers des exercices supervisés réduit la claudication et l'arrêt du tabac prévient l'amputation.
Ces thérapies et d'autres thérapies approuvées peuvent améliorer la qualité et la durée de vie des patients atteints d'AOMI ; Cependant, notre domaine continue d'être en proie à des problèmes de sous-diagnostic, de faible participation des minorités raciales aux essais cliniques et de sous-utilisation des médicaments, en partie à cause de perceptions d'une efficacité modeste. En conséquence, il existe un besoin majeur non satisfait d’élargir le portefeuille de thérapies pour la MAP, comme en témoignent les objectifs résumés ci-dessous.
Thérapies émergentes
Réduction hyperagressive des LDL et ciblage de cibles lipidiques émergentes telles que la lipoprotéine (a)
L'evolocumab, un anticorps monoclonal ciblant PCSK9 (proprotéine convertase subtilisine/kexine 9), qui réduit plus puissamment les LDL que les statines, semble avoir un effet démesuré sur les personnes atteintes de MAP. Dans l'essai FOURIER (Further Cardiovascular Outcomes Research With PCSK9 Inhibition in Subjects With Elevated Risk), l'évolocumab a induit une réduction du risque absolu de 3,5 % dans le critère d'évaluation cardiovasculaire principal chez les patients atteints d'AOMI (contre seulement une réduction du risque absolu de 1,6 % chez les patients sans PAD), tout en induisant également une réduction de 42 % des événements indésirables majeurs au niveau des membres. Dans l'essai ODYSSEY OUTCOMES, un autre inhibiteur de PCSK9, l'alirocumab, a également réduit le risque d'événements d'MAP (ischémie critique d'un membre, revascularisation d'un membre ou amputation pour ischémie non planifiée au moment de la randomisation). 37 En plus d'une réduction remarquable des LDL, les inhibiteurs de PCSK9 ont également un impact modeste sur la Lp(a). Il est possible que cela explique en partie le bénéfice démesuré chez les patients atteints de MAP, étant donné le lien génétique émergent entre la Lp(a) et la MAP. Les résultats des prochains essais antisens spécifiques à la Lp(a) seront suivis avec intérêt par la communauté de la médecine vasculaire, tout comme les études sur les thérapies émergentes qui abaissent puissamment le cholestérol résiduel, comme les inhibiteurs d'Angptl3 (angiopoietin-like 3) et d'ApoC3 (apolipoprotéine C3).
Médicaments antithrombotiques
Bien que les agents antiplaquettaires tels que l'aspirine ou le clopidogrel restent la pierre angulaire du traitement, des agents plus récents et plus puissants ont récemment été développés.
L'un de ces agents est le vorapaxar, un inhibiteur du PAR-1, qui diminue l'ischémie aiguë des membres mais augmente les saignements majeurs et les hémorragies intracrâniennes chez les personnes ayant des antécédents d'accident vasculaire cérébral.
Bien que les inhibiteurs du facteur Xa à faible dose apportent un bénéfice clinique net sans augmenter les hémorragies mortelles, ils induisent des taux de saignement plus élevés, ce qui indique un besoin non satisfait dans ce domaine.
Les nouveaux inhibiteurs du facteur XI semblent avoir un profil d'innocuité beaucoup plus favorable que les autres anticoagulants 40, bien que des essais prospectifs soient nécessaires pour démontrer une efficacité équivalente dans le domaine de l'AOMI.
Réduction de l'inflammation
L’inflammation est une autre cible séduisante renforcée par les données émergentes. Il a été démontré que les anticorps dirigés contre l'IL-1[bêta] améliorent la distance de marche maximale et sans douleur dans un essai clinique randomisé.
L'essai LEADER-PAD (Low Dose Colchicine in Patients With Peripheral Artery Disease to Address Residual Vascular Risk ; https://www.clinicaltrials.gov; identifiant unique : NCT04774159) étudie l'utilisation de colchicine à faible dose, qui pourrait modifier l'activation de l'inflammasome et prévenir les événements vasculaires chez les patients présentant une MAP symptomatique. Compte tenu du rôle crucial de l’inflammation dans la MAP, d’autres cibles génétiquement validées sont à l’étude, notamment des inhibiteurs directs de l’IL-6 tels que le ziltivekimab et un large éventail d’inhibiteurs de NLRP3 à venir. Parce que l'immunosuppression systémique est un handicap de tous les médicaments anti-inflammatoires, des efforts visant à développer des nanoparticules ciblées de type « cheval de Troie » ont été lancés pour minimiser ces efforts de traduction. Cette approche a le potentiel de supprimer l’inflammation chronique, de résoudre l’efférocytose défectueuse et de produire des bénéfices plus puissants, tout en évitant une toxicité hors cible. L'utilisation d'anticorps CD47 pour restaurer une phagocytose défectueuse et induire une régression des plaques est une autre cible émergente d'intérêt dans le domaine de la médecine vasculaire.
Régénération vasculaire
Plusieurs études précliniques suggèrent que forcer la régénération vasculaire pourrait être une méthode efficace pour restaurer la perfusion et améliorer la déambulation dans la MAP. Bien que l’efficacité de thérapies cellulaires prometteuses n’ait pas encore été reproduite dans des essais cliniques prospectifs randomisés, technologies émergentes en matière de cellules souches pourraient combler ces lacunes. Par exemple, les cellules souches pluripotentes induites peuvent désormais être différenciées en cellules endothéliales, et les fibroblastes peuvent être directement reprogrammés en tissu vasculaire par transdifférenciation. De plus, d’autres cibles thérapeutiques potentielles telles que le récepteur de l’IL-21, la variante d’épissage antiangiogénique VEGF165b (facteur de croissance endothélial vasculaire) et une gamme de micro-ARN et d’ARN longs non codants sont toutes à l’étude.
Agents cardiométaboliques
Enfin, de nouveaux agents cardiométaboliques pourraient jouer un rôle futur chez les patients atteints d’AOMI. Les inhibiteurs du SGLT2 (protéine de transport sodium-glucose 2) et les agonistes des récepteurs du GLP-1 (glucagon-like peptide 1) sont des médicaments contre le diabète associés à une réduction significative des événements cardiovasculaires indésirables majeurs. L'essai SELECT (Semaglutide Effects on Cardiovascular Outcomes in People With Overweight or Obesity) du sémaglutide a rapporté une amélioration des résultats cardiovasculaires chez les personnes obèses non diabétiques, ce qui suggère que ses effets vasculaires favorables ne dépendent pas strictement de la présence d'une hyperglycémie. Alors qu'une analyse post hoc de l'essai LEADER (Liraglutide Effect and Action in Diabetes: Évaluation of Cardiovascular Outcome Results) a rapporté un risque plus faible d'amputation liée à un ulcère du pied diabétique chez les patients sous liraglutide, et des études rétrospectives suggèrent une amélioration des événements indésirables majeurs liés aux membres. résultats avec les agonistes des récepteurs GLP-1, aucun essai PAD dédié n'a été mené jusqu'à présent. Il y a de l'espoir que ces médicaments passionnants puissent améliorer la qualité de vie et la capacité de marche des personnes atteintes de claudication, comme ils l'ont fait pour les patients souffrant d'insuffisance cardiaque.
CONCLUSIONS
Bien que souvent considérée comme une simple manifestation extracardiaque d’une maladie coronarienne, de nouvelles données ont identifié de nombreux aspects de l’AOMI qui la différencient des maladies vasculaires affectant d’autres lits tissulaires. Les progrès de la génétique humaine et une compréhension plus large des mécanismes moléculaires sous-jacents à l'AOMI donnent la priorité à de nouvelles cibles translationnelles qui promettent de sauver des vies et des membres. Les efforts futurs, y compris les essais spécifiquement dédiés à cette population à risque, feront progresser le domaine de la médecine vasculaire au cours du deuxième siècle de l'American Heart Association.
Commentaire
Ne pas oublier l'essentilel de la prise en charge de l'AOMI au stade de la claudication d'effort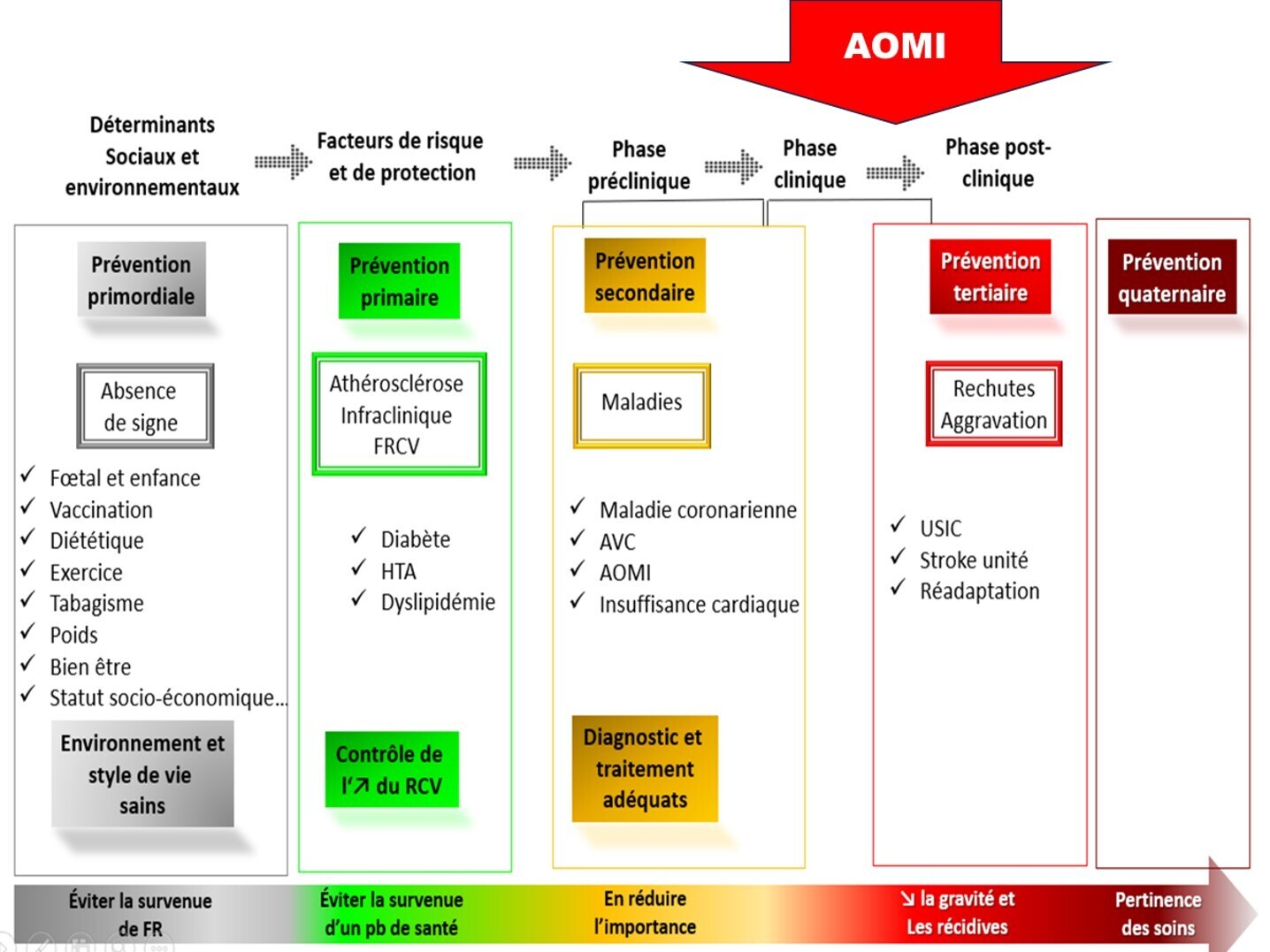
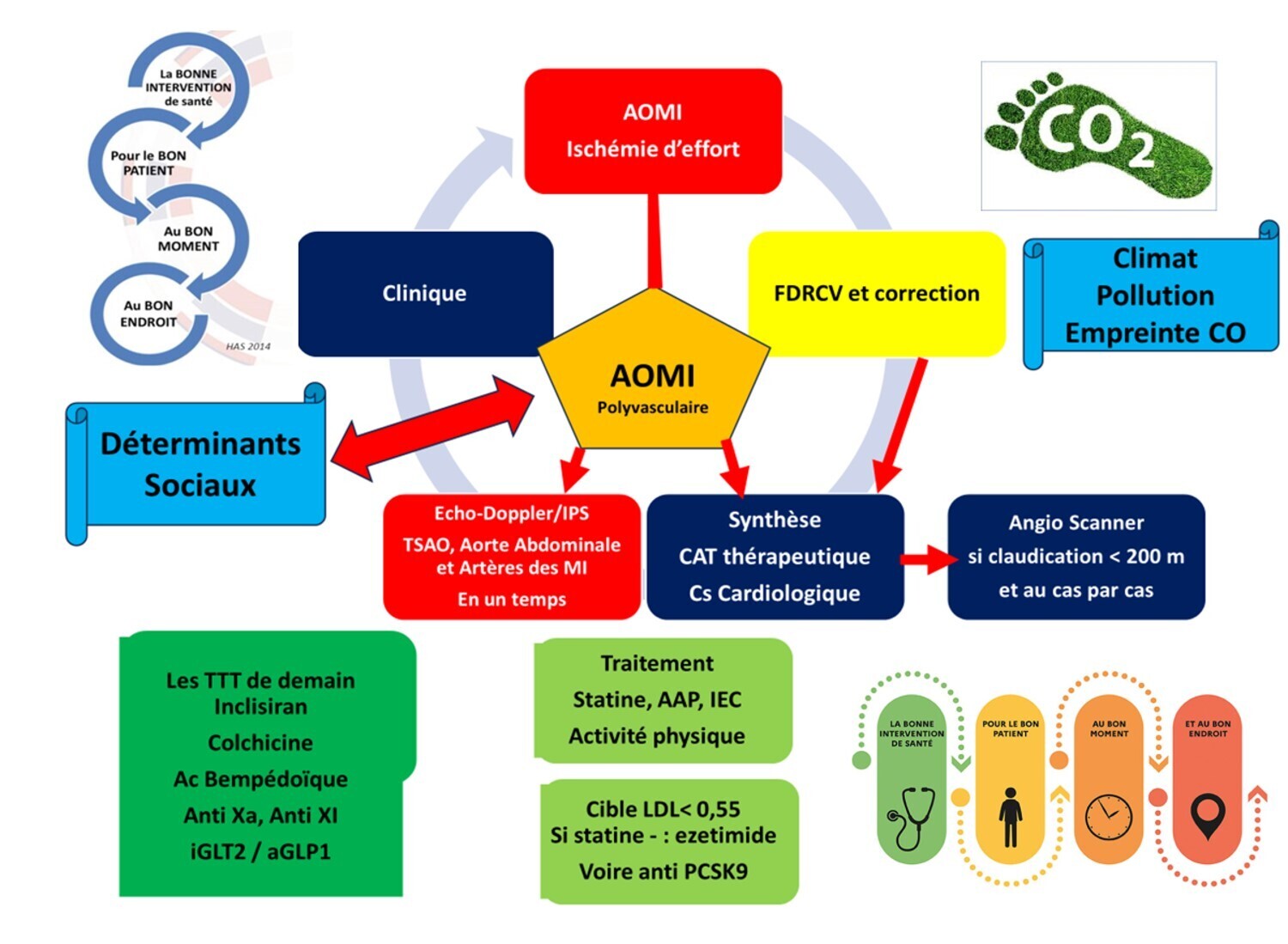 Le rôle de la Lp(a) dans l'AOMI va devenir important
Le rôle de la Lp(a) dans l'AOMI va devenir important
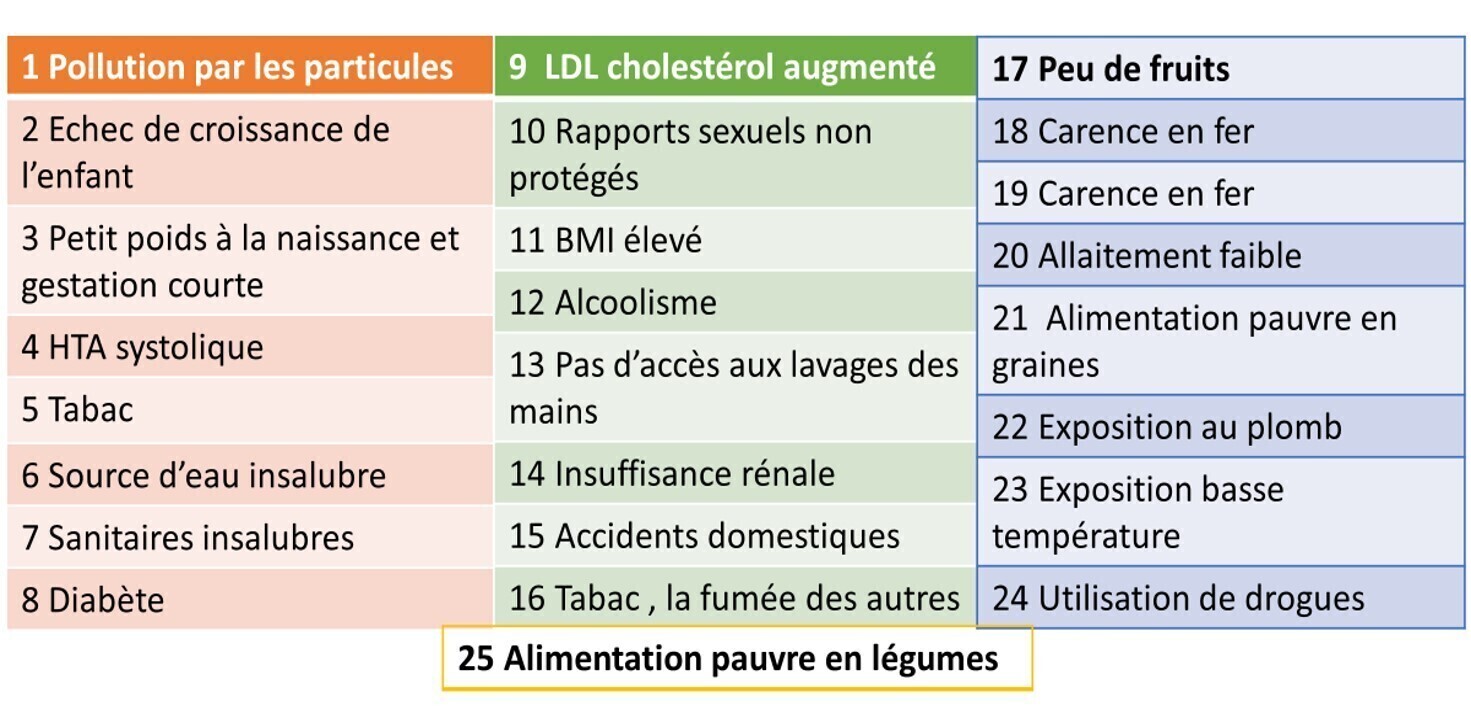 Les déterminants sociaux par ChatGPT
Les déterminants sociaux par ChatGPT"Ah, les déterminants sociaux de la santé, c'est un sujet passionnant !

En gros, ce sont tous les facteurs socio-économiques qui influencent la santé des individus et des populations.
On parle souvent de :
Le niveau de revenu et la situation économique : Plus tu es à l'aise financièrement, plus tu as accès à des soins de qualité, une alimentation saine, etc.
L'éducation : Un meilleur niveau d'éducation est souvent associé à une meilleure compréhension des comportements de santé et à un accès plus facile à l'information médicale.
L'environnement physique : Où tu vis joue un rôle énorme. Un environnement propre, sûr et sans pollution est bien meilleur pour la santé.
L'emploi et les conditions de travail : Un emploi stable et des conditions de travail décentes sont cruciaux pour le bien-être mental et physique.
Le soutien social et les réseaux communautaires : Avoir un bon réseau de soutien social peut vraiment aider à gérer le stress et les défis de la vie quotidienne.
L'accès aux services de santé : La facilité avec laquelle on peut accéder aux soins de santé est évidemment un facteur déterminant.
Les comportements individuels et les compétences en matière de santé : Les choix de vie comme l'alimentation, l'exercice, le tabagisme, etc., influencent directement la santé.
Les politiques publiques : Les lois et régulations peuvent avoir un impact énorme sur la santé publique (comme les politiques anti-tabac, par exemple).
En résumé, la santé, ce n'est pas juste une question de biologie ou de génétique. C'est une mosaïque complexe où chaque pièce a son importance"
Un programme politique en fait, chez quel parti on retrouve ces déterminants sociaux ?

