Lamperti, Massimo ; Romero, Caroline S. ; Guarracino, Fabio; Cammarota, Gianmaria; Vetrugno, Luigi; Tufegdzic, Boris ; Lozsan, Francisco ; Macias Frias, Juan José ; Douma, Andréas ; Bock, Matthias ; Rützler, Kurt ; Mulero, Silvia ; Reuter, Daniel A. ; La Via, Luigi; Rauch, Simon ; Sorbello, Massimiliano; Afshari, Arash .Évaluation préopératoire des adultes subissant une chirurgie non cardiaque élective : Lignes directrices mises à jour de la Société européenne d'anesthésiologie et de soins intensifs. Revue européenne d'anesthésiologie 42(1) : p. 1-35 janvier 2025. | DOI : 10.1097/EJA.0000000000002069
https://journals.lww.com/ejanaesthesiology/fulltext/2025/01000/preoperative_assessment_of_adults_undergoing.1.aspx
Article libre d'accès
ARRIÈRE-PLAN
Pour déterminer si un patient est apte à subir une intervention chirurgicale, une évaluation complète constitue la première étape pour l'anesthésiste. Elle permet d'évaluer les risques liés à l'intervention et les pathologies sous-jacentes du patient, et d'optimiser (dans la mesure du possible) le parcours chirurgical périopératoire. Ces recommandations de la Société européenne d'anesthésiologie et de médecine de soins intensifs (ESAIC) actualisent les recommandations précédentes et apportent de nouvelles données probantes sur des sujets existants et émergents, prenant en compte les différents aspects du parcours chirurgical du patient.
CONCEPTION
Une revue de la littérature exhaustive a porté sur l'organisation, les aspects cliniques, l'optimisation et la planification. La qualité méthodologique des études incluses a été évaluée selon la méthode GRADE (Grading of Recommendations, Assessment, Development, and Evaluation). Un processus Delphi a permis de définir la formulation des recommandations et des recommandations de pratique clinique (CPS), étayées par un minimum de preuves. Une version préliminaire des recommandations a été publiée sur le site web de l'ESAIC pendant quatre semaines, et le lien a été diffusé à tous les membres de l'ESAIC, tant individuels que nationaux, incluant la plupart des sociétés nationales d'anesthésie européennes. Les commentaires ont été recueillis et intégrés aux recommandations. Après la finalisation du projet, le comité des recommandations et le conseil d'administration de l'ESAIC ont officiellement approuvé les recommandations.
RÉSULTATS
Lors de la première phase de mise à jour des lignes directrices, 17 668 titres ont été initialement identifiés. Après suppression des doublons et restriction de la période de recherche du 1er janvier 2018 au 3 mai 2023, le nombre de titres a été réduit à 16 774, qui ont ensuite été examinés, produisant 414 résumés. Parmi ceux-ci, 267 résumés pertinents ont été identifiés, parmi lesquels 204 titres appropriés ont été sélectionnés pour une analyse GRADE complète. De plus, l'étude a pris en compte 4 revues, 16 méta-analyses, 9 lignes directrices déjà publiées, 58 études de cohorte prospectives et 83 études rétrospectives. Les lignes directrices fournissent 55 recommandations fondées sur des données probantes qui ont été votées selon un processus Delphi, atteignant un consensus solide (> 90 % d'accord).
DISCUSSION
Cette mise à jour des recommandations précédentes a abordé de nouveaux aspects organisationnels et cliniques de l'évaluation anesthésique préopératoire afin de permettre une évaluation plus objective des patients présentant un risque élevé de complications postopératoires nécessitant des soins intensifs. La télémédecine et des scores et biomarqueurs préopératoires plus prédictifs devraient guider l'anesthésiste dans le choix des analyses sanguines, radiographies, etc. préopératoires appropriées pour chaque patient, lui permettant ainsi d'évaluer les risques et de proposer le plan d'anesthésie le plus adapté.
CONCLUSION
Chaque patient doit bénéficier d'une évaluation personnalisée de son aptitude à subir des interventions nécessitant l'intervention d'un anesthésiste. Le rôle de l'anesthésiste est essentiel à cette étape pour obtenir une vision globale de l'état clinique du patient, coordonner les soins et l'aider à prendre une décision éclairée.
| Moment de l'évaluation anesthésique préopératoire |
| Quand et comment doit se dérouler l’évaluation anesthésique préopératoire ? |
| R1.1 : Nous recommandons une évaluation préopératoire précoce de l'anesthésie en ambulatoire afin de réduire les annulations le jour de l'intervention et la durée du séjour à l'hôpital. (1C) |
| R1.2 : Nous recommandons que la télémédecine et des questionnaires standardisés soient utilisés dans le cadre de l’évaluation préopératoire de l’anesthésie afin d’améliorer l’accessibilité des patients aux soins pré-anesthésiques et leur satisfaction. (1B) |
| R1.3 : Nous suggérons de réaliser un bilan préopératoire avant le jour de l’intervention, de préférence dans les 30 jours. Cependant, nous recommandons un bilan complet et actualisé par l’anesthésiste traitant dans les 48 heures précédant l’intervention. (CPS) |
| R1.4 : Nous suggérons de réaliser l'évaluation préopératoire le plus tôt possible, mais dans les 30 jours suivant l'intervention prévue pour les patients à haut risque, afin de permettre l'optimisation et l'amélioration de la condition physique du patient pour la chirurgie. (CPS) |
| Demandes de consultations préopératoires |
| Quand une consultation avec un autre spécialiste ajoute-t-elle de la valeur à l’évaluation préopératoire ? |
| R2.1 : Nous suggérons d’orienter le patient vers un spécialiste (cardiologue, pneumologue, allergologue, etc.) afin d’établir un diagnostic précis et, si l’état sous-jacent du patient peut être amélioré, de définir un calendrier et un schéma thérapeutique pour obtenir cette amélioration. Ce n’est qu’à la fin de ce processus, lorsque le patient est « optimisé », que l’anesthésiste peut prédire/estimer le risque. (CPS) |
| Qui doit coordonner les consultations des patients avec d’autres spécialistes ? |
| R2.2 : Un anesthésiste expert doit coordonner l'évaluation préopératoire impliquant une discussion en équipe multidisciplinaire si nécessaire. (CPS) |
| Évaluation cardiovasculaire |
| Quels types d’outils pourrions-nous utiliser pour évaluer le système cardiovasculaire en préopératoire ? |
| R3.1 : Nous suggérons d’utiliser le score de l’indice de risque cardiaque révisé (RCRI) dans la stratification du risque des patients préopératoires. (2C) |
| R3.2 : Lors de la prescription d'analyses sanguines préopératoires, nous suggérons d'utiliser des peptides natriurétiques comme marqueurs biologiques chez les patients à haut risque (RCRI > 2) subissant une intervention chirurgicale à haut risque. (2C) |
| R3.3 : Nous déconseillons l'utilisation des MET comme mesure subjective de la capacité fonctionnelle du patient avant toute décision médicale. L'estimation préopératoire des MET par le patient est faiblement corrélée avec les MET mesurés par l'épreuve d'effort. Néanmoins, chez certains patients, l'évaluation préopératoire des MET par le patient est utilisée comme marqueur de substitution de la performance préopératoire, même si elle ne se substitue pas aux tests cardiopulmonaires préopératoires. (1A) |
| R3.4 : Nous recommandons de combiner les peptides natriurétiques et les questionnaires Duke Activity Status Index pour évaluer la réserve cardiaque chez les patients à haut risque subissant une intervention chirurgicale à haut risque. (1C) |
| R3.5 : Nous recommandons de remplir le formulaire d'évaluation du handicap 2.0 de l'OMS chez les patients à haut risque avant la chirurgie, car cela pourrait être utile pour informer les patients des risques d'invalidité postopératoire. (1C) |
| Utilisation de l'échographie au point de service (POCUS) |
| L’échographie POCUS du cœur et des poumons devrait-elle faire partie intégrante de l’évaluation préopératoire chez tous les patients atteints d’une maladie cardiaque qui sont sur le point de subir une intervention chirurgicale à haut risque ? |
| R4.1 : Nous suggérons d'utiliser un examen POCUS ciblé du cœur et des poumons, effectué par un anesthésiste qualifié, chez les patients ayant des inquiétudes concernant une comorbidité cardiovasculaire avant une intervention chirurgicale urgente ou d'urgence pour traiter les anomalies cardiaques importantes et demander une consultation en cardiologie et déclencher une surveillance cardiovasculaire plus approfondie, mais cela ne doit pas retarder la chirurgie. (2B) |
| R4.2 : Il n’existe aucune preuve convaincante qu’un examen POCUS cardiaque ciblé préopératoire chez les patients présentant ou non une insuffisance cardiaque chronique ou une maladie coronarienne connue avant une chirurgie élective à haut risque puisse réduire la morbidité postopératoire. (2B) |
| Infection antérieure au SRAS-CoV2 (COVID-19) |
| Faut-il dépister tous les patients suspectés d’être infectés par la COVID-19 ? |
| R5.1 : Nous recommandons que les tests antigéniques préopératoires (détection de protéines spécifiques à la surface du virus SARS-CoV-2) soient effectués uniquement sur les patients symptomatiques. (1C) R5.2 : Nous recommandons de ne pas utiliser la tomodensitométrie thoracique (TDM) comme outil de dépistage pour le diagnostic du SARS-CoV-2 chez les patients asymptomatiques. (1C) |
| Les patients ayant déjà contracté la COVID-19 (quelle que soit sa gravité) mais présentant des symptômes persistants modérés ou sévères (par exemple, fatigue musculaire) doivent-ils être examinés différemment ? Qui doit coordonner les consultations des patients avec d'autres spécialistes ? |
| R5.3 : Nous suggérons que les patients hospitalisés avec un diagnostic clinico-radiologique antérieur d'infection par le SRAS-CoV-2 nécessitant une admission en unité de soins intensifs ou en unité de soins intensifs (USI) subissent une évaluation cardiorespiratoire préopératoire plus approfondie [échocardiographie, tomodensitométrie thoracique, test d'effort cardiorespiratoire (TECP)]. (CPS) |
| Évaluation des voies respiratoires |
| Quel devrait être le nombre minimum de tests requis pour une planification efficace de la gestion des voies respiratoires ? |
| R6.1 : Nous recommandons d’évaluer les voies respiratoires du patient avant toute intervention. (1C) |
| R6.2 : Nous recommandons d’effectuer plusieurs tests pour améliorer les valeurs prédictives positives et négatives de l’évaluation des voies respiratoires pré-procédurales. (1A) |
| R6.3 : Nous suggérons d’utiliser l’ensemble minimal de tests d’évaluation des voies respiratoires qui peuvent varier selon les patients en fonction de pathologies sous-jacentes spécifiques. (2C). |
| R6.4 : Pour une évaluation complète des risques, incluant les soins post-anesthésiques, l'ensemble minimal de tests d'évaluation des voies aériennes doit inclure, outre les tests anatomiques, l'évaluation de la physiologie, de l'environnement, des dispositifs et de l'expertise individuelle et de l'équipe. (1C). |
| R6.5 : Des preuves supplémentaires sont nécessaires avant que des recommandations puissent être formulées concernant la nécessité de tests instrumentaux (par exemple, échographie) pour l'évaluation des voies respiratoires. (CPS) |
| R6.6 : En cas de difficultés respiratoires prévues et antérieurement constatées, nous recommandons d'informer le patient de manière adéquate et d'obtenir son consentement pour des procédures spécifiques (par exemple, intubation éveillée), et un formulaire d'alerte doit être remis au patient en cas de procédures futures nécessitant une prise en charge des voies respiratoires. (1C) |
| Évaluation de la fonction rénale |
| Le patient présentant un dysfonctionnement rénal établi doit-il être testé avant l’opération spécifiquement pour prédire une aggravation de sa fonction rénale après l’anesthésie ? |
| R7.1 : Chez les patients atteints d'une maladie rénale chronique (MRC) connue, nous recommandons de quantifier le débit de filtration glomérulaire estimé (DFGe) et la protéinurie avant la chirurgie pour la stratification du risque concernant l'insuffisance rénale aiguë (IRA) postopératoire et l'aggravation de la MRC. (1C) |
| R7.2 : Nous suggérons d'envisager le test NT-Pro BNP combiné au DFGe pour ajouter des informations supplémentaires sur la stratification du risque de lésion rénale aiguë (IRA) postopératoire et d'aggravation de l'IRC. (2C) |
| Évaluation des troubles de la coagulation |
| Comment devons-nous gérer les patients subissant une intervention chirurgicale mineure/majeure avec des troubles de la coagulation acquis/primaires ? |
| R8.1 : Dans les interventions électives, nous suggérons que la poursuite périopératoire du traitement antithrombotique soit évaluée en fonction du risque hémorragique lié à la chirurgie, des facteurs liés au patient et du médicament antithrombotique spécifique. (2C) |
| R8.2 : Nous recommandons de poursuivre le traitement antiplaquettaire pendant 6 mois après une intervention percutanée programmée et 12 mois après une intervention coronarienne urgente. En cas d’angioplastie par ballonnet à revêtement médicamenteux, la durée de la double antiplaquettaire peut varier d’un mois minimum à 12 mois maximum, selon l’état de la maladie (stable ou instable, chronique ou aiguë), la dimension du vaisseau occlus, la présence d’une resténose intra-stent, le type de stent sténosé et le risque hémorragique. (1C) |
| R8.3 : Nous recommandons de gérer le traitement anticoagulant avant une intervention d'urgence en fonction de ses caractéristiques pharmacocinétiques, de la disponibilité de l'agent d'inversion, de la fonction rénale du patient et de la probabilité d'un saignement majeur (1A) |
| R8.4 : Nous suggérons que le risque hémorragique soit mis en balance avec le risque thrombotique pour évaluer la nécessité d’arrêter le traitement anticoagulant ou antiplaquettaire. (2C) |
| R8.5 : Nous suggérons que les patients ayant déjà subi une intervention coronarienne percutanée nécessitent une évaluation minutieuse du rapport risque-bénéfice pour gérer le traitement antiplaquettaire périopératoire. (2C) |
| R8.6 : Nous suggérons que l’évaluation préopératoire des patients subissant une chirurgie non cardiaque comprenne un programme éducatif destiné aux patients et à leurs soignants sur la gestion périopératoire de leur traitement antithrombotique. (2C) |
| R8.7 : Nous suggérons que l'évaluation périopératoire de l'état de coagulation soit mise en œuvre par thromboélastométrie et thromboélastographie chez les patients atteints de cirrhose et de coagulopathie significative, ainsi que dans un état d'hypercoagulabilité avec administration d'acide tranexamique. (2C) |
| R8.8 : Chez les patients hémophiles, un traitement guidé par la pharmacocinétique doit être mis en œuvre plutôt qu'un traitement guidé par le poids corporel réel pour garantir une atteinte périopératoire optimale de la plage de facteurs de coagulation prédéfinie. (2B) |
| R8.9 : Nous recommandons que les patients atteints d’hémophilie, de la maladie de von Willebrand et de déficit en facteur X soient pris en charge selon une approche coordonnée et multidisciplinaire. (1C) |
| Le patient à haut risque |
| Comment prendre en charge un patient à haut risque de complications postopératoires mais nécessitant une intervention à faible risque ? |
| R9.1 : Nous recommandons d’utiliser les tests de fragilité comme un outil efficace pour prédire les résultats postopératoires, en particulier pour évaluer le risque de délire. (1C) |
| R9.2 : Nous recommandons l’utilisation de l’échelle de fragilité clinique si l’examen clinique préopératoire révèle un phénotype de fragilité. Nous devrions demander une évaluation par un gériatre afin d’améliorer l’état cognitif, nutritionnel et les comorbidités en retardant l’intervention chirurgicale (intervention urgente ou élective) autant que possible. (1C) |
| R9.3 : Nous recommandons d’utiliser l’échelle de fragilité clinique en raison de sa grande faisabilité et de ses valeurs prédictives. (1C) |
| Rôle de la pré-réadaptation |
| Comment préhabiliter (kinésithérapie, nutrition) les patients à haut risque de complications postopératoires (respiratoires, cardiaques) ? |
| R10.1 : Le rôle de la pré-réadaptation devrait être établi chez les patients ayant subi une chirurgie non cardiaque. (2B) |
| R10.2 : Un soutien nutritionnel avant la chirurgie doit être envisagé chez les patients ayant subi une chirurgie non cardiaque. (2C) |
| Admission postopératoire à l'unité de soins intensifs (USI) |
| Tous les patients souffrant d’une maladie cardiaque préexistante et subissant une intervention chirurgicale majeure élective doivent-ils être systématiquement admis en unité de soins intensifs après l’opération ? |
| R11.1 : Nous ne recommandons pas l’admission systématique en réanimation chez les patients atteints de maladies cardiaques stables devant subir une intervention chirurgicale majeure programmée. Un accès sélectif en réanimation chez ce sous-groupe de patients, après une évaluation multidisciplinaire du rapport bénéfice/risque, pourrait être plus approprié. (1C) |
| Utilisation d'agonistes du GLP-1 et d'inhibiteurs du SGLT2 |
| L’utilisation d’agonistes du GLP-1 ou d’inhibiteurs du SGLT2 modifie-t-elle la prise en charge périopératoire des patients subissant des interventions nécessitant une sédation/anesthésie ? |
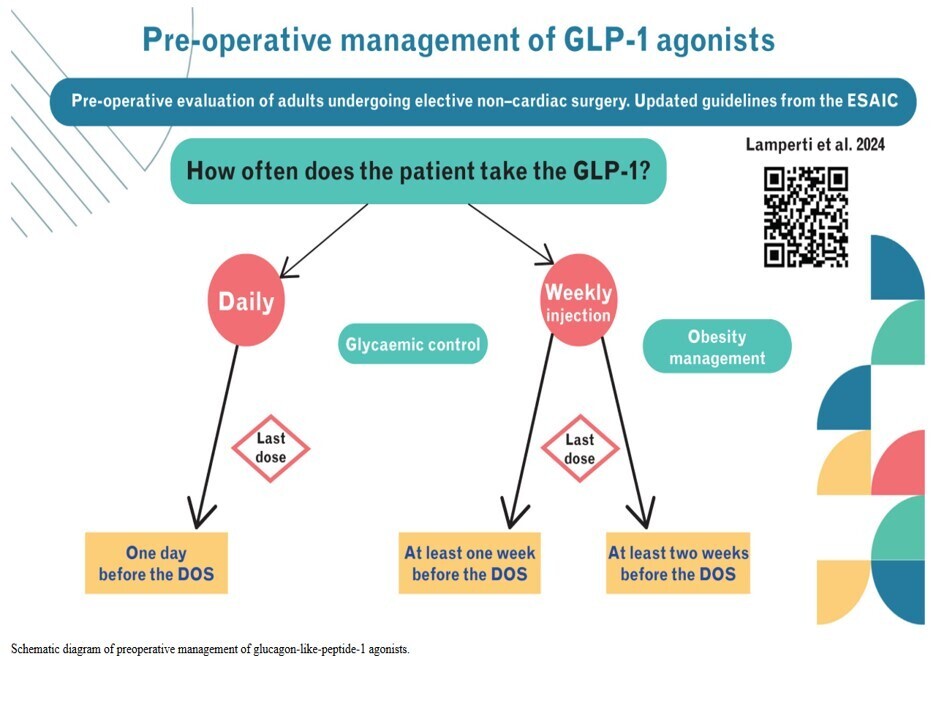
| R12.1 : Lorsqu’un agoniste du GLP-1 est prescrit en injection hebdomadaire et compte tenu de la longue demi-vie des agonistes du GLP-1, nous recommandons de suspendre le traitement au moins une semaine avant une intervention nécessitant une sédation/anesthésie. Si ces médicaments sont administrés pour traiter l’obésité, un délai de deux semaines (trois demi-vies) est recommandé. (CPS) |
| R12.2 : Si le médicament est prescrit en administration quotidienne par voie orale ou sous-cutanée, nous recommandons de suspendre les agonistes du GLP-1 le jour de l'intervention. (CPS) |
| R12.3 : Il n’existe aucune preuve démontrant que l’arrêt de ces médicaments, même une semaine avant l’intervention, éliminerait le risque de retard de la vidange gastrique, malgré le respect du jeûne habituel pour l’intervention chirurgicale. (CPS) |
| R12.4 : Un régime liquide clair pendant 24 heures avant toute intervention doit être envisagé chez les patients prenant des agonistes du GLP-1. (CPS) |
| R12.5 : Tous les patients prenant des agonistes du GLP-1 doivent être considérés comme présentant un risque d'avoir l'estomac plein malgré l'absence de symptômes gastro-intestinaux. (CPS) |
| R12.6 : Dans la mesure du possible, une échographie gastrique doit être réalisée. Si l’échographie révèle un contenu gastrique présentant un risque élevé d’aspiration, le patient doit être informé de ce risque avant de décider de procéder à une sédation ou une anesthésie générale. (CPS) |
| R12.7 : Si l'intervention est d'une telle urgence qu'un report n'est pas souhaitable, une intubation endotrachéale par induction/intubation à séquence rapide est conseillée. (CPS) |
| R12.8 : Les inhibiteurs du SGLT2 (SGLT2i) doivent être suspendus pendant 3 à 4 jours avant les interventions électives afin de réduire le risque d’acidocétose diabétique euglycémique. (CPS) |
| R12.9 : Les patients prenant des médicaments SGLT2i doivent consommer des liquides clairs environ 2 heures avant l'intervention pour maintenir une hydratation régulière. (CPS) |
| R12.10 : Une acidocétose diabétique euglycémique doit être suspectée chez cette catégorie de patients, et le dosage du β-hydroxybutyrate sanguin est un test de confirmation fonctionnel. (CPS) |
| R12.11 : Si un patient prenant des médicaments SGLT2i n'a pas arrêté le traitement à temps, la déshydratation causée par la préparation intestinale pour l'endoscopie peut augmenter les niveaux de cétones, et le patient doit être correctement hydraté avant de quitter l'hôpital. (CPS) |
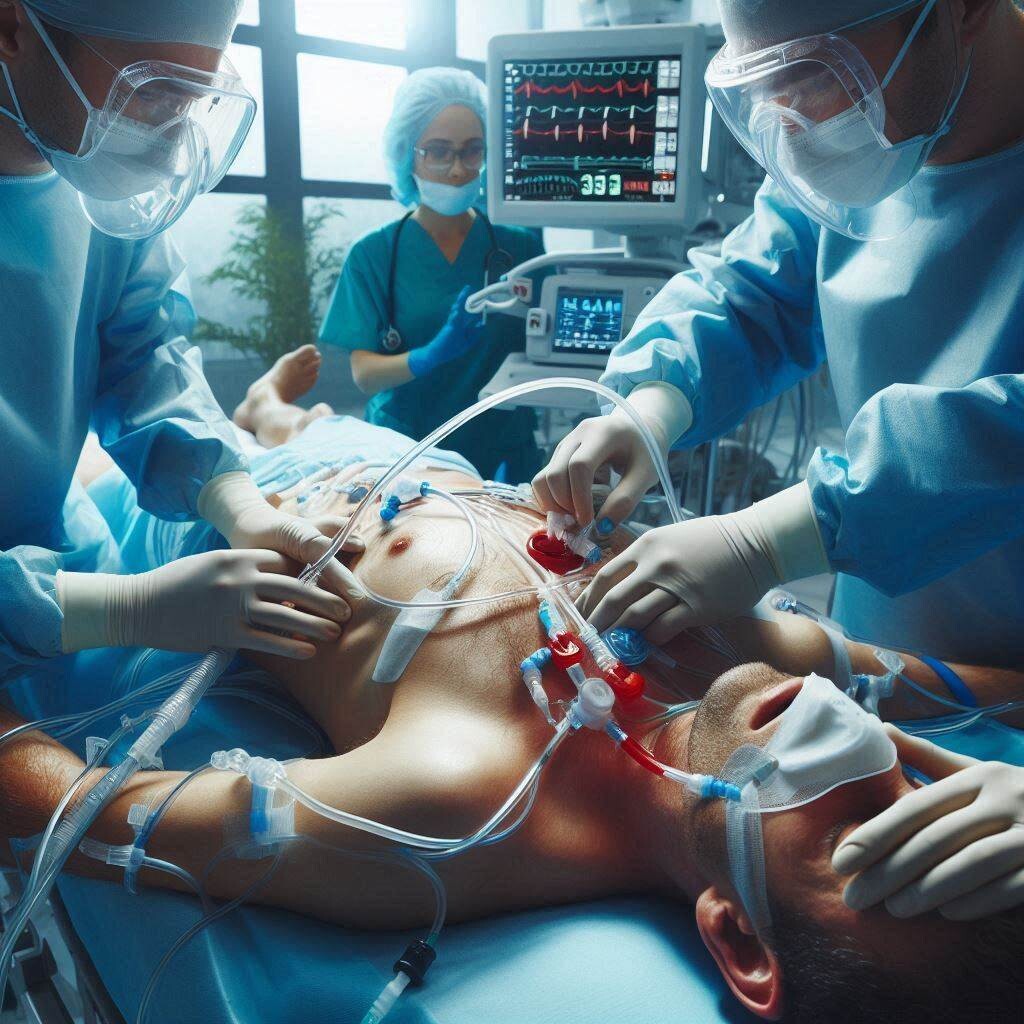
Conduite à tenir



Remarques finales
Les recommandations actuelles abordent de nouveaux sujets, non abordés dans la version 20181, et visent à fournir des conseils pratiques aux anesthésistes évaluant les patients devant bénéficier d'une sédation ou d'une anesthésie générale pour une neurochirurgie. Nous avons décidé d'inclure non seulement l'aspect organisationnel et l'évaluation clinique selon un schéma basé sur l'organe et la pathologie, mais aussi l'optimisation de la prise en charge des patients avant l'intervention chirurgicale, la planification de la prise en charge des nouveaux médicaments et la planification de l'admission postopératoire en réanimation dans un contexte de ressources limitées dans nos unités de soins intensifs.
Ces recommandations ne constituent pas une revue systématique de la littérature. Elles constituent néanmoins des recommandations fondées sur des données probantes, basées sur le système GRADE, et destinées à tous les médecins européens et internationaux, sur la manière de prodiguer les meilleurs soins lors de ce processus d'évaluation. L'évaluation préopératoire vise non seulement à évaluer l'aptitude clinique du patient à une intervention spécifique, mais aussi à inclure une discussion approfondie, avec le patient ou son entourage, sur les risques spécifiques et adaptés.
La période périopératoire n'est pas la période présentant le risque de décès le plus élevé pour de nombreux patients chirurgicaux. Selon une étude de cohorte prospective portant sur 40 000 patients âgés de 45 ans et plus ayant subi une NCS en milieu hospitalier dans 28 centres de 14 pays, 1,8 % sont décédés dans les 30 jours suivant l'intervention. Seuls cinq décès (0,7 %) sont survenus au bloc opératoire et le reste (99,3 %) est survenu après l'intervention ; 500 décès (69,9 %) sont survenus après l'intervention chirurgicale lors de l'admission initiale à l'hôpital et 210 décès (29,4 %) sont survenus après la sortie de l'hôpital. Trois complications ont représenté 44,9 % des décès : une hémorragie majeure, une lésion myocardique après NCS et une septicémie. Compte tenu de ces résultats, se concentrer sur la prévention, l'identification précoce et la prise en charge de ces trois complications est prometteur pour réduire la mortalité périopératoire. Cela se produirait principalement si nous avions une meilleure compréhension de l’état de nos patients avant l’opération et si nous planifiions quand et comment nous devrions tester les patients et optimiser leur état de santé.
Notre rôle en tant que médecins périopératoires est de fournir une évaluation des risques claire, compréhensible et applicable par les patients, afin qu'ils puissent utiliser ces informations pour prendre une décision éclairée sur les options de prise en charge anesthésique. L'évaluation anesthésique préopératoire est un élément essentiel du parcours chirurgical du patient, dont il a été démontré qu'elle réduit son anxiété .
Cette recommandation a abordé de nouveaux aspects de l'évaluation préopératoire, tels que la fragilité et l'infection antérieure ou actuelle par la COVID-19. La fragilité en soi se traduit par une diminution de la résistance au stress, notamment à l'agression chirurgicale. Il est donc primordial de réaliser un dépistage préopératoire de la fragilité et d'adopter une approche multidisciplinaire chez le patient âgé afin d'éviter le délire postopératoire et le déclin neurocognitif. Les données actuelles sur l'effet à long terme du SARS-CoV-2 ne sont pas encore suffisantes pour établir des protocoles clairs sur la manière d'évaluer les séquelles pulmonaires, cardiaques et neurologiques de cette maladie. Cependant, les vastes études rétrospectives menées sur des patients présentant des symptômes modérés suffisent à nous faire mieux comprendre le délai à partir duquel la chirurgie et l'anesthésie pourraient être considérées comme suffisamment sûres pour être entreprises.
Ce groupe de travail propose également un algorithme clinique pour les agonistes du GLP-1, mais cela nécessite davantage de données : nous espérons qu'il pourrait confirmer notre évaluation prudente de la vidange gastrique et les recommandations associées sur le jeûne préopératoire.
Ces lignes directrices mettent en œuvre et actualisent certains aspects abordés précédemment. Cependant, d'autres sujets, tels que la douleur chronique préexistante, les patients atteints de troubles neurologiques préexistants et la prise en charge des patients porteurs de pompes intradermiques continues à insuline, n'ont pas été abordés et seront inclus ultérieurement. L'objectif principal de ce document est de guider les sociétés nationales et les comités institutionnels sur la manière de mener l'évaluation préopératoire et de planifier la prise en charge ultérieure afin d'obtenir un meilleur résultat pour nos patients.
Nous continuerons à fournir les meilleures données probantes et à mettre à jour ce document rapidement ou dès que de meilleures données probantes seront disponibles.
Commentaire : texte complet et innovant, il est d'emblée applicable dans la "VRAIE VIE"
Copyright : Dr Jean Pierre Laroche / 2025

