"L'incertitude augmente la tension mais entretient l'excitation de l'espoir." Betty Mahmoody
« Plus forte est la tension, plus grand est le risque » John Welton Fischer en 1915
Desai AS, Webb DJ, Taubel J, Casey S, Cheng Y, Robbie GJ, Foster D, Huang SA, Rhyee S, Sweetser MT, Bakris GL. Zilebesiran, an RNA Interference Therapeutic Agent for Hypertension. N Engl J Med. 2023 Jul 20;389(3):228-238. doi: 10.1056/NEJMoa2208391. PMID: 37467498.
Zilebesiran, un agent thérapeutique d'interférence d'ARN pour l'hypertension
"Zilebesiran, an RNA Interference Therapeutic Agent for Hypertension"
Contexte
L'angiotensinogène est le seul précurseur des peptides de l'angiotensine et joue un rôle clé dans la pathogenèse de l'hypertension. Le zilebesiran, un agent thérapeutique expérimental d'interférence ARN avec une durée d'action prolongée, inhibe la synthèse hépatique de l'angiotensinogène.
L'angiotensinogène est le seul précurseur des peptides de l'angiotensine et joue un rôle clé dans la pathogenèse de l'hypertension. Le zilebesiran, un agent thérapeutique expérimental d'interférence ARN avec une durée d'action prolongée, inhibe la synthèse hépatique de l'angiotensinogène.
Méthodes
Dans cette étude de phase 1, les patients souffrant d'hypertension ont été répartis au hasard selon un rapport 2:1 pour recevoir soit une dose sous-cutanée ascendante unique de zilebesiran (10, 25, 50, 100, 200, 400 ou 800 mg) soit un placebo et ont été suivis pendant 24 semaines (Partie A). La partie B a évalué l'effet de la dose de 800 mg de zilebésiran sur la pression artérielle dans des conditions de régime pauvre ou riche en sel, et la partie E l'effet de cette dose lorsqu'elle est administrée en concomitance avec l'irbésartan. Les critères d'évaluation comprenaient l'innocuité, les caractéristiques pharmacocinétiques et pharmacodynamiques, et le changement par rapport au départ de la pression artérielle systolique et diastolique, tel que mesuré par la surveillance ambulatoire de la pression artérielle sur 24 heures.
Dans cette étude de phase 1, les patients souffrant d'hypertension ont été répartis au hasard selon un rapport 2:1 pour recevoir soit une dose sous-cutanée ascendante unique de zilebesiran (10, 25, 50, 100, 200, 400 ou 800 mg) soit un placebo et ont été suivis pendant 24 semaines (Partie A). La partie B a évalué l'effet de la dose de 800 mg de zilebésiran sur la pression artérielle dans des conditions de régime pauvre ou riche en sel, et la partie E l'effet de cette dose lorsqu'elle est administrée en concomitance avec l'irbésartan. Les critères d'évaluation comprenaient l'innocuité, les caractéristiques pharmacocinétiques et pharmacodynamiques, et le changement par rapport au départ de la pression artérielle systolique et diastolique, tel que mesuré par la surveillance ambulatoire de la pression artérielle sur 24 heures.
Résultats:
Sur 107 patients inscrits, 5 ont eu des réactions légères et transitoires au site d'injection. Aucun cas d'hypotension, d'hyperkaliémie ou d'aggravation de la fonction rénale ayant entraîné une intervention médicale n'a été signalé. Dans la partie A, les patients recevant du zilebesiran présentaient des diminutions des taux sériques d'angiotensinogène qui étaient corrélées à la dose administrée (r = -0,56 à la semaine 8 ; intervalle de confiance à 95 %, -0,69 à -0,39). Des doses uniques de zilebesiran (≥ 200 mg) ont été associées à des diminutions de la pression artérielle systolique (> 10 mm Hg) et de la pression artérielle diastolique (> 5 mm Hg) à la semaine 8 ; ces changements étaient constants tout au long du cycle diurne et se sont maintenus à 24 semaines. Les résultats des parties B et E étaient cohérents avec l'atténuation de l'effet sur la pression artérielle par un régime riche en sel et avec un effet accru par la co-administration avec l'irbésartan, respectivement.
Sur 107 patients inscrits, 5 ont eu des réactions légères et transitoires au site d'injection. Aucun cas d'hypotension, d'hyperkaliémie ou d'aggravation de la fonction rénale ayant entraîné une intervention médicale n'a été signalé. Dans la partie A, les patients recevant du zilebesiran présentaient des diminutions des taux sériques d'angiotensinogène qui étaient corrélées à la dose administrée (r = -0,56 à la semaine 8 ; intervalle de confiance à 95 %, -0,69 à -0,39). Des doses uniques de zilebesiran (≥ 200 mg) ont été associées à des diminutions de la pression artérielle systolique (> 10 mm Hg) et de la pression artérielle diastolique (> 5 mm Hg) à la semaine 8 ; ces changements étaient constants tout au long du cycle diurne et se sont maintenus à 24 semaines. Les résultats des parties B et E étaient cohérents avec l'atténuation de l'effet sur la pression artérielle par un régime riche en sel et avec un effet accru par la co-administration avec l'irbésartan, respectivement.
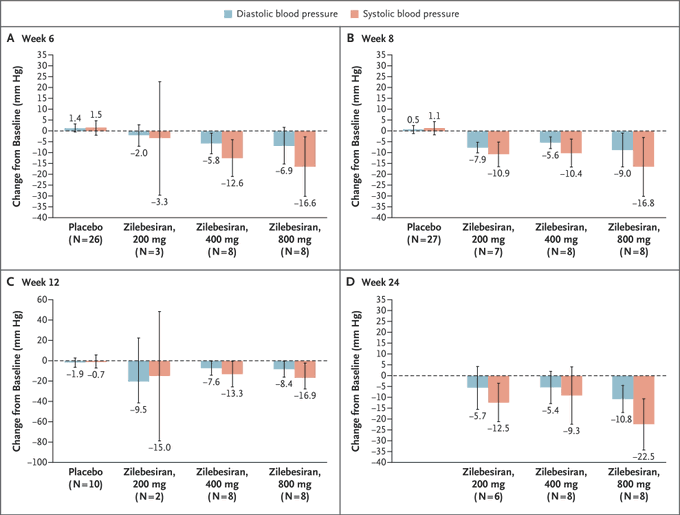
Diminutions de la pression artérielle systolique et diastolique après des doses uniques de Zilebesiran dans la partie A. Les graphiques illustrent le changement moyen par rapport au départ de la pression artérielle systolique et diastolique, tel qu'évalué par la surveillance ambulatoire de la pression artérielle, à la semaine 6 (groupe A), à la semaine 8 (groupe B), à la semaine 12 (groupe C) et à la semaine 24 (groupe D) après l'administration de doses uniques de zilébésiran dans la partie A. Les patients ont été répartis au hasard pour recevoir une seule dose sous-cutanée croissante de zilébésiran (10, 25, 50, 100 , 200, 400 ou 800 mg) ou un placebo ; les données sont présentées pour les doses de 200 mg, 400 mg et 800 mg de zilebesiran et de placebo. Dans tous les panels, les barres 𝙸 représentent des intervalles de confiance à 95 %. Les pressions artérielles systolique et diastolique moyennes initiales étaient les suivantes : placebo, 140,6 et 87,9 mm Hg ; 200 mg de zilébésiran, 138,4 et 83,3 mm Hg ; 400 mg de zilébésiran, 140,4 et 88,3 mm Hg ; et 800 mg de zilébésiran, 145,8 et 87,1 mm Hg. Au cours de l'étude, un traitement antihypertenseur d'appoint était autorisé à la discrétion de l'investigateur pour l'hypertension sévère (définie comme une pression artérielle systolique > 160 mm Hg et une augmentation de > 10 mm Hg par rapport à la pression artérielle systolique moyenne initiale qui persiste pendant ≥ 24 heures ou qui s'accompagne de symptômes hypertensifs). Un patient du groupe 200 mg a reçu un traitement antihypertenseur complémentaire avant la semaine 8. Après la semaine 8, un traitement antihypertenseur complémentaire était autorisé à la discrétion de l'investigateur pour l'hypertension non contrôlée (définie comme une pression artérielle systolique ≥ 180 mm Hg). Les patients recevant le placebo n'étaient pas tenus d'entrer dans la période de suivi prolongé (après la semaine 12). Deux patients du groupe 200 mg, un patient du groupe 400 mg et deux patients du groupe 800 mg ont reçu un traitement antihypertenseur complémentaire.
Conclusions
Les diminutions dose-dépendantes des taux sériques d'angiotensinogène et de la pression artérielle ambulatoire sur 24 heures ont été maintenues jusqu'à 24 semaines après une dose sous-cutanée unique de zilébésiran de 200 mg ou plus ; de légères réactions au site d'injection ont été observées. (Financé par Alnylam Pharmaceuticals ; numéro ClinicalTrials.gov, NCT03934307 ; numéro EudraCT, 2019-000129-39.).
 Dans cette étude, une dose unique de zilebesiran a entraîné des diminutions dose-dépendantes des taux sériques d'angiotensinogène et de la pression artérielle ambulatoire sur 24 heures, qui se sont maintenues jusqu'à 24 semaines. De légères réactions au site d'injection ont été observées. Le zilebesiran fait l'objet d'une évaluation plus approfondie en tant que traitement potentiel de l'hypertension dans deux études de phase 2 : KARDIA-1 (numéro ClinicalTrials.gov, NCT04936035. s'ouvre dans un nouvel onglet) et KARDIA-2 ( NCT05103332. s'ouvre dans un nouvel onglet).
Dans cette étude, une dose unique de zilebesiran a entraîné des diminutions dose-dépendantes des taux sériques d'angiotensinogène et de la pression artérielle ambulatoire sur 24 heures, qui se sont maintenues jusqu'à 24 semaines. De légères réactions au site d'injection ont été observées. Le zilebesiran fait l'objet d'une évaluation plus approfondie en tant que traitement potentiel de l'hypertension dans deux études de phase 2 : KARDIA-1 (numéro ClinicalTrials.gov, NCT04936035. s'ouvre dans un nouvel onglet) et KARDIA-2 ( NCT05103332. s'ouvre dans un nouvel onglet).
"« Les données publiées dans le NEJM sont indicatives du potentiel de zileberisan en tant que traitement efficace et fortement différencié, susceptible d'aider les personnes souffrant d'hypertension à bénéficier d'un contrôle durable de la tension », estime Simon Fox, Ph.D., vice-président et directeur du programme Zilebesiran chez Alnylam. « Dans cette optique, nous évaluons actuellement l'efficacité et l'innocuité de zilebesiran dans notre programme clinique de phase 2 KARDIA, soit en monothérapie (KARDIA-1) ou en bithérapie avec un médicament antihypertenseur standard (KARDIA-2) et nous sommes impatients de présenter les résultats de ces programmes à la mi et à la fin 2023, respectivement. »https://www.businesswire.com/news/home/20230719984564/fr/

L'avis d'une experte : Pr Gabrielle Sarlon-Bartoli
Médecine Vasculaire et Hypertension artérielle – Hôpital de la Timone : Marseille
Les diminutions dose-dépendantes des taux sériques d'angiotensinogène et de la pression artérielle ambulatoire sur 24 heures ont été maintenues jusqu'à 24 semaines après une dose sous-cutanée unique de zilébésiran de 200 mg ou plus ; de légères réactions au site d'injection ont été observées. (Financé par Alnylam Pharmaceuticals ; numéro ClinicalTrials.gov, NCT03934307 ; numéro EudraCT, 2019-000129-39.).
 Dans cette étude, une dose unique de zilebesiran a entraîné des diminutions dose-dépendantes des taux sériques d'angiotensinogène et de la pression artérielle ambulatoire sur 24 heures, qui se sont maintenues jusqu'à 24 semaines. De légères réactions au site d'injection ont été observées. Le zilebesiran fait l'objet d'une évaluation plus approfondie en tant que traitement potentiel de l'hypertension dans deux études de phase 2 : KARDIA-1 (numéro ClinicalTrials.gov, NCT04936035. s'ouvre dans un nouvel onglet) et KARDIA-2 ( NCT05103332. s'ouvre dans un nouvel onglet).
Dans cette étude, une dose unique de zilebesiran a entraîné des diminutions dose-dépendantes des taux sériques d'angiotensinogène et de la pression artérielle ambulatoire sur 24 heures, qui se sont maintenues jusqu'à 24 semaines. De légères réactions au site d'injection ont été observées. Le zilebesiran fait l'objet d'une évaluation plus approfondie en tant que traitement potentiel de l'hypertension dans deux études de phase 2 : KARDIA-1 (numéro ClinicalTrials.gov, NCT04936035. s'ouvre dans un nouvel onglet) et KARDIA-2 ( NCT05103332. s'ouvre dans un nouvel onglet)."« Les données publiées dans le NEJM sont indicatives du potentiel de zileberisan en tant que traitement efficace et fortement différencié, susceptible d'aider les personnes souffrant d'hypertension à bénéficier d'un contrôle durable de la tension », estime Simon Fox, Ph.D., vice-président et directeur du programme Zilebesiran chez Alnylam. « Dans cette optique, nous évaluons actuellement l'efficacité et l'innocuité de zilebesiran dans notre programme clinique de phase 2 KARDIA, soit en monothérapie (KARDIA-1) ou en bithérapie avec un médicament antihypertenseur standard (KARDIA-2) et nous sommes impatients de présenter les résultats de ces programmes à la mi et à la fin 2023, respectivement. »https://www.businesswire.com/news/home/20230719984564/fr/

L'avis d'une experte : Pr Gabrielle Sarlon-Bartoli
Médecine Vasculaire et Hypertension artérielle – Hôpital de la Timone : Marseille
"Pour améliorer l’observance et limiter la prise journalière de comprimés, plusieurs pistes ont été explorées ces dernières années dans différentes maladies notamment dans l’HTA : la dénervation rénale, ou les petits ARN interférents (siRNA) à très longue demi-vie."
Un nouveau siRNA thérapeutique, le zilebesiran, administré par voie sous-cutanée, a fait l'objet d'un essai de phase 1 et une publication récente dans le NEJM (DOI: 10.1056/NEJMoa2208391). Il s’agit d’un ARN double brins. L’un des brins est couplé à un sucre, la N-acétylgalactosamine (GalNAc) qui protège ces siARN très fragiles et qui se lie avec une très forte affinité au niveau hépatique. Le deuxième brin va se fixer sur une zone particulière de l’ARN pour empêcher la synthèse du peptide précurseur de l’angiotensine, l'angiotensinogène. S’en suit une suppression de la production d'angiotensine I et II puis une baisse de la pression artérielle durable.
Desai et coll. ont mené un essai de phase 1 chez des patients ≤ 65 ans avec HTA traitée ou non. 107 patients ont été inclus et randomisés avec soit du zilebesiran par voie sous cutanée (7 doses ont été testées de 10 à 800mg) soit du placebo. En termes de sécurité, il n’y avait pas de différence significative entre les groupes. 5 patients avec le zilebesiran ont eu des réactions transitoires modérées au site d’injection. En termes d’efficacité, des doses ≥ 200mg de zilebesiran ont permis une réduction dose dépendante de la PAS et de la PAD monitorées par MAPA et ceux dès la 8ème semaine (- 16.8mmHg de PAS et – 9mmHg de PAD à la dose de 800mg) jusqu’à la 24ème semaine (- 22.5 mmHg de PAS et – 10.8mmHg de PAD à la dose de 800mg). Un régime riche en sel semblait atténuer l’efficacité tensionnelle de la molécule, une prise de 300 mg d’irbesartan associée semblait augmenter l’effet de la molécule.
Si cela se confirme lors des essais de phase 2 et 3, l’effet continu du zilebesiran permettrait de réduire la prise orale de médicament et induirait moins de variabilité de la réponse tensionnelle.
Reste en suspens l’effet hypotenseur durable qui pose un problème de sécurité dans des circonstances d'hypovolémie et d'hypotension où il est nécessaire de rétablir rapidement la pression artérielle.
Des pistes sont en cours : fludrocortisone, régime riche en sel, et même la conception d’un antidote, le Reversir™ (Alnylam Pharmaceuticals), un oligonucléotide simple brin de haute affinité conjugué à de la GalNAc, complémentaire du brin de zilebesiran, et qui inhibe son effet au bout de 24 heures chez l’animal.
Reste en suspens l’effet hypotenseur durable qui pose un problème de sécurité dans des circonstances d'hypovolémie et d'hypotension où il est nécessaire de rétablir rapidement la pression artérielle.
Des pistes sont en cours : fludrocortisone, régime riche en sel, et même la conception d’un antidote, le Reversir™ (Alnylam Pharmaceuticals), un oligonucléotide simple brin de haute affinité conjugué à de la GalNAc, complémentaire du brin de zilebesiran, et qui inhibe son effet au bout de 24 heures chez l’animal.
Il est évident que cette approche de traitement injectable de longue durée d’action bien toléré semble une piste majeure pour lutter contre l’inobservance dans les maladies chroniques telle l’HTA.
MERCI Gabrielle pour ton expertise de gaande qualité et toujiurs pertinente
Commentaire
Une révolution dans le traitement de l'HTA, une dose sous cutanée efficace 24 semaines !
Commentaire
Une révolution dans le traitement de l'HTA, une dose sous cutanée efficace 24 semaines !
Il s'agit d'une étude de phase 1, attendons la suite
Les médicament retards se multiplient : antiPCSK9 actif sur 15 j, l'Inclisiran actif bientôt sur 1 an, une nouvelle insuline active sur 1 semaine ( Icodec ) etc.
On peut se poser une question, celle de l'adaptabilité dans le temps pour l'HTA ou le diabète; quid des associations avec d'autres molécules anti HTA ?
Ces nouvelles molécules disposeront-elles d'un antidote ? Est - ce utile ou non ?
Quiqu'il en soit en terme de compliance c'est gagnant gagnant comme l'est le concept de POLYPILL mais là c'est une autre histoire........ "industrielle"
Les médicament retards se multiplient : antiPCSK9 actif sur 15 j, l'Inclisiran actif bientôt sur 1 an, une nouvelle insuline active sur 1 semaine ( Icodec ) etc.
On peut se poser une question, celle de l'adaptabilité dans le temps pour l'HTA ou le diabète; quid des associations avec d'autres molécules anti HTA ?
Ces nouvelles molécules disposeront-elles d'un antidote ? Est - ce utile ou non ?
Quiqu'il en soit en terme de compliance c'est gagnant gagnant comme l'est le concept de POLYPILL mais là c'est une autre histoire........ "industrielle"

