“ Vivre et mourir sont les maillons d'une même chaîne. ” Antonio Rodriguez
Déséquilibre inflammatoire lié à la lipoprotéine (a) : un nouvel horizon pour le développement de l'athérosclérose
Curr Atheroscler Rep. 2024 Jun 15. doi: 10.1007/s11883-024-01215-5. Epub ahead of print. PMID: 38878139.https://link.springer.com/article/10.1007/s11883-024-01215-5#Tab2
Article libre d'accès
A lire ++++
Objectif
L'objectif principal de cette revue est d'explorer les rôles physiopathologiques et les implications cliniques de la lipoprotéine(a) [Lp(a)] dans le contexte de la maladie cardiovasculaire athéroscléreuse (ASCVD). Nous cherchons à comprendre comment la Lp(a) contribue à l'inflammation et à l'artériosclérose, dans le but de fournir de nouvelles informations sur les mécanismes de progression de l'ASCVD.
Résultats récents
Des recherches récentes mettent en évidence que la Lp(a) est un facteur de risque indépendant de la MCVAS. Des études montrent que la Lp(a) favorise non seulement les processus inflammatoires, mais interagit également avec divers composants cellulaires, entraînant un dysfonctionnement endothélial et une prolifération des cellules musculaires lisses.
Le double rôle de Lp(a) à la fois incitateur et, dans certaines conditions, atténuant
l'inflammation est particulièrement remarquable.
Cette revue révèle que la Lp(a) joue un rôle complexe dans le développement de la MCVAS par son implication dans les voies inflammatoires.
L'interaction entre les taux de Lp(a) et les réponses inflammatoires met en évidence son potentiel en tant que cible d'intervention thérapeutique.
Ces informations pourraient ouvrir la voie à de nouvelles approches dans la gestion et la prévention de la MCVAS, ce qui incite à poursuivre les recherches sur la Lp(a) en tant que cible thérapeutique.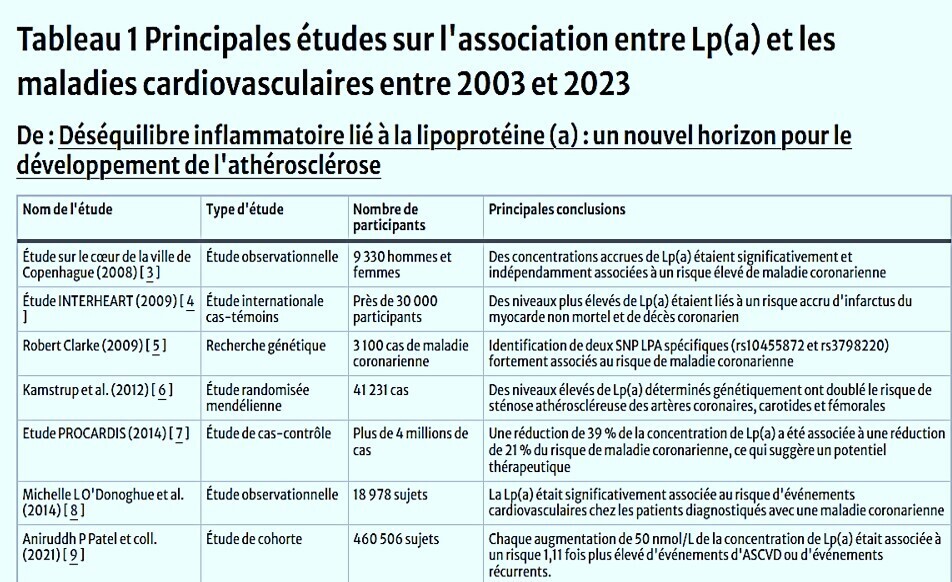
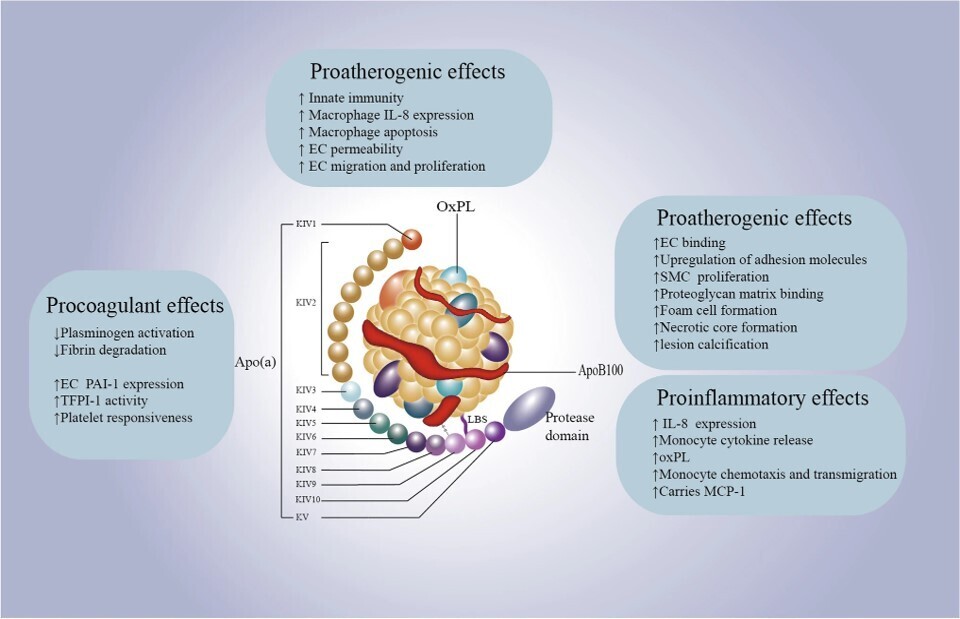
La structure et l'impact potentiel de la Lp(a) sur les processus athéroscléreux. La lipoprotéine(a) ou Lp(a) combine une particule de type LDL avec [Apo(a), liée à l'ApoB100. Sa structure unique contribue aux risques de maladies cardiovasculaires en raison de ses effets procoagulants, proinflammatoires et proathérogènes. Des niveaux élevés de Lp(a) sont associés à un risque accru d’athérosclérose et de maladie coronarienne
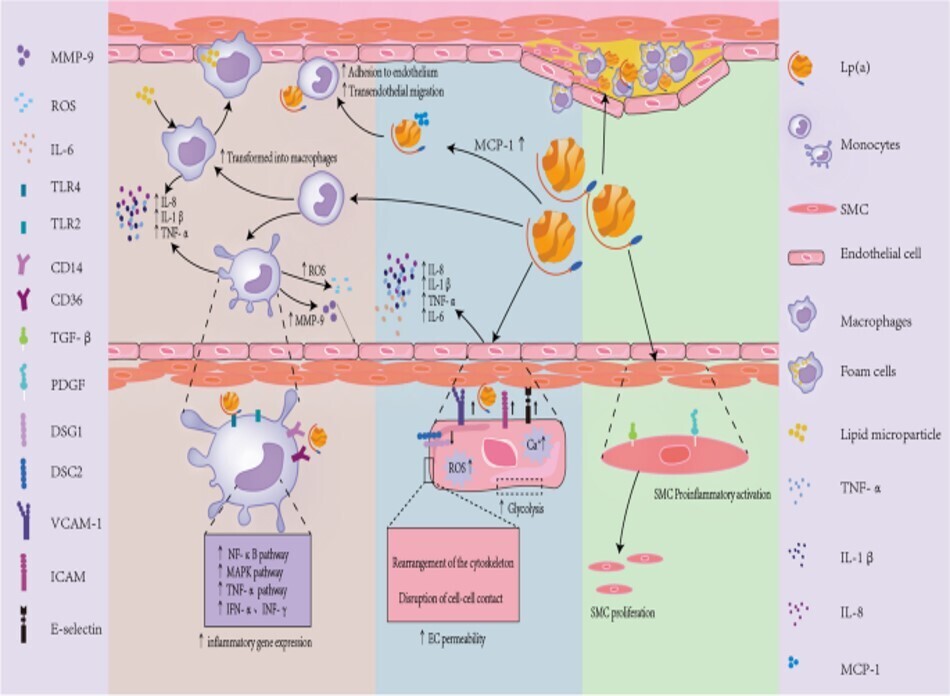
Processus d'effet inflammatoire induit par Lp(a). Les effets pro-inflammatoires de Lp(a) peuvent être largement classés en trois mécanismes principaux : l'activation des monocytes, le dysfonctionnement endothélial et la prolifération des SMC et la transformation phénotypique. (1) Effets sur les monocytes : Lp(a) se lie aux oxPL, présentant de fortes actions pro-inflammatoires. Il induit la sécrétion et la fixation de MCP-1, favorisant la migration des monocytes. De plus, Lp(a) stimule la sécrétion de CCL-1 et améliore l'expression de l'intégrine β2-Mac-1, augmentant significativement l'adhésion des monocytes aux cellules endothéliales et la migration transendothéliale, exacerbant ainsi l'inflammation de la paroi artérielle. Lp(a) régule également à la hausse l'expression des gènes inflammatoires dans les monocytes, favorisant leur différenciation en macrophages et améliorant l'absorption et le métabolisme du cholestérol, accélérant ainsi le développement et la progression de l'athérosclérose. De plus, la Lp(a) déclenche la libération d'espèces réactives de l'oxygène et de MMP-9, contribuant à l'instabilité de la plaque. Elle active également TLR2 et TLR4, ainsi que CD14 et CD36, impliquant des voies inflammatoires telles que NF-κB et favorisant la sécrétion de cytokines comme IL-8, IL-1β et TNF-α. (2) Effets sur les cellules endothéliales : La Lp(a) active les cellules endothéliales, augmentant significativement la sécrétion de molécules inflammatoires comme IL-8, IL-1β, TNF-α et IL-6, ainsi que de molécules d'adhésion telles que VCAM-1, ICAM et e-sélectines. Elle provoque un réarrangement du cytosquelette des cellules endothéliales et perturbe les jonctions d'adhésion. De plus, la Lp(a) stimule les cellules endothéliales à produire des espèces réactives de l'oxygène, diminue l'expression de DSG1 et DSC2, altérant la perméabilité des cellules endothéliales et provoquant un dysfonctionnement endothélial, ce qui peut conduire à l'autophagie des cellules endothéliales. De plus, la Lp(a) améliore la glycolyse dans les cellules endothéliales, intensifiant l'inflammation dans la paroi artérielle.(3) Effets sur les cellules musculaires lisses : la Lp(a) inhibe l'activation du TGF-β et augmente l'expression du PDGF, stimulant la prolifération des SMC et induisant une activation pro-inflammatoire des SMC. Ces mécanismes contribuent collectivement à l'environnement pro-inflammatoire associé à la Lp(a), jouant un rôle important dans le développement de l'athérosclérose et des maladies cardiovasculaires
Extraits
.....................
Bien que des niveaux élevés de Lp(a) soient reconnus comme un facteur de risque majeur de maladies cardiovasculaires, il n'existe actuellement aucun traitement ciblé pour réduire les niveaux de Lp(a) . Les efforts de recherche visant à diminuer la lipoprotéine (a) ont principalement exploré ses voies métaboliques. Bien que les statines soient cruciales pour réduire le LDL-C et prévenir les ASCVD, elles ne parviennent pas à réduire les niveaux de Lp(a) ; ils peuvent plutôt les augmenter. Une méta-analyse de 5 256 personnes a révélé que les taux de Lp(a) ont augmenté de 8,5 % à 19,6 % après 12 semaines à 2 ans de traitement par statines. Cette augmentation n'est pas bien comprise mais peut impliquer des statines améliorant l'expression de l'ARNm du LPA et de l'Apo(a) [ 80 ].
Plusieurs nouvelles classes de médicaments hypolipémiants ont montré leur potentiel pour influencer les taux plasmatiques de Lp(a). Ces médicaments offrent des stratégies plus spécifiques pour gérer les taux de Lp(a) et potentiellement réduire le risque cardiovasculaire.
Inhibiteurs de PCSK9
Des études cliniques indiquent que les inhibiteurs de PCSK9 peuvent diminuer les niveaux de Lp(a) d'environ 20 % à 30 % [ 81 , 82 ]. Plus précisément, après 48 semaines de traitement par Evolocumab, une réduction médiane de la Lp(a) de 26,9 % a été observée. Pour les patients avec des niveaux initiaux de Lp(a) supérieurs à 37 nmol/L, les inhibiteurs de PCSK9 peuvent réduire le risque d'ASCVD de 23 % . De plus, Inclisiran, le premier PCSK9siRNA, réduit les niveaux de Lp(a) d'environ 19 % à 22 % [ 84 ]. Ces données mettent en évidence que les personnes présentant des niveaux initiaux de Lp(a) élevés peuvent particulièrement bénéficier d’une réduction de Lp(a).
......................
Le pélacarsen (AKCEA-APO(a)-LRx), un nouveau médicament ciblant les taux élevés de Lp(a), est en cours de développement à l'aide de la technologie des oligonucléotides antisens pour inhiber la synthèse d'Apo(a) et réduire les concentrations de Lp(a). Des essais cliniques ont déjà montré que le pélacarsen est sûr et bien toléré, avec des réductions significatives de Lp(a) jusqu'à 72 % observées à divers dosages . De plus, l'essai de phase III HORIZON en cours vise à évaluer davantage son efficacité chez les patients atteints de maladies cardiovasculaires. Cette étude à grande échelle prévoit d'inscrire 7680 patients, assignés au hasard pour recevoir du pélacarsen ou un placebo. Le pélacarsen devrait réduire les taux de Lp(a) jusqu'à 80 %, visant à abaisser les concentrations moyennes à 20 mg/dl. Les résultats de cet essai pivot, attendus en 2024, pourraient faire du pélacarsen une nouvelle option thérapeutique pour la gestion des maladies cardiovasculaires .
Le mipomersen, une thérapie oligonucléotidique antisens, cible et réduit les lipoprotéines contenant l'apoB100, y compris la Lp(a). Un essai de phase III a montré qu'un régime de 26 semaines de 200 mg de mipomersen diminuait les niveaux de Lp(a) de 26,4 %. Malgré son efficacité, le mipomersen est associé à plusieurs effets secondaires, notamment des réactions au site d'injection, une stéatose hépatique et des enzymes hépatiques élevées.
De plus, son utilisation ne démontre aucune réduction des événements ASCVD. Par conséquent, le mipomersen est spécifiquement prescrit aux patients atteints d'hypercholestérolémie familiale....................
Conclusion
D'après les informations fournies, il est clair que la Lp(a) est une molécule structurellement complexe avec des fonctions biologiques uniques.
Elle joue un rôle important dans le processus inflammatoire par le biais de divers mécanismes, contribuant au dysfonctionnement endothélial, à l'activation des monocytes et des macrophages et à la prolifération des cellules musculaires lisses, qui favorisent tous le développement de l'AS.
Il est important de noter qu'il existe une relation bidirectionnelle complexe entre la Lp(a) et l'inflammation ; la Lp(a) peut à la fois induire et potentiellement avoir des effets anti-inflammatoires dans certaines situations.
De plus, l'inflammation peut également influencer les niveaux de Lp(a).
Les thérapies actuelles telles que les oligonucléotides antisens et les siRNA sont très prometteuses pour réduire considérablement les niveaux de Lp(a) et ne sont pas obligées d'être spécifiques à l'isoforme, compte tenu de leur mécanisme de ciblage de la synthèse d'ARN.
Par conséquent, il est crucial de rechercher les niveaux de Lp(a) et d'explorer des méthodes plus efficaces pour les réduire. Cette recherche est prometteuse pour offrir de nouvelles stratégies pour le traitement de l'athérosclérose.
Commentaire
Pas à pas nous découvrons toutes les propriétés de la Lp(a) qui devient un maillon fort de la compréhension de d'athérosclérose.
Demain des traitements appropriés devraient être très efficaces sur la Lp(a) et par là même sur l'athérosclérose.
Je ne pense que la Lp(a) soit quelque chose d'anecdotique mais c'est au contraire un élément majeur dans la connaissance de l'athérosclérose......
Nous avons encore beaucoup à découvrir de la Lp(a)
A LIRE