Eviter l'évitable
-
“Vivre sans espoir, c’est cesser de vivre.” Fiodor Dostoïevski
“L'espoir est le dernier à mourir.” Proverbe Brésilien
The Brussels International Declaration on Lipoprotein(a) Testing and Management
https://www.atherosclerosis-journal.com/article/S0021-9150(25)00116-9/fulltext
Article libre d'accès
Panneau A : Fréquence des concentrations de Lp(a) et association avec les maladies cardiovasculaires. Nous avons appliqué un facteur de conversion de 2,18∗Lp(a) en mg/dL–3,83 pour la conversion en nmol/L, comme décrit par Langsted et al. [17]).
Le panneau B présente le rapport de risque ajusté (RR) lissé et l'intervalle de confiance à 95 % (IC à 95 %) du risque à vie d'événements cardiovasculaires majeurs pour une concentration de Lp(a) donnée par rapport à la Lp(a) médiane de la population (19,7 nmol/L).
Ces données ont été estimées à l'aide d'un modèle de régression à risques proportionnels de Cox ajusté en fonction de l'âge à l'inscription, du sexe et des dix premières composantes principales de l'ascendance, puis modélisé à l'aide de splines naturelles cubiques. Cette figure est tirée de la récente déclaration de consensus de l'EAS sur la Lp(a) [4] basé sur les données de la UK Biobank et est reproduit ici sous la licence d'accès libre CC BY-NC-ND 4.0.
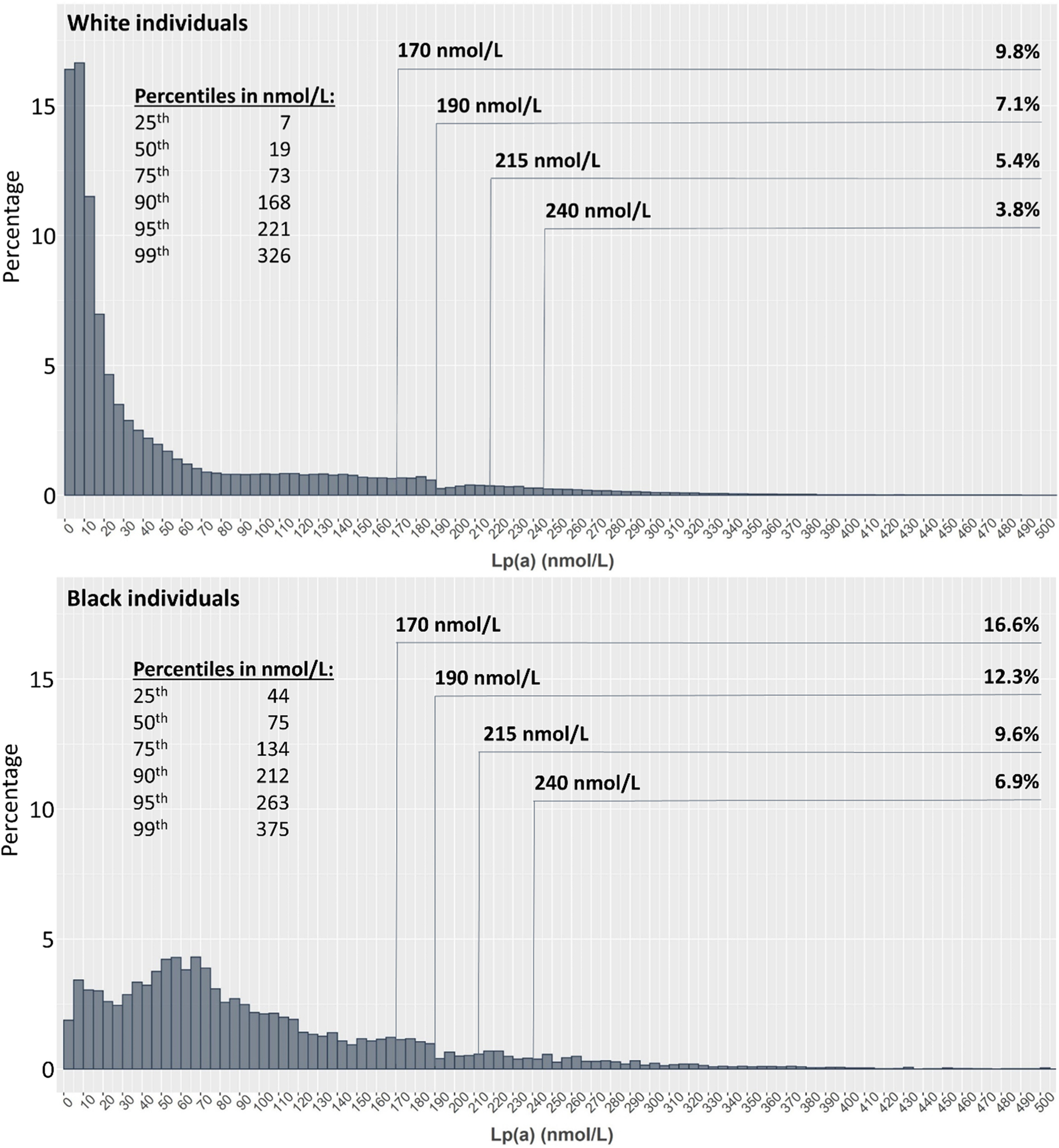
Distribution des concentrations de lipoprotéine(a) [Lp(a)] dans une population générale. Les données proviennent de la UK Biobank et montrent la distribution typique des concentrations de Lp(a) chez les personnes blanches (panneau A) et noires (panneau B) . Les pourcentages de la population présentant une concentration de Lp(a) de 170, 190, 215 et 240 nmol/L ou plus sont indiqués. Cette figure est tirée du récent consensus de l'EAS sur la Lp(a) [4] et est reproduit ici sous la licence d'accès libre CC BY-NC-ND 4.0.

Principales demandes de la Déclaration internationale de Bruxelles sur les tests et la gestion de la Lp(a) issues du Sommet mondial sur la Lp(a), tenu à Bruxelles, en Belgique, les 24 et 25 mars 2025, organisé par le groupe de travail international sur la Lp(a).
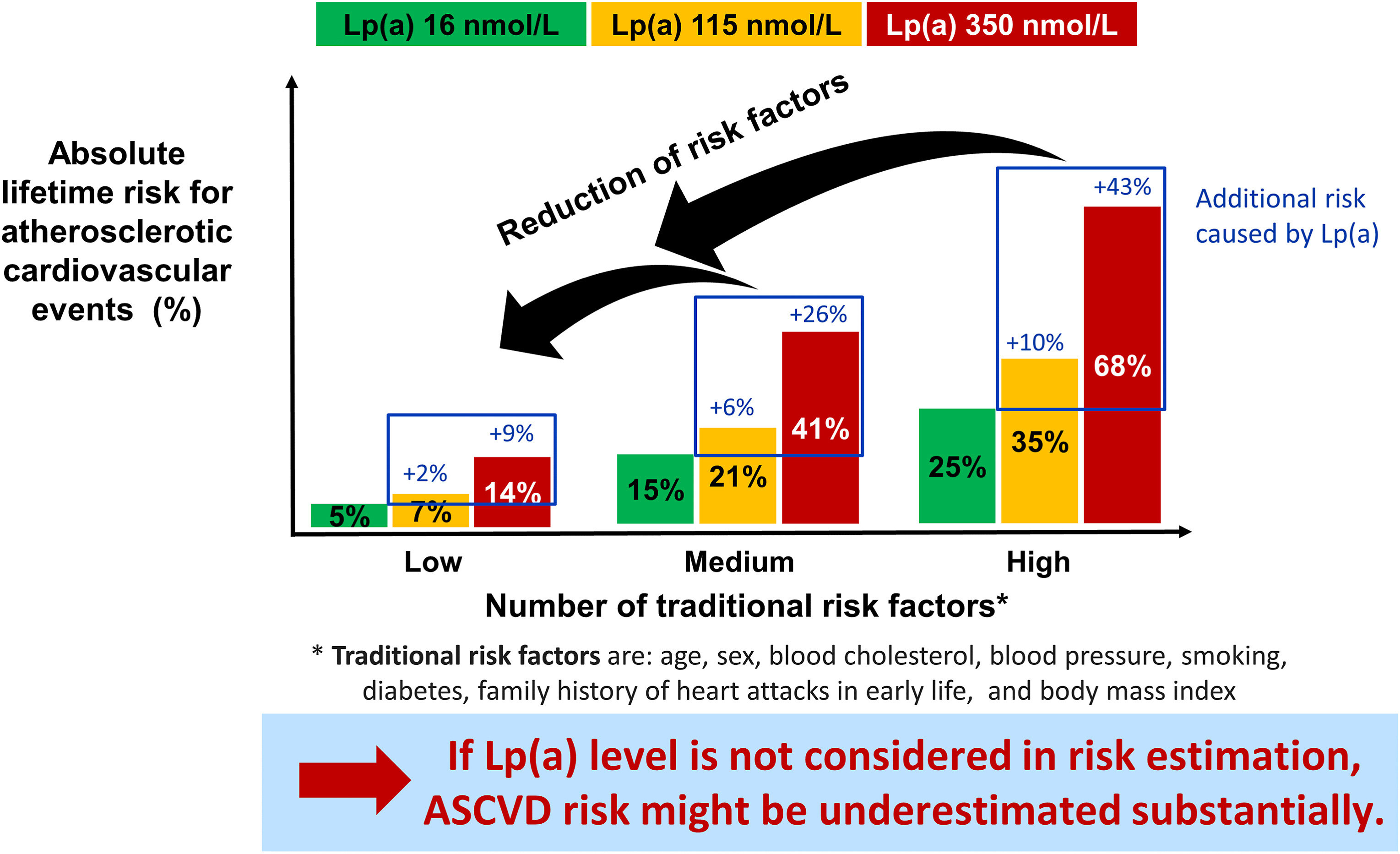
Association entre les concentrations de Lp(a) et le risque absolu de maladie cardiovasculaire athéroscléreuse au cours de la vie, stratifié selon le nombre de facteurs de risque traditionnels (modifiables). Cette figure est basée sur les calculs effectués pour la déclaration de consensus sur la Lp(a) de la Société européenne d'athérosclérose (présentée à la figure 6 ci-après).4] et présente le message principal sous une forme simplifiée. L'axe des Y montre le risque absolu estimé à vie d'événements cardiovasculaires athéroscléreux majeurs (ASCVD) parmi 415 274 participants d'ascendance européenne dans la UK Biobank. Les participants sont stratifiés en catégories de risque à vie estimé de base de 5 %, ce qui équivaut à aucun ou un faible nombre de facteurs de risque modifiables, 15 % (nombre moyen de facteurs de risque) et 25 % (nombre élevé de facteurs de risque), calculés respectivement à l'aide de l'algorithme d'estimation du risque à vie des Joint British Societies (JBS3) (basé sur les facteurs de risque traditionnels : âge, sexe, cholestérol sanguin, tension artérielle, tabagisme, diabète, antécédents familiaux de crises cardiaques en début de vie et IMC). Français Pour chacune de ces trois catégories de risque de base, le risque supplémentaire attribuable à l'augmentation des concentrations de Lp(a) de 115 nmol/L (barres jaunes) ou 350 nmol/L (barres rouges) mesurées au départ par rapport à celles dont la concentration médiane de Lp(a) est de 16 nmol/L (barres vertes) est calculé et ajouté au risque de base pour fournir le risque absolu global. Cette augmentation incrémentielle du risque causée par des concentrations de Lp(a) plus élevées de 115 nmol/L et 350 nmol/L a été estimée en ajoutant la Lp(a) comme exposition indépendante à l'algorithme d'estimation du risque JBS3. Par exemple, pour une personne ayant un risque de base de 25 % et une concentration de Lp(a) de 115 nmol/L, le risque absolu d'un événement cardiovasculaire majeur augmente de 10 %, passant de 25 % à 35 % (par rapport à une personne ayant une Lp(a) de 16 nmol/L). En cas de concentration de Lp(a) de 350 nmol/L, le risque augmente de 43 %, passant de 25 % à 68 %. La réduction des facteurs de risque traditionnels modifiables est donc l'objectif ultime en cas de concentrations élevées de Lp(a) afin de diminuer le risque global d'une personne donnée.
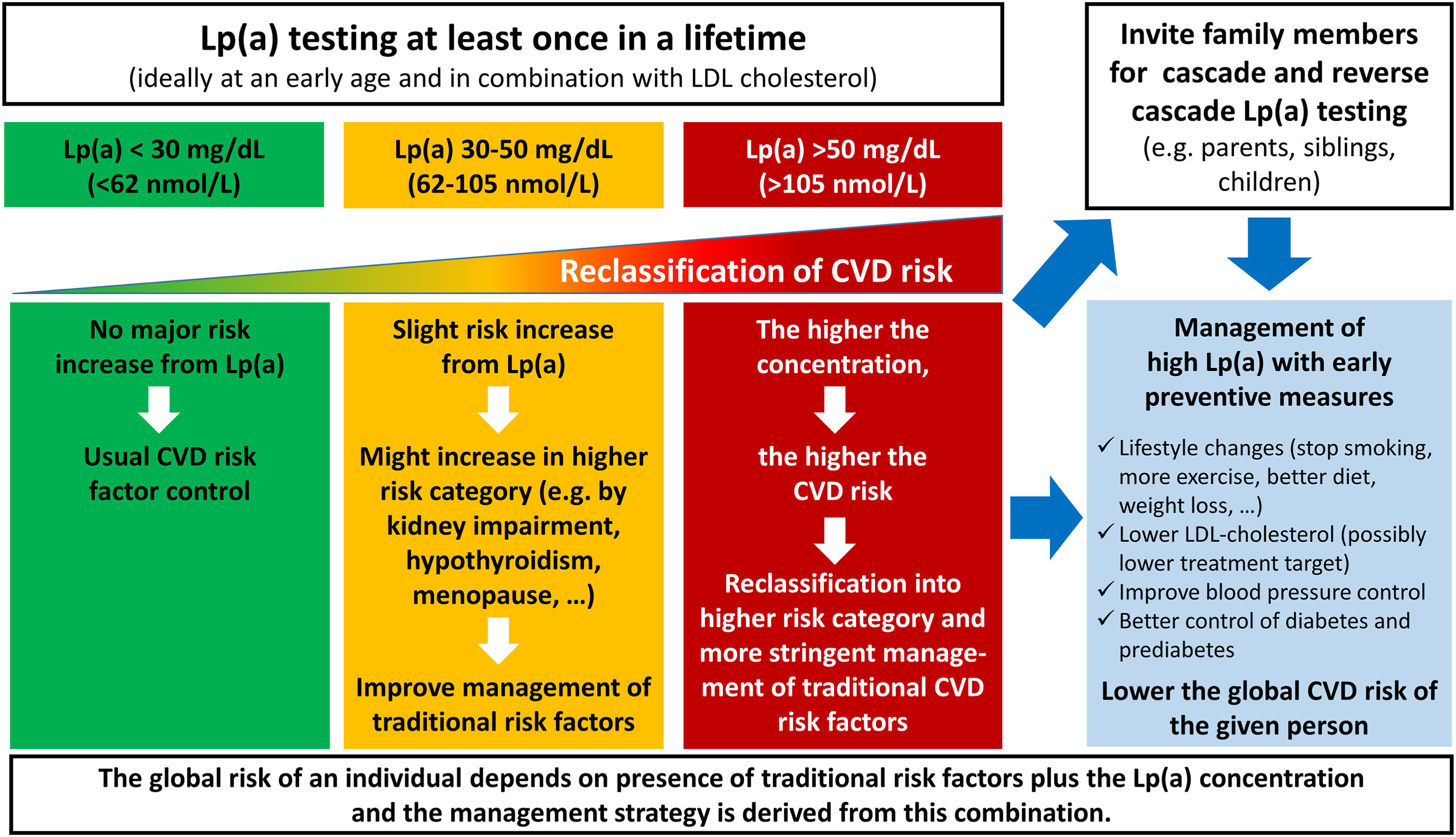
Les tests doivent être effectués dans les contextes de prévention primaire et secondaire.
Alors que les pays passent à des tests systématiques des taux élevés de Lp(a), le dépistage des individus à haut risque ne doit être considéré que comme une mesure temporaire jusqu’à ce que les tests soient largement mis en œuvre.
Une combinaison de programmes de dépistage de Lp(a) élevée et d’hypercholestérolémie familiale devrait être envisagée en fonction de l’état de préparation des systèmes de santé dans chaque pays.
Le risque cardiovasculaire des individus présentant des concentrations élevées de Lp(a) doit être reclassé dans une catégorie de risque plus élevée avec accès à une gestion appropriée de ces facteurs de risque selon un plan individualisé.
Conclusion
Cette reconnaissance, inscrite dans les conclusions du Conseil du 3 décembre 2024, signale un changement de paradigme dans le paysage politique, illustrant le consensus croissant sur la nécessité urgente de s'attaquer aux facteurs de risque de MCV génétiques et souvent sous-diagnostiqués. Elle intervient à un moment où les connaissances scientifiques, la sensibilisation du public, les nouvelles directives cliniques et la dynamique des politiques de santé s'alignent, créant une opportunité unique et sans précédent de « prévenir l'évitable ».
En intégrant la Lp(a) et l'hypercholestérolémie familiale dans les discussions stratégiques sur la détection précoce (dépistage et tests), la sensibilisation du public et la prise en charge des maladies, la Déclaration de Bruxelles ouvre la voie à une action transformatrice pour réduire le fardeau de la morbidité et de la mortalité cardiovasculaires prématurées tout en promouvant la santé cardiovasculaire pour tous. Cette évolution offre une fenêtre d’opportunité cruciale pour intégrer les données probantes dans les politiques, stimuler les investissements dans les voies de détection et de traitement et, en fin de compte, remodeler l’avenir de la prévention cardiovasculaire.
SYNTHSESE
Cet article est une déclaration internationale issue d'un sommet mondial, soulignant que la lipoprotéine(a) élevée est un facteur de risque cardiovasculaire important, indépendant et héréditaire. Malgré sa prévalence significative, le dépistage est très limité. La déclaration appelle à l'intégration du dépistage et de la gestion de la Lp(a) dans les plans de santé cardiovasculaire mondiaux et nationaux, à des investissements accrus et à des politiques de remboursement, à des tests systématiques au moins une fois dans la vie, et à l'intégration des résultats dans l'évaluation globale du risque cardiovasculaire sans discrimination. Enfin, elle insiste sur la nécessité d'une sensibilisation accrue du public et des professionnels de santé.
Un point sur les traitements à venir
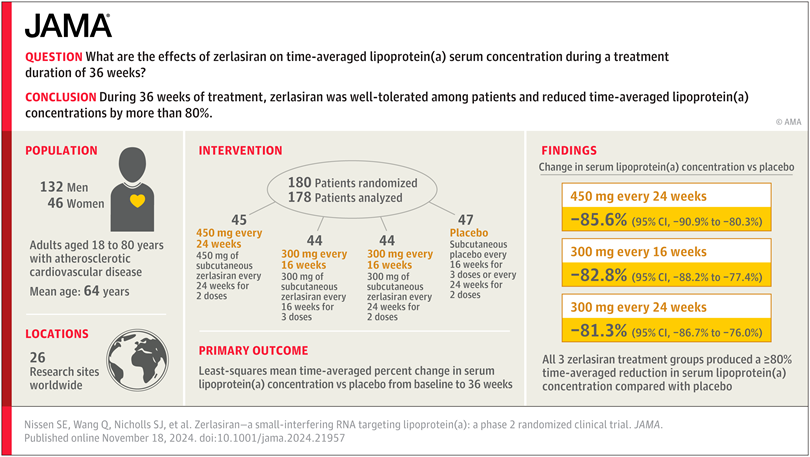
Lp(a) Une mise au point compléte
https://medvasc.info/archives-blog/lp-a-une-mise-au-point-compl%C3%A8te
COMMENTAIRE
La Lp(a), article après article fait son chemin, le chemin du "sur risque CV".
La Lp(a) est très importante pour mieux stratifier le risque CV, surtout chez les sujets à risque intermédiaire, elle permet un reclassement si elle est augmentée en sur risque CV et donc des conséquences thérapeutiques en rapport.
Ce n'est pas un nouveau "gadget médical", bien au contraire.
Lp(a) à controler en prévention CV PRIMAIRE et SECONDAIRE
Il est urgent que son dosage soit remboursé, ce n'est pas encore le cas aujourd'hui.
Attention on doit la doser qu'une fois du fait de son origine génétique.
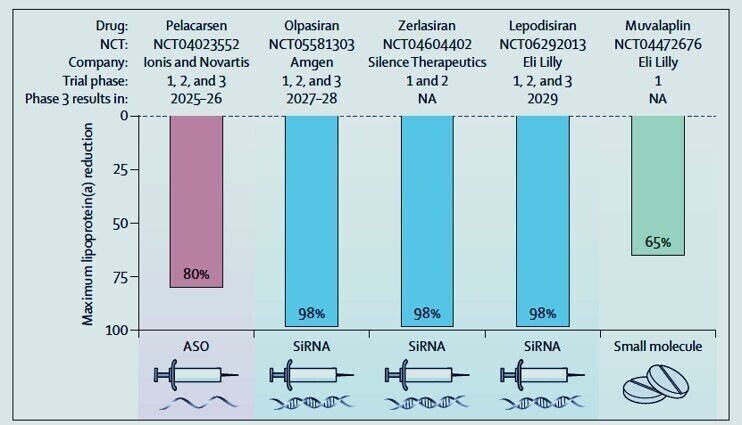
Demain des molécules adaptées et validées feront diminuer efficacement le taux de Lp(a), ce n'est qu'une question de mois......
Il faut donc intégrer la Lp(a) à la décision médicale lorsqu'il s'agit de prévention CV primaire essentiellement mais aussi secondaire
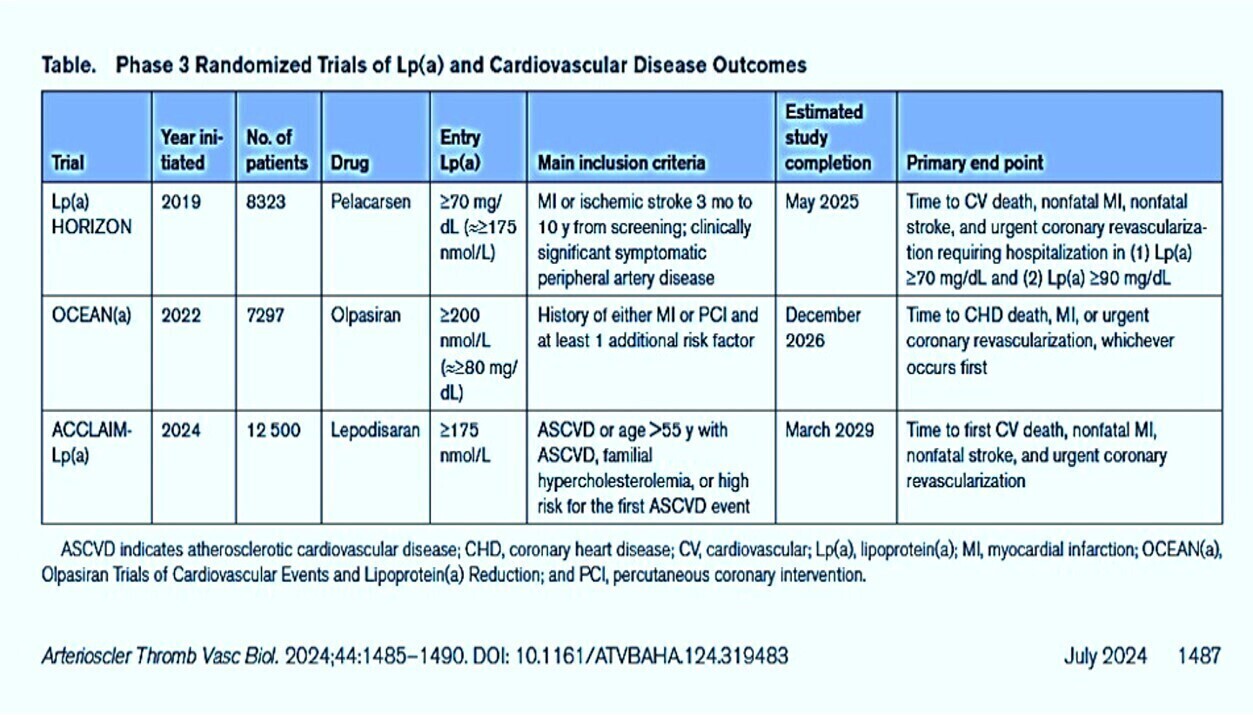
La multiplication des essais thérapeutiques pour la réduction de la Lp(a) touchent à leur fin.
Il va donc être possible enfin de réduire la Lp(a) mais quel traitement pour quel risque ?
Les traitements à venir seront ils soit "globaux" ou spécifique de tel ou tel atteinte cardiovasculaire ?
Les traitements seront ils efficaces ? Feront -ils baisser le risque CV de manière très significative, les preuves actuellement manquent cruellement actuellement,
Copyright : Dr Jean Pierre Laroche / 2025