Nouveaux , nouveaux AC
Haruki Murakami "À vrai dire, toute perception est déjà mémoire. Nous ne percevons pratiquement que le passé, le présent pur étant l’insaisissable progrès du passé rongeant l’avenir."
ARTICLE 1
Angiolillo DJ, Capodanno D. Uncoupling Thrombosis and Hemostasis by Inhibiting Factor XI. Découplage de la thrombose et de l'hémostase par inhibition du facteur XI N Engl J Med. 2025 Jan 23;392(4):400-403. doi: 10.1056/NEJMe2414209. PMID: 39842017.
https://www.nejm.org/doi/full/10.1056/NEJMe2414209
La thérapie anticoagulante est utilisée pour prévenir les événements thromboemboliques chez les patients atteints de fibrillation auriculaire, mais elle augmente le risque de saignement. Dans cette édition du Journal, Ruff* et ses collègues présentent les résultats d'une étude de phase 2b qui a évalué deux doses mensuelles d'abelacimab (un inhibiteur des facteurs XI et XIa) par rapport au rivaroxaban quotidien (un inhibiteur du facteur Xa) chez des patients atteints de fibrillation auriculaire. L'abelacimab a réduit les niveaux de facteur XI libre de 97 % et 99 % en médiane avec les doses de 90 mg et 150 mg, respectivement, après 3 mois. Comparé au rivaroxaban, l'abelacimab a diminué les saignements majeurs ou cliniquement pertinents non majeurs de 69 % et 62 % avec les doses de 90 mg et 150 mg, respectivement.
Ces résultats, associés à l'efficacité de l'abelacimab dans la prévention des événements thromboemboliques, justifient des essais à plus grande échelle
*Ruff CT, Patel SM, Giugliano RP, et al. Abelacimab versus rivaroxaban in patients with atrial fibrillation. N Engl J Med 2025; 392: 361-71.
https://medvasc.info/archives-blog/abelacimab-succ%C3%A9s
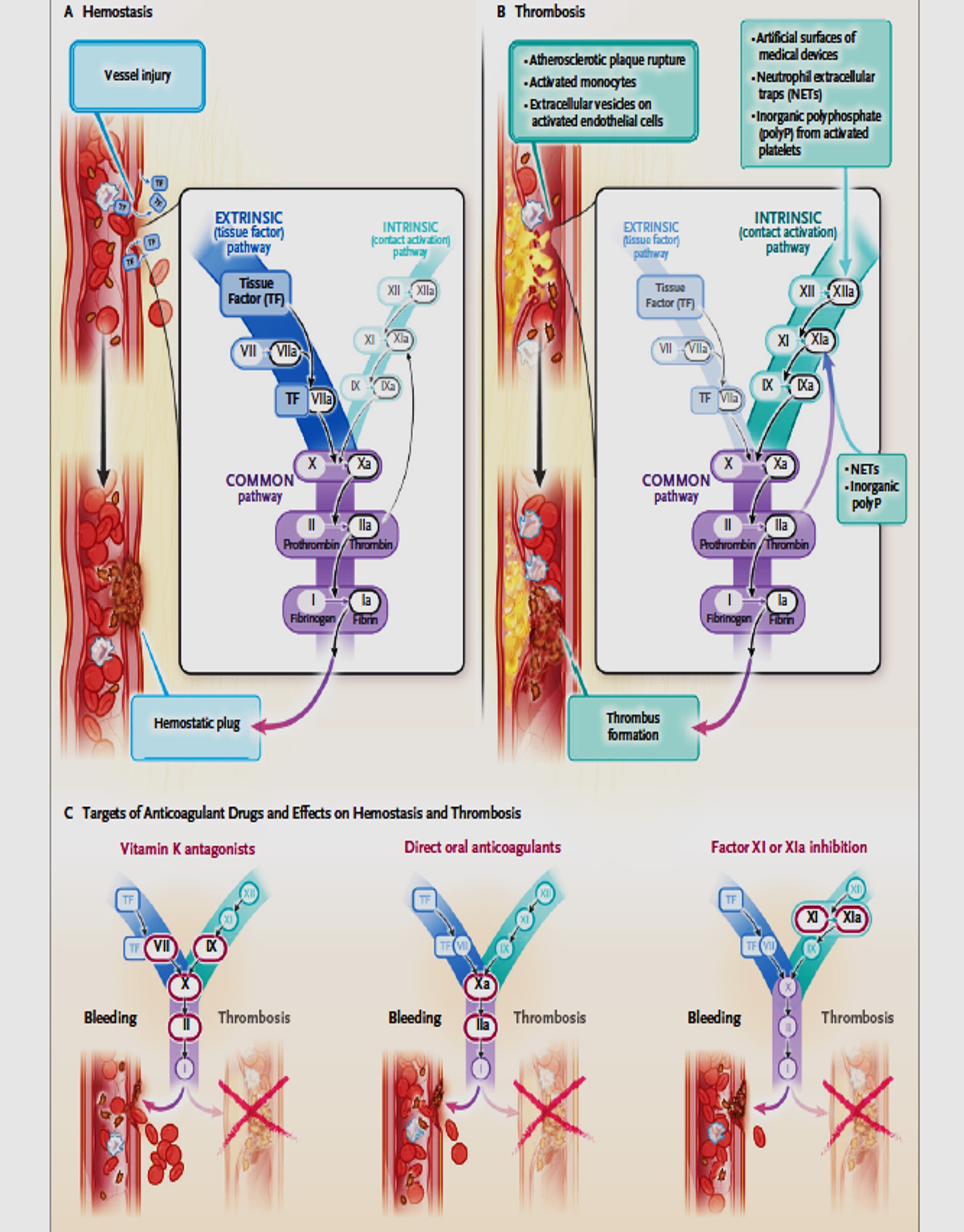
Facteur XI et découplage de la thrombose et de l'hémostase
Hémostase (Panneau A)
L'hémostase conduit à la formation d'un bouchon hémostatique qui arrête les fuites de sang d'un vaisseau endommagé. Elle est déclenchée par une lésion vasculaire, entraînant la libération de fortes concentrations de facteur tissulaire (facteur III) depuis l'adventice. Ce facteur est également exprimé et libéré par les cellules endothéliales activées, le sous-endothélium et les monocytes. Le facteur tissulaire initie une génération rapide de thrombine via la voie extrinsèque (bleu). En particulier, il se lie au facteur VIIa circulant, formant un complexe qui active le facteur X en facteur Xa. Ce dernier convertit ensuite la prothrombine en thrombine par la voie commune (violet), et la thrombine transforme le fibrinogène en fibrine, menant à la formation du bouchon hémostatique. Le complexe facteur tissulaire-facteur VIIa active aussi le facteur IX en IXa, amplifiant et maintenant la production de Xa et de thrombine pour stabiliser le bouchon hémostatique. Le facteur XII n'est pas essentiel à l'hémostase, et l'activation rétroactive du facteur XI par la thrombine a un effet limité sur cette production.
Thrombose (Panneau B)
Ces résultats, associés à l'efficacité de l'abelacimab dans la prévention des événements thromboemboliques, justifient des essais à plus grande échelle
*Ruff CT, Patel SM, Giugliano RP, et al. Abelacimab versus rivaroxaban in patients with atrial fibrillation. N Engl J Med 2025; 392: 361-71.
https://medvasc.info/archives-blog/abelacimab-succ%C3%A9s

Facteur XI et découplage de la thrombose et de l'hémostase
Hémostase (Panneau A)
L'hémostase conduit à la formation d'un bouchon hémostatique qui arrête les fuites de sang d'un vaisseau endommagé. Elle est déclenchée par une lésion vasculaire, entraînant la libération de fortes concentrations de facteur tissulaire (facteur III) depuis l'adventice. Ce facteur est également exprimé et libéré par les cellules endothéliales activées, le sous-endothélium et les monocytes. Le facteur tissulaire initie une génération rapide de thrombine via la voie extrinsèque (bleu). En particulier, il se lie au facteur VIIa circulant, formant un complexe qui active le facteur X en facteur Xa. Ce dernier convertit ensuite la prothrombine en thrombine par la voie commune (violet), et la thrombine transforme le fibrinogène en fibrine, menant à la formation du bouchon hémostatique. Le complexe facteur tissulaire-facteur VIIa active aussi le facteur IX en IXa, amplifiant et maintenant la production de Xa et de thrombine pour stabiliser le bouchon hémostatique. Le facteur XII n'est pas essentiel à l'hémostase, et l'activation rétroactive du facteur XI par la thrombine a un effet limité sur cette production.
Thrombose (Panneau B)
La thrombose est un processus intravasculaire qui entraîne la formation d'un thrombus obstruant le flux sanguin. Elle débute lorsque de faibles concentrations de facteur tissulaire dans la paroi vasculaire sont exposées au sang, par exemple après une rupture de plaque athérosclérotique ou via des monocytes activés ou des vésicules extracellulaires attachées aux cellules endothéliales activées. De petites quantités de thrombine sont générées via l'activation du facteur X par le complexe facteur tissulaire-facteur VIIa. Cependant, lorsque le thrombus s'étend au-delà du site initial de la lésion, ce complexe ne peut plus soutenir sa croissance. Le facteur XIa est alors supposé jouer un rôle clé dans l'expansion du thrombus via la voie intrinsèque (vert). Le facteur XI peut être activé par la thrombine ou le facteur XIIa, avec un rôle crucial joué par la thrombine comme activateur rétroactif du XI. Ce mécanisme est renforcé par des polyanions naturels tels que les pièges extracellulaires des neutrophiles (NETs) et les polyphosphates inorganiques libérés par les plaquettes activées, facilitant l'extension du thrombus au-delà du site initial.
Anticoagulants (Panneau C)
Les anticoagulants influencent différemment l'hémostase et la thrombose. Les antagonistes de la vitamine K inhibent les facteurs II, VII, IX et X ainsi que les protéines anticoagulantes C et S, ce qui les rend efficaces pour prévenir les thrombus mais compromet fortement l'hémostase. Les anticoagulants oraux directs inhibent soit le facteur Xa soit la thrombine (IIa), réduisant ainsi la formation de thrombus mais affectant aussi l'hémostase. Le rôle plus prononcé des facteurs XI et XIa dans la thrombose par rapport à l'hémostase en fait une cible thérapeutique prometteuse pour des anticoagulants préservant mieux l'hémostase.
ARTICLE 2
EDITORIAL de L a Revue Médicale Suisse
Recherche de l’anticoagulant idéal : beaucoup de progrès et quelques surprises. M. Righini, L. Mazzolai et P. Fontana
Rev Med Suisse 2024 ; 20 : 2263-4 | DOI : 10.53738/REVMED.2024.20.898.2263
"LA VOIE DE L’INHIBITION DU FXI EST EXTRÊMEMENT PROMETTEUSE"
Quelles sont donc les données disponibles lors de l’utilisation en clinique des inhibiteurs du facteur XI(a) ? L’essai AZALEA-TIMI 71 est la plus importante et la plus longue étude portant sur un inhibiteur du facteur XI. Plus de 1200 patients atteints de FA et présentant un risque modéré à haut d’AVC ont été traités et suivis pendant une durée médiane de 21 mois. Comparé au rivaroxaban 20 mg par voie orale, l’abelacimab 150 mg administré par voie sous-cutanée une fois par mois a permis de réduire de 67 % (p < 0,0001) le critère de jugement composite du nombre d’hémorragies majeures et d’hémorragies non majeures cliniquement relevantes. La réduction des saignements majeurs était de 74 % (p = 0,002) et celle des hémorragies gastro- intestinales de 93 % (p = 0,008).
Ces données récentes montrent donc que si la voie de l’inhibition du FXI est extrêmement prometteuse,*
Toutes les classes d’inhibiteurs et tous les différents inhibiteurs actuellement
en phase d’étude clinique ne sont probablement pas égaux en efficacité et en sécurité, et il faudra donc attendre encore quelques années avant de savoir quelles molécules"
seront disponibles en clinique."
Nonius avons mis en ligne l'essai ABELACIMAB et FA et celui de l'ASUNDEXIAN et la FA. Le premier est un succès à la fois sur la prévention des AVC en cas de FA mais surtout avec une réduction drastique du risque hémorragique L'Asundxexian est un échec
en phase d’étude clinique ne sont probablement pas égaux en efficacité et en sécurité, et il faudra donc attendre encore quelques années avant de savoir quelles molécules"
seront disponibles en clinique."
Nonius avons mis en ligne l'essai ABELACIMAB et FA et celui de l'ASUNDEXIAN et la FA. Le premier est un succès à la fois sur la prévention des AVC en cas de FA mais surtout avec une réduction drastique du risque hémorragique L'Asundxexian est un échec
Explication par nos amis suisses : "En particulier, une suppression puissante de l’activité du facteur XIa semble capitale et les données préliminaires suggèrent une inhibition du facteur XIa plus basse avec l’Asundxexian que celle de 99 % obtenue avec l’abelacimab. Une dose insuffisante pourrait donc être évoquée pour expliquer ces résultats. Des différences dans les mécanismes d’action de l’abelacimab et les petites molécules inhibitrices comme l’Asundxexian peuvent également être évoquées. En particulier, l’abelacimab est un anticorps monoclonal qui se lie à la fois au facteur XI et au facteur XIa. Par opposition, l’Asundxexian se lie uniquement au facteur XIa, ce qui pourrait être à l’origine d’une inhibition moins efficace"

Doc Pr MA Sevestre Pietri / Vasco 2024
La saga des "nouveaux nouveaux, nouveaux anticoagulants est en marche pour le plus grand bien des patients. Mieux maîtriser le risque hémorragique est un atout majeur. La forme retard de l'abelacimab est un autre atout en terme de compliance.
Reste le coût ? Wait and see
Reste les indications à venir des AntiXI/XI(a) : chez qui, cancer et MTEV ? ......
Copyright : Dr Jean Pierre Laroche / 2025

