« El que quiere interesar a los demás tiene que provocarlos. »
« Celui qui veut intéresser les autres doit les provoquer »
Salvador Dali
Gil Díaz A, Martín Guerra J, Parra Caballero P, Puche Palao G, Muñoz Rivas N, Ruiz-Giménez Arrieta N. Diagnosis and treatment of deep vein thrombosis of the lower and upper limbs. 2024 recommendations of the thromboembolic disease group of the Spanish Society of Internal Medicine.
Diagnostic et traitement des thromboses veineuses profondes des membres inférieurs et supérieurs. Recommandations 2024 du groupe des maladies thromboemboliques de la Société espagnole de médecine interne
Rev Clin Esp (Barc). 2024 Apr 17:S2254-8874(24)00051-1. doi: 10.1016/j.rceng.2024.04.004. Epub ahead of print. PMID: 38641173."La thrombose veineuse profonde (TVP) des membres est une maladie courante et entraîne une morbidité et une mortalité importantes. C'est fréquemment le prélude à une embolie pulmonaire (EP), elle peut récidiver chez 30 % des patients et dans 25 à 40 % des cas ils peuvent développer un syndrome post-thrombotique (SPT), avec un impact significatif sur l'état fonctionnel et la qualité de vie.
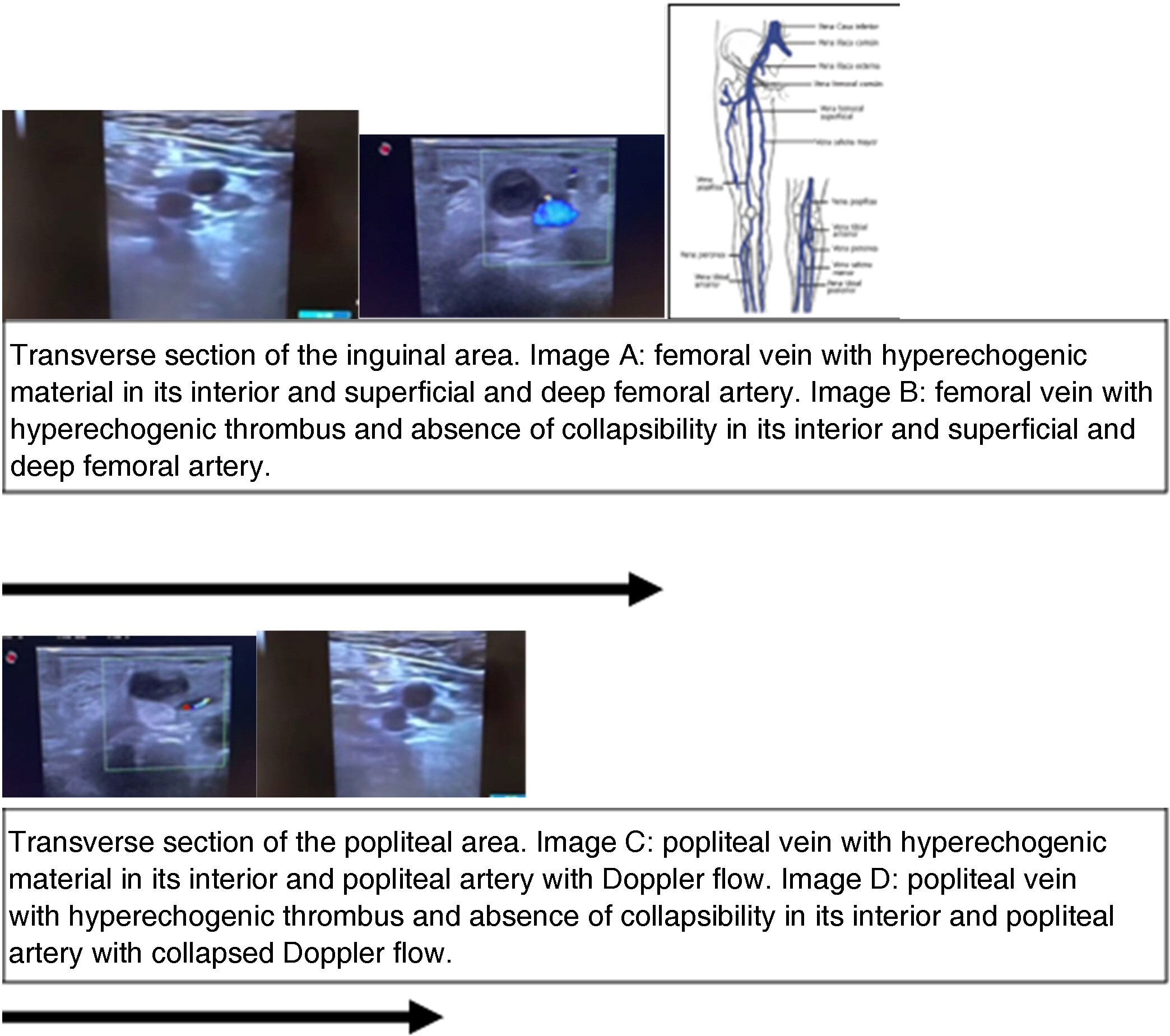 L'hémodynamique veineuse en écho-Doppler est' elle étudiés en cas de TVP ou est ce un simple test de compression ?
L'hémodynamique veineuse en écho-Doppler est' elle étudiés en cas de TVP ou est ce un simple test de compression ?Système veineux superficiel et profond des membres inférieurs.
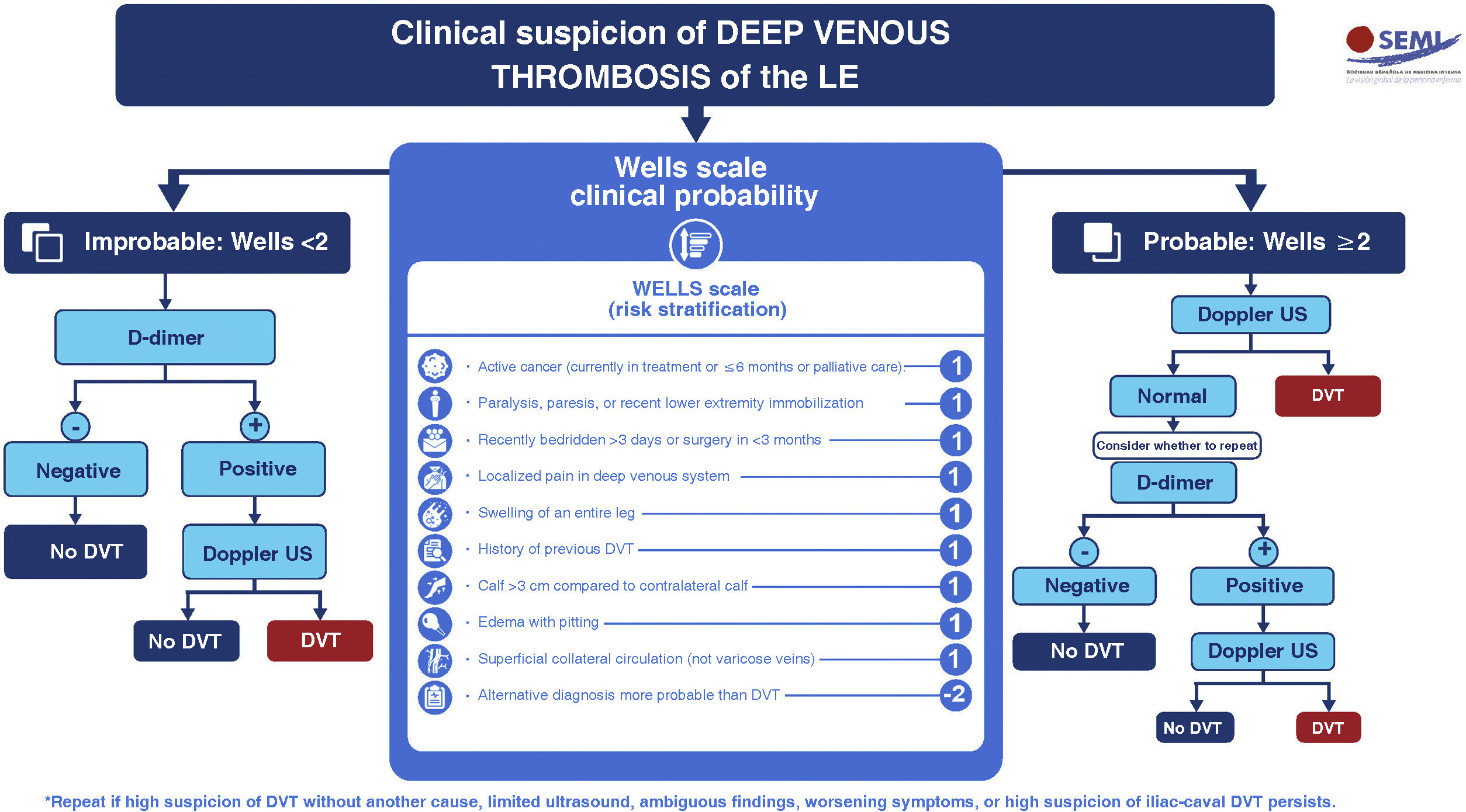
Algorithme de diagnostic de la thrombose veineuse profonde des membres inférieurs.
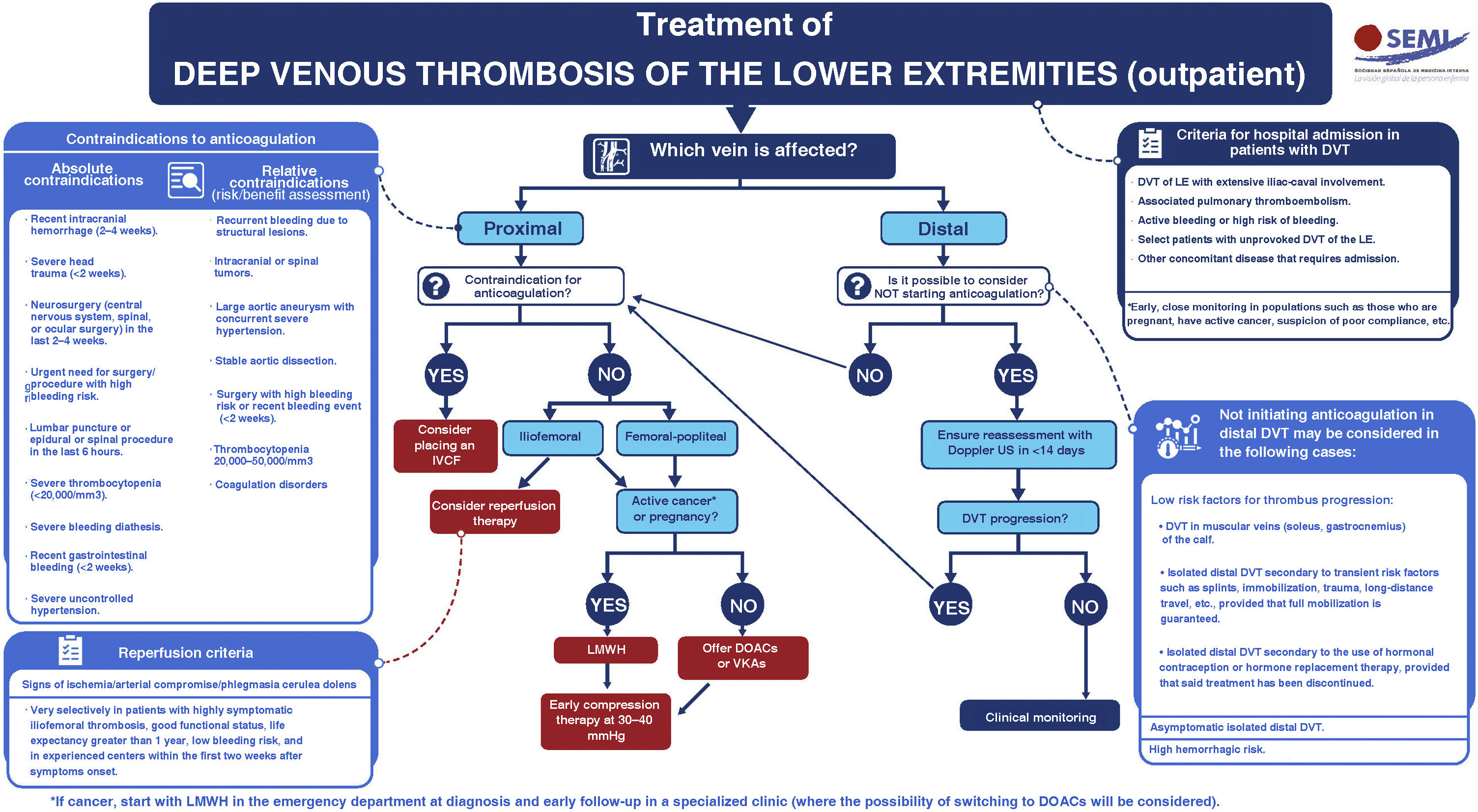
Algorithme pour la prise en charge thérapeutique des thromboses veineuses profondes du LE (M Inf)
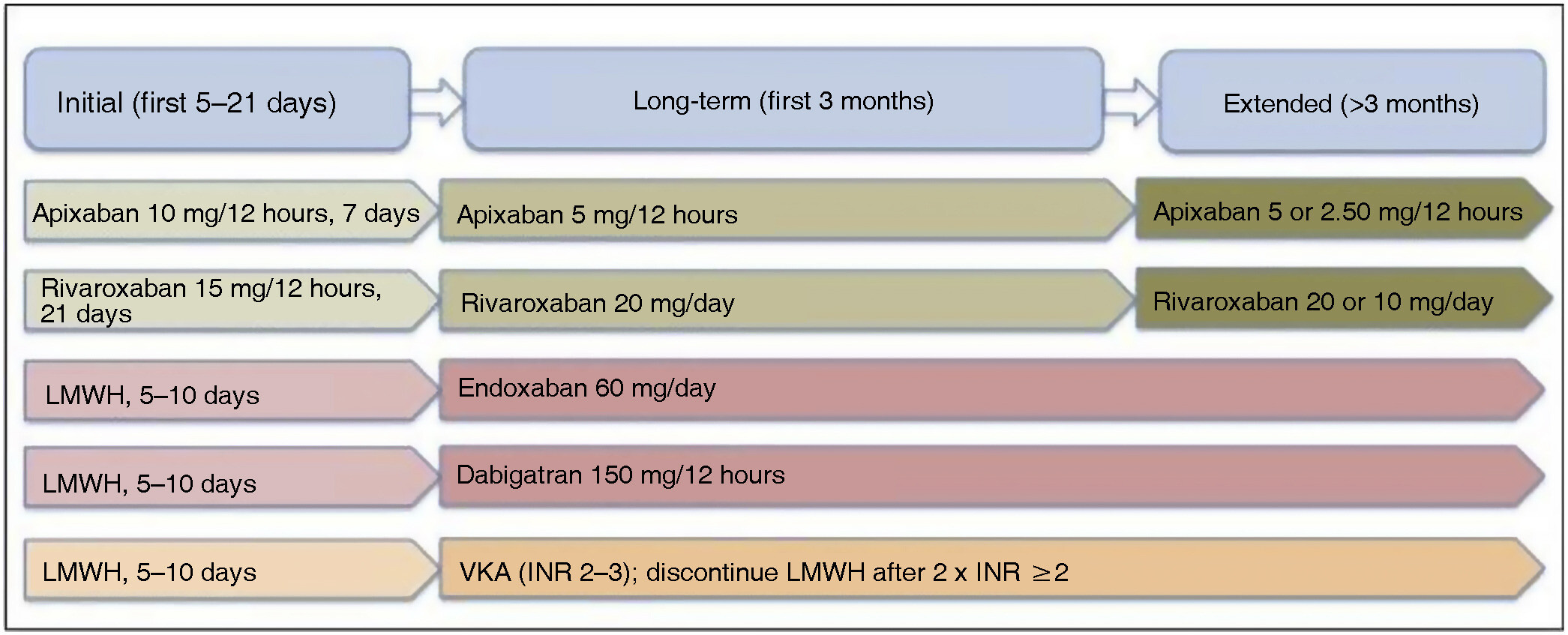 Utilisation de l'EDOXABAN ce qui n'est pas le cas en France
Utilisation de l'EDOXABAN ce qui n'est pas le cas en FrancePhases d'anticoagulation. Modifié à partir de Stevens et al. POITRINE 2021.

Liste de contrôle pour l'anticoagulation dans le VTD (MTEV)
Nos différences, il ne s'agit pas de critiques mais de montrer nos différences entre la France et l'Espagne
TVP ilio-fémorale
De manière générale, il est recommandé que ces patients soient admis à l'hôpital et qu'une anticoagulation par HBPM soit instaurée pour le suivi clinique et la finalisation de l'étude. Une angiographie tomodensitométrique de l'abdomen ou du bassin ou une angiographie IRM doivent être envisagées pour exclure des anomalies anatomiques (agénésie ou hypoplasie de la VCI ou compression de la veine iliaque gauche [syndrome de May-Thurner]).
Chez certains jeunes très symptomatiques atteints de thrombose ilio-fémorale gauche, une évaluation multidisciplinaire avec des spécialistes en chirurgie vasculaire ou en radiologie vasculaire interventionnelle doit être réalisée pour envisager des traitements endovasculaires précoces d'élimination du thrombus (thrombolyse élective dirigée par cathéter) dans le but d'assurer la perméabilité vasculaire et de réduire le risque. et la gravité du SPT, supposant un risque plus élevé de saignement"
Les TVP ilio fémorales ne sont pas systématiquement hospitalisées en France et même rarement
. La fibrinolyse précoce est peu pratiquée.
. Les AOD sont le plus souvent prescrits en première intention.
^QUID des TVP suro poplitées ou fémoro poplitées ?
TVP distale isolée
"La prise en charge des TVP distales isolées est controversée car de nombreux épisodes se résolvent spontanément et leur potentiel emboligène est inférieur à celui des TVP proximales.
Comme pour les TVP proximales, il est recommandé de commencer une anticoagulation à dose complète pendant au moins trois mois chez les patients présentant une TVP distale isolée très symptomatique ou présentant des facteurs de risque de progression du thrombus proximal . En l'absence de ces facteurs de risque d'évolution d'une TVP ou chez des patients présentant une TVP distale distale isolée asymptomatique ou présentant un risque hémorragique élevé, plusieurs options peuvent être envisagées : HBPM à doses réduites pendant quatre à six semaines ou ne pas débuter d'anticoagulation et surveillance par écho-Doppler sériel. scans entre 7 et 14 jours. Ensuite, si aucune progression thrombotique n’est observée sur les scanners, il est recommandé de poursuivre la surveillance clinique sans anticoagulation, mais en cas de progression du thrombus, il est recommandé d’instaurer une anticoagulation."
On est en phase
TVP primaire du membre supérieur
"La TVP primaire du membre supérieur (UE) englobe le syndrome de Paget-Schroetter (PSS) et la thrombose idiopathique. Elles sont rares et, contrairement aux TVP de l’UE associées à un cathéter veineux central, il n’existe pas de recommandations fermes à leur sujet.
Le SPS est rare, est associé à une compression de la veine sous-clavière lors de son passage à travers l'opercule thoracique, touche généralement les personnes jeunes qui effectuent des exercices répétés d'UE et peut entraîner des séquelles fonctionnelles importantes.
Parallèlement, la TVP idiopathique de l'UE survient plus fréquemment chez les patients adultes plus âgés et est associée à un risque plus élevé de néoplasme occulte (chez jusqu'à 25 % des patients) et à un pronostic plus sombre que celui des patients atteints de PSS.
De manière générale, bien qu'il existe peu de preuves dans la littérature, une anticoagulation initiale par HBPM est recommandée suivie d'une anticoagulation orale par AVK pendant au moins trois mois. Bien qu'il n'y ait aucune indication formelle dans les lignes directrices sur l'utilisation des AOD dans ce scénario, il existe des données encourageantes sur les AOD comme alternative anticoagulante dans la TVP de l'UE. Chez les patients atteints de SPS, une évaluation précoce par le service de chirurgie thoracique ou vasculaire est nécessaire ou, le cas échéant, une orientation vers une unité multidisciplinaire de référence pour évaluer d'autres options thérapeutiques telles que la thrombolyse locale sous cathéter (dans les deux premières semaines suivant l'apparition des symptômes), associée ou non à une chirurgie de décompression "
Utilisation plus large des AOD , en dehors de toute complication notamment hémorragique ou rénale
TVP en cas de poids extrêmes
Il n'existe pas de recommandations fermes et spécifiques pour les patients présentant un poids extrême, défini soit comme un poids corporel faible (<50 kg) ou un poids corporel extrêmement élevé (>150 kg, IMC > 40 kg/m 2 ), chez lesquels il existe des changements physiologiques pharmacocinétique du médicament (telle que le taux d'absorption, le volume de distribution et la clairance rénale) qui pourrait conduire à un surdosage ou un sous-dosage d'anticoagulants.
Les recommandations thérapeutiques pour cette population :
| N'importe quel AOD peut être utilisé chez les patients obèses ayant un indice de masse corporelle (IMC) compris entre 30 et 40 kg/2 Les AVK sont préférables chez les patients ayant un IMC compris entre 40 et 50 kg/m 2 , bien que l'apixaban ou le rivaroxaban puissent être envisagés. Les AVK doivent être utilisés chez les patients obèses avec un IMC > 50 kg/m 2 . La dose d'HBPM doit être ajustée selon la fiche technique. La surveillance des taux d'anti-Xa n'est pas systématiquement recommandée, mais peut être envisagée chez certains patients présentant un IMC ≥ 40 kg/m 2 (poids > 150 kg ou IMC > 50 kg/m 2 , instabilité hémodynamique, survenue de complications thromboemboliques ou hémorragiques, traitement prolongé pendant plus de dix jours, ou coexistence d'une maladie rénale chronique avancée (DFG < 30 mL/min). |
| L'utilisation de l'apixaban et de l'edoxaban (ajustement de la dose selon l'EAT) est suggérée chez les patients atteints de TVP pesant entre 60 et 40 kg. Chez les patients pesant <40 kg, l'utilisation d'AVK est suggérée ou, si un traitement par AOD est indiqué, les taux plasmatiques doivent être mesurés. |
|---|
On est en phase
TVP dans les maladies rénales avancées
Les preuves concernant le traitement anticoagulant chez les patients atteints de TVP et d'insuffisance rénale chronique (IRC) avancée (ClCr <30 ml/min) sont principalement basées sur des registres d'observation, car il s'agit d'une population présentant un équilibre fragile entre VTD et risque hémorragique. Les patients atteints d'IRC avancée courent un risque accru de premier événement VTD, de récidive thrombotique, d'hémorragie majeure et de mortalité toutes causes confondues à court et à long terme après un événement thrombotique.
Les recommandations de traitement pour cette population : Aux stades 1 à 3 de l'IRC (ClCr 30 à 59 ml/min), les AOD sont recommandés comme premier choix (avec ajustement de la dose en fonction de l'EAT).
Au stade 4 de l'IRC (ClCr 15–29 ml/min), le traitement doit être individualisé, ajusté en fonction du TDS, et des précautions doivent être prises avec tous les AC.
La tinzaparine est l'HBPM avec la clairance rénale la plus faible (sans danger pour le DFG jusqu'à 20 ml/min), le reste avec un ajustement de dose selon la TDS. Une surveillance de l'activité anti-Xa pourrait être envisagée en cas de traitement prolongé par HBPM SC pendant plus de dix jours. Le dabigatran est contre-indiqué. Le reste des AOD avec ajustement posologique.
Au stade 5 de l’IRC (ClCr < 15 mL/min), les AVK sont le traitement de choix. Les DOAC ne sont pas recommandés.
On est en phase
TVP chez les personnes âgées
Les patients adultes plus âgés ont une incidence plus élevée de VTD, une mortalité et une morbidité liées aux VTD plus élevées et un risque accru d'hémorragie majeure associée à l'anticoagulation. Chez ces patients, des TVP plus étendues sont diagnostiquées, elles surviennent plus fréquemment avec une EP concomitante et ils courent un risque plus élevé de développer un SPT par rapport à la population plus jeune. La pluri pathologie (insuffisance rénale, insuffisance hépatique, anémie, cancer), la polypharmacie, la malnutrition, la fragilité, les troubles cognitifs et le risque de chutes sont des facteurs qui augmentent le risque d'événements hémorragiques majeurs et mortels. De même, cette population est sous-représentée dans les essais cliniques pivots sur les anticoagulants et, par conséquent, les recommandations pour ce groupe proviennent d'études observationnelles.
Les recommandations de traitement pour cette population : Plus grande prudence avec le traitement anticoagulant (marge risque/bénéfice étroite). Ajustement de la dose en fonction du poids réel et de la fonction rénale. Évaluation complète du risque hémorragique et surveillance plus étroite.
Les AOD sont le traitement de choix : administration orale, taux d’hémorragies majeures plus faible, pas de surveillance nécessaire et moins d’interactions médicamenteuses et alimentaires que les AVK.
Le traitement par HBPM (de préférence une dose quotidienne unique, ajustée en fonction du poids et de la fonction rénale) est une autre alternative sûre et efficace au traitement conventionnel (HBPM + AVK) qui évite la surveillance et les interactions médicamenteuses, bien que le coût et l'administration sous-cutanée soient des inconvénients.
On est en phase
TVP chez les patients souffrant d'insuffisance hépatique
Ce groupe de population est exclu des essais pivots sur l'anticoagulation dans la VTD. Les patients atteints de cirrhose présentent non seulement un risque hémorragique plus élevé, mais également un risque thrombotique plus élevé, avec un équilibre hémostatique instable qui peut facilement être déséquilibré par des facteurs déclenchants (décompensation hépatique, septicémie, insuffisance rénale ou procédures invasives). La complication thrombotique la plus courante chez les patients atteints de cirrhose avancée est la thrombose portale. De même, les patients atteints de cirrhose avancée qui reçoivent un traitement anticoagulant ont un taux de mortalité plus élevé et un risque très élevé d'hémorragie majeure par rapport aux patients anticoagulants sans cirrhose.
Les recommandations de traitement pour cette population : Le pronostic d'une maladie hépatique chronique, principalement la cirrhose, doit être évalué à l'aide de la classification de Child-Pugh.
Une EGD doit être réalisée pour détecter/exclure les varices œsophagiennes ainsi que le dépistage et le conseil des troubles liés à la consommation d'alcool.
En cas de cirrhose de Child-Pugh A : des AOD ou des AVK peuvent être utilisés.
En cas de cirrhose de Child-Pugh B : des AVK ou, avec prudence, des AOD (apixaban et edoxaban) peuvent être utilisés. Le rivaroxaban est contre-indiqué et le dabigatran est contre-indiqué chez les patients atteints d'une maladie hépatique potentiellement mortelle.
Si cirrhose de Child-Pugh C : AVK au choix. Les AOD sont contre-indiqués. L'anticoagulation doit être interrompue en cas de thrombocytopénie sévère et le rapport risque/bénéfice doit être soigneusement évalué chez les patients présentant un mauvais pronostic vital et un risque hémorragique très élevé.
TVP dans la thrombocytopénie
La numération plaquettaire doit être déterminée avant de débuter un traitement antithrombotique, car elle constitue un facteur limitant l'utilisation d'anticoagulants. La thrombocytopénie (TP) ne réduit pas le risque de thrombose récidivante et expose les patients à un risque accru d'hémorragie. Les patients atteints de VTD et de TP modérés à sévères (<80 000 plaquettes/μL) ont un risque presque trois fois supérieur d'hémorragie majeure et presque deux fois plus de risque d'hémorragie mortelle que ceux ayant une numération plaquettaire normale.
L'anticoagulation dans le contexte de la TP présente le défi supplémentaire d'équilibrer les risques concurrents de saignement et de VTD récurrente. Lors de l'évaluation du risque de TVP récurrente ou progressive d'un patient, des facteurs tels que la charge du thrombus (taille, emplacement et impact), l'étiologie et le temps écoulé depuis l'événement index doivent être pris en compte. De même, le risque de saignement peut être déterminé par les antécédents médicaux de saignement ; coagulopathie concomitante (par exemple, DIC); insuffisance hépatique ou rénale ; infection; et, dans le cas de tumeurs solides ; le type et l'emplacement de la tumeur primitive et des métastases. Des considérations supplémentaires incluent la nécessité de procédures ; l'étiologie, la gravité et la durée du PT ; et les comorbidités telles que l'insuffisance rénale ou hépatique qui affectent le choix et le traitement anticoagulant.
Les recommandations de traitement pour cette population : Lorsque la numération plaquettaire est < 50 × 10 9 /L, le risque thrombotique et hémorragique ainsi que la durée attendue de la TP doivent être réévalués.
En cas de TP légère (nombre de plaquettes ≥ 50 × 10 9 /L), il est suggéré de maintenir le traitement anticoagulant à pleine dose.
En cas de TP modérée (nombre de plaquettes entre 20 × 10 × 10⁹/L et 50 × 10⁹/L), une réduction de dose d'HBPM de 50 % est proposée.
En cas de TP sévère (numération plaquettaire égale ou inférieure à 20 × 10⁹/L : dans la phase aiguë de la VTD (<30 jours), la pose d'une FIV doit être envisagée, surtout si la TP devrait également durer plus de cinq à sept jours. comme chez les patients présentant une TVP étendue ou une EP avec une faible réserve cardio-pulmonaire ou une thrombose récurrente).
La transfusion de plaquettes pourrait être envisagée pour maintenir la numération plaquettaire au-dessus de 20 × 10 9 /L (éventuellement début d'une anticoagulation à doses intermédiaires d'HBPM) ou 50 × 10 9 /L (éventuellement début d'une anticoagulation à dose complète). L'arrêt du traitement anticoagulant est suggéré chez les patients présentant une thrombocytopénie < 50 × 10 9 /L et une thrombocytopénie subaiguë (30 à 90 jours depuis l'événement) ou une TVP distale isolée.
On est en phase
TVP récurrente
Le diagnostic d'une TVP récurrente au même endroit est généralement plus difficile à établir qu'un premier épisode de thrombose veineuse. Une poussée de symptômes peut être une récidive ou un SPT de l'événement précédent, qui peut survenir chez 20 à 45 % des patients présentant une TVP proximale. En cas de confirmation d'une TVP récurrente sous anticoagulation, la première étape consiste à évaluer l'observance du traitement et à confirmer les doses complètes et l'absence d'interactions médicamenteuses.
Deuxièmement, les causes d'hypercoagulabilité, telles que les néoplasmes occultes ou évolutifs, le syndrome des antiphospholipides (APS) ou la thrombocytopénie induite par l'héparine (TIH), doivent être exclues. Une fois ces causes écartées, pour les patients récidivants sous traitement par AVK ou AOD, il est proposé de passer aux HBPM pendant au moins quatre semaines (puis d'envisager de passer aux AOD ou de revenir aux AVK avec possibilité d'augmenter l'objectif). INR à 2,5-3,5).
Chez les patients présentant une récidive sous traitement par HBPM, il est suggéré d'augmenter la dose d'HBPM de 10 à 25 %.
TVP pendant la grossesse
La grossesse entraîne une multiplication par quatre à cinq du risque de VTD, la période post-partum comportant le plus grand risque de mortalité. La TVP survient avec la même fréquence pendant la grossesse et pendant la période post-partum, tandis que l'EP est plus fréquente pendant la période post-partum.
Le diagnostic de TVP pendant la gestation peut être difficile en raison de la non-spécificité clinique, de l'utilité limitée de la DD étant donné qu'elle augmente physiologiquement et de la faible fiabilité des échelles prédictives développées pour la population générale.
Les recommandations sur le traitement des patientes enceintes atteintes de TVP : Les HBPM à doses thérapeutiques sont l'anticoagulant de choix tout au long de la grossesse et du post-partum. Les femmes qui tombent enceintes alors qu’elles reçoivent des AVK ou des AOD doivent passer aux HBPM. En post-partum, les HBPM à doses thérapeutiques ou HNF peuvent être reprises 24 h après le retrait du cathéter d'anesthésie péridurale, 6 à 12 h après un accouchement vaginal ou 12 à 24 heures après une césarienne.
Commentaire
Excellent travail très complet .
Nos différences s'expliquent par l'absence de médecins vasculaires en Espagne.
Les internistes et les chirurgiens vasculaires sont en première ligne pour la MTEV
Un problème majeur, ces recommandations ne sont pas accès libre, toutes les recommandations doivent être libre d'accès, ce péage du savoir est inadmissible , quelque soit l'éditeur

