« Lorsque vous ressentez de la tristesse ou de la colère à propos de votre cancer ou de votre sort, les masquer, c'est mener une vie artificielle " Steve Jobs
« Tout groupe organique qui se développe égoïstement pour lui-même joue le même rôle dans la société que le cancer dans le corps humain » Alexis Carrel
Comparaison des stratégies d'anticoagulation pour la thromboembolie veineuse associée au cancer actif
Les recommandationsactuelles recommandent plusieurs agents anticoagulants oraux directs (AOD) de manière égale pour la prise en charge de la thromboembolie veineuse (TEV) associée au cancer.
Objectifs
L’objectif de cette étude était d’évaluer l’efficacité et la sécurité des AOD chez les patients atteints d’un cancer actif.
Méthodes
Des recherches bibliographiques ont été menées dans PubMed, Embase et Cochrane Central en novembre 2022. Des essais contrôlés randomisés examinant les stratégies d'anticoagulation (antagonistes de la vitamine K, anticoagulation parentérale [par exemple, héparine de bas poids moléculaire] et AOD) pour la thrombose veineuse profonde chez les patients atteints d'un cancer actif ont été identifiés pour une méta-analyse en réseau. Les critères de jugement comprenaient la thrombose veineuse profonde récurrente, l'embolie pulmonaire récurrente, la thrombose veineuse profonde récurrente, l'hémorragie majeure, l'hémorragie non majeure cliniquement pertinente (CRNMB) et un critère composite d'hémorragie majeure ou de CRNMB. Les HR groupés et les IC à 95 % ont été estimés en utilisant soit le HR, soit le risque relatif fourni par chaque étude. Des modèles à effets aléatoires ont été utilisés pour toutes les analyses.
Résultats
Dix-sept essais contrôlés randomisés portant sur 6 623 patients atteints d'un cancer actif ont été inclus. Aucune différence significative n'a été constatée entre les AOD en termes d'efficacité (TEV récurrente, embolie pulmonaire et thrombose veineuse profonde). En termes d'hémorragie majeure, l'apixaban était aussi sûr que le dabigatran et le rivaroxaban, mais était associé à un risque réduit par rapport à l'édoxaban (HR : 0,38 ; IC à 95 % : 0,15-0,93). En ce qui concerne le CRNMB, l'édoxaban était aussi sûr que l'apixaban, mais était associé à un risque réduit par rapport au rivaroxaban (HR : 0,31 ; IC à 95 % : 0,10-0,91). Comparé à l'anticoagulation parentérale, l'apixaban a été associé à un risque réduit de récidive de thrombose veineuse profonde (HR : 0,60 ; IC à 95 % : 0,38-0,93) sans augmentation des saignements, l'edoxaban a été associé à un risque accru de saignement majeur ou de CRNMB (HR : 1,35 ; IC à 95 % : 1,02-1,79), et le rivaroxaban a été associé à un risque accru de CRNMB (HR : 3,76 ; IC à 95 % : 1,43-9,88).
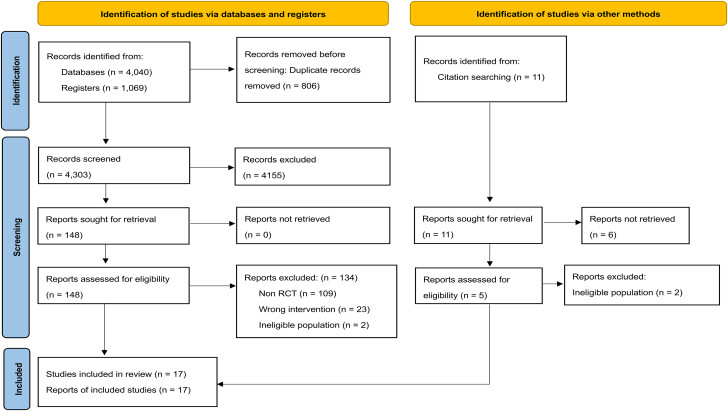
Diagramme de flux de sélection d'études
Au total, 6 623 patients issus de 17 essais ont été inclus. ECR = essai contrôlé randomisé.
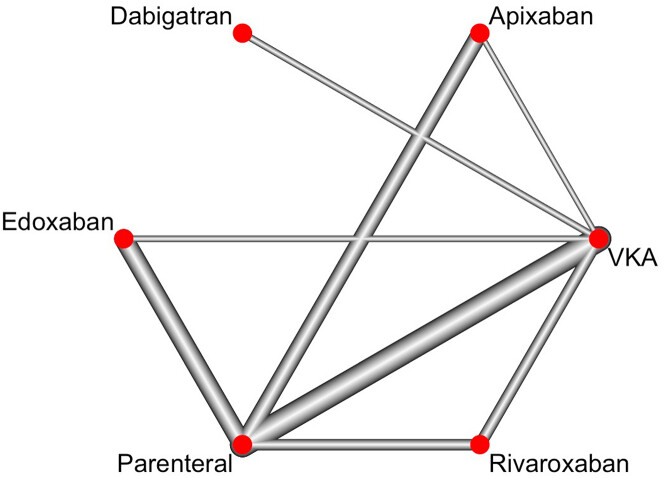
Réseau de régimes de traitement pour cette méta-analyse de réseau
L'épaisseur des lignes entre les stratégies correspond au nombre de patients dans cette comparaison. AVK = antagoniste de la vitamine K.
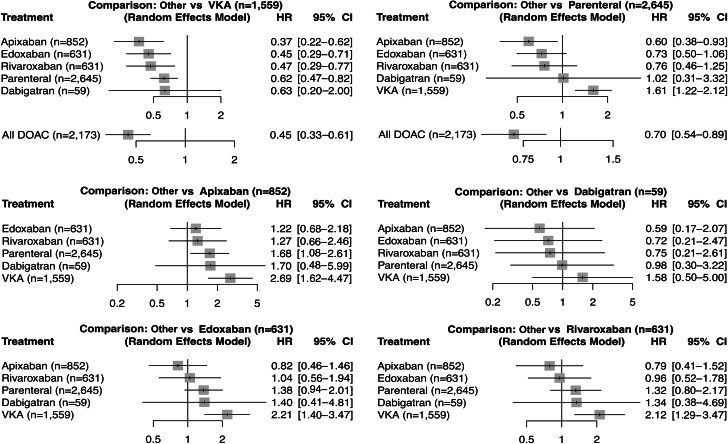
Résultats pour le critère d'efficacité principal (thromboembolie veineuse récurrente)La figure montre le HR et l'IC à 95 % pour chaque groupe de traitement. AOD = anticoagulant oral direct ; AVK = antagoniste de la vitamine K.
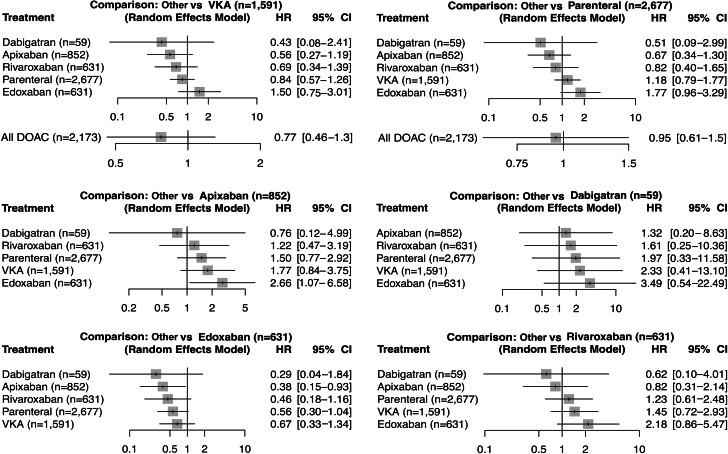
Résultats pour le critère d'évaluation principal de la sécurité (hémorragie majeure)La figure montre le HR et l'IC à 95 % pour chaque groupe de traitement
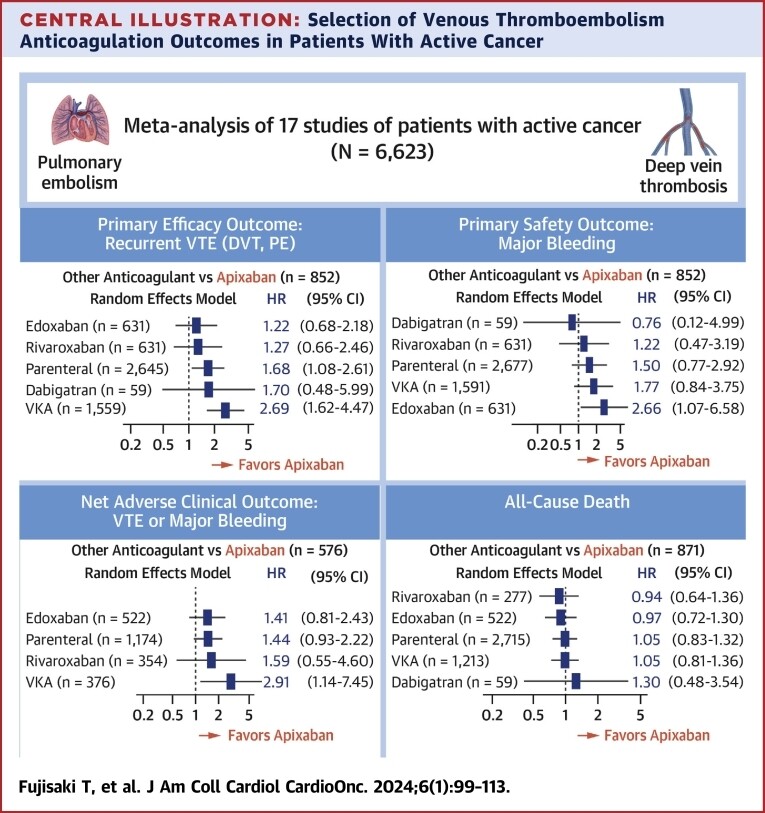
Les principaux résultats de cette méta-analyse en réseau portant sur 6 623 patients atteints d'un cancer actif et d'une thrombose veineuse (TEV) ont montré que chaque AOD avait une efficacité comparable pour le traitement et la prévention des récidives de la TEV. Cependant, chaque AOD avait un profil de sécurité significativement différent en termes d'issues hémorragiques, l'apixaban étant associé à un risque réduit d'hémorragie majeure par rapport à l'édoxaban, et l'édoxaban étant associé à un risque réduit de MBRC par rapport au rivaroxaban. De plus, par rapport à l'anticoagulation parentérale, l'apixaban était associé à un risque réduit de thrombose veineuse récurrente sans risque accru d'hémorragie, tandis que l'édoxaban et le rivaroxaban étaient associés à des risques accrus d'hémorragie.
Chez les patients atteints d'un cancer actif, divers facteurs liés à la malignité (par exemple, le type de cancer, le site primaire, le stade avancé), les facteurs liés au patient (par exemple, le vieillissement, l'état fonctionnel, les comorbidités, le faible poids corporel) et les facteurs liés au traitement (par exemple, la suppression de la moelle osseuse, l'hormonothérapie, la chirurgie, l'hospitalisation) peuvent contribuer à une interaction complexe entre les événements thrombotiques et hémorragiques. Les risques de thrombose et de saignement récurrents qui en découlent chez les patients atteints d'un cancer actif et d'une thrombose veineuse (TEV) soulignent la nature critique et difficile de l'anticoagulation thérapeutique. Minimiser le risque de ces événements indésirables est essentiel non seulement pour optimiser la qualité de vie du patient, mais également pour éviter toute interruption ou tout retard du traitement contre le cancer.
Les résultats de notre étude concordent largement avec ceux des méta-analyses précédentes et les valident. Cependant, notre recherche actuelle diffère considérablement car nous avons spécifiquement exclu les patients atteints d'un cancer non actif et différencié les AOD, dans le but de réaliser une méta-analyse en réseau robuste et méticuleuse. Nous avons effectué une comparaison approfondie de chaque AOD, révélant une découverte nouvelle et remarquable selon laquelle chaque AOD peut avoir un profil de sécurité distinct pour les résultats hémorragiques. Des méta-analyses antérieures examinant les stratégies d'anticoagulation chez les patients atteints d'un cancer actif ont démontré que les AOD étaient associés à un risque réduit de thrombose veineuse récurrente et à un risque accru d'hémorragie non majeure par rapport à l'HBPM. Cependant, ces analyses précédentes étaient considérablement limitées en termes de méthodologie car elles regroupaient l'apixaban, l'édoxaban, le rivaroxaban et le dabigatran sans effectuer de comparaisons directes. De plus, l'inclusion de populations de patients atteints à la fois d'un cancer actif et non actif a conduit à une hétérogénéité significative.
Par conséquent, ces études limitées n’ont pas permis d’identifier de différences significatives dans les résultats de sécurité entre les AOD.
Conclusions
Les AOD présentent une efficacité comparable mais des profils de sécurité différents. L'apixaban peut conférer un bénéfice antithrombotique sans risque accru de saignement, ce qui le distingue des autres stratégies anticoagulantes contemporaines chez les patients atteints d'un cancer actif et d'une thrombose veineuse.
Commentaire
Possédons-nous l'anticoagulent idéal en cas de CANCER/MTEV , non, mais on s'en rapproche. Les antiXI devraient encore améliorer la situation des patients
En matière de cancer, l'étude APICAT en attente va certainment faire évoluer les choses (Pr Isabelle Mahé) en terme notamment de posologie, de risque hémorragique etc