"Savoir, c’est pouvoir ! C’est l’action qui détermine si la connaissance est certaine." Swâmi Prâjnanpad
"Le savoir que l’on ne complète pas chaque jour diminue au quotidien." Proverbe chinois

Wei Jia· Hehe Cui · Xuemin Zhang
Journal of Thrombosis and Thrombolysis, 2026,
https://link.springer.com/article/10.1007/s11239-026-03254-y
Son incidence varie selon le type de cancer, les caractéristiques du patient et les facteurs liés au traitement anticancéreux.
La TVPI associée au cancer (TVPI-AC) est une forme spécifique de TVPI, aux conséquences cliniques graves, notamment le décès, la récidive de MTEV et les hémorragies majeures.
Malgré son importance clinique, peu d'études se sont intéressées à la prise en charge de la TVPI-AC.
Des données récentes plaident en faveur d'une stratégie d'anticoagulation individualisée et recommandent un traitement prolongé.
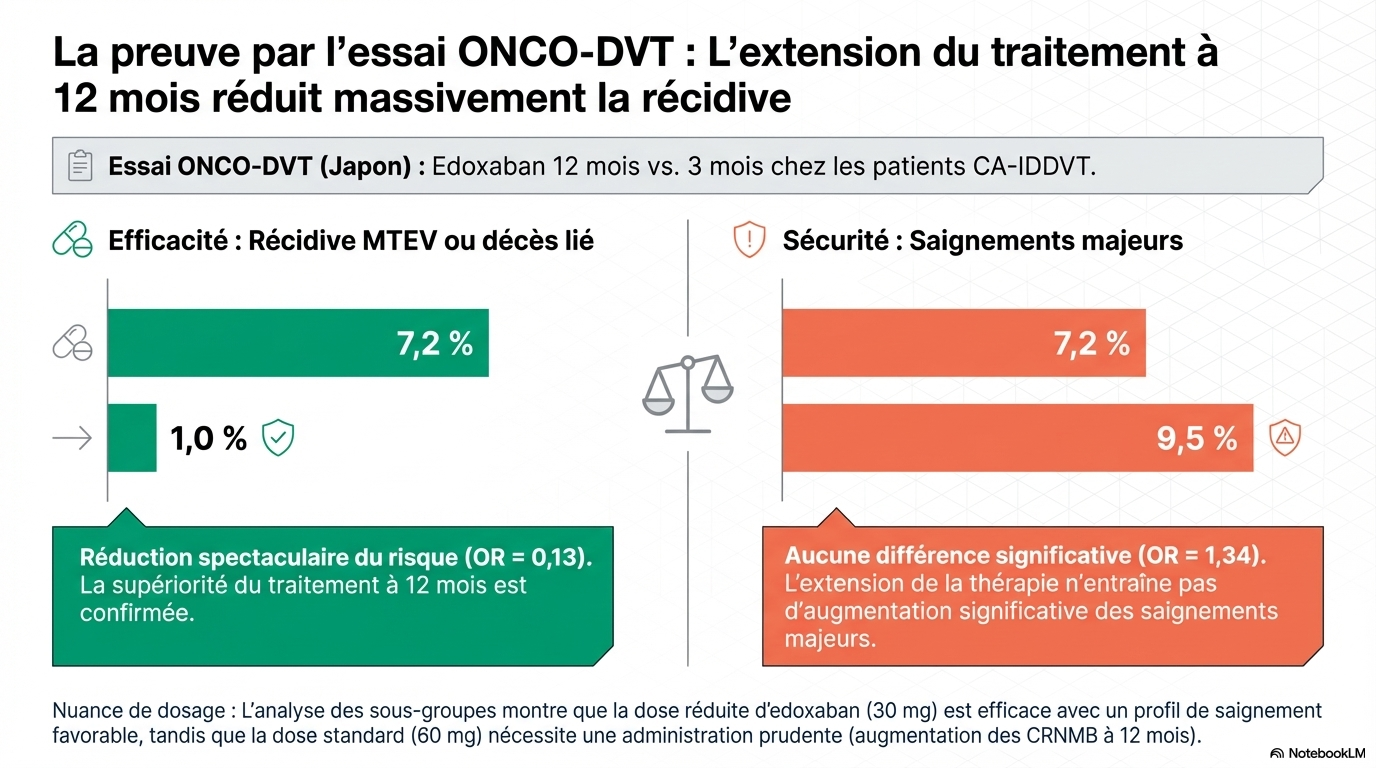
En particulier, l'essai ONCO-DVT démontre qu'un traitement prolongé par edoxaban réduit significativement le risque thrombotique sans augmenter le risque d'hémorragie majeure, soulignant ainsi son potentiel dans la prise en charge de la TVPI-AC.
Cet article passe en revue les avancées récentes concernant les facteurs cliniques, les manifestations et les stratégies thérapeutiques de la TVPI-AC, offrant de nouvelles perspectives pour une prise en charge efficace.
RÉSUMÉ GÉNÉRATIF
Ce document traite de la thrombose veineuse profonde distale isolée associée au cancer (CA-IDDVT), de ses facteurs de risque, de ses manifestations cliniques et de ses stratégies de traitement.
Gestion de la thrombose veineuse profonde liée au cancer
Une revue des avancées récentes dans la prise en charge de la CA-IDDVT, soulignant l'importance d'une stratégie individualisée d'anticoagulation prolongée. - La CA-IDDVT représente jusqu'à 50% des cas de DVT, avec des risques graves comme décès, récidive de VTE et saignements majeurs. - La gestion doit être adaptée, avec une anticoagulation prolongée recommandée, notamment avec l'edoxaban selon l'essai ONCO-DVT. - La récidive de VTE est élevée, surtout en cas de maladie active ou après chimiothérapie. - La mortalité et la récidive sont comparables à celles de la DVT proximale, mais le risque de PE est moindre en DVT distale. - La durée du traitement anticoagulant doit dépasser 6 mois pour réduire la récidive, avec une attention particulière à la balance bénéfice-risque.
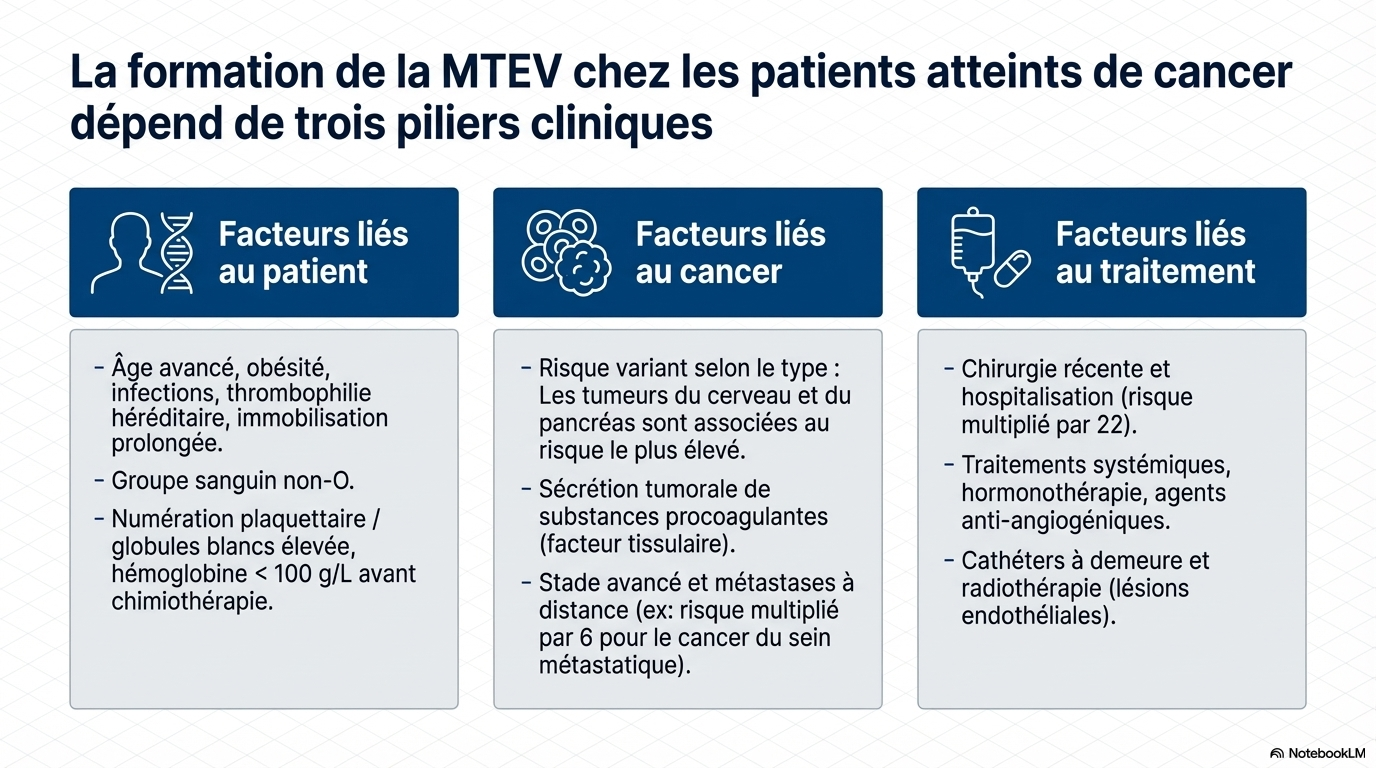
Facteurs étiologiques de la CA-IDDVT
Les causes de la CA-IDDVT sont multifactoriales, incluant des aspects liés au patient, au cancer et au traitement. - Facteurs liés au patient : âge avancé, obésité, antécédents de VTE, immobility prolongée, hypercoagulabilité acquise. - Facteurs liés au cancer : certains types comme le pancréas ou le cerveau ont un risque accru, avec sécrétion de substances procoagulantes. - Facteurs liés au traitement : chirurgie, hospitalisation, thérapies systémiques, radiothérapie, cathéters, agents antiangiogéniques. - Le risque de VTE varie selon le type, le stade et la localisation tumorale, avec un risque six fois plus élevé en cas de métastases.
Manifestations cliniques et diagnostic de la CA-IDDVT
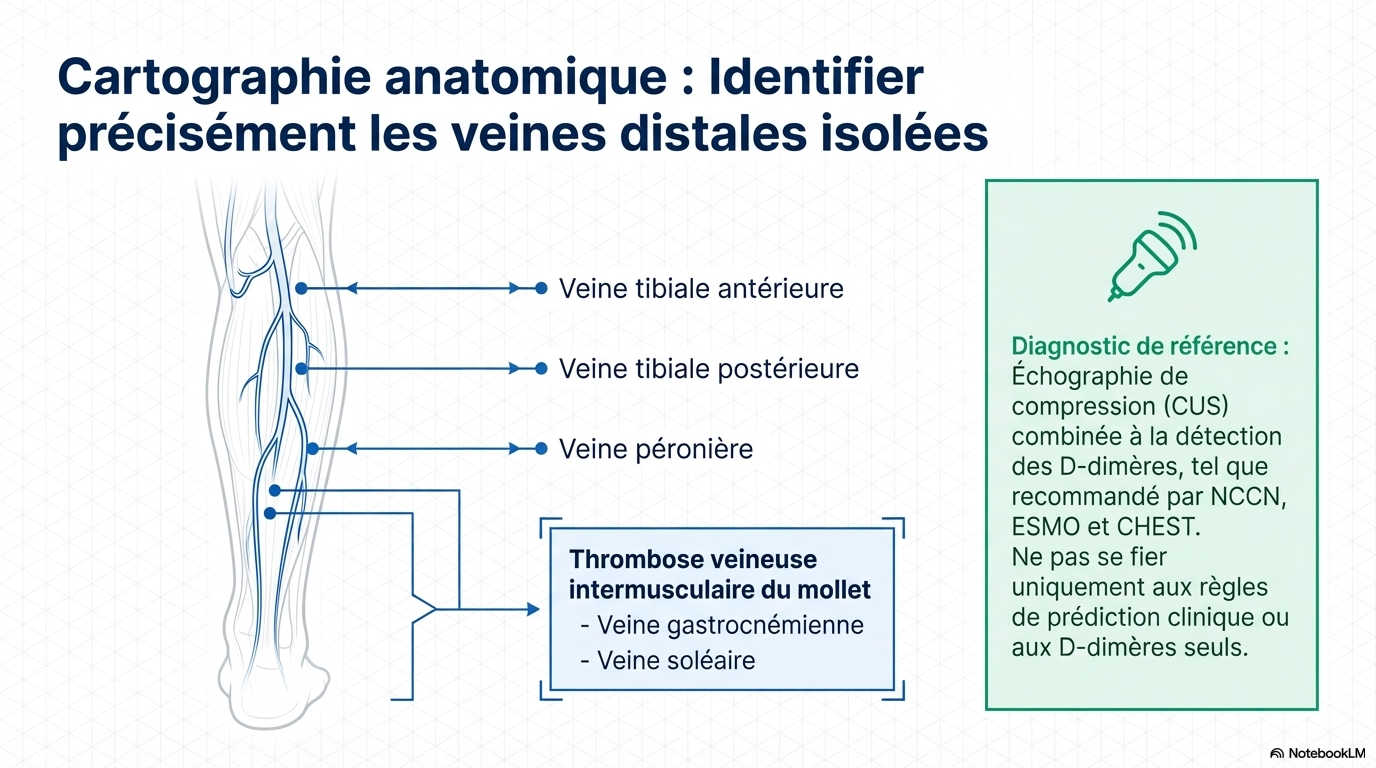
La CA-IDDVT touche plusieurs veines du mollet, avec des symptômes typiques. - Symptômes : rougeur, douleur, gonflement, œdème, veines superficielles collatérales. - Diagnostic recommandé : échographie de compression combinée à la détection de D-dimères, sans dépendre uniquement des règles cliniques. - La détection précoce est essentielle pour prévenir la progression et les complications.
Pronostic et évolution de la CA-IDDVT
Les indicateurs clés incluent la récidive, les saignements majeurs et la mortalité. - Taux de récidive de VTE : 5.65 cas pour 100 patient-années. - Saignements majeurs : 4.08 cas pour 100 patient-années. - La mortalité est élevée, avec un taux de 30.22 cas pour 100 patient-années. - La récidive est plus fréquente lors de maladie active ou après chimiothérapie. - La CA-IDDVT a des issues graves, comparables à celles de la DVT proximale, mais avec un risque moindre de PE.
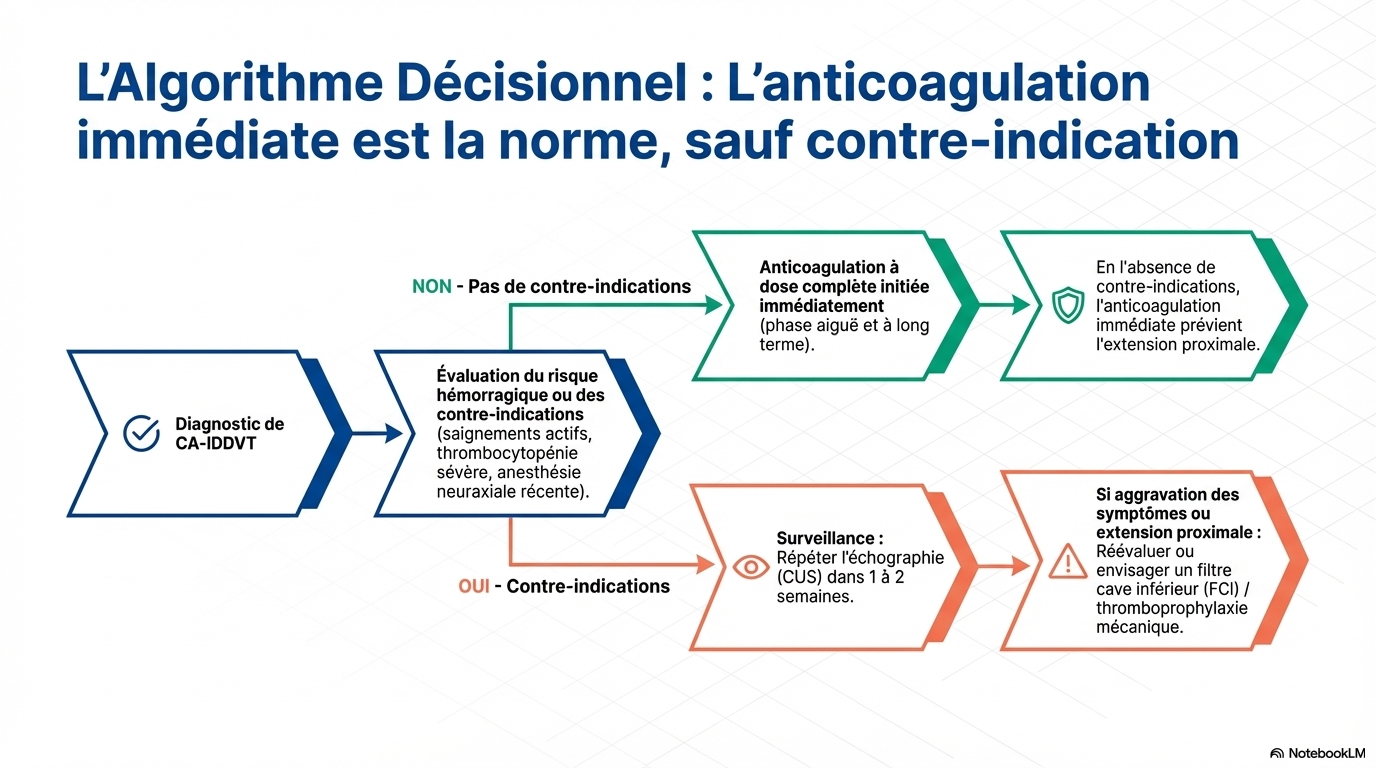
Stratégies d'anticoagulation pour CA-IDDVT
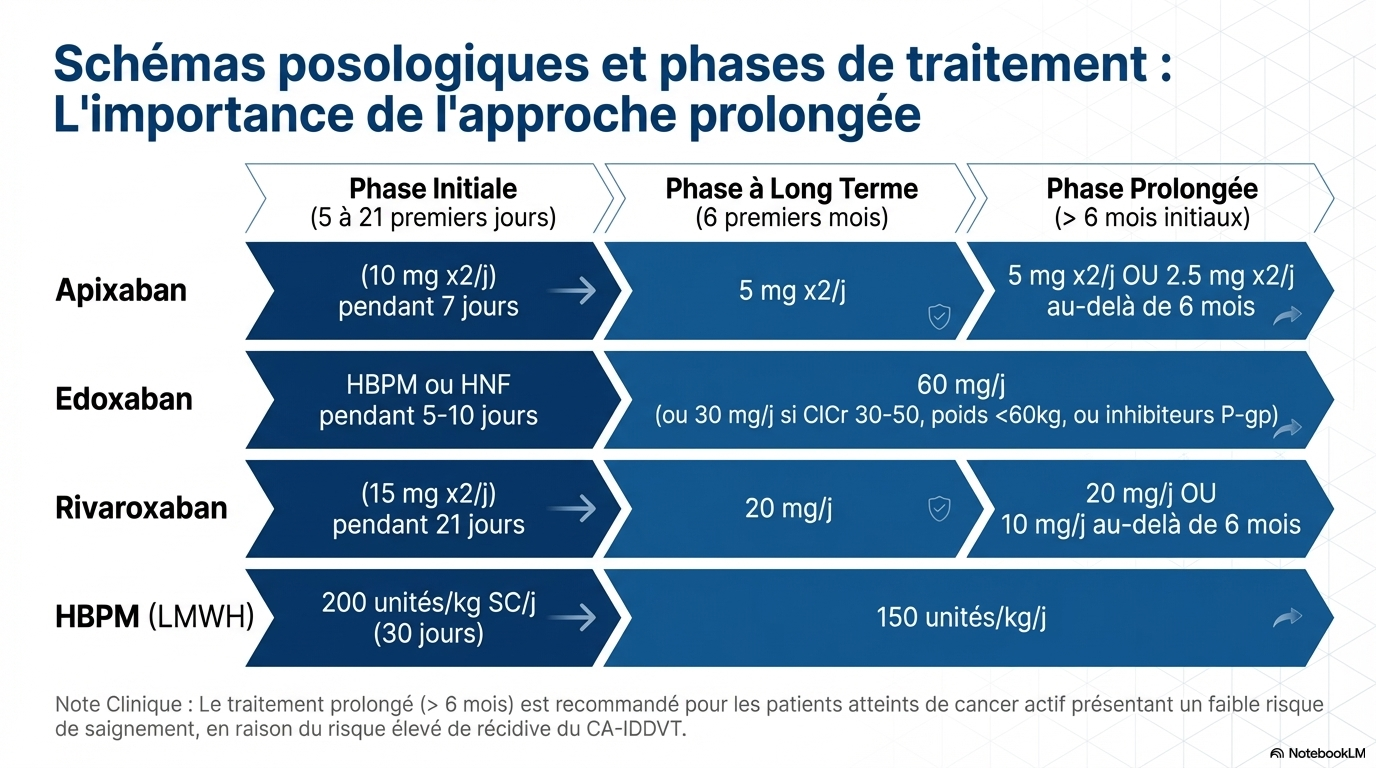
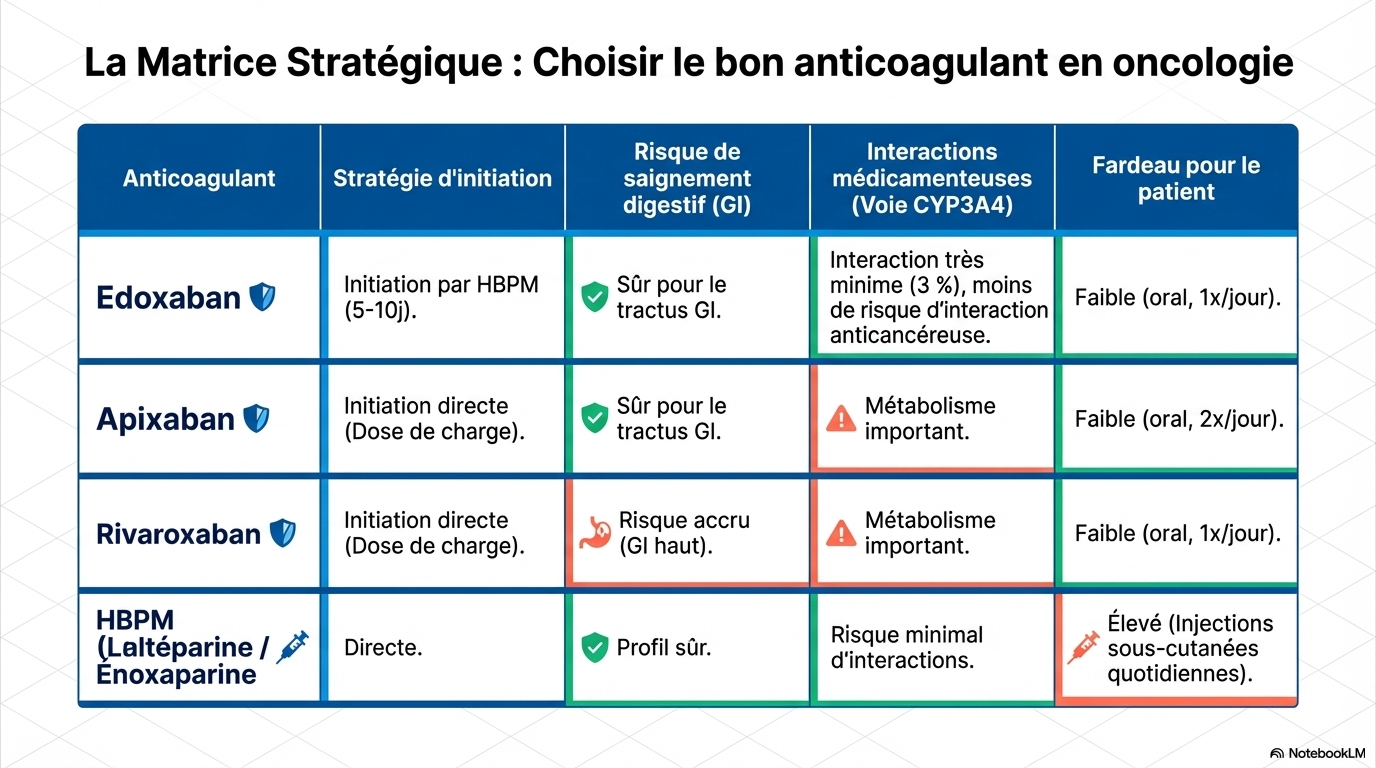
L'approche thérapeutique doit être individualisée, avec une anticoagulation prolongée. - La décision d'anticoaguler doit être prise rapidement, sauf contre-indications comme saignements actifs ou thrombopénie sévère. - Les anticoagulants préférés : DOACs (edoxaban, apixaban) et HBPM, avec une réévaluation selon le type de cancer. - La durée du traitement : au moins 6 mois, avec extension possible au-delà, notamment avec l'edoxaban pour réduire la récidive. - L'essai ONCO-DVT montre que 12 mois d'edoxaban réduisent la récidive sans augmenter les saignements majeurs. - La posologie varie selon le médicament : par exemple, apixaban 10 mg BID la première semaine, puis 5 mg BID. - La sélection du traitement doit considérer le risque de saignement, la fonction rénale, le poids, et les interactions médicamenteuses.
Efficacité et sécurité des anticoagulants
Les études cliniques soutiennent l'utilisation prolongée des DOACs pour réduire la récidive. - Edoxaban : 12 mois réduit significativement la récidive (1.0% vs 7.2% à 3 mois). - Apixaban : faible taux de récidive (5.6% à 6 mois) sans augmentation des saignements. - Rivaroxaban : réduction de la récidive à 6 mois, mais avec un risque accru de saignements majeurs. - Comparaison avec la HBPM : les DOACs sont plus efficaces et plus économiques, avec un profil de sécurité acceptable. - La gestion doit équilibrer la prévention de la récidive et le risque de saignement, en tenant compte des interactions médicamenteuses et des caractéristiques du patient.
Perspectives futures dans la gestion de la CA-IDDVT
Des recherches supplémentaires sont nécessaires pour optimiser la prise en charge. - La variabilité des critères d'inclusion, des schémas thérapeutiques et des durées de suivi complique l'interprétation des résultats. - La nécessité d'études contrôlées pour confirmer la sécurité des DOACs, notamment en cas de cancer avancé ou de traitements combinés. - L'amélioration des stratégies pour réduire les risques de saignement tout en prévenant la récidive. - La recherche doit aussi explorer les interactions médicamenteuses et la gestion personnalisée selon le profil de chaque patient.
Caractéristiques et importance de CA-IDDVT
Une sous-catégorie distincte de DVT, CA-IDDVT, présente un risque élevé de récidive et de complications graves.
- CA-IDDVT est une forme spécifique de DVT liée au cancer.
- Elle est associée à un risque accru de récidive et de complications majeures.
- La gestion optimale reste débattue, avec deux stratégies principales : anticoagulation ou surveillance.
- La preuve actuelle recommande une anticoagulation individualisée, souvent prolongée au-delà de 6 mois.
- Les anticoagulants oraux directs (DOACs) jouent un rôle central, notamment avec l'édoxaban.
- La controverse persiste sur le traitement, mais l'anticoagulation est généralement recommandée en l'absence de contre-indications.
Défis dans l'attribution de la mortalité
Difficulté à distinguer la mortalité due à la progression du cancer ou aux complications thromboemboliques.
- La complexité provient de l'hétérogénéité des stades cancéreux et de multiples facteurs en jeu.
- La gestion doit être individualisée pour chaque patient.
- Technologies innovantes comme l'impression 3D et l'IA peuvent améliorer la prise en charge.
- Des études prospectives plus larges et une meilleure documentation des résultats sont nécessaires.
- La collaboration multidisciplinaire est essentielle pour renforcer les preuves cliniques.
Approches stratégiques de traitement
Deux stratégies principales pour CA-IDDVT : anticoagulation ou surveillance.
- La première recommande une anticoagulation similaire à celle pour DVT proximal ou embolie pulmonaire.
- La seconde privilégie une stratégie de "regarder et attendre" en raison d’un risque perçu moindre d’embolie proximale.
- La gestion doit être adaptée en fonction des contre-indications et du profil du patient.
- La durée prolongée de traitement anticoagulant, souvent au-delà de 6 mois, est soutenue par des preuves.
- Les essais cliniques, comme l’étude ONCO-DVT, confirment l’efficacité et la sécurité du traitement prolongé avec le DOAC édoxaban.
Innovations technologiques pour la gestion
Les nouvelles technologies peuvent améliorer la personnalisation et la sécurité du traitement.
- La fabrication de comprimés sur mesure via l’impression 3D permet une dose adaptée.
- Les plateformes d’IA pour la pharmacogénomique aident à choisir et doser les DOAC selon le profil génétique.
- Ces innovations peuvent réduire les risques de saignement et d’échec thérapeutique.
- La recherche continue pour intégrer ces technologies dans la pratique clinique courante.
- La collaboration multidisciplinaire et les études à grande échelle sont nécessaires pour valider ces approches.
Recommandations et lignes directrices futures
Besoin d’études plus robustes et de lignes directrices pratiques pour optimiser la prise en charge.
- La collaboration entre disciplines est essentielle pour renforcer les preuves.
- La documentation précise que des résultats de mortalité et de récidive doivent être améliorés.
- Des recommandations actualisées doivent intégrer les nouvelles technologies et données cliniques.
- La gestion individualisée, notamment pour les patients atteints de cancer avancé, est prioritaire.
- La recherche doit continuer pour clarifier la meilleure stratégie thérapeutique et la durée optimale du traitement.
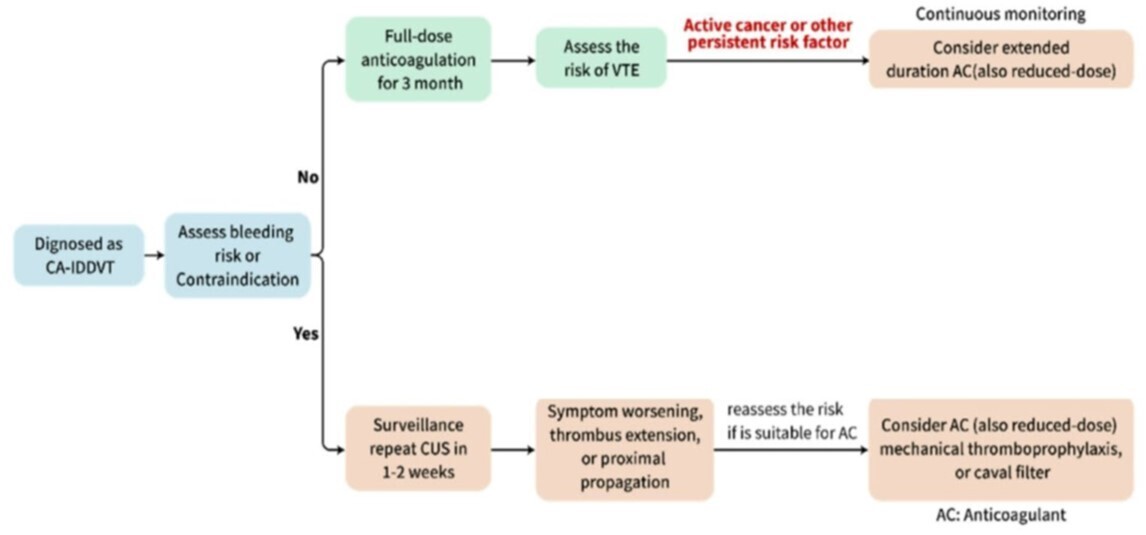

Cet article scientifique propose une revue exhaustive de la thromboembolie veineuse distale isolée associée au cancer (CA-IDDVT), une pathologie fréquente dont les risques cliniques sont souvent sous-estimés. Les auteurs soulignent que cette forme de thrombose présente des complications sévères, telles que la récidive et le décès, à des taux comparables aux thromboses proximales plus graves. L'étude met particulièrement en avant l'évolution des stratégies de prise en charge, préconisant désormais une anticoagulation prolongée au-delà de six mois plutôt qu'une simple surveillance. En s'appuyant sur des essais cliniques récents comme l'étude ONCO-DVT, le texte démontre la supériorité et la sécurité des anticoagulants oraux directs (AOD), notamment l'édoxaban, pour réduire les risques thrombotiques sans augmenter significativement les hémorragies majeures. L'objectif ultime est de disposer, pour le clinicien, d'un cadre décisionnel individualisé, permettant d'adapter le traitement en fonction du type de cancer, de la fonction rénale et des interactions médicamenteuses du patient.
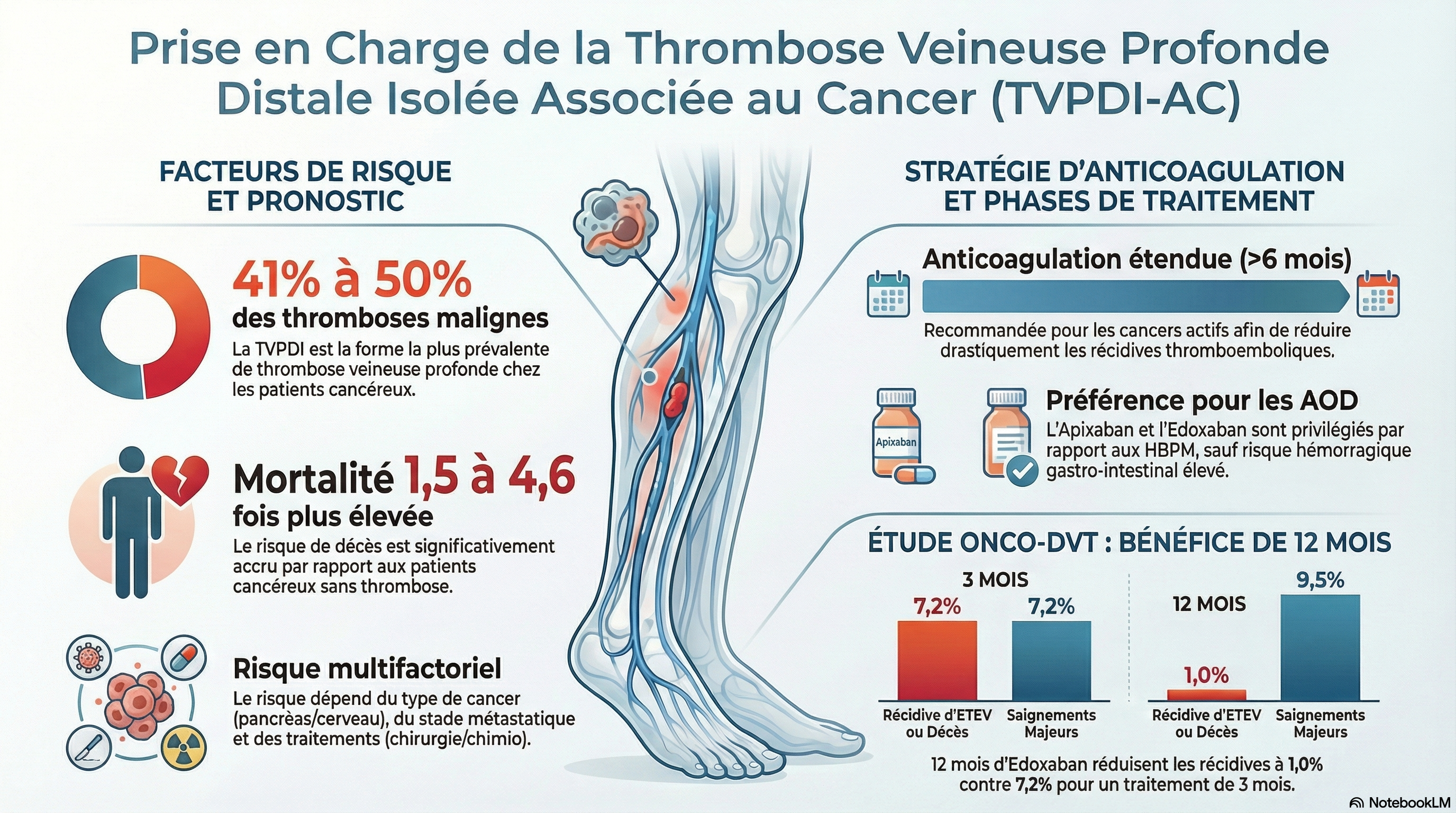

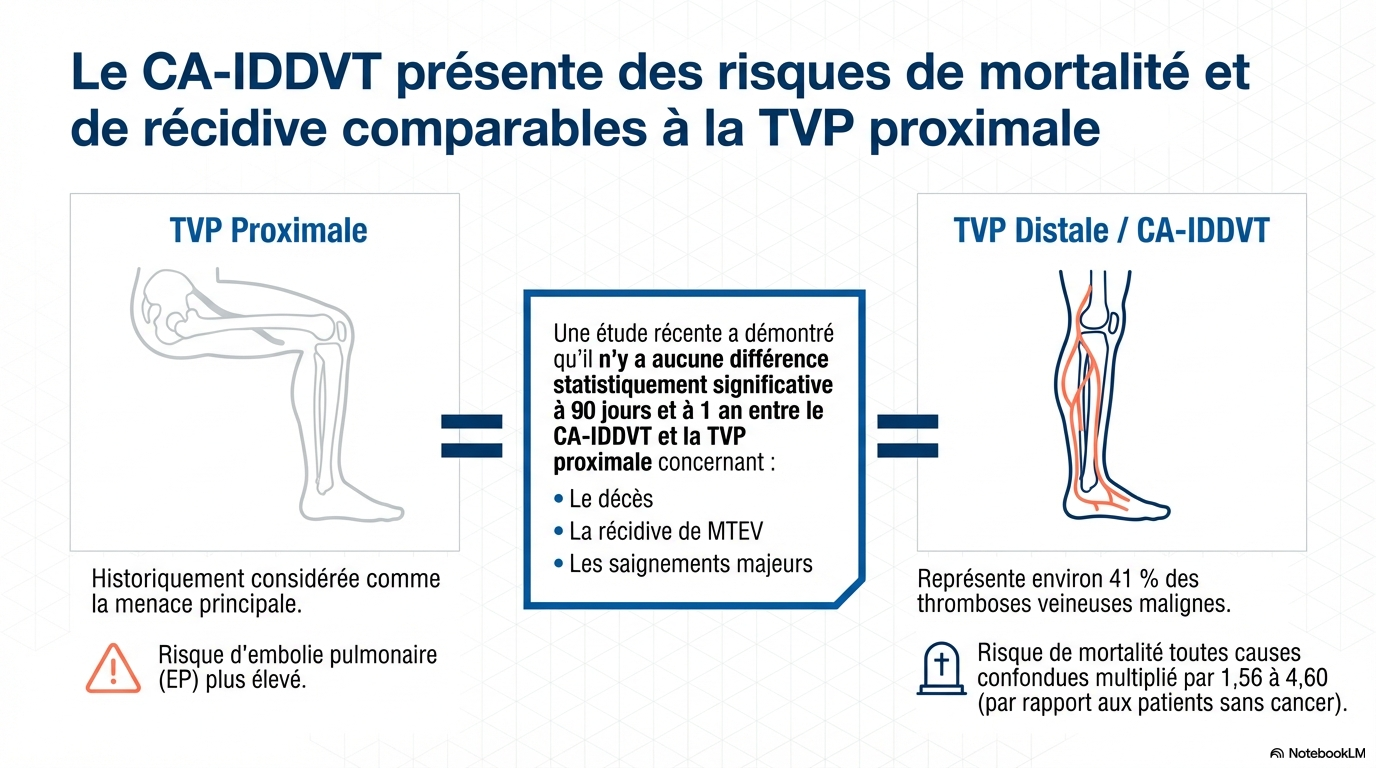


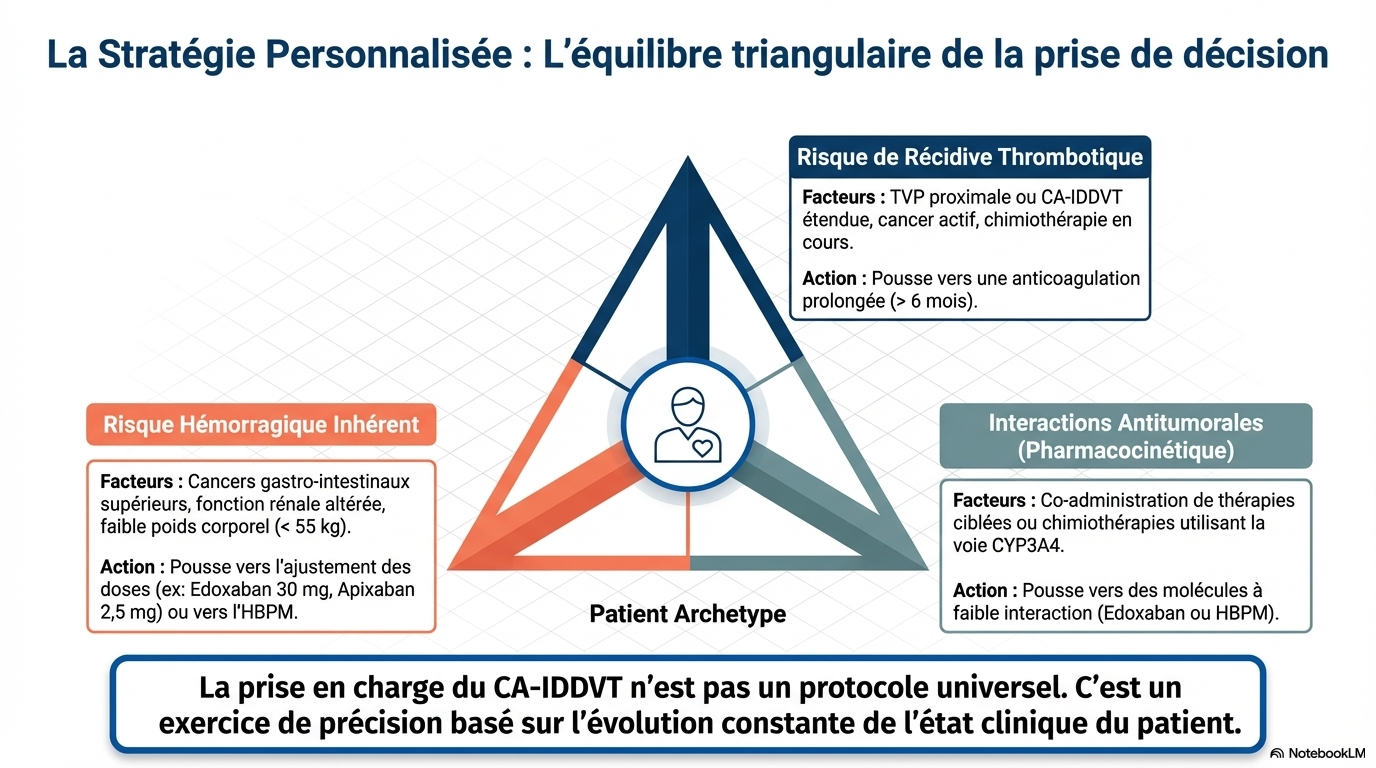

La survenue d'une TVP distale ou proximale au cours du cancer est un élément péjoratif
La TVP distale au cours du cancer doit être traitée comme une TVP proximale.
Le diagnostic d'une TVP distale ; écho-Doppler et non simple écho de compression.
Privilégier les AOD en dehors des CI et plus spécialement l'apixaban.
La durée de l'anticoagulation, au long cours tant que le cancer est actif.
Un élément important : la survenue au cours du cancer d'une TVP distale spontanée bilatérale ou d'une TVP distale associée à une TVS sur veine saine, pronostic du cancer grave.
Enfin et surtout, une TVP distale, tout comme une TVP proximale, avec ou sans embolie pulmonaire (EP) lors d'un cancer actif, constitue un facteur majeur de gravité.
API-CAT est possible pour les TVP au cours du cancer mais en débutant toujours par une "full-dose" au moins 3 mois voire 6 mois.
Pourra-t-on fabriquer des anticoagulants de dosages avec des posologies variable grâce à l'IA (étude in silico)


