MTEV
-
INNOVTE CAT / Indroductions
 Des RECOS majeures
Des RECOS majeures -
INNOVTE CAT / Patients fragiles
 Fragilité, ne jamais la sous estimer
Fragilité, ne jamais la sous estimer -
INNOVTE CAT/Soins Palliatifs
 Empathie, compassion, éthique, écoute....
Empathie, compassion, éthique, écoute.... -
INNOVTE CAT/T CEREBRALES
 Des incertitudes persistent mais moins !
Des incertitudes persistent mais moins ! -
INNOVTE/CAT : parcours de soins
 MTEV et Cancer une situation à risque
MTEV et Cancer une situation à risque -
ISTH 2022 en avant première : stress post traumatique post MTEV
 "Mais tout peut changer. Aujourd'hui, est le premier jour du reste de ta vie. "Etienne Daho"Rien ne vous emprisonne excepté vos pensées. Rien ne vous limite excepté vos peurs. Rien ne vous contrôle excepté vos croyances "Marianne Williamson
"Mais tout peut changer. Aujourd'hui, est le premier jour du reste de ta vie. "Etienne Daho"Rien ne vous emprisonne excepté vos pensées. Rien ne vous limite excepté vos peurs. Rien ne vous contrôle excepté vos croyances "Marianne Williamson
ABSTRACTPatients Reporting of Post-Traumatic Stress Disorder After Experiencing Venous Thromboembolic Event
Patients signalant un trouble de stress post-traumatique après avoir subi un événement thromboembolique veineux
R. Rosovsky 1 , W. Robertson 2 , F. Klok 31 Massachusetts General Hospital and Harvard Medical School, Newton, Massachusetts, États-Unis, 2 National Blood Clot Alliance, Philadelphie, Pennsylvanie, États-Unis, 3 Leiden University Medical Center, Leiden, Pays-Bas, Leiden, Zuid-Holland, Pays-BasRendez-vous : Congrès ISTH 2022Contexte: L'objectif principal des soins pour les patients atteints de maldie thromboembolique veineuse (MTEV) est de prévenir la récidive de la MTEV, les saignements majeurs et la mort. Bien que ceux-ci soient très pertinents, ils ne saisissent pas les résultats pertinents pour le patient tels que la qualité de vie (QOL) et les capacités fonctionnelles.Objectifs: Évaluer le degré dtrouble de stress post tarumatique (SSPT) chez les patients MTEV et son impact sur la qualité de vie et les capacités fonctionnelles.Méthodes: La liste de contrôle du trouble de stress post-traumatique (SSPT) - version civile (PCL-C) était l'un des douze instruments validés inclus dans une enquête anonyme visant à explorer les limitations fonctionnelles, la douleur, la dyspnée, la dépression et le SSPT chez les patients atteints de MTEV. L'enquête a été placée sur le site Web de la National Blood Clot Alliance et en ligne via Facebook, Instagram, LinkedIn et Twitter™ pour mieux comprendre le degré et l'impact du SSPT chez les adultes (>/= 18 ans) diagnostiqués avec une embolie pulmonaire (EP), profonde thrombose veineuse (TVP) ou les deux.Résultats: 3372 personnes ont répondu à l'enquête entre août 2021 et janvier 2022 dont 86% étaient des femmes avec un âge moyen de 43 ans (extrêmes 18-70). 36 % et 22 % des répondants avaient une EP ou une TVP, respectivement, et 42 % avaient les deux. Plus de 50 % avaient eu leurMTEV il y a > 1 an et 79 % étaient sous anticoagulation.
Sur les 2714 personnes qui ont répondu à la partie post- traumatic stress disorder (PTSD) de l'enquête, 18,2 % ont signalé peu ou pas de symptômes de PTSD, 4,6 % ont signalé certains symptômes de PTSD, 33,7 % ont signalé des symptômes de PTSD modérés à modérément élevés et 43,6 % ont signalé une gravité élevée des symptômes de PTSD (Figure 1) .
Des analyses corrélant le SSPT avec la qualité de vie, la douleur, l'anxiété, la dépression et les capacités fonctionnelles sont en cours et seront disponibles d'ici la conférence.Conclusion(s) : Il s'agit de la plus grande enquête visant à étudier les effets émotionnels à long terme chez les survivants de MTEV. Le SSPT était fréquent parmi ce groupe de répondants hautement autosélectionnés. Les informations recueillies à partir de cette enquête constituent la première étape pour acquérir une compréhension plus large de cet important résultat et peuvent aider à orienter les recherches futures.
Trouble de stress post-traumatique après un événement thromboembolique veineux. Les participants ont été invités à indiquer à quel point ils ont été dérangés par le problème au cours du dernier mois.
ARTICLE 1
Cet abstract nous faire rebondir sur cet article :
Commentaire : Do physicians contribute to psychological distress after venous thrombosis?
Les médecins contribuent-ils à la détresse psychologique après une thrombose veineuse ? Kerstin De Wit, RPTH 23 January 2022https://doi.org/10.1002/rth2.12651
Commentaire à propos de : Hernandez-Nino J, Thomas M, Alexander AB, Ott MA, Kline JA. The use of qualitative methods in venous thromboembolism research. Research and Practice in Thrombosis and Haemostasis. 2021 Aug;5(6):e12593. DOI: 10.1002/rth2.12593. PMID: 34532630; PMCID: PMC8435525.Les médecins qui traitent la maladie thromboembolique veineuse (MTEV) peuvent ne pas considérer les séquelles de santé mentale telles que la détresse psychologique, la peur et l'anxiété comme relevant de leurs attributions spécialisées, bien que la plupart conviendraient qu'une prise en charge optimale de la MTEV entraîne un rétablissement complet du patient.
Les complications telles que l'hypertension pulmonaire thromboembolique chronique, le syndrome post-thrombotique et les hémorragies sont bien caractérisées dans la littérature sur la MTEV, et de nombreuses recherches se sont concentrées sur l'optimisation du traitement pour atténuer ces effets indésirables. Cependant, les patients qui ont présenté une embolie pulmonaire ou une thrombose veineuse profonde signalent systématiquement d'autres complications de santé mentale telles que l'anxiété, la dépression et le trouble de stress post-traumatique (1-3)
En fait, lorsque les patients atteints de MTEV sont interrogés sur leur expérience vécue, ils sont rarement préoccupés par leur rétablissement physique et se concentrent plutôt sur la détresse psychologique, l'inquiétude et le bien-être.Il existe un décalage entre les objectifs des médecins et les besoins des patients en ce qui concerne la prise en charge de la MTEV, un décalage qui ne peut plus passer inaperçu et ne pas être résolu. Les symptômes tels que l'anxiété sont plus fréquents chez les patients atteints de MTEV que chez les patients souffrant d'autres affections potentiellement mortelles telles que le syndrome coronarien aigu (4) .
Les thèmes récurrents contribuant à la détresse psychologique excessive comprennent la fréquence des erreurs de diagnostic d'embolie pulmonaire (2-3) les évaluations tardives, le fait de ne pas être pris au sérieux par les médecins et les informations incohérentes concernant le diagnostic.(5)Les patients qui signalent une détresse psychologique durable après une embolie pulmonaire sont plus susceptibles de se souvenir de leur diagnostic comme d'un événement traumatisant (1)
Dans ce numéro de Research and Practice in Thrombosis and Hemostasis , Hernandez-Nino et al. explore comment les professionnels de la santé peuvent à la fois causer et exacerber la détresse psychologique découlant d'un diagnostic de MTEV.
L'impact du choix du mot du médecin est frappant et brosse le tableau de médecins tellement immergés dans la gestion de la maladie qu'ils ne peuvent pas prendre du recul pour voir un patient qui ne comprend pas ce qui se passe et qui est exclu de la conversation.
Le jargon médical est inutile et déroutant pour les patients, tandis que des termes alarmistes comme « bombe à retardement »» contribuent à la peur et à la détresse des patients. Il s'agit d'un contraste frappant avec d'autres activités des médecins, telles que l'annonce de mauvaises nouvelles, où les médecins en formation développent des compétences de communication très pointues. Les médecins n'utiliseraient jamais des termes techniques tels que le code bleu lorsqu'ils annoncent un décès à un membre de la famille, ni n'utiliseraient des euphémismes tels que passé ou disparu .Hernandez-Nino et al. soulignent également un manque de partage efficace de l'information entre les acteurs de la santé et le patient (2-5) Ce manque d'information a été rapporté ailleurs, causant des sentiments d'abandon et de colère envers les médecins. Le manque d'information est un obstacle à la participation des patients aux décisions de prise en charge de la MTEV, donnant aux patients le sentiment d'être des spectateurs de leurs propres soins (2) Le manque de contrôle perçu qui en résulte peut accroître la méfiance à l'égard du monde de la santé, et il n'est pas rare que les patients recherchent de nouveaux médecins (2-5). Les patients décrivent le manque d'informations à tous les niveaux : depuis la physiopathologie de la MTEV, comme la compréhension de ce qu'est la MTEV et si elle peut provoquer un accident vasculaire cérébral ou une crise cardiaque (1), au pronostic attendu et aux modalités pratiques de retour au travail (2)
Les retombées du vide de l'information incluent la recherche d'informations sur Internet, les membres de la famille et d'autres prestataires de soins de santé. Cependant, la recherche sur Internet et les conseils des amis et de la famille exacerbent probablement l'anxiété.
Au lieu de s'attaquer à la racine du problème (manque d'informations sur la maladie), les médecins considèrent souvent les visites répétées des patients comme une nuisance.Aucun médecin ne voudrait être le véhicule de la détresse du patient, alors comment ces situations pourraient-elles se produire ? Paradoxalement, les tests d'embolie pulmonaire inquiètent les médecins. La peur de l'embolie pulmonaire est omniprésente dans la culture médicale (6) La plupart des urgentistes ne prennent en charge un patient atteint d'embolie pulmonaire aiguë qu'une fois tous les quelques mois et peuvent s'appuyer sur une équipe d'intervention en cas d'embolie pulmonaire pour déterminer la prise en charge aiguë.
Dans cette étude, les patients se souviennent de changements soudains dans le comportement des prestataires une fois le diagnostic connu : surveillance plus étroite, médecins supplémentaires et attitude plus sérieuse. Il est compréhensible que cela cause de la confusion chez les patients puisque rien de leur état n'a changé. Hernandez-Nino et al. montrent comment un déséquilibre entre la réassurance et l'alarme, associé à des informations peu ou incomplètes, peut créer l'environnement parfait pour la peur, la détresse et l'anxiété.Comment pouvons-nous faire mieux ? La connaissance de la situation du médecin est essentielle pour améliorer les résultats et la satisfaction des patients. Assumer la responsabilité des répercussions de la MTEV sur la santé physique et mentale devrait être notre objectif principal. De bonnes compétences en communication et de l'empathie sont au cœur de la solution. Rien ne remplace le fait de prendre le temps de parler avec les patients .
Fournir des informations et des messages cohérents, expliquer ce qu'est la MTEV (et ce qu'elle n'est pas), examiner comment elle est gérée et à quoi les patients peuvent s'attendre pendant leur rétablissement est d'une importance vitale. Ces conversations ne devraient pas être l'exception mais la règle pour chaque patient diagnostiqué avec une MTEV.
Les liens entre le comportement du médecin et la détresse du patientConcrètement, cela signifie que les médecins qui diagnostiquenr et traitent les patients atteints de MTEV doivent avoir une solide compréhension du pronostic du patient et des options thérapeutiques.
Lorsque diagnostic n'est pas clair sur ces questions, les patients doivent être rapidement évalués par un expert qui a le temps de partager cette information dans un environnement calme et ininterrompu.
Il est particulièrement important que les patients qui se présentent à nouveau aux services médicaux (leur médecin de famille, le service des urgences ou la clinique) voient leurs préoccupations prises au sérieux et aient plus de temps avec un expert pour examiner les informations sur leur diagnostic et leur traitement de MTEV.
Tous les patients doivent recevoir des informations standardisées et imprimées ainsi qu'un lien vers un site Web d'informations pour les patients et un groupe de soutien. Tout comme la médecine aborde la récupération physique de la MTEV, avec un peu de réflexion et d'empathie"
Références1 Tran A, Redley M, de Wit K. The psychological impact of pulmonary embolism: a mixed-methods study. Res Pract Thromb Haemos. 2021;5:301-307.2 Hunter R, Lewis S, Noble S, Rance J, Bennett PD. “Post-thrombotic panic syndrome”: a thematic analysis of the experience of venous thromboembolism. Br J Health Psychol. 2017;22:8-25.3 Noble S, Lewis R, Whithers J, Lewis S, Bennett P. Long-term psychological consequences of symptomatic pulmonary embolism: a qualitative study. BMJ Open. 2014;4:e004561.4 Moore T, Norman P, Harris PR, Makris M. Cognitive appraisals and psychological distress following venous thromboembolic disease: an application of the theory of cognitive adaptation. Soc Sci Med. 2006;63:2395-2406.5 Rolving N, Brocki BC, Andreasen J. Coping with everyday life and physical activity in the aftermath of an acute pulmonary embolism: a qualitative study exploring patients’ perceptions and coping strategies. Thromb Res. 2019;182:185-191.6 Zarabi S, Chan TM, Mercuri M, et al. Physician choices in pulmonary embolism testing. Can Med Assoc J. 2021;193:E38.
Cet article est très important , parce que tout ce qu'il rassemble, c'est la vie réelle. La MTEV est mal vécu par les médecins, le personnel de santé et les patients. Tout un chacun sait que l'embolie pulmonaire TUE et que la thrombose veineuse des MI peut se compliquer d'embolie pulmonaire.La MTEV est mal vécu par les patients . Ces deux stress cumulés sont très invalidants pour les patients.
L'abstract sus cité fait état du stress post traumatique induit par la survenue de la MTEV l' article 1 lui fait état du stress post traumatique surajouté par le comportement du médecin. Il est donc indispensable de RASSURER et RASSURER mais sans MINIMISER les faits.
ARTICLE 2Autre réflexion
“Whole life changed” - Experiences of how symptoms derived from acute pulmonary embolism affects life. A qualitative interview studyJenny S. Danielsbacka et coll, Thrombosis Research Volume 205, September 2021, Pages 56-62,
https://www.sciencedirect.com/science/article/pii/S0049384821003972#!
« Ma vie a changé » - Expériences de la façon dont les symptômes dérivés d'une embolie pulmonaire aiguë affectent la vie. Une étude qualitative par entretien
Les points forts de l'article
• Les symptômes respiratoires ont affecté de nombreux aspects de la vie des participants
• Les participants ont vécu des changements en eux-mêmes et dans leurs relations.
• L'affection psychologique des symptômes a entraîné une crise existentielle.
• Tous les participants ont connu des changements dans leur activité physique.
• La peur des symptômes inhibe l'activité physique.
En France l'équipe de Brest de Francis Couturaud ( @FCouturaud) s'est penchée aussi sur ce problème.
Dans la vraie vie les patients ayant présenté une MTEV : embolie pulmonaire et ou thrombose veineuse développent dans l'année sui suit un véritable choc traumatique psychologique et physique , ils ne vivent plus comme avant : "ma vie a changé " docteur.
Verbatim des patients :
- Depuis mon embolie pulmonaire j'ai arrêté le sport , j'ai peur de mobiliser un caillot (patient anticoagulé)
- Je suis anticoagulé , je reste à la maison depuis ma phlébite, j'ai peur de saigner spontanément et je crains une embolie
- Un chef d'entreprise : avant l'embolie pulmonaire je voyagé beaucoup pour mon travail, mainteeant non, ça me stresse, patient qui n'est plus anticoagulé, mais comme je vous l'ai précisé en cas de voyage on peut faire une prévention, ça ne change rien, j'appréhende.
Les patients developpent souvent mais pas tous une véritable psychose post MTEV et ce quelque soit le sexe, l'âge, les facteurs de co morbdités etc.
L'EP au décours de la Covid-19 c'est la "double peine d'anxiété" pour les patients, ne pas l'oublier.
Alors commant faire pour réduire ce traumatisme psychologique ?
Cela débute dès le premier jour du diagnostic,Annoncer ce diagnostic, est le plus souvent un coup de tonnerre dans un ciel serin, car la phlébite pour les patients , c'est grave, ça fait peur et c'est synonyme de mort, l'embolie pulmonaire est tout aussi bien connue et notamment sa gravité.Il est donc important au cours de la consultation de remettre les choses à leur place, car la phlébite dès qu'elle est annoncée, c'est immédiatement pour le patient toute une série de clichés de fausses idées et de mauvaises nouvelles :
* Une phlébite c'est grave, vous allez m' hospitaliser....le plus souvent aujourd'hui non
* Pourquoi je fais une phlébite alors que je n'en n'ai jamais fait ?
* Une phlébite, c'est rester immobile pendant combien de temps ?
* Une phlébite c'est synonyme d'arrêt de travail car je vais être immobilisé ?
* Comment va-t-on faire disparaître les caillots ?...le mot thrombus est plus approprié
* Les anticoagulants c'est dangereux , on ne va pas pouvoir m'arracher des dents ou m'opérer , je vais les prendre combien de temps les anticoagulants ,1 ou 2 jours ou toute ma vie (mon père en prend depuis 10 ans pour sa phlébite,(remarque informative)
* Est ce que l'aspirine c'est bon en cas de phlébite ?
* Est qu'on peut m'opérer pour enlever ce caillot ?
* Je ne vais plus pouvoir voyager en avion, aller à la montagne , m'exposer au soleil, voire conduire....Phlébite = arrêt de toute activité sportive,mais surtout c'est un arrêt de vivre normalement........j'en passe et des meilleurs.....mais c'est une réalité, la vraie vie .
Il faut donc dans un temps imparti dédramatiser et apporter des faits tangibles, tout simplement la vérité :
* Une phlébite est une atteinte potentiellement grave quand elle n'est pas traitée correctement.
* Nous disposons de plusieurs anticoagulants , le choix est du ressort du médecin qui gère la phlébite, ils agissent très rapidement. Ils ne font pas disparaître le "thrombus" mais ils évitent son extension et la migration vers les poumons.
* Enfin les anticoagulants ne sont pas du "Destop".
Outre les anticoagulants une compression médicale , bas ou mi bas est indispensable, classe 2 ou 3 , ne pas les porter le nuit.
Cette compression réduit l'oedéme, accélère le retour veineux et concoure à une repermébilisation du thrombus. Elle a de plus un effet antalgique. Enfin les études qui ont comparé alitement versus marche (compression et anticoagulation) n'on pas objectivé plus d'embolie pulmonaire.
Une phlébite doit marcher immédiatement dès que l'anticoagulation est débutée, marche avec compression. La phlébite "alitée" n'existe plus , saut cas exceptionnel. Le slogan "j'ai une phlébite, donc je marche " est à diffuser et à répéter sans cesse car la croyance de l'immobilisation a la vie dure, notamment dans l'entourage. C'est ainsi que l'on revoit des patients 1 mois après le diagnostic qui boitent et qui vous disent "Docteur, c'est la première fois que je marche depuis 1 mois"
* La gestion des anticoagulants autorise les interventions chirurgicales, les soins dentaires sans danger en prenant les précautions "ad hoc"
* Au décours de l'anticoagulation les voyages en avion sont autorisés comme les ballades en montagne . Mais les anticoagulants peuvent faire saigner donc pas de sports de contacts, VTT de descente etc.
* Les traitements dits "veinotoniques " sont inutiles
* Le "on m'a dit dans ma famille "que si c'était une phlébite c'est très grave, que je ne pourrais plus travailler etc......l'entourage est souvent délètère avec la phlébite.
Tout cela est évident mais à répéter pour chaque patient à chaque consultation ,chez lequel on vient de diagnostiquer une phlébite et oune embolie pulmonaire, dans ce contexte les patients sont très bavards après une phase muette post annonce du diagnostic.Il faut aussi connaître le "panique syndrome post phlébite".Attention tout patient et quelque soit son âge, qui présente une phlébite et ou une embolie pulmonaire, ne vit plus comme avant , il se croit "handicapé" dans les mois qui suivent voir dans les années qui suivent. Les patients "changent leurs habitudes" . Ils voyageaient , ils ne voyagent plus, ils prenaient l'avion , ils s'en abstiennent. Ils jouaient au tennis ou ils courraient , ils arrêtent tout. Ce panique syndrome est une réalité , bien décrit dans la littérature comme nous l'avons vu.La durée de l'anticoagulation n'est pas déterminé par l'écho-Doppler, car pour les patients plus de caillot, égal arrêt des anticoagulants. Il faut donc expliquer la notion de facteur déclenchant ou de son absence , ce qui va être informatif pour la durée de l'anticoagulation et la gravité de la phlébite.Autre point, l'explication de la survenue de cette phlébite car cette question est récurrente et c'est logique : "pourquoi Docteur ?" . Avant 50 ans on trouve le plus souvent un facteur déclenchant, au-delà cela devient plus complexe en dehors d'une chirurgie ou une immobilisation récente. Il est alors important d'expliquer les raisons de la réalisation de tel ou tel examen.
L'enquête à la recherche d'un étiologie est une véritable enquête policière.Ne pas oublier que tous les événements médicaux et chirurgicaux dans les 3 mois qui précédent le diagnostic peuvent en être la cause Tout examen prescrit doit étre expliqué et justifié, y compris si on recherche un cancer. Enfin tout patient anticoagulé doit avoir sur lui un document qui l'atteste.Il faut donc faire face à la phlébite et à l'embolie pulmonaire et dédramatiser la situation, être toujours dans le vrai et combattre les idées reçues qui existent encore. Attention à la "googlisation" des patients, à la limite leur donner des adresses de sites , ce que je fais régulièrement.Mais comment aller au delà quand ce "panique syndrome s'est installé" ?
Rassuer et encore rassurer mais ce n'est pas toujours suffisant.
L'activité physique en groupe qui fait peur au patient doit être conseillée. Les techniques comme le yoga, la relaxation sont très utiles comme toutes les techniques de prise en charge du stress post traumatique car c'est de cela qu'il s'agit.
Le traitement du syndrome de stress post-traumatique fait appel aux thérapies comportementales et cognitives, à l’EMDR, une technique de désensibilisation et de reprogrammation par les mouvements oculaires mise au point dans les années 1980 aux Etats-Unis, à l’hypnose ou à la sophrologie. Elles ont toutes montré une certaine efficacité dans son traitement.
L’hypnose peut être bénéfique sur les symptômes tels que l’anxiété, les cauchemars, ou les douleurs.
Certains médicaments antidépresseurs ont également une action bénéfique.Le médecin traitant, un psychologque sont des acteurs efficaces de cette prise en charge.
L'expérience de l'EMDR est très intéressante et donne de bons résultats (https://www.vidal.fr/maladies/psychisme/etat-stress-post-traumatique-espt/traitements.html
La prise en charge de la MTEV doit prévenir et ne pas occulter le stress lié à ce diagnostic, c'est la responsabilité du médecin d'être à l'écoute de ces patients. Il faut toujours être dans la VERITE +++++.
Le point de départ de ce dossier STRESS POST TRAUMATIQUE POST MTEV était l'abstact #ISTH2022 , il sera intéressant dans un second temps d'aller plus loin avec la communication in extenso.Cette thématique est majeure pour la MTEV et toutes ses conséquences, la PANIQUE SYNDROME POST MTEV existe !A relire
https://medvasc.info/1402-ma-vie-a-chang%C3%A9
https://medvasc.info/1583-thrombose-le-stress -
ITAC2022 : MTEV/CANCER/COVID19
 “Le meilleur de vos serviteurs est celui qui ne cherche pas à entendre de vous ce qu'il souhaite, mais à souhaiter ce qu'il a entendu.”Saint Augustin
“Le meilleur de vos serviteurs est celui qui ne cherche pas à entendre de vous ce qu'il souhaite, mais à souhaiter ce qu'il a entendu.”Saint Augustin
2022 international clinical practice guidelines for the treatment and prophylaxis of venous thromboembolism in patients with cancer, including patients with COVID-19,Dominique Farge, Corinne Frere, Jean M Connors, Alok A Khorana, Ajay Kakkar, Cihan Ay, Andres Muñoz, Benjamin Brenner, Pedro H Prata, Dialina Brilhante, Darko Antic, Patricia Casais, María Cecilia Guillermo Esposito, Takayuki Ikezoe, Syed A Abutalib, Luis A Meillon-García, Henri Bounameaux, Ingrid Pabinger, James Douketis, the International Initiative on Thrombosis and Cancer (ITAC) advisory panel,Lancet Oncol 2022; 23: e334–47, https://www.ncbi.nlm.nih.gov/pmc/articles/PMC9236567/pdf/main.pdf, article libre d'accès
Recommandations internationales de pratique clinique 2022 pour le traitement et la prophylaxie de la maladie thromboembolique veineuse (MTEV) chez les patients atteints de cancer, y compris les patients atteints de COVID-19
The International Initiative on Thrombosis and Cancer (ITAC)est un groupe de travail universitaire indépendant d'experts visant à établir un consensus mondial pour le traitement et la prophylaxie de la thrombose associée au cancer.
Les lignes recommandations de pratique clinique 2013, 2016 et 2019 d'ITAC ont été mises à disposition via une application Web gratuite pour téléphone mobile. Les recommandations de pratique clinique de 2022, qui sont basées sur une revue de la littérature jusqu'au 1er janvier 2022, comprennent des conseils pour les patients atteints de cancer et de COVID-19.
Les principales recommandations (grade 1A ou 1B) comprennent :
- (1) les héparines de bas poids moléculaire (HBPM) pour le traitement initial (10 premiers jours) et le traitement d'entretien de la thrombose associée au cancer ;
- (2) des anticoagulants oraux directs pour le traitement initial et le traitement d'entretien de la thrombose associée au cancer chez les patients qui ne sont pas à haut risque d'hémorragie gastro-intestinale ou génito-urinaire, en l'absence d'interactions médicamenteuses fortes ou de troubles de l'absorption gastro-intestinale ;
- (3) HBPM ou anticoagulants oraux directs pendant au moins 6 mois pour traiter la thrombose associée au cancer ;
(4) une prophylaxie prolongée (4 semaines) avec des HBPM pour prévenir la MTEV postopératoire après une chirurgie abdominopelvienne majeure chez les patients ne présentant pas de risque élevé de saignement ;
(5) la prophylaxie primaire de la MTEV avec des HBPM ou des anticoagulants oraux directs (rivaroxaban ou apixaban) chez les patients ambulatoires atteints d'un cancer du pancréas localement avancé ou métastatique qui sont traités par un traitement anticancéreux et ont un faible risque de saignement. en l'absence d'interactions médicamenteuses fortes ou d'altération de l'absorption gastro-intestinale ;
LES RECOMMANDATIONS dans le détail

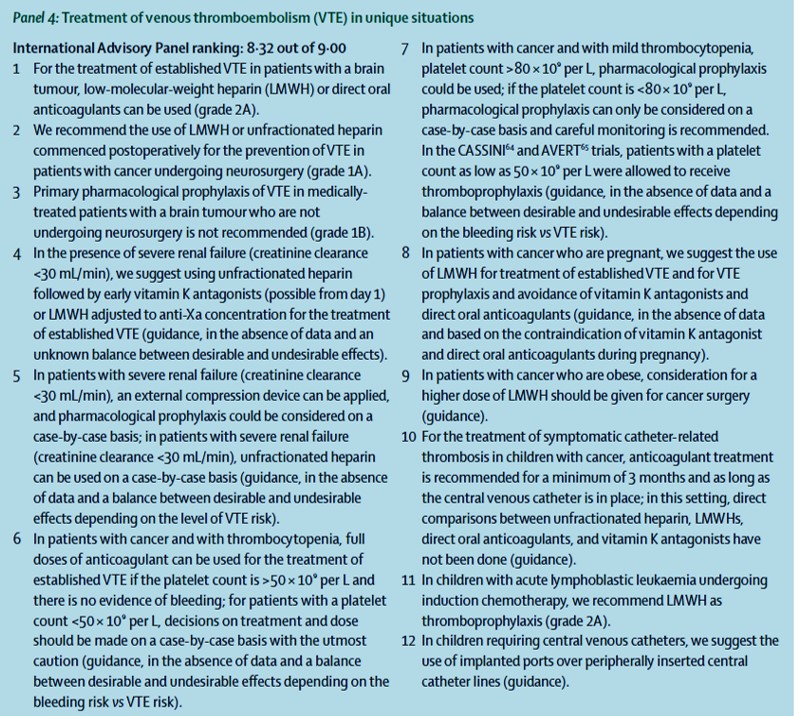
 COVID/CANCER/MTEV
COVID/CANCER/MTEV
The CoVID-TE risk assessment model for venous thromboembolism in hospitalized patients with cancer and COVID-19, Ang Li et coll, J Thromb Haemost. 2021;19:2522–2532., accès libre : https://onlinelibrary.wiley.com/doi/10.1111/jth.15463Un score de risque de MTEV chez les patients porteurs à la fois d'un cancer et de la Covid-19 , ou comment quantifier ce sur risque
Le contexte
Les patients hospitalisés atteints de COVID-19 présentent des risques accrus de maladie thromboembolique veineuse (MTEV) et artérielle (TEA). Le diagnostic et le traitement actif du cancer sont des facteurs de risque bien connu. Cependant, un modèle d'évaluation des risques par un score pour la MTEV chez les patients atteints à la fois de cancer et de COVID-19 fait défaut.
Objectifs
Évaluer l'incidence et les facteurs de risque de thrombose chez les patients hospitalisés atteints de cancer et de COVID-19.
Méthodes
Parmi les patients atteints de cancer dans l'étude de cohorte COVID-19 et Cancer Consortium Registry (CCC19), les auteurs évalué l'incidence de la MTEV et de l'ETA dans les 90 jours suivant l'hospitalisation associée au COVID-19. Un modèle de régression logistique multivariable spécifiquement pour la MTEV a été construit en utilisant des facteurs de risque cliniques déterminés a priori. Un score simplifié a été dérivé et validé en interne à l'aide de bootstrap.
Résultats
Du 17 mars 2020 au 30 novembre 2020, 2804 patients hospitalisés ont été analysés de manière rétrospective. L'incidence de la MTEV et de l'ETA était respectivement de 7,6 % et 3,9 %. L'incidence de la MTEV, mais pas de l'ETA, était plus élevée chez les patients recevant récemment un traitement anticancéreux. Un score simplifié de MTEV a été dérivé et nommé Covid-TE ( C ancer sous - type risque élevé à très élevé par le score de Khorana, score de +1, V histoire TE 2, I admission CU 2, D -dimer altitude +1, récente anti-cancer systémique T herapy +1 et non-hispaniques E thnicity +1). Le score a stratifié les patients en deux cohortes (à faible risque, 0–2 points, n = 1423 vs. à haut risque, 3+ points, n = 1034) où la MTEV est survenue chez 4,1 % des patients à faible risque et 11,3 % des patients à haut risque (statistique c 0,67, intervalle de confiance à 95 % 0,63-0,71). le score a donné de bons résultats de manière similaire dans les sous-groupes de patients ne prenant pas d'anticoagulants avant l'admission et les patients modérément malades ne nécessitant pas d'admission directe en USI.
Rappel : Score de KHORANA (https://www.researchgate.net/figure/Khorana-score-risk-factors-predictive-model-for-chemotherapy-associated-venous_tbl1_343241456)
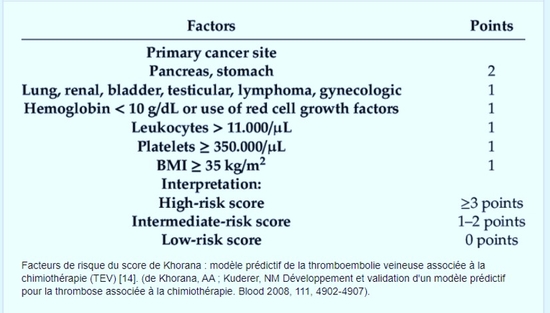
Le score CoVID-TE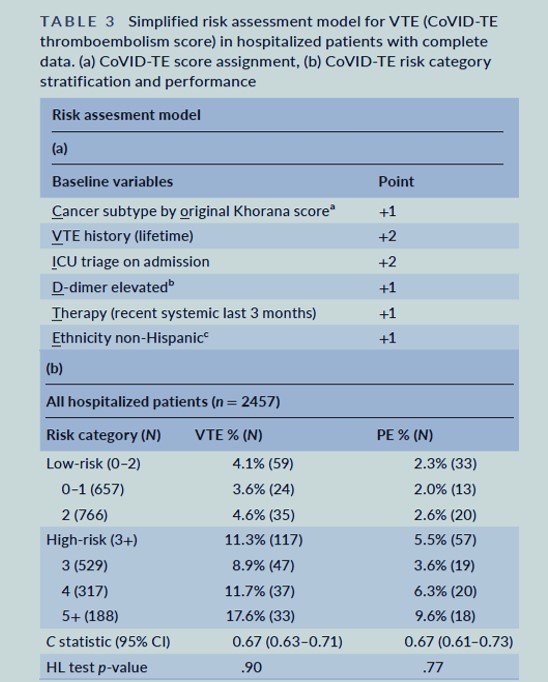
Conclusion
Les patients hospitalisés atteints de cancer et de COVID-19 présentent des risques thrombotiques élevés. Le score CoVID-TE pour la prédiction de la MTEV peut aider à prendre des décisions basées sur les données en temps réel dans cette population vulnérable.
Le risque exact de MTEV chez les patients atteints de cancer et de COVID-19 est inconnu.
Les auteurs ont évalué l'incidence de la MTEV et dérivé un modèle d'évaluation des risques (RAM), ou score dans le consortium CCC19. Les patients hospitalisés atteints à la fois d'un cancer actif et de COVID-19 ont un risque élevé de MTEV (7,6%). Un score de MTEV nouvellement dérivée à l'admission (CoVID-TE) peut stratifier le risque des patients (11,3 % contre 4,1 %). Ce qui est important pour ce type de score, plus que le score lui même ce sont les items du score. L'originalité est d'avoir inclu le score de Khorana et l'orientation en réanimation à partir de la gravité des patients, le tri des patients, si important. C'est une approche intéressante mais qui ne résoud pas tout," on avance pas à pas vers la connaissance" : quelle type de prévention par HBPM et à quelle dose compte tenu de ce score ? Une analyse précise des différentes thérapies du cancer sont aussi importantes. Ce que l'on sait depuis longtemps : le cancer augmente le risque de MTEV, les traitements du cancer aussi et enfin la Covid-19 aussi. Mais est - il possible de quantifier avec précision la sommation de ces 3 risques ? Ce qui est certain c'est que dans une telle situation la prévention de la MTEV s'impose obligatoirement , mais avec encore la même question : à quelle dose ? Pour combien de temps ? Avec quelle molécule ? Les auteurs préviennent que le score CoVID-TE, après validation externe, peut servir d'outil d'aide à la décision clinique en temps réel pour aider à des décisions personnalisées sur l'initiation de la thromboprophylaxie chez les patients hospitalisés atteints de cancer et de COVID-19. Une étude de plus qui fait avancer nos connaissances dans le bon sens. Retenez les items de de ce score afin de mieux décider notamment en RCP dans ce contexte qui reste compliqué. La fonction rénale est à ne pas oublier comme les traitements associés hors cancer et l'évaluation du risque hémorragique.
La COVID-19 vient compliquer le cancer qui lui même reste très compliqué. Aussi il est très important qu'un score ait la propriété de prévenir......qu'il est possible de mieux prévenir.
Commentaire
Belle actualisation des recommandations MTEV/CANCER et Cancer /Covid-19. Ce que l'on constate c'est la prise de pouvoir des AOD , ce qui est normal compte tenu des différentes études qui ont confirmé leur action positive en cas de MTEV et Cancer. Bine entendu les contre indications que l'on connaît bien maintenant sont rappelés. Le risque hémorragique en cas de cancer gastro intestinaux en place, les interactions médicamenteuses AOD et traitemenst des cancers. Quant à l'association Cancer/Covid-19, la prévention de la MTEV est très importante. En cas de MTEV installée, le traitement anticoagulant rest classique. Si les AOD sont très présents , les HBPM gardent encore une place significative. Un bémol en cas de MTEV et Cancer, en phase aigue le reciurs aux AOD dans la vraie vie est de plus en plus fréquente.Le recours à une RCP ONCO-THROMBOSE est de plus en plus fréquente surtout pour le choix entre HBPM et AOD , de plus la durée de l'anticiagulation fait aussi le débat. C'est au cas par cas que l'on solutionne les problèmes.Je rajouterai que la Covid-19 a générer des retards de prise en charge des patients atteints de cancer très préjudiciables.
La place des AOD "low dose " sera définitivement réglée quand API-CAT sera terminée (Pr Isabelle Mahé). Pour l'instant si on prescrit un AOD, il faut le prescrire à la dose "normale" et éviter des "cuisines personnelles" . Mais là encore dans la vrie vie les AOD "low dose" en cas de MTEV et Cancer sont prescrits, peu , mais prescrits.
La VIE REELLE en avance sur les recommandations ?
Ce qui est intéressant c'est l'évolution régulière des recommandations depuis 2013, évolution attendue et nécessaire.
Il serait intressant et nécessaire que ITAC ait un compte TWEETER poour assurer une meilleure diffusion des recommandations et de ses activités ainsi qu'un compte LINKEDIN ainsi que les leaders d'ITAC, Merci !
Appli SMARTPHONE: https://www.itaccme.com/wp-content/uploads/2021/04/Fr-2019-GFTC-pocket-CPGs_CF31122019.pdf -
L'OURS & la MTEV font la une !
 Petit ours Brun à la TV
Petit ours Brun à la TV -
le BON SENS : âge et MTEV
 Registre Riete
Registre Riete -
Les DDimères rebondissent
 Une avancée dans le diagnostic du cancer en cas de MTEV
Une avancée dans le diagnostic du cancer en cas de MTEV -
Les HBPM ne sont pas anticancéreux : la confirmation définitive
 iconographie : cancer cycle
iconographie : cancer cycle
“La recherche fondamentale ne peut être pratiquée que dans un climat de liberté intellectuelle.”Pierre Joliot
“Chercher n'est pas une chose et trouver une autre, mais le gain de la recherche, c'est la recherche même." Saint Grégoire de Nysse
Efficacy and safety of extended duration to perioperative thromboprophylaxis with low molecular weight heparin on disease-free survival after surgical resection of colorectal cancer (PERIOP-01): multicentre, open label, randomised controlled trial,
Efficacité et sécurité d'une durée prolongée de la thromboprophylaxie périopératoire par héparine de bas poids moléculaire sur la survie sans maladie après résection chirurgicale du cancer colorectal (PERIOP-01) : essai multicentrique, ouvert et contrôlé randomisé
Rebecca C Auer et Coll, BMJ 2022; 378 doi: https://doi.org/10.1136/bmj-2022-071375 (Published 13 September 2022)Cite this as: BMJ 2022;378:e071375
Objectif
Déterminer l'efficacité et l'innocuité d'une thromboprophylaxie périopératoire prolongée par héparine de bas poids moléculaire lors de l'évaluation de la survie sans maladie chez les patients subissant une résection pour cancer colorectal.Conception
Essai multicentrique, ouvert, contrôlé randomisé.12 hôpitaux du Québec et de l'Ontario, Canada, entre le 25 octobre 2011 et le 31 décembre 2020.Participants 614 adultes (âge ≥ 18 ans) étaient éligibles avec un adénocarcinome invasif du côlon ou du rectum confirmé pathologiquement, aucun signe de maladie métastatique, une concentration d'hémoglobine ≥ 8 g/dL et devaient subir une résection chirurgicale.Interventions
Attribution aléatoire à une thromboprophylaxie de durée prolongée utilisant de la tinzaparine sous-cutanée quotidienne à 4500 UI, commençant à la décision d'opérer et se poursuivant pendant 56 jours après l'opération, par rapport à la thromboprophylaxie postopératoire en milieu hospitalier uniquement.Principaux critères de jugement
Le critère de jugement principal était la survie sans maladie à trois ans, définie comme la survie sans récidive locorégionale, métastases à distance, deuxième primaire (même cancer), deuxième primaire (autre cancer) ou décès. Les critères de jugement secondaires comprenaient la thromboembolie veineuse, les complications hémorragiques majeures postopératoires et la survie globale à cinq ans. Les analyses ont été faites dans la population en intention de traiter.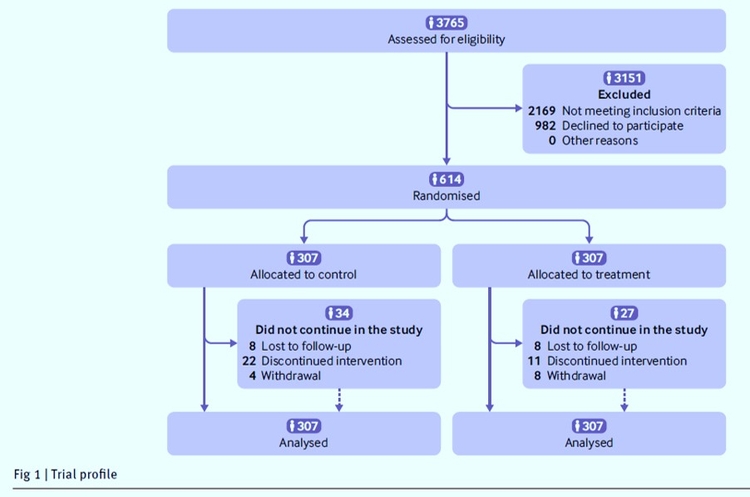
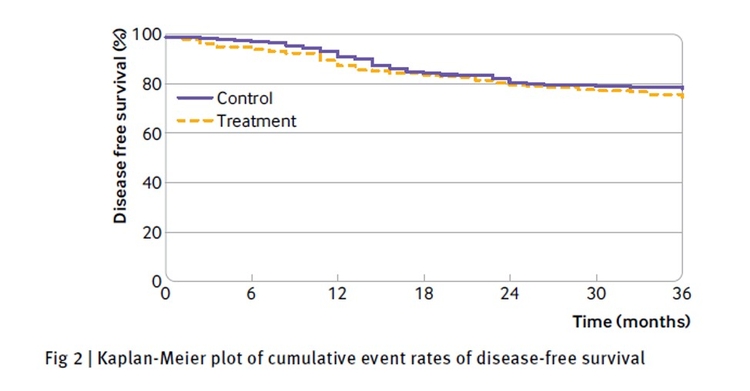 Résultats
Résultats
L'essai a arrêté le recrutement prématurément après l'analyse intermédiaire de futilité. Le critère de jugement principal est survenu chez 235 (77 %) des 307 patients du groupe de durée prolongée et chez 243 (79 %) des 307 patients du groupe de thromboprophylaxie à l'hôpital (risque relatif 1,1, intervalle de confiance à 95 % de 0,90 à 1,33 ; P= 0.4). Une thromboembolie veineuse postopératoire est survenue chez cinq patients (2 %) dans le groupe durée prolongée et chez quatre patients (1 %) dans le groupe thromboprophylaxie hospitalière (P = 0,8). Une hémorragie majeure liée à la chirurgie au cours de la première semaine postopératoire a été signalée chez une personne (<1 %) dans la durée prolongée et chez six personnes (2 %) dans le groupe thromboprophylaxie à l'hôpital (P = 0,1).Conclusions
La durée prolongée de l'anticoagulation périopératoire avec la tinzaparine n'a pas amélioré la survie sans maladie ou la survie globale chez les patients atteints d'un cancer colorectal subissant une résection chirurgicale par rapport à la thromboprophylaxie postopératoire en hospitalisation seule. Les incidences de thromboembolie veineuse et d'hémorragie majeure postopératoire étaient faibles et similaires entre les groupes.
Qu'est-ce qu'on sait déjà à ce sujet
L'héparine de bas poids moléculaire atténue les métastases cancéreuses dans des modèles précliniques et a été reproduite dans de nombreux modèles animaux
Cet effet ne s'est pas traduit par une réduction des métastases ou une amélioration des résultats du cancer chez les patients
La période périopératoire pourrait être le cadre idéal pour étudier les effets antimétastatiques de l'héparine de bas poids moléculaire, car la chirurgie entraîne un état d'hypercoagulabilité et une incapacité à éliminer la maladie micrométastatique, entraînant une récidive potentielle du cancer et une pire survie.
Ce que cette étude ajoute
La durée prolongée de la thromboprophylaxie périopératoire avec la tinzaparine n'entraîne pas d'amélioration de la survie sans maladie à trois ans par rapport à la thromboprophylaxie à l'hôpital chez les patients atteints d'un cancer colorectal invasif localisé sans signe de maladie métastatique qui étaient éligibles pour subir une résection chirurgicale
Les taux de thromboembolie veineuse et de complications hémorragiques majeures postopératoires étaient faibles dans cette population de patients et similaires entre les groupes
Retour en arrière.....du temps où on croyait aux vertus anti tumorales des HBPM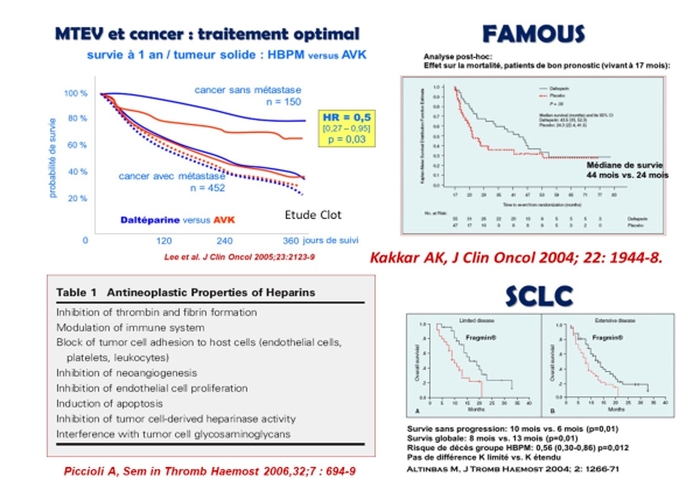
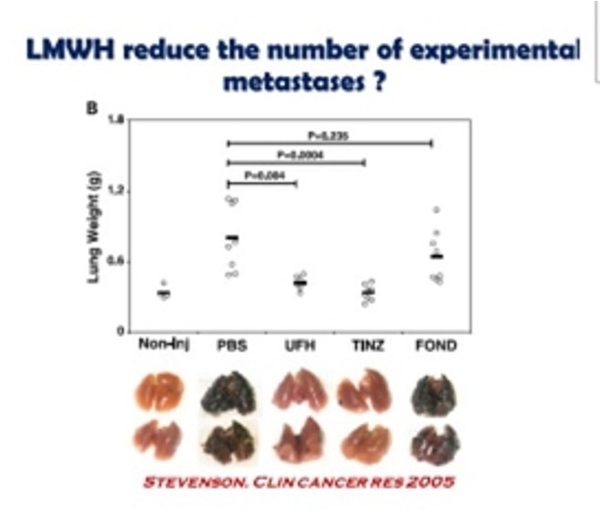
CommentaireGuy Meyer a été le premier (une fois encore) a démontrer que les HBPM n'avaient pas de proriétés anti carcinologioques dans l'étude TILT sur le cancer du poumon. Résultats de l'étude TILT publiés en 2018
Effet anti-tumoral de l'héparine de bas poids moléculaire dans le cancer pulmonaire localisé : un essai clinique de phase III, Tilt Trial, Guy Meyer et Coll, Eur Respir J
.4 octobre 2018;52(4):1801220. doi : 10.1183/13993003.01220-2018.
https://erj.ersjournals.com/content/52/4/1801220.long
Article libre d'accés
Voici le résumé de cet article...qui a écrit l'histoire celle de la saga HBPM/MTEV/Cancer
Les propriétés anti-tumorales et anti-métastatiques des héparines n'ont pas été testées chez les patients atteints d'un cancer à un stade précoce. L'impact de la tinzaparine sur la survie des patients atteints d'un cancer du poumon non à petites cellules (NSCLC) réséqué a été étudié.Les patients atteints d'un CPNPC de stade I, II ou IIIA complètement réséqué ont été répartis au hasard pour recevoir de la tinzaparine sous-cutanée 100 UI·kg −1 une fois par jour pendant 12 semaines ou aucun traitement en plus des soins standards. L'essai était ouvert avec une décision centrale en aveugle sur les résultats de l'étude. Le critère de jugement principal était la survie globale.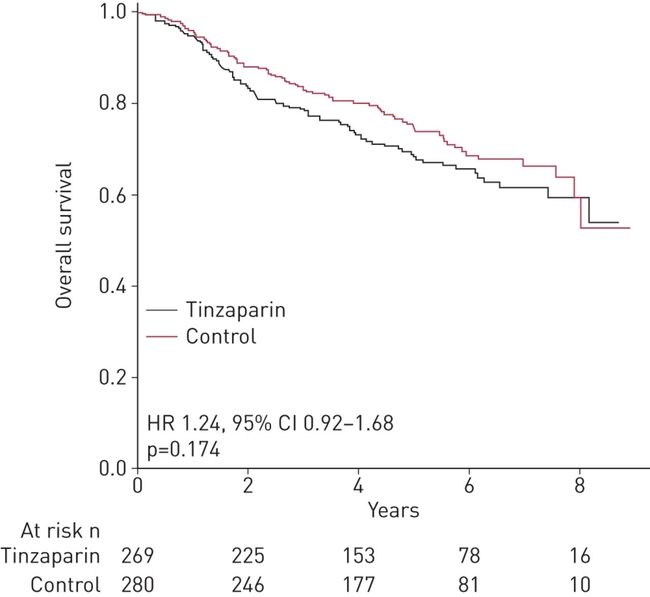 Survie globale dans la population en intention de traiter. Estimations de Kaplan-Meier de la survie globale selon le groupe de traitement dans la population en intention de traiter. La survie globale à 5 ans a été estimée à 68,2 % (IC à 95 % 62,5–74,4 %) dans le groupe tinzaparine contre 74,2 % (IC à 95 % 68,9–79,9 %) dans le groupe témoin. La valeur de p a été calculée à l'aide du test du log-rank. HR : rapport de risque.Chez 549 patients randomisés pour recevoir la tinzaparine (n = 269) ou le groupe témoin (n = 280), l'âge moyen ± sd était de 61,6 ± 8,9 ans, 190 (34,6 %) patients avaient une maladie de stade II-III et 220 (40,1 %) patients ont reçu chimiothérapie adjuvante. Le suivi médian était de 5,7 ans. Il n'y avait pas de différence significative dans la survie globale entre les groupes (risque relatif (HR) 1,24, IC à 95 % 0,92-1,68 ; p = 0,17). Il n'y avait aucune différence dans l'incidence cumulée des récidives entre les groupes (sous-distribution HR 0,94, IC à 95 % 0,68-1,30 ; p = 0,70).La tinzaparine adjuvante n'a eu aucun impact détectable sur la survie globale et sans récidive des patients atteints d'un CPNPC de stade I-IIIA complètement réséqué. Ces résultats ne supportent pas une évaluation clinique plus poussée des HBPM en tant qu'agents anti-tumoraux.
Survie globale dans la population en intention de traiter. Estimations de Kaplan-Meier de la survie globale selon le groupe de traitement dans la population en intention de traiter. La survie globale à 5 ans a été estimée à 68,2 % (IC à 95 % 62,5–74,4 %) dans le groupe tinzaparine contre 74,2 % (IC à 95 % 68,9–79,9 %) dans le groupe témoin. La valeur de p a été calculée à l'aide du test du log-rank. HR : rapport de risque.Chez 549 patients randomisés pour recevoir la tinzaparine (n = 269) ou le groupe témoin (n = 280), l'âge moyen ± sd était de 61,6 ± 8,9 ans, 190 (34,6 %) patients avaient une maladie de stade II-III et 220 (40,1 %) patients ont reçu chimiothérapie adjuvante. Le suivi médian était de 5,7 ans. Il n'y avait pas de différence significative dans la survie globale entre les groupes (risque relatif (HR) 1,24, IC à 95 % 0,92-1,68 ; p = 0,17). Il n'y avait aucune différence dans l'incidence cumulée des récidives entre les groupes (sous-distribution HR 0,94, IC à 95 % 0,68-1,30 ; p = 0,70).La tinzaparine adjuvante n'a eu aucun impact détectable sur la survie globale et sans récidive des patients atteints d'un CPNPC de stade I-IIIA complètement réséqué. Ces résultats ne supportent pas une évaluation clinique plus poussée des HBPM en tant qu'agents anti-tumoraux.
L'étude PERIOP-O1 (CANADA) ne fait que confirmer ce que l'on savait pour le cancer du poumon dans le cancer du colon.
Ce qu'il faut retenir définitivement : aucun anticoagulant (Héparine, HBPM, AVK ,AOD, Fondaparinux) n'ont un effet anticarcinologique. Aucun d'eux n'augmentent la survie des patients atteints de cancer. Ils traitent la MTEV complication du cancer , mais ils ne traitent pas le cancer.
En 2020 l'équipe de Sainté Etienne, Silvy Laporte and Co publie une méta anlyse sur ce sujet :
Malgré des données expérimentales à l'appui et des résultats cliniques précoces, l'effet antitumoral prometteur des HBPM chez les patients atteints de cancer s'est progressivement estompé au fil du temps vers une absence d'impact sur la survie globale. Ce résultat suggère un "p-hacking" et un rapport sélectif des résultats positifs des analyses de sous-groupes post hoc dans les premières études.
L'outil de méta-analyse cumulative permet de mettre en évidence précocement
l'absence d'effet antitumoral des HBPM sur le la survie des patients atteints de cancer et la stabilité de cette résultat depuis plusieurs années.
On doit refermer la page HBPM et activité anticarcinologique de manière définitive.
A savoirRémission ou rémission complète ?
Au cours de la prise en charge médicale d’un cancer, différents bilans sont pratiqués pour évaluer le résultat des traitements. Et ce jusqu’à la rémission complète, lorsque plus aucun examen ne montre la trace d’un quelconque résidu de cancer.Mais, même à ce stade, le malade n’est pas nécessairement au bout de ses peines, car un résultat d'examen "normal" peut avoir deux significations.* Soit toutes les cellules cancéreuses ont été éliminées ou détruites. Aucune récidive ne se manifestera ultérieurement et le malade est définitivement guéri.
* Soit quelques cellules malignes ont survécu, mais elles sont trop petites pour être détectées quels que soient les examens pratiqués. Au fil des multiplications de ces cellules cancéreuses résiduelles, la maladie va tôt ou tard récidiver.
Même si cela semble parfois difficile à admettre, la rémission ne permet donc pas nécessairement d’interrompre les traitements. C'est cependant une étape importante qui doit encourager la poursuite des traitements, puisqu’on peut tabler sur une efficacité démontrée.Rémission complète ou guérison ?
Pour déterminer si une rémission complète est ou non synonyme de guérison, il n'y a qu'une seule solution : attendre et surveiller. Au fil du temps, si aucune récidive du cancer ne se manifeste, on considérera que la guérison est définitive.
Combien de temps faudra-t-il attendre avant de parler de guérison ?
Tout dépend du type de cancer. Arbitrairement, la barre a été fixée à 5 ans, mais il n’est pas toujours nécessaire de patienter aussi longtemps pour parler de guérison. À l’inverse, dans de rares cas, une récidive reste possible après plus de 5 ans. Demandez à votre médecin ce qu’il en est pour votre cas particulier. En règle générale, plus une rémission se prolonge, plus il y a de chances d’être définitivement guéri.
https://www.cancer.be/les-cancers/r-mission-de-quoi-s-agit-ilA LIRE -
MORPHEUS
 MTEV Récidine MORHEUS
MTEV Récidine MORHEUS -
MTEV : événements CV ? Place des AOD ?
“La vie elle-même change tellement vite. C'est tellement difficile aujourd'hui de faire des pronostics sur ce que seront les choses dans dix ans. ” Simone VeilAnticoagulation for Venous Thromboembolism: Impact on the Risk of Major Adverse Cardiovascular Events
Noumegni SR, Le Mao R, de Moreuil C, Hoffmann C, Le Moigne E, Tromeur C, Mansourati V, Nasr Md B, Gentric JC, Guegan M, Poulhazan E, Bressollette L, Lacut K, Didier R, Couturaud F. Anticoagulation for Venous Thromboembolism: Impact on the Risk of Major Adverse Cardiovascular Events. Chest. 2022 Jun 14:S0012-3692(22)01087-X. doi: 10.1016/j.chest.2022.05.038. Epub ahead of print. PMID: 35714709.
https://pubmed.ncbi.nlm.nih.gov/35714709/
Anticoagulation pour la thromboembolie veineuse : impact sur le risque d'événements cardiovasculaires indésirables majeurs
Résumé
Contexte
Il a été récemment établi que les patients qui ont développé une maladie thromboembolique veineuse (MTEV) courent un risque accru d'événements cardiovasculaires indésirables majeurs (MACE) par rapport à la population générale. Cependant, la question de savoir si l'anticoagulation utilisée pour la MTEV influence le risque de MACE reste non décrite.Question de recherche
Le traitement anticoagulant de la MTEV a-t-il un impact sur le risque de MACE ultérieur ?Design et méthodes de l'étude
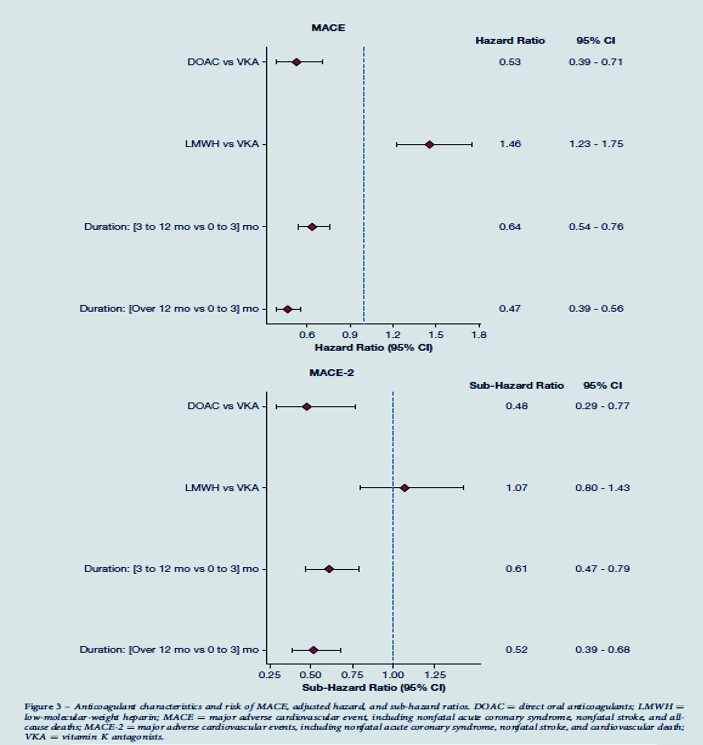
Nous avons inclus des patients d'une large cohorte prospective, n'ayant reçu qu'une seule famille de traitement anticoagulant après la phase aiguë de TEV, parmi lesquels, anti-vitamine K (AVK), et anticoagulants oraux directs (AOD). Les MACE comprenaient le syndrome coronarien aigu non mortel, l'AVC non mortel et le décès toutes causes confondues. Le critère de jugement secondaire, MACE-2, incluait les décès cardiovasculaires au lieu des décès toutes causes confondues. Les modèles Cox proportionnel et Fine-Gray ont servi à étudier la relation entre les caractéristiques d'anticoagulation et le risque de résultats.Résultats
Au total, 3790 patients (47,2 % d'hommes, âge moyen : 60,48 ans) ont été inclus. 1228 patients (32,4%) ont été traités pendant 0 à 3 mois (médiane dans la population globale : 6 mois). Comparativement à ces patients, ceux traités pendant 3 à 12 mois (HR : 0,64, IC 95 % : 0,54 - 0,76) ou sur 12 mois (HR : 0,47, IC 95 % : 0,39 - 0,56) avaient un risque significativement réduit de MACE après ajustement pour les facteurs de confusion. Les résultats étaient similaires pour MACE-2 (HR-3-12 mois : 0,61, IC à 95 % : 0,47 - 0,79 ; HR-sur 12 mois : 0,52, IC à 95 % : 0,39 - 0,68). Après ajustement pour les facteurs de confusion, il y avait un risque réduit de MACE (HR : 0,53, IC à 95 % : 0,39 - 0,71) et de MACE-2 (HR : 0,48, IC à 95 % : 0,29 - 0,77) chez les patients traités par AOD (vs. VKA).Interprétation
Le traitement de la MTEV pendant plus de 3 mois est associé à un risque réduit de MACE, tout comme le traitement par AOD par rapport à AVK. Ces résultats, qui peuvent influencer le choix des stratégies d'anticoagulation pour la MTEV, doivent être confirmés par des essais cliniques randomisés.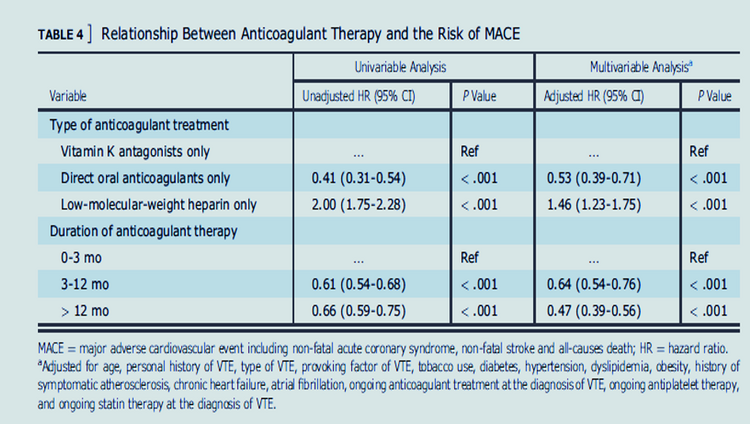
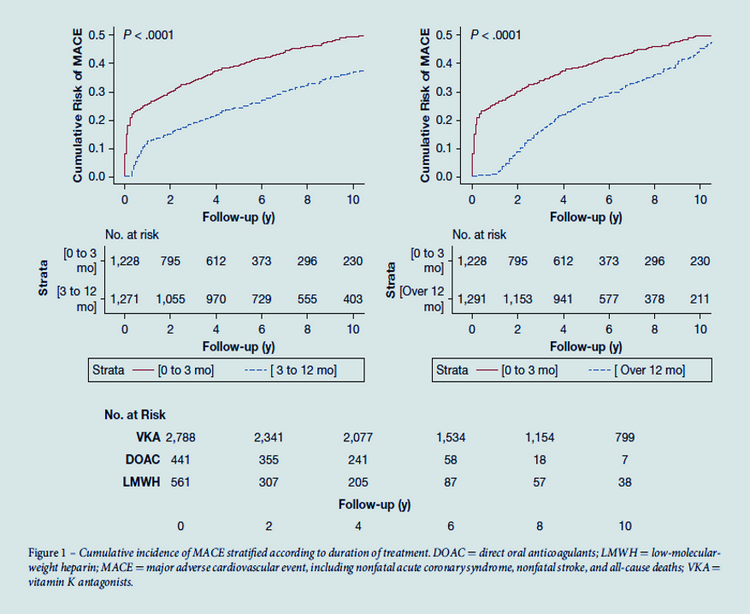
Commentaire
La MTEV est-elle annonceuse d'un évévement vasculaire artériel indésirable ? Cette question est envisagée mais non tranchée à ce jour. Cependant de nombreux faits le laissent penser.Quel est le rôle exact des AOD ? Présenter une MTEV alors que l'on a déjà une atteinte coronarienne, ou une atteinte cérébro vasculaire ou une AOMI, est-ce licite ou non de stopper l'anti agrégant plaquettaire et s'en remettre uniquement aux AOD ? Beaucoup de questions avec des réponses en suspend, mais la réponse semble imminente. MTEV et atteintes CV semblent intimement liées, affaire à suivre.
En cas de MTEV, l'évaluation et la correction des FDRCV sont nécessaires. La survenue d'une MTEV doit être un signal d'alarme. Quant aux AOD, seraient-ils des protecteurs CV ? Et à quelle dose ?
Merci à l'équipe de Brest de construire par ses études , la saga de la MTEV ! -
MTEV : good news !
 Etre en bonne santé réduit le risque de MTEV
Etre en bonne santé réduit le risque de MTEVMTEV : nouveaux horizons thérapeutiques

MTEV, nouveaux paradigmes
MTEV : situations particulières
 MTEV et ses difficultés de prise en charge
MTEV et ses difficultés de prise en chargeMTEV :changement de paradigme ?
 MTEV : anticoagulant à vie ?
MTEV : anticoagulant à vie ?MTEV à 90 ans /RIETE
 MTEV au delà de 90 ans
MTEV au delà de 90 ansMTEV en Espagne
 Made in Spain
Made in SpainMTEV et antiplaquettaire
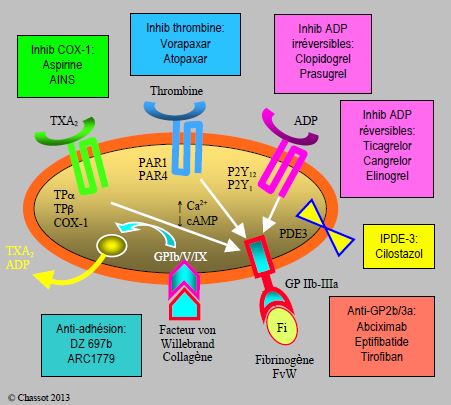 iconographie : antiplaquettaire
iconographie : antiplaquettaire
"En naissant tout homme est un Faust qui doit tout embrasser, tout éprouver, tout exprimer. Ce sont les erreurs de ses prédécesseurs et de ses contemporains qui ont fait de Faust un savant. Les progrès de la science obéissent à la loi de la répulsion : pour faire un pas en avant, il faut commencer par renverser la domination de l'erreur et des fausses théories. Les progrès de l'art se font selon la loi de l'attraction : pour faire un pas en avant, il faut commencer par suivre et par imiter ses prédécesseurs et pas s'incliner devant eux."
Heestermans, M.; Poenou, G.; Duchez, A.-C.; Hamzeh-Cognasse, H.; Bertoletti, L.; Cognasse, F. Immunothrombosis and the Role of Platelets in Venous Thromboembolic Diseases. Int. J. Mol. Sci. 2022, 23, 13176. https://doi.org/10.3390/ijms232113176
Immunothrombose et rôle des plaquettes dans les maladies thromboemboliques veineuses
Article libre d'accésRésumé
"La thromboembolie veineuse (MTEV) est la troisième principale cause de décès cardiovasculaire et est traditionnellement traitée avec des anticoagulants qui s'opposent directement à la coagulation.
Cependant, des données récentes ont démontré que les plaquettes jouent également un rôle crucial dans la physiopathologie de la MTEV.
Dans la présente revue, nous décrivons comment les plaquettes sont impliquées à tous les stades de la thrombose veineuse expérimentale.
Les plaquettes interviennent dans l'initiation de la maladie en se fixant à la paroi vasculaire sur laquelle elles interviennent dans le recrutement des leucocytes.
Ce processus est appelé immunothrombose et, dans ce nouveau concept, les cellules inflammatoires telles que les leucocytes et les plaquettes entraînent directement la progression de la MTEV.
En plus de leur implication dans l'immunothrombose, les plaquettes activées peuvent entraîner directement la thrombose veineuse en favorisant la coagulation et en sécrétant des facteurs procoagulants.
De plus, la fibrinolyse et la résolution des vaisseaux sont (en partie) médiées par les plaquettes.
Enfin, sont résumés comment la thérapie antiplaquettaire conventionnelle peut prévenir la thrombose veineuse expérimentale et avoir un impact sur la MTEV (récurrente) chez l'homme."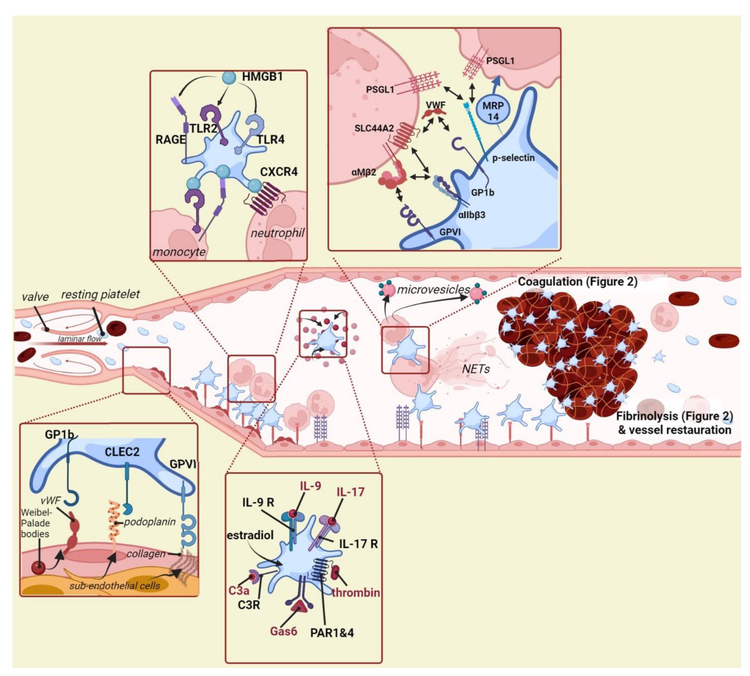
Rôle des plaquettes dans différents aspects de la thrombose veineuse. Les plaquettes jouent un rôle crucial dans la physiopathologie de la thrombose veineuse. Ils peuvent être recrutés sur la paroi vasculaire et peuvent interagir avec les neutrophiles et les monocytes. De plus, les plaquettes activées peuvent induire une thrombose veineuse, notamment via la stimulation de la coagulation et de la fibrinolyse (voir Figure 2).NETs : pièges extracellulaires des neutrophiles, vWF : facteur von Willebrand, GP1b : glycoprotéine 1b, CLEC2 : récepteur de type lectine de type C 2, GPVI : glycoprotéine VI, RAGE : TLR : récepteur de type Toll, HMGB1 : boîte de groupe à haute mobilité 1, CXCR4 : récepteur de chimiokines CXC de type 4, PSGL-1 : ligand-1 de la glycoprotéine de sélectine P, SLC44A2 : Solute Carrier Family 44 Member 2, αMβ2 : intégrine αMβ2 ou Mac-1 (antigène du macrophage 1), MRP14 : facteur inhibiteur de la migration -protéine 14 apparentée, IL : interleukine, PAR1-4 : récepteur activé par la protéase 1–4, C3a : facteur de complément 3a, GAS6 : arrêt de croissance spécifique 6. L'image est créée à l'aide de Biorender.com.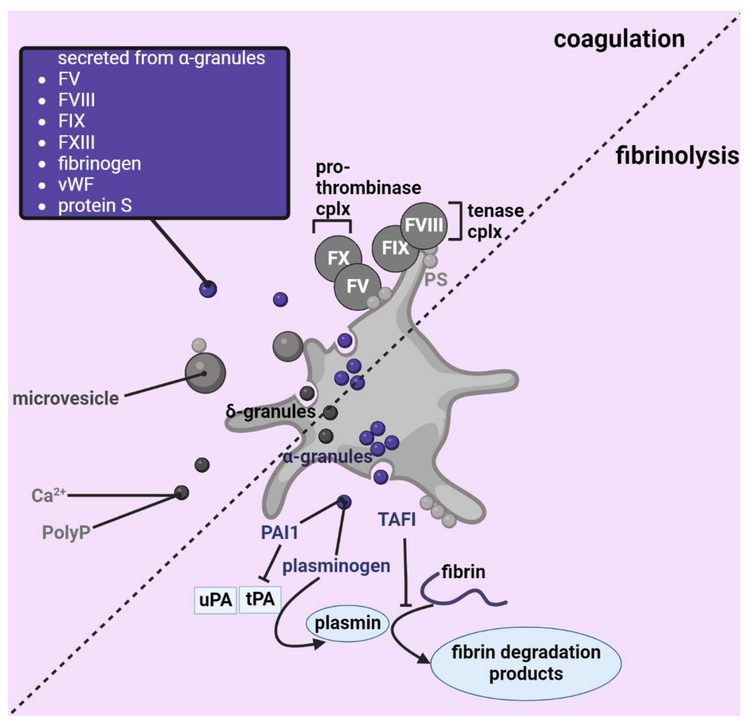
Le rôle des plaquettes dans la coagulation et la fibrinolyse. Les plaquettes sont impliquées à la fois dans la coagulation et la fibrinolyse. Lors de l'activation, ils peuvent sécréter des microvésicules, des facteurs de coagulation et de fibrinolyse à partir de leurs granules α, et du Ca 2+ et des polyphosphates (polype) à partir de leurs granules denses. De plus, ils exposent la phosphatidylsérine sur leur membrane pour favoriser à la fois la coagulation et la fibrinolyse. FV : facteur de coagulation V, FVIII : facteur de coagulation VIII, FIX : facteur de coagulation IX, FXIII : facteur de coagulation XIII, vWF : facteur de von Willebrand, FX : facteur de coagulation X, PAI1 : inhibiteur de l'activateur du plasminogène 1, TAFI : inhibiteur de la fibrinolyse activable par la thrombine, uPA/tPA : urokinase/activateur tissulaire du plasminogène, δ-granules : granules denses. L'image est créée à l'aide de Biorender.com.
Extraits de l'article
"Contrairement aux études sur la thrombose veineuse expérimentale, l'efficacité du traitement antiplaquettaire dans la prévention de la TEV humaine (secondaire) est encore débattue, et seule l'aspirine a été testée dans des études cliniques dédiées. Les directives de pratique clinique actuelles de l'American Academy of Orthopaedic Surgeons, de l'American College of Chest Physicians, de l'American Society of Hematology et du National Institute of Health recommandent l'aspirine comme agent thromboprophylactique potentiel, comme l'héparine de bas poids moléculaire (HBPM) ou les anticoagulants oraux directs (AOD) sans aucune préférence exprimée en termes d'options thérapeutiques. Dans l'étude EPCAT, l'aspirine s'est avérée efficace dans la prévention de la TEV après 5 jours de traitement par l'inhibiteur du FXa, le rivaroxaban, en chirurgie orthopédique au prix d'une légère augmentation du risque hémorragique . En revanche, l'essai CRISTAL n'a pas réussi à démontrer la non-infériorité de l'aspirine par rapport à l'HBPM . Les résultats d'un autre essai en cours, l'essai PEPPER (NCT02810704) compare l'aspirine au rivaroxaban et à la warfarine, et cet essai pourrait fournir plus d'informations sur l'utilisation de l'aspirine pour prévenir la TEV primaire."......
........"Pendant des décennies, les plaquettes ont été considérées comme des acteurs cruciaux dans la thrombose artérielle, et cette maladie peut être efficacement prévenue ou guérie par une thérapie antiplaquettaire. Plus récemment, les données précliniques ont fourni une quantité écrasante de preuves suggérant que les plaquettes jouent également un rôle central dans la thrombose veineuse en tant que médiateurs de l'immunothrombose. Les plaquettes sont impliquées dans l'inflammation vasculaire initiale, la sécrétion plaquettaire de modificateurs de la réponse biologique, le recrutement et/ou l'activation des leucocytes, la progression et la résolution du thrombus ainsi que le remodelage de la paroi vasculaire. Dans cette revue, nous avons cherché à fournir un aperçu des rôles connus des plaquettes dans la thrombose veineuse expérimentale et à décrire les implications dans le contexte de la MTEV humaine. La versatilité des plaquettes, notamment au regard de leurs propriétés inflammatoires, est une source constante d'émerveillement et de nombreuses questions restent sans réponse quant à leur rôle dans la thrombose veineuse expérimentale, et comment extrapoler ces résultats in vivo à la pathologie humaine. Enfin, selon le scénario clinique, il sera très intéressant d'établir si le traitement antiplaquettaire est une option viable en complément ou en remplacement du traitement anticoagulant chez les patients MTEV."
Commentaire
Une fois de plus l'aspirine fait débat dans la MTEV.
Est ce que l'Aspirine ou un autre antiagrégant va briser le plafond de verre des anticoagulants.......en prévention primaire , secondaire ou en prévention du risque résiduel post MTEV. Ce risque existe.....et semble incompressible pour l'instant, rôle des antiplaquettaires ? Mais aussi rôle des statines ?
Quelle place des AOD LOW DOSE, RENOVE va nous apporter prochainement la réponse comme APICAT dans le cancer.
Mais le rôle des antiplaquettaires dans la MTEV est prometteur comme dans la MTEV et CANCER.Place des anticorps monoclonaux dans la MTEV...à venirBRAVO pour cet article novateur et nécessaire, l'IMMUNOTHROMBOSE un nouveau challenge !

